أنيلين
| أنيلين | |
|---|---|
 |
 |
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
Aniline[1] |
|
| تسمية الاتحاد الدولي للكيمياء | |
Benzenamine |
|
| أسماء أخرى | |
Phenylamine |
|
| المعرفات | |
| رقم CAS | 62-53-3 142-04-1 (HCl) |
| بوب كيم (PubChem) | 6115 8870 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C6H7N |
| كتلة مولية | 93.13 غ.مول−1 |
| المظهر | سائل عديم اللون |
| الكثافة | 1.0297 غ/مل |
| نقطة الانصهار | −6.30 °س، 267 °ك، 21 °ف |
| نقطة الغليان | 184.13 °س، 457 °ك، 363 °ف |
| الذوبانية في الماء | 3.6 غ/100 مل عند 20 °س |
| ضغط البخار | 0.6 mmHg (20° س)[2] |
| حموضة (pKa) |
|
| قابلية مغناطيسية | −62.95·10−6 سم3/مول |
| معامل الانكسار (nD) | 1.58364 |
| اللزوجة | 3.71 cP (3.71 mPa·s عند 25 °س) |
| كيمياء حرارية | |
| تغير الإنتالبي القياسي للاحتراق ΔcH |
−3394 كيلوجول/مول |
| المخاطر | |
| رمز الخطر وفق GHS |      |
| وصف الخطر وفق GHS | خطر |
| بيانات الخطر وفق GHS | H301, H311, H317, H318, H331, H341, H351, H372, H400 |
| بيانات وقائية وفق GHS | P201, P202, P260, P261, P264, P270, P271, P272, P273, P280, P281, P301+310, P302+352, P304+340 |
| مخاطر | potential occupational carcinogen |
| NFPA 704 |
|
| حدود الاشتعال | 1.3–11%[2] |
| حد التعرض المسموح به U.S | TWA 5 ppm (19 mg/m3) [skin][2] |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
وهو من أبسط وأهم الأمينات العطرية، ويستخدم كمركب أولي للمواد الكيميائية الأكثر تعقيدًا. ويستخدم بشكل أساسي في تصنيع عديد إيثان اليوريا. وكما هو الحال في معظم الأمينات الطيارة، فإن الأنيلين يمتلك نوعا ما رائحة غير سارة تشبه رائحة السمك الفاسد وطعم عطري محروق، وهو سم لاذع بشكل كبير. وهو يشتعل بسهولة، ويحترق بلهب ذي دخان.
التسمية[عدل]
مصطلح 《أنيلين》 دخل إلى اللغات الأجنبية من الكلمة العربية النيلة.
البنية[عدل]
تأخذ جزيئة الأنيلين شكلًا مقاربًا للشكل الهرمي قليلًا، وتهجين ذرة النيتروجين يقع بين sp3 و sp2، ونتيجة لذلك يمتلك النيتروجين مزدوجًا إلكترونيًا في الأوربيتال المهجن spx تغلب عليه صفات الأوربيتال p. تكون مجموعة الأمين في الأنيلين أكثر تسطحًا من نظيرتها في الأمينات الأليفاتية، ويعود ذلك إلى التعاقب الحاصل بين المزدوج الإلكتروني في وإلكترونات مجموعة الأريل.
يعكس الشكل الهندسي لهذه الجزيئة توازنًا بين عاملين هما: 1) استقرار المزدوج الإلكتروني الموجود على ذرة النيتروجين في أوربيتال تغلب عليه صفات الأوربيتال s يوجّه الجزيئة نحو الشكل الهرمي (تكون طاقة الأوربيتالات التي تغلب عليها صفات الأوربيتال s منخفضة) 2) لا موقعية المزدوج الإلكتروني على ذرة النتيروجين يوجّه الجزيئة نحو الشكل المسطح (وجود المزدوج الإلكتروني في أوربيتال p خالص يمنح أفضل ازدواج بين الأوربيتالات من نوع π في حلقة البنزين).[4]
طريقة الاصطناع[عدل]
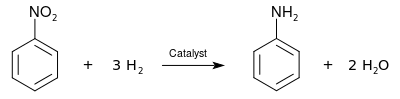
يُنتج الأنيلين صناعيًا بخطوتين بدءًا من البنزين:
- أولا، تجرى عملية نترتة البنزين باستخدام مزيج مركز من حمض النتريك وحمض الكبريتيك عند درجة حرارة من 50° إلى 60°م، وينتج عن هذه العملية النيتروبنزين.
- في الخطوة الثانية، يتم هدرجة النتروبنزين، عند درجة حرارة (200-300 °م) بوجود فلزكمحفز ليعطي الأنيلين.
أول من اختزل النيتروبنزين إلى الأنيلين كان نيكولاي زينين سنة 1842 باستخدام سلفيد غير عضوي كعامل مختزل (تفاعل زينين). وقد أجريت عملية اختزال النيتروبنزين إلى الأنيلي كجزء من تفاعلات اختزال أجراها أنطوان بيشامب سنة 1854 باستخدام الحديد كعامل مختزل (اختزال بيشامب).
وكطريقة بديلة، يمكن تحضير الأنيلين من الفينول والأمونيا، حيث يشتق الفينول من الكومين(Cumene).[5]
التفاعلات[عدل]
تمتاز تفاعلات الأنيلين بالتنوع والكثرة ويعود ذلك إلى توفّر هذا المركب بأثمان زهيدة ومنذ فترة طويلة.
الأكسدة[عدل]
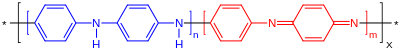
لقد أجريت دراسات مكثفة على تفاعلات أكسدة الأنيلين، وغالبًا ما تُجرى هذه التفاعلات على ذرة النيتروجين وتؤدي غالبًا إلى تكوين روابط C-N جديدة. في المحاليل القلوية، ينتج الآزوبنزين، ويُنتج تفاعل حمض الزرنيخيك مع الأنيلين إلى إنتاج الصبغة البنفسجية فيولأنيلين violaniline. يحوّل حمض الكروميك الأنيلين إلى الكوينون، وتتفاعل الكلورات مع الأنيلين بوجود بعض الأملاح الفلزية (وعلى وجه الخصوص الفاناديوم) لتكوّن أسود الأنيلين. يتفاعل حمض الهيدروكلوريك وكلورات البوتاسيوم مع الأنيلين لتكوين الكلورانيل. ويؤكسد بيرمنغنات البوتاسيوم الأنيلين في المحاليل المتعادلة لتكوين النيتروبنزين، وفي المحاليل القلوية لتكوين الآزوبنزين والأمونيا وحمض الأوكساليك، وفي المحاليل الحامضية لتكوين أسود الأنيلين. يتفاعل حمض الهيبوكلوروز مع الأنيلين لتكوين 4-أمينوفينول وبارا-أمينو ثنائي فنيل أمين[6]. وينتج عن تفاعل البيرسلفات مع الأنيلين أنواع مختلفة من الأنيلينات المتعددة، وتمتلك هذه البوليمرات خصائص تأكسدية وحامضية-قاعدية متنوعة.
تفاعلات النيتروجين[عدل]
القاعدية[عدل]
يعدّ الأنيلين قاعدة ضعيفة، وتكون الأمينات الأروماتية مثل الأنيلين، قواعد أضعف بكثير من نظائرها الأليفاتية. يتفاعل الأنيلين مع القواعد القوية لتكوين أيون الأنيلينيوم (C6H5-NH3+) أو ما يعرف بأيون الفنيل أمونيوم.[7]
تعزى قاعدية الأنيلين إلى تعاضد التأثير الحثي الناتج من ذرات الكربون ذات التهجين sp2 والتي تمتلك سالبية كهربائية أعلى وتأثير الرنين الذي ينتج من لا موقعية المزدوج الإلكتروني في نظام باي في حلقة البنزين (انظر الصورة في أدناه):

الأسيلة[عدل]
يتفاعل الأنيلين مع كلوريدات الأسيل مثل كلوريد الأسيتيل لتكوين الأميدات.
الاستخدامات[عدل]
جاءت القيمة التجارية الكبيرة لاكتشاف الأنيلين بسبب جاهزية الحقل الذي سيستخدم فيه، وهو صناعة الأصبغة. اكتشاف صباغ الموف (اللون البنفسجي الزاهي) في 1856 من قبل ويليام هنري بيركن، وهو الأول من سلسلة من الأصبغة الصنعية التي أصبحت يقدر عددها الآن بالمئات. ويمكن قراءة مقالات الصباغة، وصباغ الفوكسين، وصباغ الصفرنين، وصباغ الإندولين، لمزيد من التفاصيل عن هذا الموضوع. وبالإضافة إلى استخدامه كمركب أولي للأصبغة، فهو مركب أولي لتصنيع العديد من الأدوية، مثل الباراسيتامول (تايلينول) والفيكودين.
اقرأ أيضاً[عدل]
المراجع[عدل]
- ^ Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: الجمعية الملكية للكيمياء. 2014. ص. 416, 668. DOI:10.1039/9781849733069-FP001. ISBN:978-0-85404-182-4.
Aniline, for C6H5-NH2, is the only name for a primary amine retained as a preferred IUPAC name for which full substitution is permitted on the ring and the nitrogen atom. It is a Type 2a retained name; for the rules of substitution see P-15.1.8.2. Substitution is limited to substituent groups cited as prefixes in accordance with the seniority of functional groups explicitly expressed or implied in the functional parent compound name. The name benzenamine may be used in general nomenclature.
- ^ أ ب ت "NIOSH Pocket Guide to Chemical Hazards #0033". المعهد الوطني للسلامة والصحة المهنية (NIOSH).
- ^ Vollhardt, P.؛ Schore, Neil (2018). Organic Chemistry (ط. 8th). W. H. Freeman. ص. 1031. ISBN:9781319079451.
- ^ Alabugin, Igor V. (Professor) (2016). Stereoelectronic effects : a bridge between structure and reactivity. Chichester, UK. ISBN:978-1-118-90637-8. OCLC:957525299.
{{استشهاد بكتاب}}: صيانة الاستشهاد: مكان بدون ناشر (link) - ^ Thomas Kahl, Kai-Wilfrid Schröder, "Aniline" in Ullmann's Encyclopedia of Industrial Chemistry 2007; John Wiley & Sons: New York.
- ^ Chisholm 1911، صفحة 48.
- ^ قالب:McMurry3rd
| أنيلين في المشاريع الشقيقة: | |
| |