تحلل الجلوكوز

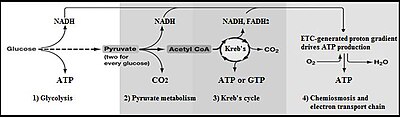
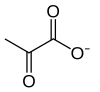
تحلل السكر[1] (من جلوكوز، مصطلح قديم الأجل[2] لتحلل الغلوكوز) هو مسار أيضي يحول الجلوكوز C6H12O6 إلى البيروفات، CH3COCOO− + H+. فإن الطاقة الحرة التي تصدر في هذه العملية تستخدم لتشكيل جزيئات عالية الطاقة من أدينوسين ثلاثي الفوسفات ATP والعامل المختزل نيكوتيناميد الأدينين ثنائي النوكليوتيد (NADH).[3]
تحلل السكر هو تسلسل محدد لعشرة تفاعلات محفّزة بوساطة الانزيمات. المركبات الوسيطة توفر نقاط دخول إلى تحلل الجلوكوز. على سبيل المثال، معظم السكريات الأحادية مثل الفركتوز والجلاكتوز، يمكن تحويلها إلى واحدة من هذه المركبات الوسيطة. المركبات الوسيطة قد تكون أيضا مفيدة مباشرةً. على سبيل المثال، المركب الوسيط فوسفات ثنائي هيدروكسي الأسيتون DHAP هو مصدر من الجليسرول الذي يتحد مع 3 أحماض الدهنية ليشكل دهون (ثلاثي الجليسريد).
تحلل الجلوكوز هو تسلسل أيضي لا يعتمد على الأوكسجين، وهذا يعني أنه لا يستخدم الأكسجين (أي الأوكسجين الجوّي) لأي من تفاعلاته. ومع ذلك فإن نواتج تحلل الجلوكوز (البيروفات وNADH + H+) في بعض الأحيان تستقلب باستخدام الأوكسجين الجوّي.[4] عندما يستخدم الأوكسجين الجزيئي في عملية التمثيل الغذائي لنواتج هذه العملية عادةً ما يشار إليها باسم الهوائية، بينما إذا لم يستخدم الأكسجين فتسمّى اللاهوائية.[5] .إذاً تحلّل الجلوكوز يحدث -مع وجود اختلافات- في جميع الكائنات الحية تقريباً، سواء التحلّلالهوائي أو اللاهوائي. وحدوث هذه العملية بشكل واسع يدل على أنها واحدة من أقدم المسارات الأيضية.[6] وفي الواقع، فإن التفاعلات التي تشكل تحلل الجلوكوز ومساره الموازي (مسار خماسي الفوسفات)، تحدث بتحفيز من المعادن تحت ظروف خالية من أوكسجين محيطات الأركايا (الدهر السحيق) وأيضا في غياب الأنزيمات.[7] و عملية تحلّل السكر يمكن أن تكون قد نشأت من المواد الكيميائية المقيدة التي تسبق التكوين الجنيني، أي قبل ملايين السنين.
تحلل السكر يحدث في معظم الكائنات الحية في العصارة الخلوية (السايتوسول) للخلية. إن النوع الأكثر شيوعاً من تحلّل السكر هو مسار إمبدن- مايرهوف-بارناس (مسار EMP) الذي تم اكتشافه من قبل غوستاف امبدن، أوتو مايرهوف، جيكوب كارول بارناس. تحلل السكر يشير أيضا إلى مسارات أخرى، مثل مسارإنتنر-دودوروف ، ومسارات التخمّر المتجانسة وغير المتجانسة المتنوعة. على الرغم من ذلك، سيقتصر الشرح هنا على مسار إمبدن- مايرهوف-بارناس.[8]
إن تحلل الجلوكوز الكامل يمكن تقسيمه إلى مرحليتن منفصلتين:[9]
- المرحلة التحضيرية/ مرحلة الاستثمار – حيث أنه يتم فيها استهلاك الATP
- مرحلة الدفع/ المكافأة– حيث يتم إنتاج ATP .
نظرة عامة[عدل]
التفاعل الكامل لتحلل السكر هو:
إن استخدام الرموز في هذه المعادلة يجعل الأمر يبدو غير متوازن فيما يتعلق بذرات الأكسجين، وذرات الهيدروجين والشحنات. إن تعادل الذرة يحفظ بمجموعتي الفوسفات (Pi):[10]
- كل مركب موجود على شكل فوسفات الهيدروجين سالب الشحنة (HPO4−2)، يتفكك ليساهم في إنتاج أيوني هيدروجين (+2H) بشكل كلي.
- كل مركب يحرر ذرة الأكسجين عندما يرتبط بجزيء أدينوسين ثنائي الفوسفات، ليساهم في إنتاج 2O بشكل كلي.
يتم معادلة الشحنات عن طريق الاختلاف بين ADP و ATP. في الخلية، جميع الثلاث مجموعات من الهيدروكسيل من الADP تتفكك إلى -O و+H وهذا الأيون يميل للتواجد على شكل رابطة أيونية مع Mg+2، لينتج -ADPMg. أدينوسين ثلاثي الفوسفات ATP يتصرف تماماً بنفس الطريقة باستثناء احتوائه على أربع مجموعات من الهيدروكسيل، لينتج ATPMg−2. عندما تتواجد هذه الاختلافات في الشحنات على طول مع الشحنات الثابتة على مجموعتي الفوسفات، فإنّ الشحنات الكلية (-4) على جانبي المعادلة تكون متعادلة. لتفاعلات التخمر البسيط، استقلاب جزيء واحد من الجلوكوز إلى جزيئين من البيروفات ينتج بشكل نهائي جزيئين من ATP. معظم الخلايا سوف تقوم بمزيد من التفاعلات 'لسداد' NAD+ المستخدم وإنتاج المركب النهائي من الإيثانول أو حمض اللبنيك. العديد من البكتيريا تستخدم المركبات الغير العضوية مثل مستقبلات الهيدروجين لإعادة إنتاج +NAD. الخلايا التي تقوم بعملية التنفس الهوائي تنتج ATP أكثر، ولكن ليس كجزء من تحلل الجلوكوز. وأيضاً، هذه التفاعلات الهوائية تستخدم البيروفات وNADH و+H من تحلل السكر.و التنفس الهوائي للكائنات حقيقية النواة ينتج حوالي 34 جزيء إضافي من ال ATP لكل جزيء الجلوكوز، ولكن معظم هذه الجزيئات تنتجها آلية مختلفة إلى حد كبير عن تفاعلات فسفرة مستوى الارتكاز في تحلل الجلوكوز. الإنتاج منخفض الطاقة، لكل جزيء جلوكوز، من التنفس اللاهوائي نسبة إلى التنفس الهوائي، يعطي نواتج أكثر تدفقاً من خلال المسار الذي يحدث تحت ظروف قليلة الأكسجين، إلا إذا تواجدت مصادر بديلة لركائز مؤكسدة لاهوائياً مثل الأحماض الدهنية.
| أيض السكريات الأحادية المعروفة، وتتضمن استحداث الجلوكوز وتكون الغليكوجين وتحلل الغليكوجين. |
|---|
 |
نظرة تاريخية[عدل]
مسار تحلل الجلوكوز كما نعرفه الآن احتاج إلى ما يقارب 100 سنة حتى يتم اكتشافه بشكل كامل. دمج نتائج العديد من التجارب الصغيرة كان مطلوباً لفهم هذا المسار بشكل كامل.
الخطوات الأولى في فهم تحلل الجلوكوز بدأت في القرن التاسع عشر مع صناعة الخمور. لأسباب اقتصادية، صناعة الخمرة الفرنسية عملت على دراسة سبب تحول طعم الخمور إلى طعم بغيض، بدلاً من أن يتحول إلى كحول عبر التخمر. بحث العالم الفرنسي لويس باستور في هذه القضية في عام 1850، وكانت نتائج تجاربه بداية طريق طويل نحو تفسير مسار تحلل الجلوكوز.[11] لقد بيّنت تجاربه أن التخمّر يحدث بسبب وجود كائنات حيّة دقيقة، وأنّ استهلاك خميرة الجلوكوز يقل تحت الظروف الهوائية، مقارنةً بالظروف اللاهوائية (تأثير باستير).[12]

بينما كانت تجارب باستور هي الرائدة في ذلك الوقت، معرفة الخطوات المكونة لتحلل الجلوكوز زُوّد عن طريق تجارب التخمّر اللاخلوي لإيدوارد بوخنر خلال فترة ال1890.[13] بيّن بوخنر أنّ تحول الجلوكوز إلى إيثانول كان ممكناً باستخدام مستخلص غير حيّ من الخميرة (بسبب عمل الإنزيمات في المستخلص[14]). لم يقتصر دور هذه النتائج على إحداث ثورة في الكيمياء الحيوية فحسب، ولكنها أيضاً مكّنت العلماء فيما بعد لدراسة هذا المسار بطريقة أكثر تحكمّاً داخل المختبر. في سلسة من التجارب (1905-1911)، العالميّن أوثر هاردن وويليام يونغ قاما باكتشاف أجزاء أكثر عن تحلل الجلوكوز.[15] قاما باكتشاف التأثيرات التنظيمية لأدينوسين ثلاثي الفوسفات على استهلاك الجلوكوز خلال عملية تخمّر الكحول. قاما أيضاً بإلقاء الضوء على وظيفة مركب واحد باعتباره مركب وسيط في عملية تحلل الجلوكوز، و هو ال فركتوز -1,6-ثنائي الفوسفات.[14]
تمت دراسة دور هذا المركب عن طريق قياس مستويات ثاني أكسيد الكربون، الذي كان ينتج عند وضع الجلوكوز مع عصارة الخميرة. إنتاج ثاني أكسيد الكربون كان يزداد بسرعة في البداية ثم بعد ذلك يتباطأ. هاردن ويونغ لاحظا أنّ هذه العملية تبدأ من جديد في حال إضافة فوسفات غير عضوي للمزيج. هاردن ويونغ استخلصا أنّ هذه العملية تنتج إيسترات الفوسفات العضوي، وتجارب أخرى إضافية مكّنتهم من استخلاص الفركتوز ثنائي الفوسفات.
توصل آرثر هاردن وويليام يونغ مع نيك شيبارد من خلال تجربة أخرى إلى أنّ الجزء ما دون الخلوي الحساس للحرارة ذا الكتلة الجزيئية العالية (الإنزيمات) والجزء السيتوبلازمي الغير حساس للحرارة ذا الكتلة الجزيئية الصغيرة (أدينوسين ثلاثي الفوسفات وأدينوسين ثنائي الفوسفات وثنائي نوكليوتيد الأدنين وأميد وعوامل مرافقة أخرى) يجب تواجدهم مع بعضهم البعض حتى تستمر عملية التخمّر. هذه التجربة بدأت مع ملاحظة أنّ عصارة الخميرة النقية غير قادرة على التخمّر أو حتى إنتاج سكر الفوسفات.هذا المزيج عاد عند إضافة الخميرة الغير نقية التي تم غليها. غليان الخميرة يبقي جميع البروتينات غير فعّالة (حيث أنها تفسدها). قدرة المستخلص المغليّ مع العصارة النقية على إكمال التخمّر يقترح أن العوامل المساعدة ليست بروتينات في صفاتها.[15]

في فترة ال 1920 أوتتو مايرهوف كان قادراً على ربط العديد من الأجزاء الفردية من تحلل الجلوكوز التي تم اكتشافها عن طريق بوخنر، هاردن، ويونغ. مايرهوف وفريقه كانوا قادرين على استخلاص العديد من الإنزيمات الجلايكولية من نسيج عضليّ، ووضعها مع بعضها ليتم إنتاج المسار صناعياً من الجلايكوجين لحمض اللاكتيك.[13][16]
خلال بحث واحد، مايرهوف والعالم رينات جونوويكس كوكالتي بحثا في التفاعل الذي يقسم الفركتوز 1، 6 -ثنائي الفوسفات إلى جزيئين من السكر ثلاثي الفوسفات، عمل سابق افترض أن هذا الانقسام حدث بوساطة 1,3-دايفوسفوغليسر ألديهايد إضافةً إلى إنزيم مؤَكسِد و cozymase. مايرهوف وجونوويكس وجدا أن ثابت الإتزان لتفاعل الأيزومارايز والألدوز لم يتأثر بوساطة الفوسفات غير العضوي أو أي مساعد إنزيم آخر أو أي إنزيمات مؤكسِدَة. قاما أيضاً باستبعاد دايفوسفوغليسر ألديهايد كوسيط محتمل خلال عملية تحلل الجلوكوز.[16]
مع جميع هذه الأجزاء التي كانت متوفرة خلال فترة ال1930، جوستاف إيمبيدن افترض مسار مفصّلاً خطوة بخطوة للمسار الذي نعرفه اليوم باسم مسار تحلل الجلوكوز[17] ، أكبر التحديات كانت في معرفة تعقيدات هذا المسار بسبب الفترة القصيرة جداً التي يحدث خلالها بالإضافة إلى التراكيز المنخفضة لوسائط التفاعلات الجلايكولية. مع فترة ال 1940، مايرهوف، إيمبيدن والعديد من من علماء الكيماء الحيوية أخيراً قاموا بإكمال لغز تحلل الجلوكوز.[18] فهم المسار المعزول توسع في العقود اللاحقة، ليتضمن تفاصيل أكثر عن تنظيمه وتكامله مع المسارات الأيضية الأخرى.
تسلسل التفاعل[عدل]
المرحلة التحضيرية[عدل]
أول خمس خطوات تعتبر المرجلة التحضيرية (أو الاستثمارية)، لأنها تستهلك الطاقة لتحويل الجلوكوز إلى اثنين من سكر فوسفاتي ثلاثي الكربون (G3P).[9]
|
||||||||||||||||||||
الخطوة الأولى في تحلل السكر هي فسفرة الجلوكوز من قبل عائلة من الإنزيمات تسمى الهكسوكيناز لتكون جلوكوز 6-فوسفات (G6P). هذا التفاعل يستهلك ATP، ولكنه يعمل للحفاظ على تراكيز الجلوكوز منخفضة، وتشجيع مستمر على نقل الجلوكوز إلى داخل الخلية من خلال نواقل على غشاء البلازما. بالإضافة إلى ذلك، فإنه يمنع السكر من التسرب للخارج (الخلية لا تحتوي نواقل ل G6P)، والانتشار الحر لل GDP إلى خارج الخلية لا يحدث بسبب طبيعته المشحونة. الجلوكوز بدلاً من ذلك يمكن أن يتكون من فسفرة أو من تحلل النشا أو الغلايكوجين داخل الخلية.
في الحيوانات، النظير الإنزيمي للهيكسوكيناز يسمى جلوكوكيناز يستخدم أيضاَ في الكبد، الذي لديه قدرة أقل بكثير على الارتباط بالجلوكوز (ك م قريب من المستوى الطبيعي لسكر الدم)، ويختلف في الخواص التنظيمية. اختلاف قوة الارتباط بالجزيء الارتكازي والتنظيم المختلف لهذا الإنزيم هو انعكاس لدور الكبد في الحفاظ على مستويات السكر في الدم.
العوامل المساعدة: Mg+2
|
||||||||||||||||||||
بعد ذلك، يتم إعادة ترتيب G6P على شكل فركتوز سداسي الفوسفات (F6P) عن طريق جلوكوز فوسفات أيزوميراز. الفركتوز يمكنه أيضاً أن يدخل مسار تحلل السكر عن طريق الفسفرة في هذه المرحلة. التغير في البناء يسمى (isomeration)، التي يتم فيها تحويل G6P إلى F6P. التفاعل يتطلب إنزيم حتى يستمر، وهذا الإنزيم هو (phosphohexose isomerase).
هذا التفاعل هو تفاعل عكسي حر تحت الظروف الخلوية الطبيعية. ولكن، غالبا ما يكون مدفوع للأمام بسبب انخفاض تركيز F6P، الذي يتم استهلاكه باستمرار خلال الخطوة التالية من تحلل الجلوكوز. في ظل ظروف ارتفاع تركيز F6P، هذا التفاعل بسهولة يعمل في الاتجاه المعاكس. هذه الظاهرة يمكن تفسيرها من خلال مبدأ ليتشاتلييه. عملية الIsomerization إلى سكر كيتوني ضروري لإسقرار الأيون الكربوني السالب في الخطوة الرابعة من التفاعل (أدناه).
|
||||||||||||||||||||
إنفاق الطاقة لجزيء ATP آخر في هذه الخطوة يتم في خطوتين: عملية تحلل السكر (هذه الخطوة) لا رجعة فيها الآن أي تكون باتجاه واحد، الطاقة المستهلكة تزعزع استقرار الجزيء. لأن التفاعل المحفز بوساطة فوسفوفركتوكيناز-1 (PFK-1) يدمج مع عملية التحلل المائي للATP (خطوة ملائمة لإنتاج الطاقة) وهي في جوهرها لا رجعة فيها، ومسار كيميائي مختلف يجب أن يستخدم للقيام بالتحويل العكسي من خلال استحداث السكر. وهذا يجعل التفاعل نقطة تنظيمية رئيسية (انظر أدناه). وهي أيضا خطوة محددة لسرعة التفاعل.
علاوة على ذلك، الفسفرة التالية ضرورية للسماح بإنتاج مجموعتين مشحونتين (بدلاً من واحدة فقط) في خطوة لاحقة من تحلل السكر، لضمان الانتشار الحر لعناصر الارتكاز خارج الخلية.
نفس التفاعل يمكن أيضاً أن يتم تحفيزه بوساطة فسفوفروكتوكيناز التي تعتمد على بيروفوسفات(PFP / PPi-PFK)، الموجود في معظم النباتات، بعض البكتيريا، البكتيريا البدائية، الطلائعيات، ولكن ليس في الحيوانات. هذا الإنزيم يستخدم البيروفوسفات (PPi) كمانح للفوسفات بدلاً من ATP. وهو تفاعل عكسي، يزيد من مرونة التمثيل الغذائي للسكر.[19] مجموعة أكثر ندرة من الإنزيم البديل ((PFK تعتمد على الADP وجدت في بعض أنواع البكتيريا البدائية.[20]
عوامل مساعدة: Mg+2
|
||||||||||||||||||||||||||
زعزعة الجزيء في التفاعل السابق يسمح للحلقة السداسية أن تفصل بوساطة الألدولاز إلى جزيئي سكر ثلاثي: فوسفات ثنائي هيدروكسي أسيتون (كيتوز)، غليسيرألدهيد 3-الفوسفات (ألدوز). هناك نوعان من الألدوليز: النوع الأول موجودة في الحيوانات والنباتات والنوع الثاني موجود في الفطريات والبكتيريا؛ النوعين يستخدمان طرق مختلفة في فصل حلقة الكيتوز. الإلكترونات المتمركزة في رابطة الكربون-الكربون المنفصلة ترتبط مع مجموعة الكحول. مما يؤدي إلى أن الأيون كربوني السالب يستقر عن طريق تركيب الأيون الكربوني السالب نفسه عبر توزيع رنين الشحنات عن طريق وجود عامل مرافق مشحون.
|
||||||||||||||||||||
تريوز فوسفات أيزوميراز يحول بسرعة الفوسفات ثنائي هيدروكسي الأسيتون إلى غليسيرألدهيد ثلاثي الفوسفات (GADP) الذي يستمر في تحلل السكر إلى حد أبعد. وهذا مميز له، لأنه يوجه الفوسفات ثنائي هيدروكسي الأسيتون إلى الأسفل في نفس مسار غليسيرألدهيد ثلاثي الفوسفات، وبالتالي يساهم في تنظيم التفاعل.
مرحلة الدفع/ الاكتساب[عدل]
النصف الثاني من مرحلة تحلل السكر معروفة بمرحلة الدفع أو الاكتساب، تتصف بأنها كسب لجزيئات عالية الطاقة ATP و NADH.[9] لأن الهدف من الأيض أساسا هو تحويل المواد الغذائية (وهنا السكر) إلى ATP الذي يعتبر «بطارية الخلية الحية». ونظراً بأن الجلوكوز ينتج جزيئي سكر ثلاثي خلال المرحلة التحضيرية، كل تفاعل في مرحلة الدفع يحدث مرتين في جزيء الجلوكوز الواحد. هذا ينتج جزيئين NADH و 4 جزيئات ATP، مما يؤدي إلى اكتساب كلي لجزيئين NADH و جزيئينATP من مسار التحلل الغلايكولي لجزيء السكر الواحد.
|
||||||||||||||||||||
مجموعات الألدهايد لجزيئات السكر الثلاثي تتأكسد ويضاف إليها الفوسفات غير العضوي، منتجاً (1,3)-غليسيريت ثنائي الفوسفات (بالإنجليزية:1,3-Bisphosphoglyceric acid) الهيدروجين يستخدم لاختزال جزيئين من NAD+، ناقل للهيدروجين، لإنتاج +NADH + H+ لكل جزيء سكر ثلاثي. توازن ذرة الهيدروجين وتوازن شحنتها يتم الحفاظ عليهما على حد سواء لأن مجموعة الفوسفات (Pi) موجودة في الواقع غلى شكل الأنيون (فوسفات الهيدروجين (HPO4−2)[10]، الذي يتفكك للمساهمة بأيونات الهيدروجين H+ الإضافية وإعطاء شحنة كلية (-3) على كلا الجانبين. هنا، الزرنيخات (AsO4−3)، هو أيون سالب أقرب إلى الفوسفات غير العضوي وقد يحل محل الفوسفات باعتبارها الركيزة لتشكيل 1-arseno-3-phoshoglycerate. ولكن هذا غير مستقر ويتحلل ليكون 3-phosphoglycerate، الوسيط الكيميائي في الخطوة التالية من المسار. نتيجة لتجاوز هذه الخطوة، جزيء ال ATP الناتج من (1,3)-غليسيريت ثنائي الفوسفات (بالإنجليزية:1,3-Bisphosphoglyceric acid) في التفاعل التالي لن يتم إنتاجه، على الرغم من ذلك التفاعل سيستمر. ونتيجة لذلك، الزرنيخات هو (uncoupler) لتحلل السكر.[21]
|
||||||||||||||||||||
هذه الخطوة هي عبارة عن التحول الانزيمي لمجموعة فوسفات من (1,3)- غليسيريت ثنائي الفوسفات (بالإنجليزية:1,3-Bisphosphoglyceric acid) إلى ADP عن طريق الإنزيم الكيناز (phosphoglycerate)(بالإنجليزية: phoshoglycerate kinase), لإنتاج ATP و3-phosphoglycerate. في هذه الخطوة، اتحلل الغلايكولي يصل إلى نقطة التعادل: جزيئين من الATP يتم استهلاكهما، وجزيئين جديدين يتم إنتاجهما. هذه الخطوة، واحدة من خطوتي فسفرة مستوى الارتكاز (بالإنجليزية:substrate-level phosphorylation) يتطلب ADP; إذاً، عندما تكزن الخلية لديها فائض من ال ATP (وقليلاً من ال ADP), هذا التفاعل لا يحدث. لأن ال ATP يضمحل بسرعة نسبيا عندما لا يتم استقلابه وهذه هي نقطة تنظيمية مهمة في مسار تحلل السكر. ADP موجود بالفعل على شكل ADPMg- و ATP موجود على شكل -ATPMg2 ليتم معادلة الشحنات على -5 في كلا الجانبين.
العوامل المساعدة: Mg+2
|
||||||||||||||||||||
عوامل مساعدة: 2Mg+2:
|
||||||||||||||||||||
العوامل المساعدة 2Mg+2: أيون«متكون جزئياً» ينسق مع مجموعة الكربوكسيل في عامل الارتكاز، والأيون الآخر «حفاز» الذي يشارك في تفاعل إزالة الماء.
|
||||||||||||||||||||
الآن فسفرة مستوى الارتكاز النهائية (بالإنجليزية:substrate-level phosphorylation) تكون جزيء من البيروفات و جزيءATP عن طريق إنزيم بيروفات كيناز. وهذا يعمل كخطوة إضافية تنظيمية، وذلك مشابه لخطوة phosphoglycerate كيناز. عوامل مساعدة:Mg+2
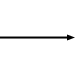
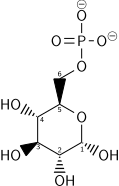
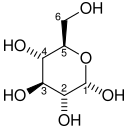
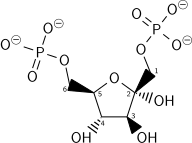
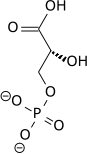
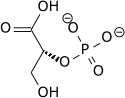
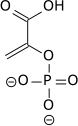
البنية الكيميائية لمكونات تحلل الجلوكوز بناءً على تخطيط فيشر والنموذج المتعدد الأضلاع[عدل]
الوسائط الكيميائية من تحلل الجلوكوز بناءً على تخطيط فيشر تصور التغيرات الكيميائية خطوة بخطوة. هذه الصورة يمكن مقارنتها مع نموذج متعدد الأضلاع.
رؤية بيوكيميائية[عدل]
وجود أكثر من نقطة تنظيمية تشير إلى أن الوسائط الكيميائية بين هذه النقاط تدخل وتغادر مسار التحل الجلايكولي بوساطة عمليات أخرى، على سبيل المثال، في أول خطوة منظمة، الهكسوكيناز يحول جلوكوز إلى جلوكوز-6-فوسفات بدلأً من الاستمرار في مسار تحلل السكر، هذا الوسيط الكيميائي يمكن أن يتم تحويله إلى جزى ئات تخزن الجلوكوز مثل الغلايكوجين أو النشا. التفاعل العكسي، التكسر، مثلاً، الغلايكوجين، ينتج بشكل أساسي جلوكوز-6-فوسفات؛ كمية قليلة جداً من الجلوكوز الحر يتنج من التفاعل. الجلوكوز -6- فوسفات الذي ينتج أيضاً يمكنه أن يدخل مسار تحلل السكر بعد أول نقطة تحكم.
الخطوة التنظيمية الثانية (الخطوة الثالثة من تحلل الجلوكوز)، فوسفوفركتوكيناز يحول الفركتوز-6-فوسفات إلى فركتوز (6,1) ثنائي الفوسفات، الذي بعد ذلك يتحول إلى غليسرألديهايد ثلاثي الفوسفات وثنائي هيدروكسي أسيتون الفوسفات. ثنائي هيدروكسي أسيتون الفوسفات يمكن أن يتم إزالته من التحلل الجلايكولي عن طريق التحول إلى الجلسرول-3-الفوسفات، الذي يمكن بعد ذلك استخدامه لتكوين الدهون الثلاثية.[22] على العكس من ذلك، الدهون الثلاثية ثلاثي الغليسريد يمكن أن يتم تحطيمها إلى الأحماض الدهنية والجلسرول؛ الأخير، بدوره، يمكن أن يتحول إلى ثنائي هيدروكسي أسيتون الفوسفات، الذي يمكنه الدخول إلى التحلل الجلايكولي بعد خطوة التحكم الثانية.
تنظيم الانزيمات المحددة لسرعة التفاعل[عدل]
الأربع إنزيمات التنظيمية هي هكسوكيناز، غلوكوكيناز، فوسفوفركتوكيناز، البيروفات كايناز. فإن التدفق خلال مسار تحلل السكر يتم التحكم به استجابة للظروف سواء داخل أو خارج الخلية. العوامل الداخلية التي تنظم تحلل السكر في المقام الأول توفر ATP بكميات كافية لاحتياجات الخلية. العوامل الخارجية تعمل في المقام الأول على الكبد، الأنسجة الدهنية والعضلات، التي يمكنها إزالة كميات كبيرة من الجلوكوز من الدم بعد وجبات الطعام (وبالتالي منع ارتفاع السكر في الدم عن طريق تخزين الجلوكوز الزائد كدهون أو جليكوجين، اعتمادا على نوع الأنسجة). الكبد هو أيضا قادرة على الإفراج عن الجلوكوز في الدم بين الوجبات، أثناء الصيام، وممارسة التمارين الرياضية وبالتالي الوقاية من نقص السكر في الدم عن طريق تحلل الغليكوجين واستحداث السكر. هذه التفاعلات الكيميائية تتزامن مع وقف تحلل الجلوكوز في الكبد.
في الحيوانات، تنظيم مستويات الجلوكوز في الدم عن طريق البنكرياس بالتزامن مع الكبد هو جزء حيوي من التوازن. فإن خلايا بيتا في جزر لانغرهانس حساسة لتركيز السكر في الدم.[23] الارتفاع في تركيز السكر في الدم يسبب لها لإفراز الأنسولين في الدم، مما له تأثير وخاصة على الكبد، ولكن أيضا على خلايا الدهون والعضلات، مما يتسبب لهذه الأنسجة إلى إزالة الجلوكوز من الدم. عندما تكون نسبة السكر في الدم منخفضة تتوقف خلايا بيتا في البنكرياس عن إنتاج الأنسولين، ولكن بدلا من ذلك تعمل على تحفيز خلايا ألفا المجاورة في البنكرياس إلى إفراز غلوكاغون في الدم.[23] وهذا بدوره يؤدي أن يعمل الكبد على إفراز الجلوكوز في الدم عن طريق تحطيم الغلايكوجين المخزن، وعن طريق استحداث السكر. إذا كان الانخفاض في مستوى السكر في الدم بشكل خاص سريع أو حاد، أجهزة استشعار الجلوكوز الأخرى تسبب إفراز الأدرينالين من الغدد الكظرية في الدم. وهذا له نفس تأثير الغلوكاغون على استقلاب الجلوكوز، ولكن تأثيره أكثر وضوحا.[23] في الكبد، الجلوكاجون والادرينالين يسببان الفسفرة للإنزيمات الرئيسية المحددة لسرعة تحلل الجلوكوز، وتصنيع الأحماض الدهنية، بناء الكولسترول، استحداث السكر وتحلل الغليكوجين. الأنسولين له تأثير معاكس على هذه الإنزيمات.[4] الفسفرة ونزع الفوسفات (dephosphorylation) من هذه الإنزيمات (في النهاية، نتيجة لمستوى الجلوكوز في الدم) هو المتحكم الذي عن طريقه يتم التحكم في هذه المسارات في الكبد والدهون والعضلات. وبالتالي فسفرة الفوسفوفركتوكيناز يمنع تحلل الجلوكوز، في حين أن نزع الفوسفات (dephosphorylation) من خلال عمل الإنسولين يحفز تحلل الجلوكوز.[4]
إضافة لذلك، هكسوكيناز وغلوكوكيناز يعملان بشكل مستقل عن التأثيرات الهرمونية كضوابط تحكيم في نقاط دخول الجلوكوز إلى خلايا الأنسجة المختلفة. هكسوكيناز يستجيب إلى مستوى جلوكوز-6-فوسفات (G6P) في الخلية، و، في حالة غلوكوكيناز، فهو يستجيب إلى مستوى السكر في الدم لنقل ضوابط التحكم بمسار تحلل السكر تماماً في الأنسجة المختلفة (انظر أدناه).[24]
عندما يتم تحويل الجلوكوز إلى G6P من قبل هكسوكيناز أو غلوكوكيناز، فإنه يمكن إما أن يتم تحويلها إلى غلوكوز-1-فوسفات (G1P) ليتحول إلى الغلايكوجين، أو بدلاً من ذلك تحويلها عن طريق تحلل السكر إلى البيروفات، الذي يدخل الميتوكندريون حيث يتم تحويلها إلى أسيتيل مرافق الإنزيم-أ ثم إلى سيتريت. السيتريت الزائدة تخرج من المايتوكنريون إلى العصارة الخلوية، حيث أن ATP citrate lyase يعمل على تجديد إنتاج أسيتيل مرافق الإنزيم –أ وأوكسالوآسيتات (OAA).إن أسيتيل مرافق الإنزيم-أ يتم استخدامه لتكوين الأحماض الدهنية والكولسترول، وهما من أهم الطرق للاستفادة من الجلوكوز الزائد عندما تكون تراكيزه عالية في الدم. الإنزيمات المحددة لسرعة التفاعل المحفزة لهذه التفاعلات تقوم بهذه الوظائف عندما تكون منزوعة الفوسفات من خلال عمل الأنسولين في خلايا الكبد. بين وجبات الطعام أثناء الصوم، ممارسة التدريب البدني أو نقص مستوى السكر في الدم، الجلوكاجون والأدرينالين يتم إفرازهما في الدم. هذا يسبب أن يتم تحويل الجليكوجين في الكبد مرة أخرى إلى G6P، ومن ثم تحويلهاإلى جلوكوز عن طريق إنزيم متخصص في الكبد الغلوكوز 6-فسفاتاز وإفرازه إلى الدم. الجلوكاجون والأدرينالين أيضا يحفزان استحداث السكر، الذي يحول الركائز (غير الكربوهيدرات) إلى G6P الذي يرتبط في G6P المستمد من الجليكوجين، أو بدائل له عندما يستنفذ مخزن الجليكوجين في الكبد. هذا الأمر بالغ الأهمية من أجل وظيفة الدماغ، لأن الدماغ يستخدم الجلوكوز كمصدر للطاقة في أغلب الأحيان [25]، هذه الفسفرة المستمرة، خاصة للفوسفوفركتوكيناز، ولكن أيضًا، إلى حد ما للبيروفات كيناز تمنع حدوث تحلل الجلوكوز بنفس الوقت مع استحداث السكر وتحلل الغليكوجين.
الهكسوكيناز والجلوكوكيناز[عدل]

جميع الخلايا تحتوي الإنزيم هكسوكيناز، الذي يحفز تحول الجلوكوز الذي يدخل الخلية إلى جلوكوز-6-فوسفات (G6P) (بالإنجليزية: Glucose 6-phosphate). نظراً لأنّ غشاء الخلية لا يمرر G6P، الهيكسوكيناز ضروري لنقل الجلوكوز إلى الخلايا التي لا يستطيع المغادرة منها بعد ذلك. يتم تثبيط الهكسوكيناز عن طريق المستويات العالية من G6P داخل الخلية. لذلك فإنّ معدل دخول الجلوكوز إلى داخل الخلايا يعتمد بشكل جزئي على مدى سرعة تحلل الG6P خلال تحلل الجلوكوز، وعن طريق تصنيع الغليكوجين (في الخلايا التي تخزن الجلايكوجين، وهي خلايا الكبد والعضلات).[4][26]
الغلوكوكيناز، مختلف عن الهكسوكيناز، لا يتم تثبيطه بوساطة G6P. وهو موجود في خلايا الكبد، ويقوم فقط بفسفرة الجلوكوز الذي يدخل الخلية لتكوين جلوكوز-6-فوسفات (G6P)، (بالإنجليزية: Glucose 6-phosphate)، عندما يكون السكر موجود في الدم. هذه هي أول خطوة في المسار الجلايكولي داخل الكبد، وهي لذلك تنقل طبقة إضافية للتحكم في المسار الجلايكولي داخل الكبد.[4]
الفوسفوفركتوكيناز[عدل]
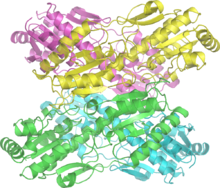
الفوسفوفركتوكيناز (بالإنجليزية: phosphofruktokinase 1) هو عبارة عن نقطة تحكم مهمة في مسار التحلل الجلايكولي، وذلك لأنه واحد من الخطوات الغير عكسية ولديه مؤثرات تفارغية مهمة، أدينوسين أحادي الفوسفات AMP وفركتوز 6,2-ثنائي الفوسفات (F2,6BP) (بالإنجليزية: Fructose 2,6-bisphosphate).
فركتوز 6,2-ثنائي الفوسفات (F2,6BP)،(بالإنجليزية: Fructose 2,6-bisphosphate)، محفز قوي جداً لفوفسفوفركتوكيناز (PFK-1). الذي يتم إنتاجه عندما يتم فسفرة F6P بوساطة فوسفوفركتوكيناز ثانٍ (PFK2)، بالإنجليزية:Phosphofructokinase 2). في الكبد، عندما يكون السكر منخفض في الدم والغلوكاغون يرفع cAMP، يتم فسفرة PFK2،(بالإنجليزية: Fructose 2,6-bisphosphate)، عن طريق البروتين كيناز أ. عملية الفسفرة تثبط PFK2 ،(بالإنجليزية: Fructose 2,6-bisphosphate)، ومجموعة أخرى على البروتين تصبح محفزة كما هو الحال بالنسبة للفركتوز فوسفاتاز 2، الذي يحول F2,6BP إلى F6P. كلاً من الغلوكاغون والأدرينالين يسببان مستويات عالية من الcAMP في الكبد. المستويات المنخفضة من فركتزو 1,6-ثنائي الفوسفات داخل الكبد هي نتيجة لانخفاض في نشاط الفوسفوفركتوكيناز وزيادة في نشاط فركتوز 1،6-ثنائي الفوسفات، ولذلك فإن استحداث السكر (في جوهره، «معاكس للتحلل الجلايكولي») يكون مفضلاً. وهذا يكون بالتزامن مع وظيفة الكبد في مثل هذه الحالات ، لأن ردة فعل الكبد لهذه الهرمونات هو إفراز السكر إلى الدم.
ATP يتنافس مع AMP على موقع المؤثر التفارغي على إنزيم PFK. تراكيز ال ATP في الخلايا أعلى بكثير من تراكيز الAMP، عادةً أكثر بمئة ضعف [27]، ولكن تركيز الATP لا يتغيرأكثر من حوالي 10% تحت الظروف الفسيولوجية، بينما أن الانخفاض وتركيز الATP بمقدار 10% يؤدي إلى زيادة بتراكيز الAMP بمقدار ستة أضعاف.[28] لذلك فإن ملائمة الATP كمؤثر تفارغي مشكوك فيها. أي زيادة في الAMP هو نتيجة لنقصان في شحنة الطاقة داخل الخلية.
السيترات يثبط الفوسفوفركتوكيناز عندما يتم فحصه في المختبر عن طريق تحسين التأثير المثبط لجزيء الATP. على الرغم من ذلك، هناك شك بوجود تأثير حقيقي داخل الجسم، لأن السترات في العصارة الخلوية يتحول بشكل أساسي إلى أسيتل مساعد الإنزيم-أ ليتم استخدامه في تصنيع الأحماض الدهنية والكولسترول.
TIGAR، إنزيم محفز بوساطة P53، مسؤول عن تنطيم فوسفوفركتوكيناز، (بالإنجليزية: Phosphofructokinase 1)، ويعمل على الحماية من الأكسدة.[29] TIGAR هو إنزيم وحيد يمتلك وظيفة ثنائية تنطم F2,6BP. يمكنه أن يتصرف مثل الفوسفاتاز (الفركتوز -2,6- ثنائي الفوسفات) الذي يفصل الفوسفات عن ذرة الكربون (2) لينتج F6P. كما يمكنه أيضا العمل ككيناز (PFK2) عن طريق إضافة فوسفات على ذرة الكربون (2) في F6-P لينتج F2,6BP.[30]
البيروفات كيناز[عدل]

إنزيم البيروفات كيناز يحفز آخر خطوة في تحلل الجلوكوز، التي يتم فيها إنتاج البيروفات و الATP. البيروفات كيناز يحفز انتقال مجموعة فوسفات من الفوسفواينول بيروفات PEP إلى ADP، ليتم إنتاج جزيء واحد من البيروفات وجزيء واحد من الATP.
البيروفات كايناز في الكبد يُنَظّم بشكل غير مباشر بوساطة الأدرينالين والغلوكاغون، من خلال البروتين كايناز أ. هذا البروتين كايناز يعمل على فسفرة البيروفات كايناز داخل الكبد لتثبيطه. البيرفات كايناز في العضلات لا يتم تثبيطه عن طريق تنشيط الأدرينالين للبروتين كايناز أ. الجلوكاجون يستشعر الصيام (عدم وجود جلوكوز). ولهذا، التحلل الجلايكولي يتم تثبيطه في الكبد ولكنه لا يتأثر في العضلات في حالة الصيام. أي زيادة في مستويات السكر في الدم تؤدي إلى إفراز الأنسولين، الذي يعمل على تحفيز فسفرة الفوسفاتاز 1، مؤدياً إلى نزع الفوسفات (dephsphorylation) وتنشيط البيروفات كايناز . هذه العمليات التنظيمية تمنع التفاعل العكسي (بيروفات كاربوكسيلاز (يالانجليزية: pyruvate carboxylase) وفوسفواينول بيروفات كاربوكسي كايناز (يالانجليزية: phosphoenolpyruvayte carboxykinase))، وبالتالي يمنع الحلقة المغلقة (بالإنجليزية: futile cycle).
الأمراض المتعلقة بتحلل الجلوكوز[عدل]
السكري[عدل]
دخول السكر للخلايا يعتمد على إشارات من الإنسولين ، والسكر يتم تكسيره مباشرةً خلال مسار تحلل الجلوكوز ، وبالتالي تخفيض مستويات السكر في الدم . على الرغم من ذلك ، مستويات الإنسولين المنخفضة الناتجة عن مرض السكري تؤدي إلى مستويات عالية من السكر في الدم ، حيث تزداد مستويات السكر في الدم والجلوكوز لا يدخل للخلايا بطريقة صحيحة . خلايا الكبد أيضاً تساهم في ارتفاع مستويات السكر في الدم عن طريق عملية استحداث السكر. تحلل السكر في داخل خلايا الكبد يتحكم بإنتاج السكر عن طريق الكبد، وعندما يتم إنتاج الجلوكوز عن طريق الكبد بشكل كبير بدون وجود طرق لتكسيره داخل الجسم ، فإن ذلك يتسبب بارتفاع مستوى السكر في الدم .
الأمراض الوراثية[عدل]
الطفرات الجينية هي بشكل عام نادرة بسبب أهمية المسار الأيضيّ، هذا يعني أنّ أغلب الطفرات الحينية التي تحدث تؤدي إلى عدم قدرة الخلية على التنفس، وبالتالي تسبب موت الخلية خلال مرحلة مبكرة. ومع ذلك، هناك بعض الطفرات الجيننية التي تم ملاحظتها، من ضمنها نقص البيروفات كيناز الذي يعد مثالاً ملحوظاً وبارزاً، الذي يؤدي إلى أنيميا انحلالية مزمنة.
السرطان[عدل]
الخلايا السرطانية الخبيثة تقوم بعملية التحلل الجلايكولي بمعدل أسرع بعشر مرات من النسيج الغير سرطاني المكون من نفس نوع الخلايا، خلال عملية التكوين، هنالك دعم محدد من الشعيرات الدموية يزود الخلايا السرطانية بالدم، مما يؤدي إلى نقص الأكسجين الواصل إليها. ولذلك، هذه الخلايا تعتمد على العمليات الأيضية اللاهوائية مثل التحلل الحلايكولي لجزيء أدينوسين ثلاثي الفوسفات (ATP). بعض الخلايا السرطانية تنتج إنزيمات محددة خاصة بهذه العملية بكميات كبيرة (بإفراط) فينتج عن ذلك معدلات أعلى لحدوث عملية تحلل السكر. عادة هذه الإنزيمات هي الآيسوإنزايمات، لعملية التحلل الجلايكولي التقليدية، التي تختلف التي تختلف في قابليتها للاستجابة للتغذية الراجعة المثبطة لهذه التفاعلات. إن زيادة نشاط تحلل السكر في النهاية يواجه نتائج نقص الأكسجين بوساطة إنتاج كمية كافية من الأدينوسين ثلاثي الفوسفات في هذا المسار اللاهوائي.[31] هذه الظاهرة تم شرحها لأول مرة عام 1930 م عن طريق أوتو فاربورغ وأطلق عليها تأثير واربيرغ. فرضية فاربورغ تدعي بأن السرطان يحدث نتيجة اختلال وظيفي للتفاعلات الأيضية داخل المايتوكندريا بشكل أساسي، بدلاً من أن تكون بسبب نمو غير طبيعي للخلايا. عدد من النظريات تم تطوريها لتفسير تأثير واربيرغ. إحدى هذه النظريات تقترح أن زيادة معدل التحلل الجلايكولي هو عملية حماية طبيعية للجسم والتغير الخبيث يمكن أن يكون سببه الأساسي هو استقلاب الطاقة.[32]
إن معدل تحلل السكر العالي حصل على تطبيقات طبية مهمة، لأن معدل تحلل السكر الهوائي السريع بواسطة الخلايا السرطانية الخبيثة تم استخدامه سريرياً بشكل علاجي لتشخيص والتحكم في استجابة علاجات السرطان وذلك عن طريق تصوير كيميائي لدخول فلوروديوكسي غلوكوز (FDG) إلى الخلايا (فهو يعد ركيز تحلل إشعاعي معدل للهكسوكيناز) باستخدام التصوير المقطعي بالإصدار البوزيتروني (PET).[33][34]
هناك بحث مستمر للتأثير على الإستقلاب داخل الميتوكندريا وعلاج السرطان عن طريق تقليل معدل استقلاب السكر وبالتالي حرمان الخلايا السرطانية بطرق متنوعة، من ضمنها النظام الغذائي الكيتوني.[34]
اقرأ أيضا[عدل]
المراجع[عدل]
- ^ محمد مرعشي (2003). معجم مرعشي الطبي الكبير (بالعربية والإنجليزية). بيروت: مكتبة لبنان ناشرون. ص. 221. ISBN:978-9953-33-054-9. OCLC:4771449526. QID:Q98547939.
- ^ Webster's New International Dictionary of the English Language, 2nd ed. (1937) Merriam Company, Springfield, Mass.
- ^ Bailey، Regina. "10 Steps of Glycolysis". مؤرشف من الأصل في 2016-11-19.
- ^ أ ب ت ث ج Stryer، Lubert (1995). "Glycolysis.". In: Biochemistry (ط. Fourth). W.H. Freeman and Company. ص. 483–508. ISBN:0 7167 2009 4.
- ^ Anderson، Douglas M.، المحرر (2003). Dorland’s Illustrated Medical Dictionary (ط. 30th). Saunders. ص. 35, 71. ISBN:0 8089 2288 2.
- ^ Romano، AH؛ Conway، T (1996). "Evolution of carbohydrate metabolic pathways". Res Microbiol. ج. 147 ع. 6–7: 448–55. DOI:10.1016/0923-2508(96)83998-2. PMID:9084754.
- ^ Keller؛ Ralser؛ Turchyn (أبريل 2014). "Non-enzymatic glycolysis and pentose phosphate pathway-like reactions in a plausible Archean ocean". Mol Syst Biol. ج. 10 ع. 4: 725. DOI:10.1002/msb.20145228. PMID:24771084.
- ^ Kim BH, Gadd GM. (2011) Bacterial Physiology and Metabolism, 3rd edition.
- ^ أ ب ت Glycolysis – Animation and Notes نسخة محفوظة 30 أغسطس 2017 على موقع واي باك مشين.
- ^ أ ب Lane، A. N.؛ Fan، T. W. -M.؛ Higashi، R. M. (2009). "Metabolic acidosis and the importance of balanced equations". Metabolomics. ج. 5 ع. 2: 163–165. DOI:10.1007/s11306-008-0142-2.
- ^ "Home Page - Pasteur Brewing". Pasteur Brewing (بالإنجليزية الأمريكية). Archived from the original on 2018-10-05. Retrieved 2018-05-20.
- ^ "Nature Research: science journals, jobs, information and services". www.nature.com (بالإنجليزية). Archived from the original on 2019-05-29. Retrieved 2018-05-20.
- ^ أ ب "Nobelprize.org". www.nobelprize.org. مؤرشف من الأصل في 2019-05-29. اطلع عليه بتاريخ 2018-05-20.
- ^ أ ب Jakoby، William B. (1999-01). "New Beer in an Old Bottle: Eduard Buchner and the Growth of Biochemical Knowledge. Edited by Athel Cornish-Bowden. Universitat de Valencia, Valencia, 1997, 252 pp". Analytical Biochemistry. ج. 266 ع. 1: 165. DOI:10.1006/abio.1998.2911. ISSN:0003-2697. مؤرشف من الأصل في 2019-12-14.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ أ ب "New Chapters Approved". BIOS. ج. 82 ع. 4: 127–127. 2011-12. DOI:10.1893/011.082.0407. ISSN:0005-3155. مؤرشف من الأصل في 2020-03-24.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ أ ب Zou، W. (3 يناير 2006). "The Interferon-inducible Ubiquitin-protein Isopeptide Ligase (E3) EFP Also Functions as an ISG15 E3 Ligase". Journal of Biological Chemistry. ج. 281 ع. 7: 3989–3994. DOI:10.1074/jbc.m510787200. ISSN:0021-9258. مؤرشف من الأصل في 2019-12-14.
- ^ "Encyclopedia.com | Free Online Encyclopedia". www.encyclopedia.com (بالإنجليزية). Archived from the original on 2019-05-30. Retrieved 2018-05-20.
- ^ KOYAMA، Junichiro (2007). "ISSN (International Standard Serial Number), ISSN Network and Japanese National Centre for ISSN". Journal of Information Processing and Management. ج. 50 ع. 3: 144–154. DOI:10.1241/johokanri.50.144. ISSN:0021-7298. مؤرشف من الأصل في 2019-12-14.
- ^ Reeves، R. E.؛ South D. J.؛ Blytt H. J.؛ Warren L. G. (1974). "Pyrophosphate: D-fructose 6-phosphate 1-phosphotransferase. A new enzyme with the glycolytic function 6-phosphate 1-phosphotransferase". J Biol Chem. ج. 249 ع. 24: 7737–7741. PMID:4372217.
- ^ Selig، M.؛ Xavier K. B.؛ Santos H.؛ Schönheit P. (1997). "Comparative analysis of Embden-Meyerhof and Entner-Doudoroff glycolytic pathways in hyperthermophilic archaea and the bacterium Thermotoga". Arch Microbiol. ج. 167 ع. 4: 217–232. PMID:9075622.
- ^ Garrett، Reginald H.؛ Grisham، Charles M. (2012). Biochemistry. Cengage Learning; 5 edition. ISBN:978-1-133-10629-6.
- ^ Berg, J. M.; Tymoczko, J. L.; Stryer, L. (2007). Biochemistry (6th ed.). New York: Freeman. p. 622. ISBN 0-7167-8724-5.
- ^ أ ب ت Koeslag، Johan H.؛ Saunders، Peter T.؛ Terblanche، Elmarie (2003). "Topical Review: A reappraisal of the blood glucose homeostat which comprehensively explains the type 2 diabetes-syndrome X complex". Journal of Physiology. ج. 549 ع. Pt 2: 333–346. DOI:10.1113/jphysiol.2002.037895. PMC:2342944. PMID:12717005.
- ^ Stryer, Lubert (1995). "Glycolysis.". In: Biochemistry (Fourth ed.). New York: W.H. Freeman and Company. pp. 483–508. ISBN 0 7167 2009 4.
- ^ Stryer, Lubert (1995). Biochemistry (Fourth ed.). New York: W.H. Freeman and Company. p. 773. ISBN 0 7167 2009 4.
- ^ Voet، Donald؛ Judith G. Voet؛ Charlotte W. Pratt (2006). Fundamentals of Biochemistry, 2nd Edition. John Wiley and Sons, Inc. ص. 547, 556. ISBN:0-471-21495-7. مؤرشف من الأصل في 2020-01-09.
- ^ Beis، I.؛ Newsholme، E. A. (1975). "The contents of adenine nucleotides, phosphagens and some glycolytic intermediates in resting muscles from vertebrates and invertebrates". Biochem J. ج. 152 ع. 1: 23–32. DOI:10.1042/bj1520023. PMC:1172435. PMID:1212224.
- ^ Voet D., and Voet J. G. (2004). Biochemistry 3rd Edition (New York, John Wiley & Sons, Inc.).
- ^ Lackie، John (2010). TIGAR. Oxford Reference Online: Oxford University Press. ISBN:9780199549351.
- ^ Bensaad، Karim (16 يوليو 2006). https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867406007628%3Fshowall%3Dtrue "TIGAR, a p53-Inducible Regulator of Glycolysis and Apoptosis". Cell. 126, Issue I: 107–120. مؤرشف من https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867406007628%3Fshowall%3Dtrue الأصل في 2019-12-14 – عبر www.cell.com.
{{استشهاد بدورية محكمة}}: تحقق من قيمة|مسار أرشيف=(مساعدة) وتحقق من قيمة|مسار=(مساعدة) - ^ Cox, David L. Nelson, Michael M. (2005). Lehninger principles of biochemistry (4th ed.). New York: W.H. Freeman. ISBN 0-7167-4339-6.
- ^ "What is Cancer?". Retrieved September 8, 2012.
- ^ "PET Scan: PET Scan Info Reveals..." Retrieved December 5, 2005.
- ^ أ ب 4320139 549..559" (PDF). Retrieved December 5, 2005.
| في كومنز صور وملفات عن: تحلل الجلوكوز |