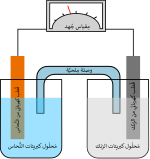
بطارية أيونات الصوديوم

بطارية أيونات الصوديومSodium-ion battery (ملاحظة 1) هي نوع من أنواع البطاريات القابلة للشحن والشبيهة ببطارية أيونات الليثيوم من حيث المبدأ، ولكن باستخدام أيونات الصوديوم من أجل حمل الشحنة الكهربائية.
بدأت بطاريات أيونات الصوديوم تأخد موضع الاهتمام منذ العقد الثاني للقرن الحادي والعشرين، خاصة مع ازدياد الاهتمام بتنويع مصادر الطاقة الكهربائية؛ إذ تتميز هذه البطاربات بالمقارنة مع البطاربات الأخرى أنها ليست محصورة بمواقع جغرافية معينة، خاصة مع وفرة الصوديوم الكبيرة في الطبيعة؛[1] وذلك سيقلل بلا شك من كلفة إنتاج البطاريات الكهربائية، خاصة بالمقارنة مع بطاريات أيونات الليثيوم.[2]
أعلنت شركة NIU Technologies الصينية المصنعة للسكوتر الكهربائي أنها ستزود الطرازات الأولى بـبطاريات أيونات الصوديوم SIB اعتبارًا من عام 2023 لتقليل تكاليف الإنتاج.
مركم أيونات الصوديوم[عدل]

على غرار التعريف الضيق للمصطلح مركم أيونات الليثيوم ، والذي يستثني بطارية ليثيوم n مع أقطاب الليثيوم المعدنية ، يمكن تعريف مركمات أيونات الصوديوم بطريقة تستخدم لتخزين أيونات الصوديوم التي سوف تشحن في الأقطاب الكهربائية. يستثنى من ذلك خلايا الصوديوم السائلة المذكورة أعلاه ، حيث لا يوجد الصوديوم كأيونات.
يتم تشغيل بطاريات أيون الصوديوم في درجة حرارة الغرفة ومع كهارل (إلكتروليتات) مائية عضوية أو غير عضوية. الميزة الرئيسية لنموذج الإلكتروليتات العضوية هي أنه يعطي جهد للخلية أعلى من المحاليل المائية.
بطاريات أيون الصوديوم مع إلكتروليتات مائية غير عضوية تسمى أيضًا "بطاريات المياه المالحة". إنها أرخص من المتغيرات التي تحتوي على إلكتروليتات عضوية. ومع ذلك ، فإن كثافة الطاقة لمراكم أيون الصوديوم مع إلكتروليت مائي أقل من كثافة الطاقة في الإلكتروليت العضوي. لذلك فهي بالكاد مناسبة للاستخدام المحمول ، ولكنها تستخدم كبطاريات ثابتة ، على سبيل المثال كمخزن منزلي للطاقة الشمسية. بطاريات أيون الصوديوم من نوع المياه المالحة غير قابلة للاشتعال وبالتالي فهي أكثر أمانًا من بطاريات الليثيوم ثاني أكسيد الكوبالت التي يمكن يحدث فيهاانفلات حراري وقد يصل إلى الانفجار.
مزايا بطاريات أيون الصوديوم[عدل]
الصوديوم أرخص بكثير من الليثيوم وهو متاح بسهولة وعمليًا بشكل غير محدود في جميع أنحاء العالم. ينتج عن هذا ميزة التكلفة المنخفضة للمواد الخام المستخدمة في إنتاج البطاريات. يعتبر كلوريد الصوديوم ثاني أكبر مكون لمياه البحر من حيث الكمية ، وقد تم استخراج (ملح البحر) وتعدين الرواسب الجوفية منذ قرون. تحدث كميات كبيرة من أملاح الصوديوم أيضًا كمنتج ثانوي لعمليات التحلل الأخرى مثل استخراج أملاح البوتاس. والأهم من ذلك ، يمكن لبعض تصاميم بطاريات أيون الصوديوم الاستغناء عن النحاس والكوبالت والنيكل. على سبيل المثال ، أظهر تقدير أولي أن تقنية أيون الصوديوم أرخص من تقنية أيونات الليثيوم. [3] نظرًا لاستخدام المواد الوفيرة وبالتالي الرخيصة ، تعتبر بطاريات أيون الصوديوم تصميمًا واعدًا للبطارية لتخزين الطاقة حيث لا يكون وزن البطارية مهمًا ، مثل محطات طاقة تخزين البطاريات الثابتة لطاقة الرياح والطاقة الشمسية. ]
تعد خلايا الصوديوم أيضًا بديلاً مفيدًا من حيث الاستدامة والتعامل (انظر: المخاطر عند التعامل مع بطاريات الليثيوم أيون). بالإضافة إلى ذلك ، يمكن تصنيع الخلايا على نفس أنظمة بطاريات الليثيوم أيون.
الكفاءة[عدل]
البيانات التالية عند 25 درجة مئوية.
| مادة الكاثود | سعة الشحن الأول (أمبير-ساعة/كيلوجرام) | سعة التفريغ الأول (أمبير-ساعة/كيلوغرام) | فاقد السعة للشحنة الأولى (أمبير-ساعة /كيلوغرام) | كفاءة الانعكاس للشحنة الأولى (%) | كفاء التفريغ بعد 20 دورة شحن (أمبير-ساعة/كيلوجرام) | كفاءة السعة بعد 20 دورة شحن (%) |
|---|---|---|---|---|---|---|
| NaV0.92Cr0.08PO4F | 83.3 | 75.2 | 8.1 | 90.3 | 68.8 | 91.4 |
| NaV0.96Cr0.04PO4F | 93.3 | 82.6 | 10.7 | 88.5 | 67.9 | 82.2 |
| NaVPO4F | 106.9 | 87.7 | 19.2 | 82.0 | 64.5 | 73.5 |
بطاريات الصوديوم تعمل أحسن من يطاريات الليثوم في درجات الحرارة المنخفضة.
بطاريات أيون الصوديوم مع إلكتروليتات مائية[عدل]
يتم تسويق هذا النوع من المركمات ، من بين أشياء أخرى ، مع تسميات مثل بطارية الماء المالح {Salt water battery}. ميزة خاصة لهذا النوع من المركمات هي أنها ، على عكس معظم المركمات - وخاصة مجموعة بطاريات الليثيوم أيون - فهي مقاومة للتفريغ العميق ويمكن تفريغها إلى جهد تفريغ نهائي قدره 0 فولت دون أن تتضرر.
عند 12 إلى 24 واط ساعة لكل لتر ، تكون كثافة طاقة بطاريات أيون الصوديوم المائية أقل بكثير من تلك الموجودة في بطاريات الرصاص أو بطاريات الليثيوم أيون ، [3] وهي ليست مشكلة للأنظمة الثابتة ، ولكن بالنسبة لبطاريات أيون الصوديوم هذه ، تطبيقات الجوال غير مناسبة. لديهم أيضًا استقرار دورة أقل.[3]
السعة التي يمكن استخلاصها تعتمد بشكل كبير على تيار التفريغ. لذلك ، تعد بطاريات أيون الصوديوم أكثر ملاءمة للتطبيقات التي تتطلب تيارات منخفضة إلى متوسطة ، ولكن لفترات طويلة من الزمن.[4]
مراكم أيون الصوديوم مع إلكتروليتات عضوية[عدل]

في مجموعة بطاريات تخزين أيون الصوديوم ذات الإلكتروليتات العضوية ، والتي يتم بحثها حاليًا بشكل مكثف ، هناك مجموعة كبيرة ومتنوعة من المواد المقترحة لـ الأنود ، الكاثود والإلكتروليت.[5] ينتج عن هذا العديد من التركيبات التي يمكن تصورها والتي تؤدي إلى معلمات تراكم مختلفة ، والتي تشمل جهد الخلية على وجه الخصوص. الإلكتروليتات الأكثر شيوعًا المقترحة لبطاريات أيون الصوديوم هي ، على نحو مشابه لبطاريات أيون الليثيوم ، محاليل أملاح الصوديوم مثل سداسي فلورو فوسفات الصوديوم. بيركلورات الصوديوم ، التي تُستخدم غالبًا في البحث الأكاديمي ، غير مناسبة للأغراض التجارية نظرًا لخطر الانفجار.[6] يتكون المذيب عادةً من ثنائي أو مخاليط ثالثية من مواد عضوية مختلفة كربونات مثل كربونات البروبيلين ، كربونات الإيثيلين وكربونات ثنائي إيثيل. اعتمادًا على الخصائص المطلوبة ، يتم استخدام سلسلة قصيرة إيثر أحيانًا.[7] من بين أشياء أخرى ، يتم استخدام الكربون في شكل الجرافين كمادة الأنود - على الرغم من أن الصوديوم المعدني مادة أنود ممكنة من حيث المبدأ ، إلا أن المعدن القلوي يتعرض لهجوم كيميائي بواسطة المواد الموجودة في الإلكتروليت. كمواد كاثودية ، يتم البحث عن مواد مختلفة تحتوي على أيونات الصوديوم مثل فوسفات وثنائي فوسفات ، على سبيل المثال فوسفات حديد الصوديوم.
اعتمادًا على المواد المستخدمة ، ينتج عن هذا جهد الخلية في النطاق بين 2 و 3.5 فولت.[3]
توافرها في السوق[عدل]
في عام 2017 ، لعبت مركمات أيون الصوديوم دورًا اقتصاديًا ثانويًا فقط ، ولكنها كانت موضوعًا للعمل البحثي بأشكال وتنوعات مختلفة. في عام 2018 ، تحسن وضع بطاريات أيون الصوديوم إلى حد ما ، حيث انخفضت تكاليف التصنيع مقارنةً ببطاريات الليثيوم ، وكان من المتوقع المزيد من الترشيد من خلال بناء أبسط بكميات أعلى.
قامت شركة Farradion البريطانية ، بالشراكة مع أكبر شركة لتصنيع البطاريات في المملكة المتحدة AMTE ، وشركة CATL الصينية ، ومورد Tesla وأكبر مصنع للبطاريات في العالم ، بتطوير نموذج أولي لبطارية أيون الصوديوم للتنقل الكهربائي. وفقًا لـ CATL ، فإن الجيل الأول من مركمات أيونات الصوديوم الخاصة بهم يحقق ما يصل إلى 160 واط/كجم ، ويهدف الجيل الثاني إلى إنتاج ما يصل إلى 200 واط / كجم ، وهو ما يمثل تقريبًا كثافة الطاقة لمراكم فوسفات الليثيوم والحديد (LFP) أو بطاريات ليثيوم فوسفات الحديد والمنغنيز (LMFP) القابلة لإعادة الشحن.[8] وفقًا للشركة فإنها تستخدم اللون الأزرق البروسي كمادة الكاثود والكربون الصلب المطوّر حديثًا كمادة الأنود ، بينما يستخدم الألمنيوم كرقائق موصل بدلاً من النحاس كما هو الحال مع بطاريات أيونات الليثيوم. هذا الأخير ممكن ، لأنه على عكس الليثيوم لا يتفاعل الصوديوم مع الألمنيوم ويوفر ميزة القدرة على تفريغ المركمات بعمق دون إتلافها ، لأن الألمنيوم - على عكس النحاس - لا يشكل أي جسور (ماس كهربائى) ، ولهذا السبب ، على عكس بطاريات الليثيوم أيون ، فهي ليست بضائع خطرة. في درجة حرارة الغرفة ، ويمكن شحن المراكم من 0 إلى 80٪ في غضون 15 دقيقة مع الاحتفاظ بـ 90٪ من سعتها عند -20 درجة مئوية.[8] نظرًا لأن جميع المواد المستخدمة في تصنيع المراكم رخيصة ومتوفرة بكثرة (الصوديوم ، والألمنيوم، والأزرق البروسي ، والكربون وما إلى ذلك) ويمكن استخدام نفس المعدات في التصنيع كما هو الحال في تصنيع بطاريات أيونات الليثيوم ؛ يبلغ السعر الأولي 77 دولارًا/ كيلوواط ساعة والإنتاج الضخم اللاحق أقل من 40 دولارًا/ كيلوواط ساعة.[9] وبحسب الشركة فمن المقرر أن يبدأ إنتاج الجيل الأول في عام 2023. anlaufen.[8]
أعلنت شركة NIU Technologies الصينية المصنعة للسكوتر الكهربائي أنها ستزود الطرازات الأولى بـبطاريات أيونات الصوديوم SIB اعتبارًا من عام 2023 لتقليل تكاليف الإنتاج.
هوامش[عدل]
- ملاحظة 1 باللغة الإنجليزية sodium-ion battery اختصاراً (NIB)
اقرأ أيضا[عدل]
- شركة كاتل لبطاريات أيون الصوديوم
المراجع[عدل]
- ^ Peters, Jens F.; Peña Cruz, Alexandra; Weil, Marcel (2019). "Exploring the Economic Potential of Sodium-Ion Batteries". Batteries (بالإنجليزية). 5 (1): 10. DOI:10.3390/batteries5010010.
- ^ Abraham، K. M. (2020). "How Comparable Are Sodium-Ion Batteries to Lithium-Ion Counterparts?". ACS Energy Letters. ج. 5 ع. 11: 3544–3547. DOI:10.1021/acsenergylett.0c02181.
- ^ أ ب ت اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعsod1 - ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعphotovolt - ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعPalomares2012 - ^ قالب:Literature
- ^ قالب:Literature
- ^ أ ب ت اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجع:0 - ^ Steve Hanley (30 Jul 2021). "CATL Reveals Sodium-Ion Battery With 160 Wh/kg Energy Density" (بالإنجليزية الأمريكية). Retrieved 2022-09-03.
| بطارية أيونات الصوديوم في المشاريع الشقيقة: | |
| |