بوريد
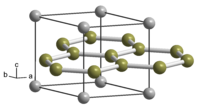
البوريدات هي مركبات كيميائية تكون حاوية على عنصر البورون، والذي يكون مرتبطاً مع عنصر آخر له على الأغلب كهرسلبية أقل من البورون. غالباً ما يشار بالبوريدات إلى مركبات البورون مع الفلزات.
تتميز البوريدات على العموم أنها من المواد السيراميكية، التي لها خصائص فيزيائية وميكانيكية مميزة.
أنواع البوريدات[عدل]
يمكن تصنيف البوريدات بشكل تقريبي إلى بوريدات غنية بالبورون أو غنية بالفلز. على سبيل المثال، فإن بوريد الإتيربيوم YB66 هو من البوريدات غنية البورون، في حين أن المركب Nd2Fe14B هو من البوريدات الغنية بالفلز. يمكن اعتبار أن نسبة ذرات البورون إلى ذرات الفلز 4:1 هي النسبة التي يمكن على أساسها اعتماد التصنيف.
البوريدات الغنية بالبورون[عدل]
تشكل العديد من عناصر الجدول الدوري طيفاً واسعاً من مركبات البوريدات الغنية بالبورون، بحيث يمكن أن تصل في حالات قصوى إلى حالة مثل بوريد الإتيربيوم YB66. تختلف خصائص البوريدات من مركب إلى آخر، حيث يمكن أن تمتلك هذه البوريدات خصائص ذات ناقية كهربائية مميزة، ويمكن أن تستخدم في صناعة أشباه الموصلات، كما أن لها خصائص مغناطيسية استثنائية.[1]
إن بعض البوريدات الفلزية تكون ذات بنية عشرونية السطوح، غي حين ان بوريدات عناصر أخرى مثل الإتريوم والزركونيوم واليورانيوم لها بنية مكعب ثماني مقطوع cuboctahedron.[2]
يكون سداسي بوريد اللانثانوم هو مادة حرارية تستخدم في صناعة المهابط الساخنة، وذلك لانخفاض دالة الشغل، والتي تعطي معدل مرتفع من الإصدار الأيوني الحراري للإلكترونات، لذلك، على سبيل المثال، تستخدم بلورات YB66 المتشكلة عن طريق الصهر النطاقي في صناعة موحّدات اللون في أجهزة المسرّع الدوراني التزامني للأشعة السينية منخفضة الطاقة.[3]
البوريدات الغنية بالفلزات[عدل]
تميل الفلزات الانتقالية إلى تشكيل البوريدات الغنية بالفلزات. تكون هذه البوريدات خاملة كيميائياً، وذات نقطة انصهار مرتفعة، ولها العديد من التطبيقات الميكانيكية المهمة. من الأمثلة على هذه البوريدات كل من ثنائي بوريد الألومنيوم AlB2 وثنائي بوريد التيتانيوم TiB2.
نظهر بعض البوريدات خصائص أخرى مميزة، مثل الموصلية الفائقة عند 39 كلفن لمركب ثنائي بوريد المغنيسيوم، أو ظاهرة عدم الانضغاط الفائقة لمركبات ثنائي بوريد الأوزميوم OsB2 و ثنائي بوريد الرينيوم ReB2.
المراجع[عدل]
- ^ Lundstrom T (1985). "Structure, defects and properties of some refractory borides". Pure & Applied Chem (free download pdf). ج. 57 ع. 10: 1383. DOI:10.1351/pac198557101383.
- ^ Matkovich، V.I.؛ J Economy؛ R F Giese Jr؛ R Barrett (1965). "The structure of metallic dodecaborides" (PDF). Acta Cryst. ج. 19 ع. 6: 1056–1058. DOI:10.1107/S0365110X65004954. مؤرشف من الأصل (PDF) في 2014-12-22. اطلع عليه بتاريخ 2008-08-28.
- ^ Wong، Jo؛ T Tanaka؛ M Rowen؛ F Schäfer؛ B R Müller؛ Z U Rek (1999). "YB66 – a new soft X-ray monochromator for synchrotron radiation. II. Characterization". J Synchrotron Rad. ج. 6 ع. 6: 1086–1095. DOI:10.1107/S0909049599009000.
| بوريد في المشاريع الشقيقة: | |
| |
