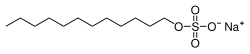
كبريتات لوريل الصوديوم
| كبريتات لوريل الصوديوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
Sodium dodecyl sulfate |
|
| أسماء أخرى | |
Sodium monododecyl sulfate; Sodium lauryl sulfate; Sodium monolauryl sulfate; Sodium dodecanesulfate; Sodium coco-sulfate; dodecyl alcohol, hydrogen sulfate, sodium salt; n-dodecyl sulfate sodium; Sulfuric acid monododecyl ester sodium salt; |
|
| المعرفات | |
| رقم CAS | 151-21-3 |
| بوب كيم | 3423265 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | NaC12H25SO4 |
| الكتلة المولية | 288.38 غ/مول |
| المظهر | مسحوق أبيض |
| الكثافة | 1.01 غ/سم3 |
| نقطة الانصهار | 206 °س |
| نقطة الغليان | ? °س |
| الذوبانية في الماء | ? غ/100 مل ماء عند ؟؟ °س |
| الذوبانية | ? |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
كبريتات لوريل الصوديوم (أو سلفات دوديسيل الصوديوم، اختصاراً SDS) هو مركب كيميائي له الصيغة الكيميائية (NaC12H25SO4)، وهو مؤثر سطحي أيوني، يستخدم في معاجين الأسنان والشامبو نظراً لقدرته على تشكيل رغوة يسمى تجارياً تكسابون.
الخواص[عدل]
مادة خافضة للتوتر السطحي وله قدرة عالية على إعطاء الرغوة اللازمة للتنظيف.[3]
له القدرة على ازالة الزيوت والأوساخ بفعالية عالية. إضافة إلى كونه رخيص الثمن مما يجعل استعماله واسع الانتشار[4]
آثاره السلبية[عدل]
بعض الدراسات التي طبقت على الحيوانات والإنسان تشير أن استخدام هذا المركب يعرض الشخص إلى أخطار عديدة أهمها إصابة الجلد بالتهيج والالتهابات نتيجة قدرته على اختراق الجلد، كذلك قد يسبب تهيجًا والتهابات في العين ينتج عنها خلل في نمو العين خصوصا عند الأطفال واعتام عدسة العين عند الأكبر سنًا.[5]
ويستخدم أيضًا في تركيب معجون الاسنان لانه يعطي الشعور بالانتعاش والتعقيم داخل الفم ولكن وجد من خلال الدراسات أنه قد يكون له اثر سلبي على وجود التقرحات الفموية من ناحية وزيادة الالم وفترة الشفاء.[6] هناك بعض الدراسات تشير أنه من الممكن أن يمكث في الجسم ويتراكم في بعض الاجزاء مسببًا زيادة في حجم الكبد وزيادة في حجم الخلايا الكبدية وخللًا في إفراز إنزيمات الكبد[7] علاوة على ذلك يمكن أن يسبب زيادة في نسبة الغلوكوز في الدم وانه قد يكون مادة مسرطنة وهذا ما لم يثبت بشكل تام ولكنه يعزز احتمالية أن يسبب كبريتات لوريل الصوديوم اضطرابا في جهاز الغدد الصماء.[8] يعتمد الخطر المرافق لاستخدامه على تركيز المادة المستخدمة ومدة التعرض له.[5]
- الوقاية من الآثار السلبية
هذا المركب ليس مصمما للاستعمال طويل الأمد لذلك يجب شطفه بسرعة وبشكل كامل بعد الاستعمال؛ لأن بقائه على الجلد فترة طويلة يمكن أن يسبب بعض المشاكل.[5]
الاستخدامات[عدل]
يستخدم بشكل أساسي في المنظفات، والشامبو، ومعجون الأسنان، معاجين الحلاقة والصابون السائل، إضافة إلى فعاليته في تنظيف محركات السيارات[4]
طالع أيضاً[عدل]
المصادر[عدل]
- ^ أ ب ت Sodium dodecyl sulfate (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Bondi, C. A., Marks, J. L., Wroblewski, L. B., Raatikainen, H. S., Lenox, S. R., & Gebhardt, K. E. (2015). Human and environmental toxicity of sodium lauryl sulfate (SLS): evidence for safe use in household cleaning products. Environmental health insights, 9, EHI. S31765.
- ^ أ ب semanticscholar. (2010). Sodium lauryl sulfate. The main cleaning agent in soap and detergent. Retrieved from: https://pdfs.semanticscholar.org/e03d/371a050ebab19ccfbcca51db2652fc585caf.pdf نسخة محفوظة 7 مارس 2019 على موقع واي باك مشين.
- ^ أ ب ت CIR. (2005). Annual review of cosmetic ingredient safety assessment- 2002/2003. Retrieved from https://online.personalcarecouncil.org/ctfa-static/online/lists/cir-pdfs/pr216.pdf نسخة محفوظة 1 يوليو 2020 على موقع واي باك مشين.
- ^ Sälzer, S., Rosema, N., Martin, E., Slot, D., Timmer, C., Dörfer, C., & van der Weijden, G. (2016). The effectiveness of dentifrices without and with sodium lauryl sulfate on plaque, gingivitis and gingival abrasion—a randomized clinical trial. Clinical Oral Investigations, 20(3), 443-450.
- ^ OECD. (2007). Sids initial assessment profile. Retrieved from https://hpvchemicals.oecd.org/ui/handler.axd?id=97AEE5B8-EFE9-4096-859B-D3AFBFD03CFD نسخة محفوظة 2018-12-24 على موقع واي باك مشين.
- ^ Moore, A. (1983). Final report on the safety assessment of sodium lauryl sulphate and ammonium lauryl sulphate. Journal of the American College of Toxicology, 2, 127-181.
| كبريتات لوريل الصوديوم في المشاريع الشقيقة: | |
| |