أورام الغدد العصبية الصماء
| أورام الغدد العصبية الصماء | |
|---|---|
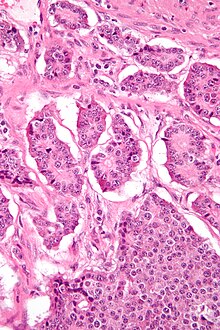 صورة مجهرية لورم غدد عصبية صماء. صبغة الهيماتوكسيلين واليوزين
| |
| معلومات عامة | |
| الاختصاص | أورام الغدد الصماء |
| من أنواع | مرض نادر، ومرض |
| المظهر السريري | |
| الأعراض | تورد، وإسهال[1]، وألم البطن[1]، وألم ظهر[1] |
| الإدارة | |
| أدوية | |
| تعديل مصدري - تعديل | |
أورام الغدد العصبية الصماء هي أورام تنشأ من خلايا الغدد الصماء (الهرمونية) والجهاز العصبي. أكثرها شيوعا يحدث في الأمعاء، حيث غالبا ما يطلق عليها الأورام السرطانية، ولكن توجد أيضا في البنكرياس والرئة وبقية أجزاء الجسم.
على الرغم من وجود العديد من أنواع أورام الغدد العصبية الصماء، إلا أنها تُعامل كمجموعة من الأنسجة لأن خلايا هذه الأورام تشترك في ميزات مشتركة، مثل المظهر المتشابه، ولديها حبيبات إفرازية خاصة، وغالبًا ما تنتج الأمينات الحيوية وهرمونات البولي ببتيد.[2]
التصنيف[عدل]
منظمة الصحة العالمية[عدل]
تُصنِف منظمة الصحة العالمية (WHO) أورام الغدد العصبية الصماء إلى ثلاث فئات رئيسية، التي تؤكد على درجة الورم بدلا من الأصل التشريحي:[3][4]
- أورام الغدد العصبية الصماء متباينة بشكل جيد، وتنقسم كذلك إلى أورام حميدة وأولئك الذين لديهم سلوك غير مؤكد
- سرطانات الغدد العصبية الصماء المتمايزة جيدًا (منخفضة الدرجة) مع سلوك خبيث منخفض الدرجة
- أورام الغدد العصبية الصماء السرطانية (درجة عالية) غير متمايزة، وهي سرطان الغدد العصبية الصماء والخلايا الصغيرة.
بالإضافة إلى ذلك، تقر خطة منظمة الصحة العالمية أن الأورام مختلطة مع كل من ميزات سرطان الغدد العصبية الصماء والظهارية، مثل سرطان الخلايا الكأسية، وهو ورم نادر في الجهاز الهضمي.[5]
يعتمد وضع ورم معين في إحدى هذه الفئات على السمات النسيجية المحددة جيدًا: كالحجم، وإنتهاك الأوعية اللمفاوية، والتهم الانقسامي، ومؤشر وضع العلامات بروتين Ki-67، وإنتهاك الأعضاء المجاورة، ووجود انبثاث وما إذا كانت تنتج الهرمونات.[3][4]
التوزيع التشريحي[عدل]
تقليديا، تم تصنيف أورام الغدد العصبية الصماء حسب موقعها التشريحي. يمكن أن تنشأ الشبكات في العديد من مناطق الجسم المختلفة، وغالبًا ما تقع في الأمعاء أو البنكرياس أو الرئتين. توجد أنواع مختلفة من الخلايا التي يمكن أن تؤدي إلى الشبكات في الغدد الصماء، كما يتم توزيعها بشكل منتشر في جميع أنحاء الجسم، وخلايا المعوية الأكثر شيوعًا أو الخلايا المماثلة الشبيهة بالأمعاء المعوية، والتي تكون أكثر شيوعًا نسبيًا في الجهاز الهضمي والرئوي.[6]
تتضمن الشبكات أورامًا معينة في الجهاز الهضمي وخلايا جزيرة البنكرياس،[2] بعض أورام الغدة الصعترية وأورام الرئة، وسرطان النخاع في الخلايا المجاورة للغدة الدرقية. في بعض الأحيان يتم تضمين الأورام التي لها خصائص خلوية مشابهة في الغدة النخامية والغدة الجار درقية والغدة الكظرية[7] أو يتم استبعادها.
ضمن الفئة الواسعة من أورام الغدد العصبية الصماء، هناك العديد من أنواع الأورام المختلفة:[8] يتم تقديم هذا المخطط لتسهيل استرجاع المعلومات. أورام الغدد العصبية الصماء غير شائعة في العديد من هذه المناطق، وكثيراً ما تمثل نسبة صغيرة جدًا من الأورام أو السرطانات في هذه المواقع.
- الغدة النخامية: ورم الغدد العصبية الصماء للغدة النخامية الأمامية
- الغدة الدرقية: أورام الغدة الدرقية العصبية، خاصة سرطان النخاع
- أورام الغدة الدرقية
- أورام الغدة الصعترية وسرطان المنصف[9][10]
- أورام الغدد العصبية الرئوية الصماء[11][12]
- القصبات الهوائية
- الأورام السرطانية: سرطاني نموذجي (درجة منخفضة)؛ سرطاني غير نمطي (درجة متوسطة)
- سرطان الرئة صغير الخلايا
- سرطان الغدد الصم العصبية ذو الخلايا الكبيرة في الرئة[13]
- سرطان الخلايا الصغيرة خارج الرئة
- أورام الغدد الصماء المعدي المعوي البنكرياس.[14][15]
- أورام غدد الجزء الأمامي للقناة الهضمية المعدي المعوي الصماء (يمكن للأورام الأمامية أن تشمل، من الناحية المفاهيمية، ليس فقط شبكات المعدة والأثني عشر القريبة، ولكن أيضًا البنكرياس وحتى الغدة الصعترية والرئة وا[ بحاجة لمصدر ]لقصبات)
- [ بحاجة لمصدر ]أورام غدد البنكرياس الصماء (إذا تم النظر فيها بشكل منفصل عن أورام الجزء الأمامي للقناة الهضمية للغدد الصماء المعدي المعوي البنكرياس[16]
- أورام غدد الجزء الأوسط من القناة الهضمية المعدي المعوي الصماء (من النصف البعيد من الجزء الثاني من العفج إلى الثلثين القريبين من القولون المستعرض)
- الزائدة الدودية،[17] بما في ذلك شبكات متباينة بشكل جيد (حميدة)؛ شبكات متباينة بشكل جيد (إمكانات خبيثة غير مؤكدة)؛ سرطان الغدد العصبية الصماء متباينة بشكل جيد (مع إمكانات خبيثة منخفضة)؛ سرطان الغدد الصماء العصبية المختلطة مختلط (سرطان الخلايا الكأسية، ويسمى أيضًا الخلايا الغدية وسرطانية غدية مخاطية)
- أورام الغدد الصماء المعدي المعوي خلفي[18][19]
- أورام غدد الجزء الأمامي للقناة الهضمية المعدي المعوي الصماء (يمكن للأورام الأمامية أن تشمل، من الناحية المفاهيمية، ليس فقط شبكات المعدة والأثني عشر القريبة، ولكن أيضًا البنكرياس وحتى الغدة الصعترية والرئة وا[ بحاجة لمصدر ]لقصبات)
- الكبد[20][21][22] والمرارة[23]
- أورام الغدة الكظرية، وخاصة أورام الغدة الكظرية
- ورم القواتم
- أورام الجهاز العصبي المحيطي، مثل:
- الثدي[24]
- الجهاز البولي التناسلي
- سرطان خلايا ميركل في الجلد (سرطان التربيق)
- عدة شروط موروثة:[30]
الانطلاق[عدل]
لا يوجد حاليًا نظام مرحلي واحد لجميع أورام الغدد العصبية الصماء. عادة ما يكون للآفات المتمايزة بشكل جيد نظامها التدريجي الخاص بها استنادًا إلى الموقع التشريحي، في حين يتم تقديم الآفات المتمايزة والمختلطة بشكل سيئ كأورام سرطانية في ذلك الموقع. على سبيل المثال، يتم تنظيم سرطان المعدة والغدد الصماء المعدي المختلط كسرطان أساسي للمعدة.[36]
العلامات والأعراض[عدل]
أورام الغدد الصماء المعدي المعوي[عدل]
من الناحية النظرية، هناك نوعان رئيسيان من الشبكة ضمن هذه الفئة: تلك التي تنشأ من الجهاز الهضمي وتلك التي تنشأ من البنكرياس. في الاستخدام، غالبًا ما يتم تطبيق مصطلح «كارسينويد» على كليهما، على الرغم من أنه يتم تطبيقه في بعض الأحيان بشكل مقيد على شبكات من منشأ الجهاز الهضمي (كما هو الحال هنا)، أو كبديل لتلك الأورام التي تفرز هرمونات وظيفية أو عديد الببتيدات المرتبطة بالأعراض السريرية. [ بحاجة لمصدر ]
أورام سرطانية[عدل]
غالبًا ما تؤثر الكارسينويد على الأمعاء الدقيقة، وخاصة الدقاق، وهي أكثر الأورام الخبيثة شيوعًا في الزائدة الدودية. العديد من السرطانات لا تظهر أعراضها ولا يتم اكتشافها إلا بعد الجراحة لأسباب غير ذات صلة. هذه السرطانات المصادفة شائعة؛ وجدت إحدى الدراسات أن شخصًا واحدًا من كل عشرة لديه.[37] لا تسبب العديد من الأورام أعراضًا حتى عندما تكون منتشرة.[38] يمكن للأورام الأخرى حتى لو كانت صغيرة جدًا أن تنتج تأثيرات ضارة عن طريق إفراز الهرمونات.[39]
تفرز 10 في المائة (10٪)[40] أو أقل من السرطانات، بعض سرطانات الأمعاء الدقيقة في المقام الأول، مستويات مفرطة من مجموعة من الهرمونات، وأبرزها السيروتونين (اتش بي_5) أو المادة ص،[41] مما تسبب في مجموعة من الأعراض تسمى متلازمة الكارسينويد:
- تورد
- إسهال
- الربو أو الصفير
- قصور القلب الاحتقاني
- التشنج في البطن
- وذمة محيطية
- خفقان القلب
مراجع[عدل]
- ^ https://www.cancer.gov/types/pancreatic/patient/pnet-treatment-pdq.
{{استشهاد ويب}}:|url=بحاجة لعنوان (مساعدة) والوسيط|title=غير موجود أو فارغ (من ويكي بيانات) (مساعدة) - ^ أ ب "Guidelines for the management of gastroenteropancreatic neuroendocrine (including carcinoid) tumours". Gut. 54. ج. 54 ع. Suppl 4: iv1–iv16. يونيو 2005. DOI:10.1136/gut.2004.053314. PMC:1867801. PMID:15888809. مؤرشف من الأصل في 2008-12-09.
- ^ أ ب Klimstra، D.S.؛ Modlin، I.R.؛ Coppola، D.؛ Lloyd، R.V.؛ Suster، S. (2010). "The Pathologic Classification of Neuroendocrine Tumors". Pancreas. ج. 39 ع. 6: 707–12. DOI:10.1097/MPA.0b013e3181ec124e. PMID:20664470. مؤرشف من الأصل في 2020-05-14.
- ^ أ ب Tan، E.H.؛ Tan، C. (2011). "Imaging of gastroenteropancreatic neuroendocrine tumors". World Journal of Clinical Oncology. ج. 2 ع. 1: 28–43. DOI:10.5306/wjco.v2.i1.28. PMC:3095463. PMID:21603312.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Van Eeden، S.؛ Offerhaus، G.J.A.؛ Hart، A.A.M.؛ Boerrigter، L.؛ Nederlof، P.M.؛ Porter، E.؛ Van Velthuysen، M.L.F. (2007). "Goblet cell carcinoid of the appendix: A specific type of carcinoma". Histopathology. ج. 51 ع. 6: 763–73. DOI:10.1111/j.1365-2559.2007.02883.x. PMID:18042066.
- ^ "Microtubule-associated protein-2: a new sensitive and specific marker for pulmonary carcinoid tumor and small cell carcinoma". Mod. Pathol. ج. 14 ع. 9: 880–85. سبتمبر 2001. DOI:10.1038/modpathol.3880406. PMID:11557784.
- ^ "Imaging of neuroendocrine tumors". Semin Nucl Med. ج. 36 ع. 3: 228–47. يوليو 2006. DOI:10.1053/j.semnuclmed.2006.03.007. PMID:16762613.
- ^ Soga، J. (2003). "Carcinoids and their variant endocrinomas. An analysis of 11842 reported cases". Journal of Experimental & Clinical Cancer Research. ج. 22 ع. 4: 517–30. PMID:15053292.
- ^ Soga، J.؛ Yakuwa، Y.؛ Osaka، M. (1999). "Evaluation of 342 cases of mediastinal/thymic carcinoids collected from literature: A comparative study between typical carcinoids and atypical varieties". Annals of Thoracic and Cardiovascular Surgery. ج. 5 ع. 5: 285–92. PMID:10550713.
- ^ Oberg، K.؛ Jelic، S.؛ Esmo Guidelines Working، G. (2008). "Neuroendocrine bronchial and thymic tumors: ESMO Clinical Recommendation for diagnosis, treatment and follow-up". Annals of Oncology. ج. 19: ii102–ii103. DOI:10.1093/annonc/mdn116. PMID:18456740.
- ^ Beasley، M.؛ Brambilla، E.؛ Travis، W. (2005). "The 2004 World Health Organization classification of lung tumors". Seminars in Roentgenology. ج. 40 ع. 2: 90–97. DOI:10.1053/j.ro.2005.01.001. PMID:15898407.
- ^ Gustafsson، B.I.؛ Kidd، M.؛ Chan، A.؛ Malfertheiner، M.V.؛ Modlin، I.M. (2008). "Bronchopulmonary neuroendocrine tumors". Cancer. ج. 113 ع. 1: 5–21. DOI:10.1002/cncr.23542. PMID:18473355.
- ^ Wick، M.؛ Berg، L.؛ Hertz، M. (1992). "Large cell carcinoma of the lung with neuroendocrine differentiation. A comparison with large cell "undifferentiated" pulmonary tumors". American Journal of Clinical Pathology. ج. 97 ع. 6: 796–805. DOI:10.1093/ajcp/97.6.796. PMID:1317668.
- ^ Massironi، S.؛ Sciola، V.؛ Peracchi، M.؛ Ciafardini، C.؛ Spampatti، M.؛ Conte، D. (2008). "Neuroendocrine tumors of the gastro-entero-pancreatic system". World Journal of Gastroenterology. ج. 14 ع. 35: 5377–84. DOI:10.3748/wjg.14.5377. PMC:2744160. PMID:18803349.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Modlin، I.M.؛ Oberg، K.؛ Chung، D.C.؛ Jensen، R.T.؛ De Herder، W.W.؛ Thakker، R.V.؛ Caplin، M.؛ Delle Fave، G.؛ Kaltsas، G.A. (2008). "Gastroenteropancreatic neuroendocrine tumours". The Lancet Oncology. ج. 9 ع. 1: 61–72. DOI:10.1016/S1470-2045(07)70410-2. PMID:18177818.
- ^ Metz، D.C.؛ Jensen، R.T. (2008). "Gastrointestinal Neuroendocrine Tumors: Pancreatic Endocrine Tumors". Gastroenterology. ج. 135 ع. 5: 1469–92. DOI:10.1053/j.gastro.2008.05.047. PMC:2612755. PMID:18703061.
- ^ Griniatsos، J.؛ Michail، O. (2010). "Appendiceal neuroendocrine tumors: Recent insights and clinical implications". World Journal of Gastrointestinal Oncology. ج. 2 ع. 4: 192–96. DOI:10.4251/wjgo.v2.i4.192. PMC:2999180. PMID:21160597.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Ni، S.؛ Sheng، W.؛ Du، X. (2010). "Pathologic research update of colorectal neuroendocrine tumors". World Journal of Gastroenterology. ج. 16 ع. 14: 1713–19. DOI:10.3748/wjg.v16.i14.1713. PMC:2852818. PMID:20380002.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Konishi، T.؛ Watanabe، T.؛ Nagawa، H.؛ Oya، M.؛ Ueno، M.؛ Kuroyanagi، H.؛ Fujimoto، Y.؛ Akiyoshi، T.؛ Yamaguchi، T. (2010). "Treatment of colorectal carcinoids: A new paradigm". World Journal of Gastrointestinal Surgery. ج. 2 ع. 5: 153–56. DOI:10.4240/wjgs.v2.i5.153. PMC:2999232. PMID:21160865.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Soga، J. (2002). "Primary hepatic endocrinomas (carcinoids and variant neoplasms). A statistical evaluation of 126 reported cases". Journal of Experimental & Clinical Cancer Research. ج. 21 ع. 4: 457–68. PMID:12636090.
- ^ C.، C.؛ M.، N.؛ V.، M. (2004). "Primary hepatic carcinoid tumours". HPB. ج. 6 ع. 1: 13–17. DOI:10.1080/13651820310017228. PMC:2020649. PMID:18333038.
- ^ Moriura، S.؛ Ikeda، S.؛ Hirai، M.؛ Naiki، K.؛ Fujioka، T.؛ Yokochi، K.؛ Gotou، S. (1993). "Hepatic gastronoma". Cancer. ج. 72 ع. 5: 1547–50. DOI:10.1002/1097-0142(19930901)72:5<1547::AID-CNCR2820720510>3.0.CO;2-C. PMID:8348490.
- ^ Soga، J. (2003). "Primary endocrinomas (carcinoids and variant neoplasms) of the gallbladder. A statistical evaluation of 138 reported cases". Journal of Experimental & Clinical Cancer Research. ج. 22 ع. 1: 5–15. PMID:12725316.
- ^ Soga، J.؛ Osaka، M.؛ Yakuwa، Y. (2001). "Gut-endocrinomas (carcinoids and related endocrine variants) of the breast: An analysis of 310 reported cases". International Surgery. ج. 86 ع. 1: 26–32. PMID:11890336.
- ^ Murali، R.؛ Kneale، K.؛ Lalak، N.؛ Delprado، W. (2006). "Carcinoid tumors of the urinary tract and prostate". Archives of Pathology & Laboratory Medicine. ج. 130 ع. 11: 1693–1706. DOI:10.1043/1543-2165(2006)130[1693:CTOTUT]2.0.CO;2 (غير نشط 24 مارس 2020). ISSN:1543-2165. PMID:17076534. مؤرشف من الأصل في 2020-05-14.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: وصلة دوي غير نشطة منذ 2020 (link) - ^ Mikuz، G. (1993). "Non-urothelial tumors of the urinary tract". Verhandlungen der Deutschen Gesellschaft für Pathologie. ج. 77: 180–98. PMID:7511278.
- ^ Soga، J.؛ Osaka، M.؛ Yakuwa، Y. (2001). "Gut-endocrinomas (carcinoids and related endocrine variants) of the uterine cervix: An analysis of 205 reported cases". Journal of Experimental & Clinical Cancer Research. ج. 20 ع. 3: 327–34. PMID:11718210.
- ^ Usmani، S؛ Orevi، M؛ Stefanelli، A؛ Zaniboni، A؛ Gofrit، ON؛ Bnà، C؛ Illuminati، S؛ Lojacono، G؛ Noventa، S (يونيو 2019). "Neuroendocrine differentiation in castration resistant prostate cancer. Nuclear medicine radiopharmaceuticals and imaging techniques: A narrative review". Critical Reviews in Oncology/Hematology. ج. 138: 29–37. DOI:10.1016/j.critrevonc.2019.03.005. PMID:31092382.
- ^ Davies، AH؛ Beltran، H؛ Zoubeidi، A (مايو 2018). "Cellular plasticity and the neuroendocrine phenotype in prostate cancer". Nature Reviews. Urology. ج. 15 ع. 5: 271–86. DOI:10.1038/nrurol.2018.22. PMID:29460922.
- ^ Jensen، R.T.؛ Berna، M.J.؛ Bingham، D.B.؛ Norton، J.A. (2008). "Inherited pancreatic endocrine tumor syndromes: Advances in molecular pathogenesis, diagnosis, management, and controversies". Cancer. ج. 113 ع. 7 Suppl: 1807–43. DOI:10.1002/cncr.23648. PMC:2574000. PMID:18798544.
- ^ Hirsch، N.P.؛ Murphy، A.؛ Radcliffe، J. (2001). "Neurofibromatosis: Clinical presentations and anaesthetic implications". British Journal of Anaesthesia. ج. 86 ع. 4: 555–64. DOI:10.1093/bja/86.4.555. PMID:11573632.
- ^ Lodish، M.B.؛ Stratakis، C.A. (2010). "Endocrine tumours in neurofibromatosis type 1, tuberous sclerosis and related syndromes". Best Practice & Research Clinical Endocrinology & Metabolism. ج. 24 ع. 3: 439–49. DOI:10.1016/j.beem.2010.02.002. PMC:2939061. PMID:20833335.
- ^ Dworakowska، D.؛ Grossman، A.B. (2008). "Are neuroendocrine tumours a feature of tuberous sclerosis? A systematic review". Endocrine-Related Cancer. ج. 16 ع. 1: 45–58. DOI:10.1677/ERC-08-0142. PMID:18978035.
- ^ OMIM - Online Mendelian Inheritance in Man. Carney Complex, type 1; CNC1 (OMIM 160980) omim.org نسخة محفوظة 17 ديسمبر 2019 على موقع واي باك مشين.
- ^ OMIM – Online Mendelian Inheritance in Man. Carney Complex, type 2; CNC2 (OMIM 605244)
- ^ Amin، المحرر (2017). AJCC Cancer Staging Manual (ط. 8). سبرنجر. ص. 351. ISBN:978-3-319-40617-6.
- ^ "Clinical pathology of endocrine tumors of the pancreas. Analysis of autopsy cases". Dig. Dis. Sci. ج. 36 ع. 7: 933–42. يوليو 1991. DOI:10.1007/BF01297144. PMID:2070707. "[In] 800 autopsy cases,... incidence of tumor was 10% (6/60) in individuals having histiological studies of all sections of the pancreas"
- ^ "Chapter 15 Neuroendocrine Gastro-Entero-Pancreatic (GEP) Tumors". Gastrointestinal and Liver Tumors. Berlin: Springer. 2003. ص. 195–233. ISBN:978-3-540-43462-7.
- ^ Pommier R. 2003. The role of surgery and chemoembolization in the management of carcinoid. California Carcinoid Fighters Conference. October 25, carcinoid.org نسخة محفوظة 2015-09-15 على موقع واي باك مشين.
- ^ Health Communities. Carcinoid Tumor Overview. healthcommunities.com نسخة محفوظة 2012-03-03 على موقع واي باك مشين.
- ^ Kvols LK. 2002. Carcinoid Tumors and the Carcinoid Syndrome: What's New in the Therapeutic Pipeline. (The Carcinoid Cancer Foundation: Carcinoid Symposium 2002) carcinoid.org نسخة محفوظة 2015-01-05 على موقع واي باك مشين.
| أورام الغدد العصبية الصماء في المشاريع الشقيقة: | |
| |
