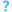فيروس رملي
فيروس رملي | |
|---|---|
فيريون فيروس لاسا
| |
| المرتبة التصنيفية | جنس[1][2] |
| تصنيف الفيروسات | |
| المجموعة: | ((-)ssRNA) V مجموعة
|
| الفصيلة: | فيروسات رملية |
| الجنس: | فيروس رملي |
| الاسم العلمي | |
| Arenavirus[1][2] | |
| تعديل مصدري - تعديل | |
الفيروس الرملي (بالإنجليزية: Arenavirus) هو جنس من الفيروسات من عائلة الفيروسات الرملية، يصيب القوارض، والثعابين، وأحيانا البشر، فهناك على الأقل ثمانية أنواع من الفيروسة الرملية معروفة بأنها تسبب أمراض للإنسان. وتختلف تلك الأمراض في شدتها، حيث يمكن أن ينشأ التهاب السحايا العقيم، وهو مرض بشري حاد يسبب التهابات الدماغ والحبل الشوكي، من عدوى فيروس التهاب السحايا والمشيميات اللمفاوي.
متلازمة الحمى النزفية، بما في ذلك حمى لاسا، مشتقة من عدوى مثل فيروس جواناريتو، أو فيروس جونين، أو فيروس لاسا، أو فيروس لوجو،[7] أو فيروس ماتشوبو، أو فيروس أيرويو المياه البيضاء.[8] وتنقسم الفيروسات الرملية إلى مجموعتين: فيروسات العالم القديم وفيروسات في العالم الجديد، وتبرز الاختلافات بين هذه المجموعات جغرافيا ووراثيا. وبسبب الارتباط الوبائي مع القوارض، يتم تصنيف بعض الفيروسات الرملية على أنها فيروسات تنتقل عن طريق القوارض.
التركيب[عدل]
تحتوي الفيروسات الرملية في المقطع العرضي على جسيمات محببة تكتسب ريبوسومات من خلايا المضيف. وقد اكتسبت تلك الفيروسات اسمها من هذه الخاصية، حيث كلمة arena من أصل لاتيني وتعني الرمل. ولا يعتقد أن هياكل الريبوسوم ضرورية لتكرار الفيروس. كما أن جزيئات الفيروس أو الفيريونات متعددة الأشكال (متغير في الشكل) ولكنها غالبا كروية بقطر يتراوح بين 60 - 300 نانومتر، ومغطاة ببروتينات سكرية سطحية.[9]
يحتوي الفيروس على قشرة بروتينية محببة مع قطعتين من الحمض النووي الريبوزي ذو الشريط الواحد، وتتكون القشرة من نواة من الحمض النووي المغلق في طبقة بروتينية. وعلى الرغم من أنها غالبا ما تصنف على أنها فيروسات ذات اتجاه سالب، إلا أن الفيروسات الرملية لها اتجاه سالب وموجب. وينبع ذلك الخلط من حقيقة أنه في حين أن أجزاء من الجينوم تعتبر ذات اتجاه سالبا، وتشفر جينات في الاتجاه العكسي، فإن أقسامًا أخرى تشفر جينات في الاتجاه المعاكس (الاتجاه إلى الأمام / الموجب). ويُنظَر إلى هذا الهيكل المعقد للتعبير الجيني على أنه نظام تنظيمي بدائي، مما يسمح للفيروس بالتحكم في ما يتم توليفه من البروتينات في أي نقطة من دورة الحياة. وتقتصر دورة حياة الفيروس على السيتوبلازم الخلوي.
التصنيف[عدل]
داخل عائلة الفيروسات الرملية، تم وضع جميع الفيروسات في السابق في جنس الفيروس الرملي، ولكن تم إعادة تصنيفها مؤخرًا (2014) في جنس الماممرينا لتلك التي لديها مضيف من الثدييات، وفي جنس الريبتارينا لتلك التي تصيب الثعابين.[10][11]
يمكن تقسيم الفيروسات الرملية إلى مجموعتين مصليتين، والتي تختلف من الناحية الجينية والتوزيع الجغرافي:[12] عندما يصنف الفيروس من مجموعة «العالم القديم»، هذا يعني أنه تم العثور عليه في نصف الكرة الشرقي في أماكن، مثل أوروبا، وآسيا، وأفريقيا. وعندما يتم العثور عليه في نصف الكرة الغربي في أماكن، مثل الأرجنتين، وبوليفيا، وفنزويلا، والبرازيل، والولايات المتحدة، يتم تصنيفه على أنه من مجموعة «العالم الجديد». وفيروس التهاب السحايا والمشيميات اللمفاوي هو الفيروس الوحيد الذي يوجد في كلا المنطقتين ولكنه يصنف على أنه فيروس العالم القديم.
وتم وصف مجموعة ثالثة من الفيروسات من الثعابين،[13] وتنظيم الجينوم هو نموذجي في الفيروسات الرملية، ولكن البروتينات السكرية لها تشبه تلك الموجودة في الفيروسات الخيطية.
فيروسات ماممارينا[عدل]
العالم القديم[عدل]
- فيروس داندينونج
- فيروس جيرو
- فيروس إيبي
- فيروس كودوكو
- فيروس لاسا
- فيروس لوجو
- فيروس لونا
- فيروس لونك
- فيروس التهاب السحايا والمشيميات اللمفاوي
- فيروس مارينتال
- فيروس ميرينو ووك
- فيروس مينيكري
- فيروس موبالا
- فيروس موروجورو
- فيروس موبيا
- فيروس ونتشو
العالم الجديد[عدل]
مجموعة أ
- فيروس ألبايو
- الفيروس المرن
- فيروس بارانا
- فيروس بيشيندي
- فيروس بيرتال
مجموعة ب
- فيروس أماباري
- فيروس كيوبكسي
- جواناريتو
- فيروس جونين
- فيروس ماتشوبو
- فيروس تكاريبي
- فيروس سابي
مجموعة ج
- فيروس لاتيني
- فيروس اوليفروس
مجموعة د
- فيروس أرويو
- فيروس الدب كانيون
- فيروس تامي
- فيروس أرويو المياه البيضاء
أخرى
- فيروس شباري
- فيروس ماتشوبو
- فيروس باتاوي
- فيروس زابوري
فيروسات ريبتارينا[عدل]
- فيروس أكاديمية كاليفورنيا للعلوم
- فيروس البوابة الذهبية
- فيروس جامعة هلسنكي
الجينوم[عدل]
تحتوي الفيروسات الرملية على جينوم مجزأ من الحمض النووي الريبوزي الذي يتكون من اثنين من الحمض النووي الريبوزي أحادي الشريط.[14] وكما هو الحال مع جميع الفيروسات ذات الحمض النووي الريبوزي ذات الاتجاه السلبي، فإن جينوم الحمض النووي الريبوزي وحده ليس معديا، ولا بد من استخدام آلية النسخ الفيروسي للشروع في العدوى داخل الخلية المضيفة،[15] لذا يجب نسخ جينوم الحمض النووي الريبوزي المعنى المعبأ داخل الفيروس الرملي أولاً إلى حمض نووي ريبوزي رسول موجب الاتجاه من أجل إنتاج بروتين فيروسي.[16] ويشار إلى قطعتي الحمض النووي الريبوزي الصغيرة (S) والكبيرة (L)،[14][17] وهما يشفران أربعة بروتينات فيروسية في إستراتيجية تشفير فريدة من نوعها،[18][19] حيث تشفر كل قطعة اثنين من البروتينات الفيروسية في اتجاه معاكس بحيث يعمل جينوم الحمض النووي الريبوزي ذو الاتجاه السلبي كقالب لنسخ حمض نووي ريبوزي رسول واحد، والنسخة الموجبة من جينوم الحمض النووي الريبوزي تقوم بنسخ حمض نووي ريبوزي رسول ثاني.[16] وتنقسم متواليات التشفير المنفصلة للبروتينين الفيروسيين بواسطة تسلسل من الحمض النووي الذي يُطوى إلى هيكل مستقر.[20]
وتحتوي نهاية لكل جزء من الحمض النووي على تسلسل 19 نوكليوتيد محمي بشكل كبير، وهو أمر حاسم لتوظيف آلات النسخ الفيروسي والبدء بنسخ الحمض النووي الرسول الفيروسي والتكرار الجيني.[21][22][23][24][25] كما أن متواليات النهاية 5 'و 3' المحفوظة مكملة وتسمح لكل جزء من الحمض النووي الريبوزي بتبني بنية مجدولة ذات الشريط المضاعف[26] والتي تحافظ على النهايات في قربها وينتج عنها مظهر دائري للقوالب الجينومية للفيروسات الرملية التي تظهر بالمجهر الإلكتروني.[27][28] إن هيكل الحمض النووي الريبوزي المزدوج المجدول يمثل أهمية حاسمة لتخليق الحمض النووي الفيروسي الفعال،[24][29] ولكن تفاعلات الحمض النووي المزدوج المتقطعة المحتملة يجب أن تكون عابرة من أجل توظيف البوليميراز الفيروسي.[25]
يبلغ طول القطعة الصغيرة (S) من الحمض النووي الريبوزي 3.5 كيلوبايت تقريبًا، وتشفر البروتين النووي الفيروسي والبروتين السكري،[30] بينما يبلغ طول قطعة الحمض النووي الريبوزي الطويلة (L) حوالي 7.2 كيلوبايت، وتشفر بوليمراز الحمض النووي الريبوزي المعتمد على الحمض النووي الريبي الفيروسي وبروتين (Z) صغير يحتوي على مجال RING.[31][32][33]
يشكل بروتين Z مركبات قليلة الوحدات متماثلة ومكوِّنًا هيكليًا للفيريونات.[34] وتشكيل هذه المركبات هو خطوة أساسية لتجميع الجسيمات والتبرعم، حيث يلزم الارتباط بين البروتين Z ومركب البروتين السكري المغلف الفيروسي ليكون الفريون معدي. ويبدو أن نشاط البوليميريز مشكَّل من خلال الارتباط بين البروتينين L وZ، ويعتبر التفاعل بين بروتين Z والبروتين النووي أمرًا ضروريًا لتغليف الجينوم.
التطور[عدل]
لقد تم دراسة تطور جنس الماممارينا.[35] وقد تشعبت فصائل العالم الجديد والعالم القديم منذ أقل من 45,000 عام، حيث تطورت أنواع العالم الجديد بين 41,400 و3,300 سنة في منطقة أمريكا اللاتينية والكاريبي، وتطورت أنواع العالم القديم بين 23,100 و1880 عامًا، على الأرجح في الجنوب الأفريقي.
البيولوجيا الجزيئية[عدل]
يتم تصنيع البروتين السكري كجزيء بدائي،[36] وهو ومنقسم إلى ثلاثة أجزاء: بروتين سكري 1 وبروتين سكري 2 وببتيد ثابت الإشارة، حيث يتم تحفيز هذه التفاعلات عن طريق بيبتيداز الإشارة الخلوية والإنزيم الخلوي Subtilisin Kexin Isozyme-1/Site-1 Protease. وهذه العمليات ضرورية لكفاءة الاندماج وإدماج البروتين السكري الناضج في جسيمات الفيرون الناشيء الوليد.
المكمن أو المستودع[عدل]
بعض الفيروسات الرملية هي ممرضات حيوانية المنشأ، وترتبط بشكل عام بالأمراض المنقولة عن طريق القوارض لدى البشر. ويرتبط كل فيروس عادة بنوع معين من أنواع مضيفات القوارض، وتستمر الفيروسات الرملية في الطبيعة عن طريق إصابة القوارض أولاً ثم تنتقل إلى البشر. ويمكن أن يصاب البشر من خلال تعرض المخاط للرذاذ أو عن طريق الاتصال المباشر للجلد المجروح مع المواد المعدية المشتقة من القوارض المصابة.[9] وينتج الرذاذ من إفرازات القوارض الجافة، وخاصة البول. وتكون معظم الفيروسات الرملية التي تصيب الإنسان مصدرها تلك القوارض التي تتخذ من بيوتهم مأوى. ويمكن أن يوجد الفيروس في المصانع، أو بالأغذية الملوثة، أو في مناطق العمل الزراعي. ويرتبط خطر إصابة الإنسان بالفيروس الرملي بالعمر أو العِرق أو الجنس من خلال درجة التلامس مع إفرازات القوارض الجافة.
وبائيات[عدل]
المضيف[عدل]
| الفيروس | المرض | المضيف | التوزيع الجغرافي |
|---|---|---|---|
| فيروس التهاب السحايا والمشميات اللمفاوي | التهاب السحايا والمشيميات اللمفاوي | فأر المنازل | جميع أنحاء العالم |
| فيروس لاسا | حمى لاسا | فأر متعدد الأثداء | غرب إفريقيا |
| فيروس جونين | حمى الأرجنتين النزفية | فأر الأراضي الجافة | الأرجنتين |
| فيروس ماتشوبو | الحمى البوليفية النزفية | الفأر الكبير | بوليفيا |
| فيروس جواناريتو | حمى فنزويلا النزفية | فأر السكر قصير الذيل | فنزويلا |
| فيروس سابي | الحمى النزفية البرازيلية | غير معروف | البرازيل |
| فيروس تاكاريب | الخفاش | ترينيداد | |
| الفيروس المرن | مرض شبيه بالإنفلونزا | جرذ الأرز | البرازيل |
| فيروس أرويو المياه البيضاء | حمى نزفية | جرذ الخشب | جنوب غرب الولايات المتحدة |
أمراض سريرية[عدل]
- تتسبب فيروسات التهاب السحايا والمشيميات اللمفاوي في مرض الحمى الشبيه بالأنفلونزا، ولكنها قد تسبب في بعض الأحيان التهاب السحايا مصحوبة بشكل مميز بأعداد كبيرة من الخلايا اللمفاوية في السائل الدماغي النخاعي.
- يسبب فيروس لاسا حمى لاسا، وتلك الحمى متوطنة في غرب أفريقيا. وتم عزل الفيروس لأول مرة من قِبل الأمريكيين المتمركزين في قرية لاسا بنيجيريا، ويمكن انتقال الفيروس من شخص إلى شخص.
- الأمراض دون الإكلينيكية: تشير الدراسات السيرولوجية إلى أن الإصابات غير الظاهرة خاصة بين أفراد قبائل الصيد شائعة.
- الالتهابات السريرية: تتميز حمى لاسا بالحمى المرتفعة، وألم عضلي شديد، واعتلال تجلط الدم، وطفح جلدي نزفي، ونزيف حشوي في بعض الأحيان بالإضافة إلى نخر في الكبد والطحال.
- تسبب فيروسات أخرى، مثل فيروس جونين، فيروس ماتشوبو الحمى النزفية.
وتشكل كل هذه الأمراض تهديدا كبيرا للصحة العامة في المناطق التي تحدث فيها. على سبيل المثال، عندما يتحول فيروس العالم القديم لاسا إلى حمى لاسا، يؤدي هذا عادةً إلى حدوث قدر كبير من الوفيات. وبالمثل فإن فيروس جونين العالم الجديد يسبب الحمى النزفية الأرجنتينية. هذه الحمى هي عدة أمراض ذات مظاهر نزفية وعصبية وتصل حالات الوفاة من خمسة عشر إلى ثلاثين في المئة.[9] والطريقة التي ينتشر بها هذا الفيروس هي زيادة السفر من وإلى المناطق الموبوءة، حيث أدى هذا السفر إلى استيراد حمى لاسا إلى المناطق الحضرية غير المتوطنة في جميع أنحاء العالم.
التفشيات الأخيرة[عدل]
قد تم ربط نوع جديد من الفيروسات الرملية يدعى فيروس لوجو بخمسة مرضى أظهروا أعراض الحمى النزفية الفيروسية في جنوب أفريقيا.[37] وقد نشأ المرض بالقرب من لوساكا وزامبيا وانتشر إلى جوهانسبرغ بجنوب أفريقيا، بعد نقل المريض الأول إلى المستشفى هناك. وقدمت نتائج اختبارات التسلسل الجيني التي أجراها علماء الأوبئة في جامعة كولومبيا في مدينة نيويورك بالولايات المتحدة الأمريكية، وفي فرع الممرضات الخاص لمراكز مكافحة الأمراض في أتلانتا بالولايات المتحدة الأمريكية، دليلاً على أن العامل المسبب للمرض هو فيروس من أسرة الفيروسات الرملية، والتي أدت في نهاية المطاف إلى وفاة أربعة من المصابين الخمسة في زامبيا وجنوب أفريقيا خلال تفشي المرض الذي بدأ في سبتمبر 2008.
كما أشار أرينافيروس مؤخرا إلى سبب وفاة ثلاثة متلقين من المتبرعين في أستراليا الذين أصيبوا بالفيروس بعد تلقيهم تبرعات من الكلى والكبد من أحد المتبرعين بالأعضاء المصابة في أواخر عام 2006. وتوفي الثلاثة في الأسبوع الأول من عام 2007.[38]
وتواصل منظمة الصحة العالمية وشركاؤها من المنظمة العالمية للإنذار بحدوث الوباءات ومواجهتها دعم وزارتي الصحة في البلدين في مختلف أوجه التحقيق في الوباء، بما في ذلك التشخيص المختبري، والتحقيقات، وإيجاد الحالات النشطة ومتابعة الأشخاص المتواصلين مع المريض.[39]
العلاجات[عدل]
يمكن أن يكون هذا الفيروس مدمرًا جدًا ولكن هناك طرق علاج قليلة جدًا متاحة. إن الافتقار الحالي إلى لقاح مرخص وخيارات علاجية محدودة للفيروس الرملي تجعله من أكثر الفيروسات إهمالاً التي يمكن معالجتها، والدواء الوحيد المرخص لعلاج عدوى الفيروس هو ريبافيرين النوكليوسيد التماثلي،[40] حيث يقلل ريبافيرين من المراضة والوفيات لدى البشر الذين لديهم فيروسات رملية معينة، إذا تم أخذه في المراحل المبكرة من المرض. ويُظهر ريبافيرين نجاحًا متباينًا في علاج مرض الفيروس الرملي الوخيم ويرتبط بسمية كبيرة.[41] ويجب إنتاج الأدوية الفعالة المضادة للفيروسات بتكلفة منخفضة، تؤخذ عن طريق الفم، وقادرة على تحمل المناخات الاستوائية بسبب المناطق التي تحدث فيها هذه العدوى؛ لهذا السبب، يمكن أن يكون الفحص عالي الإنتاجية للمجموعات الجزيئية الصغيرة هو الحل لإيجاد علاج أفضل، حيث يجمع الفحص عالي الإنتاجية مجموعات من جزيئات اصطناعية صغيرة يمكن استخدامها لتحديد الجزيئات التي تحفز أو تثبط بروتينات التفاعل،[40] وكذلك يمكن اكتشاف أدوية مضادة للفيروسات المسببة للأمراض البشرية الجديدة المحتملة.
روابط خارجية[عدل]
- Viralzone: Arenavirus
- Detailed genomic and bioinformatic information about Arenaviridae at NIH-funded database.
- Arenaviridae Genomes database search results from the Viral Bioinformatics Resource Center.
- Google.Org blog info on recent outbreak.
- Virus Pathogen Database and Analysis Resource (ViPR): Arenaviridae
- Arenaviruses
- "Arenavirus". NCBI Taxonomy Browser. 11618. مؤرشف من الأصل في 2020-04-14.
المراجع[عدل]
- ^ أ ب ت International Committee on Taxonomy of Viruses, ed. (30 Jun 2014), ICTV Master Species List 2013 v2 (بالإنجليزية), QID:Q18810383
- ^ أ ب ت ICTV Master Species List 1971 (بالإنجليزية), 1971, QID:Q69584206
- ^ ICTV Master Species List 2005 (بالإنجليزية), 2005, QID:Q69579583
- ^ ICTV Master Species List 2009 (بالإنجليزية), 2009, QID:Q69578243
- ^ ICTV Master Species List 2011 (بالإنجليزية), 2011, QID:Q69577927
- ^ ICTV Master Species List 2012 (بالإنجليزية), 2013, QID:Q69577800
- ^ Briese T، Paweska JT، McMullan LK، وآخرون (مايو 2009). "Genetic detection and characterization of Lujo virus, a new hemorrhagic fever-associated arenavirus from southern Africa". PLoS Pathog. ج. 5 ع. 5: e1000455. DOI:10.1371/journal.ppat.1000455. PMC:2680969. PMID:19478873.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Botten، J؛ Whitton، JL؛ Barrowman، P؛ Sidney، J؛ Whitmire، JK؛ Alexander، J؛ Kotturi، MF؛ Sette، A؛ Buchmeier، MJ (2010). "A Multivalent Vaccination Strategy for the Prevention of Old World Arenavirus Infection in Humans". Journal of Virology. ج. 84 ع. 19: 9947–56. DOI:10.1128/JVI.00672-10. PMC:2937778. PMID:20668086. مؤرشف من الأصل في 2011-08-21. اطلع عليه بتاريخ 2011-04-28.
- ^ أ ب ت Emonet، Sebastien E.؛ Urata، Shuzo؛ De La Torre، Juan C. (2011). "Arenavirus reverse genetics: New approaches for the investigation of arenavirus biology and development of antiviral strategies". Virology. ج. 411 ع. 2: 416–425. DOI:10.1016/j.virol.2011.01.013. PMC:3057228. PMID:21324503.
- ^ ICTV proposals 2014.011a-dV et al., Mark D. Stenglein et al. نسخة محفوظة 04 مارس 2016 على موقع واي باك مشين. [وصلة مكسورة]
- ^ ICTV proposals 2014.012aV et al., Michael J. Buchmeier et al. نسخة محفوظة 04 مارس 2016 على موقع واي باك مشين. [وصلة مكسورة]
- ^ Delgado S، Erickson BR، Agudo R، وآخرون (أبريل 2008). "Chapare virus, a newly discovered arenavirus isolated from a fatal hemorrhagic fever case in Bolivia". PLoS Pathog. ج. 4 ع. 4: e1000047. DOI:10.1371/journal.ppat.1000047. PMC:2277458. PMID:18421377.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Stenglein MD، Sanders C، Kistler AL، وآخرون (2012). "Identification, characterization, and in vitro culture of highly divergent arenaviruses from boa constrictors and annulated tree boas: candidate etiological agents for snake inclusion body disease". MBio. ج. 3 ع. 4: e00180–12. DOI:10.1128/mBio.00180-12. PMC:3419519. PMID:22893382. مؤرشف من الأصل في 2020-02-23.
- ^ أ ب Añón MC، Grau O، Segovia ZM، Franzefernández MT (يونيو 1976). "RNA composition of Junin virus". J. Virol. ج. 18 ع. 3: 833–8. PMC:354781. PMID:178925.
- ^ Lee KJ، Novella IS، Teng MN، Oldstone MB، de La Torre JC (أبريل 2000). "NP and L proteins of lymphocytic choriomeningitis virus (LCMV) are sufficient for efficient transcription and replication of LCMV genomic RNA analogs". J. Virol. ج. 74 ع. 8: 3470–7. DOI:10.1128/jvi.74.8.3470-3477.2000. PMC:111854. PMID:10729120.
- ^ أ ب Meyer BJ، de la Torre JC، Southern PJ (2002). "Arenaviruses: genomic RNAs, transcription, and replication". Curr. Top. Microbiol. Immunol. ج. 262: 139–57. PMID:11987804.
- ^ Pedersen IR (مارس 1973). "Different classes of ribonucleic acid isolated from lymphocytic choriomeningitis virus". J. Virol. ج. 11 ع. 3: 416–23. PMC:355116. PMID:4734917.
- ^ Auperin DD، Romanowski V، Galinski M، Bishop DH (ديسمبر 1984). "Sequencing studies of pichinde arenavirus S RNA indicate a novel coding strategy, an ambisense viral S RNA". J. Virol. ج. 52 ع. 3: 897–904. PMC:254611. PMID:6492264.
- ^ Auperin DD، McCormick JB (فبراير 1989). "Nucleotide sequence of the Lassa virus (Josiah strain) S genome RNA and amino acid sequence comparison of the N and GPC proteins to other arenaviruses". Virology. ج. 168 ع. 2: 421–5. DOI:10.1016/0042-6822(89)90287-0. PMID:2916333.
- ^ Auperin DD، Galinski M، Bishop DH (أبريل 1984). "The sequences of the N protein gene and intergenic region of the S RNA of pichinde arenavirus". Virology. ج. 134 ع. 1: 208–19. DOI:10.1016/0042-6822(84)90286-1. PMID:6324469.
- ^ Auperin D، Dimock K، Cash P، Rawls WE، Leung WC، Bishop DH (يناير 1982). "Analyses of the genomes of prototype pichinde arenavirus and a virulent derivative of Pichinde Munchique: evidence for sequence conservation at the 3' termini of their viral RNA species". Virology. ج. 116 ع. 1: 363–7. DOI:10.1016/0042-6822(82)90429-9. PMID:6278715.
- ^ Auperin DD، Compans RW، Bishop DH (أغسطس 1982). "Nucleotide sequence conservation at the 3' termini of the virion RNA species of New World and Old World arenaviruses". Virology. ج. 121 ع. 1: 200–3. DOI:10.1016/0042-6822(82)90130-1. PMID:6287720.
- ^ Mattsson L (1989). "Chronic non-A, non-B hepatitis with special reference to the transfusion-associated form". Scand J Infect Dis Suppl. ج. 59: 1–55. PMID:2502835.
- ^ أ ب Hass M، Westerkofsky M، Müller S، Becker-Ziaja B، Busch C، Günther S (ديسمبر 2006). "Mutational analysis of the lassa virus promoter". J. Virol. ج. 80 ع. 24: 12414–9. DOI:10.1128/JVI.01374-06. PMC:1676312. PMID:17005649.
- ^ أ ب Kranzusch PJ، Schenk AD، Rahmeh AA، وآخرون (نوفمبر 2010). "Assembly of a functional Machupo virus polymerase complex". Proc. Natl. Acad. Sci. U.S.A. ج. 107 ع. 46: 20069–74. DOI:10.1073/pnas.1007152107. PMC:2993349. PMID:20978208.
- ^ Bishop DH، Auperin DD (1987). "Arenavirus gene structure and organization". Curr. Top. Microbiol. Immunol. ج. 133: 5–17. PMID:2435460.
- ^ Young PR، Howard CR (أبريل 1983). "Fine structure analysis of Pichinde virus nucleocapsids". J. Gen. Virol. ج. 64 ع. 4: 833–42. DOI:10.1099/0022-1317-64-4-833. PMID:6682139.
- ^ Palmer EL، Obijeski JF، Webb PA، Johnson KM (سبتمبر 1977). "The circular, segmented nucleocapsid of an arenavirus-Tacaribe virus". J. Gen. Virol. ج. 36 ع. 3: 541–5. DOI:10.1099/0022-1317-36-3-541. PMID:199698.
- ^ Perez M، de la Torre JC (يناير 2003). "Characterization of the genomic promoter of the prototypic arenavirus lymphocytic choriomeningitis virus". J. Virol. ج. 77 ع. 2: 1184–94. DOI:10.1128/jvi.77.2.1184-1194.2003. PMC:140842. PMID:12502835.
- ^ Ghiringhelli PD، Rivera-Pomar RV، Lozano ME، Grau O، Romanowski V (سبتمبر 1991). "Molecular organization of Junin virus S RNA: complete nucleotide sequence, relationship with other members of the Arenaviridae and unusual secondary structures". J. Gen. Virol. ج. 72 ع. 9: 2129–41. DOI:10.1099/0022-1317-72-9-2129. PMID:1654373.
- ^ Iapalucci S، López N، Rey O، Zakin MM، Cohen GN، Franze-Fernández MT (نوفمبر 1989). "The 5' region of Tacaribe virus L RNA encodes a protein with a potential metal binding domain". Virology. ج. 173 ع. 1: 357–61. DOI:10.1016/0042-6822(89)90257-2. PMID:2510403.
- ^ Iapalucci S، Lopez R، Rey O، وآخرون (مايو 1989). "Tacaribe virus L gene encodes a protein of 2210 amino acid residues". Virology. ج. 170 ع. 1: 40–7. DOI:10.1016/0042-6822(89)90349-8. PMID:2718387.
- ^ Salvato MS، Shimomaye EM (نوفمبر 1989). "The completed sequence of lymphocytic choriomeningitis virus reveals a unique RNA structure and a gene for a zinc finger protein". Virology. ج. 173 ع. 1: 1–10. DOI:10.1016/0042-6822(89)90216-X. PMID:2510401.
- ^ Loureiro ME، D'Antuono A، Levingston Macleod JM، López N (سبتمبر 2012). "Uncovering viral protein-protein interactions and their role in arenavirus life cycle". Viruses. ج. 4 ع. 9: 1651–67. DOI:10.3390/v4091651. PMC:3499824. PMID:23170177. مؤرشف من الأصل في 2018-12-26.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Forni D, Pontremoli C, Pozzoli U, Clerici M, Cagliani R, Sironi M (2018) Ancient evolution of Mammarenaviruses: Adaptation via changes in the L Protein and no evidence for host-virus codivergence. Genome Biol Evol 10(3):863-874. doi: 10.1093/gbe/evy050.
- ^ Burri DJ، da Palma JR، Kunz S، Pasquato A (أكتوبر 2012). "Envelope glycoprotein of arenaviruses". Viruses. ج. 4 ع. 10: 2162–81. DOI:10.3390/v4102162. PMC:3497046. PMID:23202458. مؤرشف من الأصل في 2018-12-26.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Scientists identify new lethal virus in Africa نسخة محفوظة 11 يونيو 2009 على موقع واي باك مشين. [وصلة مكسورة]
- ^ "Virus identified - nurse ill". News24.com. مؤرشف من الأصل في 2008-10-13. اطلع عليه بتاريخ 2008-10-13.
- ^ "Virus kills organ recipients". www.theage.com.au. مؤرشف من الأصل في 2012-11-07. اطلع عليه بتاريخ 2009-10-16.
- ^ أ ب Lee، A. M.؛ Pasquato، A.؛ Kunz، S. (2011). "Novel approaches in anti-arenaviral drug development". Virology. ج. 411 ع. 2: 163–169. DOI:10.1016/j.virol.2010.11.022. PMC:3057354. PMID:21183197.
- ^ Mendenhall، M.؛ Russell، A.؛ Juelich، T.؛ Messina، E. L.؛ Smee، D. F.؛ Freiberg، A. N.؛ Holbrook، M. R.؛ Furuta، Y.؛ وآخرون (2010). "T-705 (Favipiravir) Inhibition of Arenavirus Replication in Cell Culture". Antimicrobial Agents and Chemotherapy. ج. 55 ع. 2: 782–787. DOI:10.1128/AAC.01219-10. PMC:3028760. PMID:21115797.
| Arenavirus في المشاريع الشقيقة: | |
| |