تصبن: الفرق بين النسختين
| [نسخة منشورة] | [نسخة منشورة] |
ط بوت:إصلاح رابط (1) |
Mr.Ibrahembot (نقاش | مساهمات) ط بوت:إضافة قوالب تصفح (1) |
||
| سطر 1: | سطر 1: | ||
[[ملف:Saponificación.svg|تصغير|300 بك| تصبن [[الدهنيات]] بوجود [[هيدروكسيد البوتاسيوم]].]] |
[[ملف:Saponificación.svg|تصغير|300 بك| تصبن [[الدهنيات]] بوجود [[هيدروكسيد البوتاسيوم]].]] |
||
'''التصبن''' هي عملية [[تحلل مائي|حلمهة]] لل[[إستر]] في وسط [[قلوي]]، لتشكيل [[كحول|الكحول]] و[[ملح الطعام|ملح]] يحتوي على [[مجموعة كربوكسيل|مجموعة الكربوكسيل]].<ref>{{استشهاد ويب|مسار=https://www.bbc.co.uk/bitesize/410.shtml|ناشر=BBC |عمل=GCSE Bitesize|عنوان= Double bonds and hydrogenation| مسار أرشيف = https://web.archive.org/web/20171115054056/http://www.bbc.co.uk/schools/gcsebitesize/science/aqa/plantoilsanduses/vegoilsrev4.shtml | تاريخ أرشيف = 15 نوفمبر 2017 | وصلة مكسورة = yes }}</ref><ref>{{استشهاد بكتاب|doi=10.1002/14356007.a15_423| |
'''التصبن''' هي عملية [[تحلل مائي|حلمهة]] لل[[إستر]] في وسط [[قلوي]]، لتشكيل [[كحول|الكحول]] و[[ملح الطعام|ملح]] يحتوي على [[مجموعة كربوكسيل|مجموعة الكربوكسيل]].<ref>{{استشهاد ويب|مسار=https://www.bbc.co.uk/bitesize/410.shtml|ناشر=BBC |عمل=GCSE Bitesize|عنوان= Double bonds and hydrogenation| مسار أرشيف = https://web.archive.org/web/20171115054056/http://www.bbc.co.uk/schools/gcsebitesize/science/aqa/plantoilsanduses/vegoilsrev4.shtml | تاريخ أرشيف = 15 نوفمبر 2017 | وصلة مكسورة = yes }}</ref><ref>{{استشهاد بكتاب|doi=10.1002/14356007.a15_423|الفصل=Lubricants and Lubrication|عنوان=Ullmann's Encyclopedia of Industrial Chemistry|سنة=2003|الأخير1=Bartels|الأول1=Thorsten|الأخير2=Bock|الأول2=Wolfgang|الأخير3=Braun|الأول3=Jürgen|الأخير4=Busch|الأول4=Christian|الأخير5=Buss|الأول5=Wolfgang|last6=Dresel|first6=Wilfried|last7=Freiler|first7=Carmen|last8=Harperscheid|first8=Manfred|last9=Heckler|first9=Rolf-Peter|last10=Hörner|first10=Dietrich|last11=Kubicki|first11=Franz|last12=Lingg|first12=Georg|last13=Losch|first13=Achim|last14=Luther|first14=Rolf|last15=Mang|first15=Theo|last16=Noll|first16=Siegfried|last17=Omeis|first17=Jürgen|isbn=3-527-30673-0|ناشر= Wiley-VCH|مكان= Weinheim}}</ref><ref>{{استشهاد بكتاب|doi=10.1002/14356007.a24_247|الفصل=Soaps|عنوان=Ullmann's Encyclopedia of Industrial Chemistry|سنة=2000|الأخير1=Schumann|الأول1=Klaus|الأخير2=Siekmann|الأول2=Kurt|isbn=3-527-30673-0|ناشر= Wiley-VCH|مكان= Weinheim}}</ref> يستخدم التصبن بشكل شائع للإشارة إلى تفاعل مادة قلوية معدنية مع ال[[دهن|دهون]] أو [[زيت|الزيت]] لتشكل [[صابون|الصابون]]. والمواد القابلة للتصبن هي المواد التي يمكن تحويلها إلى [[صابون|الصابون]]. |
||
:CH<sub>2</sub>-OOC-R - CH-OOC-R - CH<sub>2</sub>-OOC-R (دهن) + 3 [[هيدروكسيد الصوديوم|NaOH]] (أو [[هيدروكسيد البوتاسيوم|KOH]]) |
:CH<sub>2</sub>-OOC-R - CH-OOC-R - CH<sub>2</sub>-OOC-R (دهن) + 3 [[هيدروكسيد الصوديوم|NaOH]] (أو [[هيدروكسيد البوتاسيوم|KOH]]) |
||
| سطر 17: | سطر 17: | ||
إن [[حريق|الحرائق]] الناتجة عن [[زيت|الزيوت]] أو ال[[دهن|دهون]] المستخدمة في الطعام(تصنف على أنها صنف ك)، تحترق بشكل أعلى سخونة من غيرها من السوائل [[اشتعالية|القابلة للاشتعال]]، جاعلة [[جهاز إطفاء الحريق|أجهزة إطفاء الحريق]] المستخدمة مع الصنف B غير فاعلة. مثل هذه [[حريق|الحرائق]] ينبغي أن تطفئ باستخدام مطافئ بمواد كيميائية رطبة (''wet chemical extinguisher''). يعتمد مبدأ إطفاء هذه المواد على تصبنها. يحول وسيط الإطفاء المادة المحترقة بسرعة إلى [[صابون]] غير قابل للاحتراق. هذه العملية [[تفاعل ماص للحرارة|ماصة للحرارة]]، مما يعني أنها تمتص الطاقة (في هذه الحالة، [[طاقة حرارية|الطاقة الحرارية]]) من المناطق المحيطة بها، والحد من درجة الحرارة والقضاء على [[حريق|الحريق]]. |
إن [[حريق|الحرائق]] الناتجة عن [[زيت|الزيوت]] أو ال[[دهن|دهون]] المستخدمة في الطعام(تصنف على أنها صنف ك)، تحترق بشكل أعلى سخونة من غيرها من السوائل [[اشتعالية|القابلة للاشتعال]]، جاعلة [[جهاز إطفاء الحريق|أجهزة إطفاء الحريق]] المستخدمة مع الصنف B غير فاعلة. مثل هذه [[حريق|الحرائق]] ينبغي أن تطفئ باستخدام مطافئ بمواد كيميائية رطبة (''wet chemical extinguisher''). يعتمد مبدأ إطفاء هذه المواد على تصبنها. يحول وسيط الإطفاء المادة المحترقة بسرعة إلى [[صابون]] غير قابل للاحتراق. هذه العملية [[تفاعل ماص للحرارة|ماصة للحرارة]]، مما يعني أنها تمتص الطاقة (في هذه الحالة، [[طاقة حرارية|الطاقة الحرارية]]) من المناطق المحيطة بها، والحد من درجة الحرارة والقضاء على [[حريق|الحريق]]. |
||
==انظر أيضًا== |
== انظر أيضًا == |
||
* [[صابون]] |
* [[صابون]] |
||
* [[قيمة تصبن]] |
* [[قيمة تصبن]] |
||
| سطر 34: | سطر 34: | ||
* [http://www.gutenberg.org/etext/21724 The Handbook of Soap Manufacture] - A book from 1908. |
* [http://www.gutenberg.org/etext/21724 The Handbook of Soap Manufacture] - A book from 1908. |
||
* التصبن [http://www.syrianclinic.com/vb/threads/1676-التصبن-Saponification العيادة السورية] |
* التصبن [http://www.syrianclinic.com/vb/threads/1676-التصبن-Saponification العيادة السورية] |
||
{{زيت النخيل}} |
|||
{{شريط بوابات|الكيمياء}} |
{{شريط بوابات|الكيمياء}} |
||
{{روابط شقيقة|commons=Saponification}} |
{{روابط شقيقة|commons=Saponification}} |
||
[[تصنيف:تفاعلات استبدال]] |
[[تصنيف:تفاعلات استبدال]] |
||
[[تصنيف:صابون]] |
[[تصنيف:صابون]] |
||
نسخة 17:23، 17 سبتمبر 2020
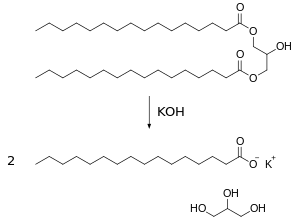
التصبن هي عملية حلمهة للإستر في وسط قلوي، لتشكيل الكحول وملح يحتوي على مجموعة الكربوكسيل.[1][2][3] يستخدم التصبن بشكل شائع للإشارة إلى تفاعل مادة قلوية معدنية مع الدهون أو الزيت لتشكل الصابون. والمواد القابلة للتصبن هي المواد التي يمكن تحويلها إلى الصابون.
يتم تسخين المادتين:
- CH2-OH -CH-OH - CH2-OH (جليسرول) + 3 R-CO2-Na (صابون)
- حيث R=(CH2)14CH3 في المثال (يمين)
هيدروكسيد الصوديوم (NaOH) هي مادة قلوية كاوية. وإذا استخدم هيدروكسيد الصوديوم يتشكل عندنا صابون قاسي، في حين استخدام هيدروكسيد البوتاسيوم (KOH) يعطي الصابون السائل. الزيوت النباتية والدهون الحيوانية هي استرات دهنية في شكل ثلاثي الغليسريد. تقوم المادة القلوية بتحطيم رابطة الإستر وتطلق حمض دهني وجليسرول. إذا لزم الأمر، يمكن ترسيب الصابون بمعالجته بالملح (كلوريد الصوديوم المشبع).
الجثث
التصبن يمكن أن يشير أيضًا إلى الأنسجة اللينة حيث تتحول الدهون في الجثة إلى شحم شمعي، وغالبًا ما يسمى شمع القبر. وهذه العملية أكثر شيوعًا عندما تكون كمية الأنسجة الدهنية عالية، مع غياب عوامل التحلل أو وجودها بكمية صغيرة، وأرض المدفن قلوية.
أجهزة إطفاء الحريق
إن الحرائق الناتجة عن الزيوت أو الدهون المستخدمة في الطعام(تصنف على أنها صنف ك)، تحترق بشكل أعلى سخونة من غيرها من السوائل القابلة للاشتعال، جاعلة أجهزة إطفاء الحريق المستخدمة مع الصنف B غير فاعلة. مثل هذه الحرائق ينبغي أن تطفئ باستخدام مطافئ بمواد كيميائية رطبة (wet chemical extinguisher). يعتمد مبدأ إطفاء هذه المواد على تصبنها. يحول وسيط الإطفاء المادة المحترقة بسرعة إلى صابون غير قابل للاحتراق. هذه العملية ماصة للحرارة، مما يعني أنها تمتص الطاقة (في هذه الحالة، الطاقة الحرارية) من المناطق المحيطة بها، والحد من درجة الحرارة والقضاء على الحريق.
انظر أيضًا
مراجع
- ^ "Double bonds and hydrogenation". GCSE Bitesize. BBC. مؤرشف من الأصل في 2017-11-15.
- ^ Bartels، Thorsten؛ Bock، Wolfgang؛ Braun، Jürgen؛ Busch، Christian؛ Buss، Wolfgang؛ Dresel، Wilfried؛ Freiler، Carmen؛ Harperscheid، Manfred؛ Heckler، Rolf-Peter؛ Hörner، Dietrich؛ Kubicki، Franz؛ Lingg، Georg؛ Losch، Achim؛ Luther، Rolf؛ Mang، Theo؛ Noll، Siegfried؛ Omeis، Jürgen (2003). "Lubricants and Lubrication". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a15_423. ISBN:3-527-30673-0.
- ^ Schumann، Klaus؛ Siekmann، Kurt (2000). "Soaps". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a24_247. ISBN:3-527-30673-0.
وصلات خارجية
- Soapmaking at Bellaonline - Soapmaking articles, forum and supplier links.
- Soap Naturally Web and Mailing List - Resources for natural handmade soapmakers.
- Soap Recipe Corner - Soapmaking explained.
- About Candle and Soap Making - Soap making at About.com
- Glossary for the Modern Soap Maker - A collection of terms, definitions and acronyms for today's soap maker.
- Adipocere - A collection of resources on soap mummies and adipocere formation.
- The Handbook of Soap Manufacture - A book from 1908.
- التصبن العيادة السورية
| تصبن في المشاريع الشقيقة: | |
| |

