سيلينيد
تحتاج النصوص المترجمة في هذه المقالة إلى مراجعة لضمان معلوماتها وإسنادها وأسلوبها ومصطلحاتها ووضوحها للقارئ، لأنها تشمل ترجمة اقتراضية أو غير سليمة. |
سيلينيد هو مركب كيميائي من أنيون سيلينيوم مع حالة الأكسدة −2 (Se2−). كيميائية السيلينيد تشبه الكبريتيد، في المحلول المائي، أيون سيلينيد يكون مسيطر فقط بظروف بسيطة جدا. في الظروف الطبيعية، أيون هيدروجين سيلينيد HSe− هو الأكثر شيوعا ، في الظروف الحمضية، يتشكل هيدروجين سيلينيد H2Se.
بعض السيلينيدات تتفاعل وتتأكسد مع الهواء. لأن معظم الطاقة تتنقص في السيلينيد أو معادن السيلينيدات فمن السهل تتفككها إلى العناصر الأولية أكثر من الكبريتيد (تلوريدات هي حتى أسهل بالتفكك من هؤلاء). تتميه معادن السيلينيدات موجبة الشحنة مثل الألمنيوم سيلينيد بسهولة، حتى في الهواء الرطب وتطلق غاز سيلينيد الهدروجين السام.
الذرات الكمية لمعدن السيلينيد
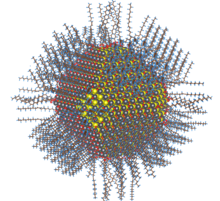
تستعمل الذرات الكمية لمعدن السيلينيد والذرات بحجم النانو لتركيب عدد من الأنظمة المتوفرة، معظمها يتطلب حرارة عالية ومكونات خطيرة.[1] يمكن أن تعد هذه الذرات لمجموعة متنوعة من التطبيقات بتغيير نوع الربيطة المتناسقة مع الطبقة الخارجية للشحنة الموجبة. معظم تفاعلات تحويل الربيطة متوفرة للاستعمال، تحويل ربيطة من نوع X أو L وZ ، الألية لفعل ذلك ماتزال تحت الدراسة.[2]
الاستعمالات
انتشرت الذرات الكمية المعتمدة على المعادن السيلينيدات لخصائصها الطيفية المميزة.[3] يستخدم لب قشرة السبائك من الكادميوم والسيلينيد والكبريتيد في العلاج بالضوء والتصوير.[4]
طالع أيضاً
المراجع
- ^ . DOI:10.1002/anie.200804266/asset/8638_ftp.pdf https://web.archive.org/web/20200127202826/https://onlinelibrary.wiley.com/store/10.1002/anie.200804266/asset/8638_ftp.pdf?s=0dd9c41d2f909a2d6f93a33228e2883a1270b3d5&t=ii22tcl6&v=1. مؤرشف من الأصل (PDF) في 27 يناير 2020. اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد بدورية محكمة}}: الاستشهاد بدورية محكمة يطلب|دورية محكمة=(مساعدة)، تحقق من التاريخ في:|تاريخ الوصول=(مساعدة)، والوسيط|title=غير موجود أو فارغ (مساعدة) - ^ Anderson، Nicholas C.؛ Owen، Jonathan S. (8 يناير 2013). "Soluble, Chloride-Terminated CdSe Nanocrystals: Ligand Exchange Monitored by 1H and 31P NMR Spectroscopy". Chemistry of Materials. ج. 25 ع. 1: 69–76. DOI:10.1021/cm303219a. ISSN:0897-4756. مؤرشف من الأصل في 2019-12-08.
- ^ Larson, Daniel R.; Zipfel, Warren R.; Williams, Rebecca M.; Clark, Stephen W.; Bruchez, Marcel P.; Wise, Frank W.; Webb, Watt W. (30 May 2003). "Water-Soluble Quantum Dots for Multiphoton Fluorescence Imaging in Vivo". Science (بالإنجليزية). 300 (5624): 1434–1436. DOI:10.1126/science.1083780. ISSN:0036-8075. PMID:12775841. Archived from the original on 2019-12-08.
- ^ Hessel، Colin M.؛ Pattani، Varun P.؛ Rasch، Michael؛ Panthani، Matthew G.؛ Koo، Bonil؛ Tunnell، James W.؛ Korgel، Brian A. (8 يونيو 2011). "Copper Selenide Nanocrystals for Photothermal Therapy". Nano Letters. ج. 11 ع. 6: 2560–2566. DOI:10.1021/nl201400z. ISSN:1530-6984. PMC:3111000. PMID:21553924. مؤرشف من الأصل في 2019-12-08.
