غلايكولالدهيد: الفرق بين النسختين
أنشأ الصفحة ب'{{صندوق معلومات دواء|Verifiedfields=|O=2|KEGG=C00266|ChEBI_Ref={{ebicite|correct|EBI}}|ChEBI=17071|ChEMBL_Ref=|ChEMBL=|NIAID_ChemDB=|C=2|H=4|N=|molecular_weight=60.052 غرام لكل مول|UNII=W0A0XPU08U|smiles=O=CCO|InChI=1/C2H4O2/c3-1-2-4/h1,4H,2H2|InChIKey=WGCNASOHLSPBMP-UHFFFAOYAH|StdInChI_Ref={{stdinchicite|correct|chemspider}}|StdInChI=1S/C2H4O2/c3-1-2-4/h1,4H,2H2|StdInChIKey_Ref={{stdinchicite|correct|chemspider}}|StdInChIKey=WGCNASOHLSPBM...' وسمان: تمت إضافة وسم nowiki تحرير مرئي |
(لا فرق)
|
نسخة 05:05، 29 نوفمبر 2021
| غلايكولالدهيد | |
|---|---|
| اعتبارات علاجية | |
| معرّفات | |
| CAS | 141-46-8 |
| بوب كيم | CID 756 |
| ECHA InfoCard ID | 100.004.987 |
| كيم سبايدر | 736 |
| المكون الفريد | W0A0XPU08U |
| كيوتو | C00266 |
| ChEBI | CHEBI:17071 |
| بيانات كيميائية | |
| الصيغة الكيميائية | C2H4O2 |
| الكتلة الجزيئية | 60.052 غرام لكل مول |
| بيانات فيزيائية | |
| نقطة الانصهار | 97 °C (207 °F) |
| تعديل مصدري - تعديل | |
غلايكولالدهيد هو مركب عضوي صيغته الجزيئيّة هي HOCH2-CHO، وهو أصغر جزيء لمركب كيميائيّ يحتوي على كل من مجموعة الألدهيد، ومجموعة الهيدروكسيل، وهو مركّب شديد التفاعل موجود في كل من المحيط الحيوي والوسط بين النجمي.
يوجد مركّب الغلايكولالدهيد كمادة صلبة بيضاء. وبشكل عام، لا يعتبر الغلايكولالدهيد من السكريات، على الرغم من أن تركيبه الجزيئيّ يتوافق مع الصيغة العامة للكربوهيدرات.[1]
البنية التركيبيّة
يوجد الغلايكولالدهيد في الطبيعة في المحيط الحيويّ وفي المادّة المكوّة للوسط بين النجوم كغاز، وفي حالته الصلبة، وفي مصهوره السائل، فهو مركب ثنائى الوحدات، أما في محلوله المائي، فيوجد كمزيج من أربعة أنواع على الأقل، وتكون هذه الانواع سريعة التحول.[2] وقد اكتشف العالمان كولينز، وجورج باستخدام الرنين المغناطيسي النووي توازن مركّب الغلايكولالدهيد في الماء.[3][4]
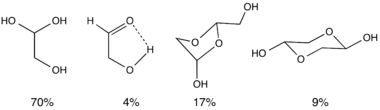
يُعتبر مركّب الغلايكولالدهيد هو المركب ثنائي الكربون الوحيد الممكن. لا يُعتبر مركّب الغلايكولالدهيد مركباً سكريّا حقيقيًا، فهو مركّب أحادي السكاريد ثنائي الكربون، وليس سكاريدًا بشكلٍ صارم، إلا أنه أبسط جزيء[5] مرتبط بالسكر، ويقال أن له مذاقاً حلواً.[6]
التخليق
يُعتبر مركّب الغلايكولالدهيد هو ثاني أكثر المركبات وفرة عند تحضير زيت الانحلال الحراري، والذي تصل نسبة مركّب الغلايكولالدهيد فيه حتى 10٪ من الوزن.[7]
ويمكن تصنيع مركّب الغلايكولالدهيد عن طريق أكسدة الإيثيلين غلايكول باستخدام بيروكسيد الهيدروجين في وجود كبريتات الحديد الثنائي.[8]
التخليق الحيوي
يمكن أن ينشأ مركّب الغلايكولالدهيد طبيعيّاً نتيجة لتأثير الكيتوليز على الفركتوز 1،6-بيسفوسفات في مسار بديل لتحلل السكر، ثم يعمل بيروفوسفات الثيامين على إفراز مركّب الغلايكولالدهيد أثناء تحويل فوسفات البنتوز.
في أيض البيورين، يتمّ تحويل الزانثين أولاً إلى يورات، ثم تتحوّل اليورات إلى 5-هيدروكسي أيزورات، والتي ينتزع منها الكربوكسيل، وتتحوّل بدورها إلى آلانتوين وحمض آلانتويك. يؤدّي التحلل المائي لليوريا إلى تكون مادة سكريّة، والتي تتحوّل بدورها إلى الغلايكولالدهيد بعد التحلل المائي الثاني لليوريا، ثمّ تتكثف الغلايكولالدهيدات لتكوين إريثروز 4-فوسفات، والذي يتمّ إلى تحويلة فوسفات البنتوز مرة أخرى.
دوره في تفاعل فورموز
يلعب الغلايكولالدهيد دوراً كوسيط كيميائيّ في تفاعل فورموز. في تفاعل فورموز، يتكثف جزيء فورمالدهيد لإنتاج الغلايكولالدهيد، ثم يتم تحويل الغلايكولالدهيد إلى غلسيرالديهيد. يوضح وجود الغلايكولالدهيد في هذا التفاعل كيف يمكن أن يلعب دورًا هامّاً في تكوين اللبنات الكيميائية الأساسيّة للحياة، حيث تعتمد النيوكليوتيدات، على سبيل المثال، على تفاعل فورموز لتكوين وحدة السكر لها. تؤلف النيوكليوتيدات المعلومات الجينية للخلايا الحيّة مما يجعلها ضروريّة للحياة.
دوره في النشوء التلقائي
غالباً ما يُستخدم الغلايكولالدهيد في التدليل على صحّة نظريات النشوء التلقائي.[9][10] حيث يمكن تحويل الغلايكولالدهيد في المختبر إلى أحماض أمينية،[11] وثنائي الببتيدات قصيرة السلسلة ممّا قد يسهّل تكوين السكريات المعقدة.[12] فقد استخدم مركّب إل فاليل إل فالين على سبيل المثال، كمحفز لتكوين رباعية من الغلايكولالدهيدات.
أظهرت الحسابات النظرية بالإضافة إلى ذلك جدوى التخليق المحفز ثنائي الببتيد من البنتوز.[13] أظهر هذا التخليق التكوين التحفيزي الفراغي النوعي للدي ريبوز، وهو المتصاوغ المرآتي الوحيد الطبيعي المنشأ للريبوز. استخدمت العديد من النظريات المرتبطة بالنشوء التلقائي مركب الغلايكولالدهيد منذ اكتشافه في تطوير الطرق الكيميائية المختلفة لشرح آليّة تكوينه في الأنظمة النجميّة.
المراجع
- ^ Mathews, Christopher K. (2000). Biochemistry. Van Holde, K. E. (Kensal Edward), 1928-, Ahern, Kevin G. (ط. 3rd). San Francisco, Calif.: Benjamin Cummings. ص. 280. ISBN:978-0805330663. OCLC:42290721.
- ^ Yaylayan، Varoujan A.؛ Harty-Majors، Susan؛ Ismail، Ashraf A. (1998). "Investigation of the mechanism of dissociation of glycolaldehyde dimer (2,5-dihydroxy-1,4-dioxane) by FTIR spectroscopy". Carbohydrate Research. ج. 309: 31–38. DOI:10.1016/S0008-6215(98)00129-3.
- ^ "Prediction of Isomerization of Glycolaldehyde In Aqueous Solution by IBM RXN – Artificial Intelligence for Chemistry" (بالإنجليزية الأمريكية). Retrieved 2019-11-19.
- ^ Collins، G. C. S.؛ George، W. O. (1971). "Nuclear magnetic resonance spectra of glycolaldehyde". Journal of the Chemical Society B: Physical Organic: 1352. DOI:10.1039/j29710001352. ISSN:0045-6470.
- ^ Carroll, P.؛ Drouin, B.؛ Widicus Weaver, S. (2010). "The Submillimeter Spectrum of Glycolaldehyde" (PDF). Astrophys. J. ج. 723 ع. 1: 845–849. Bibcode:2010ApJ...723..845C. DOI:10.1088/0004-637X/723/1/845.
- ^ Shallenberger, R. S. (6 Dec 2012). Taste Chemistry (بالإنجليزية). Springer Science & Business Media. ISBN:9781461526667.
- ^ Moha، Dinesh؛ Charles U. Pittman, Jr.؛ Philip H. Steele (10 مارس 2006). "Pyrolysis of Wood/Biomass for Bio-oil: A Critical Review". Energy & Fuels. ج. 206 ع. 3: 848–889. DOI:10.1021/ef0502397. S2CID:49239384.
- ^ {{Hans Peter Latscha, Uli Kazmaier und Helmut Alfons Klein : Organic Chemistry: Chemistry Basiswissen-II '. Springer, Berlin; 6, vollständig überarbeitete Auflage 2008, (ردمك 978-3-540-77106-7), S. 217}}
- ^ Kim، H.؛ Ricardo, A.؛ Illangkoon, H. I.؛ Kim, M. J.؛ Carrigan, M. A.؛ Frye, F.؛ Benner, S. A. (2011). "Synthesis of Carbohydrates in Mineral-Guided Prebiotic Cycles". Journal of the American Chemical Society. ج. 133 ع. 24): 9457–9468. DOI:10.1021/ja201769f. PMID:21553892.
- ^ Benner، S. A.؛ Kim, H.؛ Carrigan, M. A. (2012). "Asphalt, Water, and the Prebiotic Synthesis of Ribose, Ribonucleosides, and RNA". Accounts of Chemical Research. ج. 45 ع. 12: 2025–2034. DOI:10.1021/ar200332w. PMID:22455515. S2CID:10581856.
- ^ Pizzarello، Sandra؛ Weber, A. L. (2004). "Prebiotic amino acids as asymmetric catalysts". Science. ج. 303 ع. 5661: 1151. CiteSeerX:10.1.1.1028.833. DOI:10.1126/science.1093057. PMID:14976304. S2CID:42199392.
- ^ Weber، Arthur L.؛ Pizzarello, S. (2006). "The peptide-catalyzed stereospecific synthesis of tetroses: A possible model for prebiotic molecular evolution". Proceedings of the National Academy of Sciences of the USA. ج. 103 ع. 34: 12713–12717. Bibcode:2006PNAS..10312713W. DOI:10.1073/pnas.0602320103. PMC:1568914. PMID:16905650.
- ^ Cantillo، D.؛ Ávalos, M.؛ Babiano, R.؛ Cintas, P.؛ Jiménez, J. L.؛ Palacios, J. C. (2012). "On the Prebiotic Synthesis of D-Sugars Catalyzed by L-Peptides Assessments from First-Principles Calculations". Chemistry: A European Journal. ج. 18 ع. 28: 8795–8799. DOI:10.1002/chem.201200466. PMID:22689139.


