قلوية
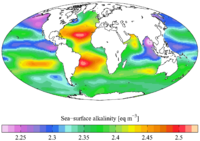
القلوية وهي على العموم وصف لمقدار السعة الكمّيّة لمحلول مائي كي يعدّل حمضاً.[1] يستخدم مصطلح القلوية على الخصوص في المجالات البيئية لوصف مقدرة التربة والصخور والماء في الطبيعة على الارتباط مع الأحماض. بالتالي تعتمد درجة القلوية على كمية الأيونات ذات التأثير القاعدي، وخاصة أيون الكربونات.
عادة ما يميز عند قياس القلوية بين القلوية الكلّيّة، وبين قلوية الكربونات. إن قياس قلوية المياه معيار مهم عند تحديد مقدرة المجرى المائي على معادلة الملوثات الحمضية القادمة من الأمطار الحمضية أو من مياه الصرف الصحي، أو من أي مصدر حمضي.[2]
المفهوم العام[عدل]
يشير مصطلح القلوية بشكل عام إلى كمية القواعد في محلول والتي يمكن أن تحوّل إلى أنواع كيميائية غير مشحونة باستخدام حمض قوي.[3] يمكن قياس القلوية من خلال المعايرة باستخدام حمض معروف التركيز وبوجود مؤشر الأس الهيدروجيني.[4]
قلوية الكربونات[عدل]
يعتمد مفهوم قلوية الكربونات AC على نظام انحلالية غاز ثنائي أكسيد الكربون CO2 في الماء، حيث تتشكل في الماء، إلى حد ما، الأنواع التالية: الكربونات 2−CO3 والبيكربونات −HCO3 بالإضافة إلى حمض الكربونيك. بالتالي فإن كمية CO2 المنحلة في الماء CT يمكن التعبير عنها بالمعادلة التالية:[5]
- CT = [CO2*] + [HCO3−] + [CO32−]
بالتالي يمكن الحصول على فلوية الكربونات على الشكل:
- AC = [HCO3−] + 2 · [CO32−] + [OH−] − [H3O+]
القلوية الكلية[عدل]
تعرّف القلوية الكلية، والتي يرمز لها AT (وذلك من Total Alkalinity)، على أنها الكمية المكافئة للقواعد التي يمكن معايرتها باستخدام حمض قوي.[6]
على العموم هناك العديد من التعريفات التي تصف القلوية الكلية، والتي يمكن تخصيصها حسب الأيونات الموجودة في المحلول المائي.[7] على سبيل المثال، يمكن تعميم المفهوم بحيث يمكن أن يشمل جميع القواعد وحتى الأحماض الضعيفة (pKa > 4.5 عند 25 °س) وذلك كجزء من القلوية الكلية:
- AT = [HCO3−] + 2 · [CO32−] + [OH−] − [H3O+] + [B(OH)4−] + 2 · [PO43−] + [HPO42−] − [H3PO4] + [SiO(OH)3−] + [NH3] - …
أو يمكن تضييق المفهوم بحيث أن تؤخذ قيمة تقريبية مبسّطة بحيث أن مفهوم القلوية الكلية يشمل إضافة تركيز أيون رباعي هيدروكسي البورات فقط إلى قلوية الكربونات:
- AT ≈ [HCO3−] + 2 · [CO32−] + [OH−] − [H3O+] + [B(OH)4−]
بالتالي فإن مفهوم القلوية الكلية للعينات المائية يعتمد على نوع الأيونات وعلى مجال الاختصاص الذي على أساسه تؤخذ العينات.
المراجع[عدل]
- ^ "Alkalinity". The WQA Glossary of Terms. 31 مارس 2000. مؤرشف من الأصل في 2013-12-24. اطلع عليه بتاريخ 2013-03-06.
- ^ "Total Alkalinity". United States Environment Protection Agency. مؤرشف من الأصل في 2015-09-08. اطلع عليه بتاريخ 2013-03-06.
- ^ Drever، James I. (1988). The Geochemistry of Natural Waters, Second Edition. Englewood Cliffs, NJ: Prentice Hall. ص. 51–58 [52]. ISBN:0-13-351396-3.
- ^ Wissenschaft-Online-Lexika: Eintrag zu Alkalinität im Lexikon der Geowissenschaften.
- ^ A. G. Dickson, C. Goyet: Handbook of Methods for the Analysis of the Various Parameters of the Carbon Dioxide System in Sea Water, Kapitel 2, S. 3. نسخة محفوظة 3 مارس 2012 على موقع واي باك مشين.
- ^ Stumm, W. & J.J Morgan (1981). Aquatic Chemistry, 2n Ed. New York: Wiley-Interscience. ص. 780.
- ^ Richard E. Zeebe, Dieter A. Wolf-Gladrow: CO2 in Seawater: Equilibrium, Kinetics, Isotopes. Elsevier, 2001, ISBN 978-0444505798.
