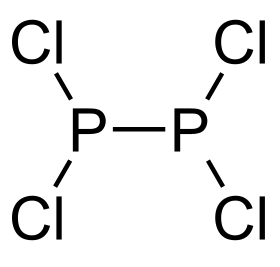
رباعي كلوريد ثنائي الفسفور
المظهر
| رباعي كلوريد ثنائي الفسفور | |
|---|---|
| أسماء أخرى | |
Diphosphorus tetrachloride |
|
| المعرفات | |
| CAS | 13497-91-1 |
| بوب كيم | 139480 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | P2Cl4 |
| الكتلة المولية | 203.76 غ/مول |
| المظهر | سائل عديم اللون |
| نقطة الانصهار | −28 °س |
| نقطة الغليان | 180 °س |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
رباعي كلوريد ثنائي الفوسفور هو مركب كيميائي ينتمي إلى هاليدات الفوسفور، صيغته P2Cl4، ويوجد على شكل سائل عديم اللون.[1]
التحضير
[عدل]يمكن أن يحضر المركب من تفاعل اختزال بتكثيف ثلاثي كلوريد الفوسفور بوجود بخار من فلز النحاس.[2] كما يمكن أن تتم عملية الاختزال بوجود جو من غاز الهيدروجين.[1][3]
الخواص
[عدل]يوجد المركب في الشروط القياسية على شكل سائل عديم اللون، ويكون للفوسفور في هذا المركب في حالة أكسدة مقدارها +2، وترتبط الذرات فيما بينها بروابط أحادية؛ ولذلك يمكن اعتبار هذا الهاليد كلوريداً للفوسفور الثنائي. لا يعد هذا المركب مستقراً في الشروط العادية، إذ يتفاعل مع الماء والرطوبة، ويتفكك عند درجات حرارة أعلى من 0 °س؛[4]
طالع أيضاً
[عدل]مراجع
[عدل]- ^ ا ب Karl A. Hofmann: Anorganische Chemie. Springer-Verlag, 2013, ISBN 978-3-663-14240-9, S. 273
- ^ A. F. Holleman, N. Wiberg: Anorganische Chemie. 103. Auflage. 1. Band: Grundlagen und Hauptgruppenelemente. Walter de Gruyter, Berlin / Boston 2016, ISBN 978-3-11-049585-0
- ^ Antonio A. Sandoval, H. C. Moser: Preparation of Diphosphorus Tetrachloride. In: Inorganic Chemistry. Band 2, Nr. 1, Februar 1963, S. 27–29, doi:10.1021/ic50005a008
- ^ Charles B. Lindahl, William L. Jolly: The Reactions of Diphosphorus Tetrachloride with Nickel Carbonyl and Boron Tribromide. In: Inorganic Chemistry. Band 3, Nr. 11, November 1964, S. 1634–1636, doi:10.1021/ic50021a035