ثلاثي بروميد الفسفور
| ثلاثي بروميد الفوسفور | |
|---|---|
 |
 |
| الاسم النظامي (IUPAC) | |
Phosphorus tribromide |
|
| أسماء أخرى | |
phosphorus(III) bromide, |
|
| المعرفات | |
| CAS | 7789-60-8 |
| بوب كيم | 24614 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | PBr3 |
| الكتلة المولية | 270.69 غ/مول |
| المظهر | سائل عديم اللون |
| الكثافة | 2.85 غ/سم3 |
| نقطة الانصهار | −41.5 °س |
| نقطة الغليان | 173 °س |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
ثلاثي بروميد الفوسفور هو مركب كيميائي ينتمي إلى هاليدات الفوسفور، صيغته PBr3، ويوجد على شكل سائل عديم اللون.
التحضير[عدل]
يحضر المركب صناعياً من التفاعل المباشر بين الفوسفور الأحمر وغاز البروم؛ وذلك بكميات ستوكيومترية من البروم مع فائض من الفوسفور من أجل تجنب تشكل خماسي بروميد الفوسفور:[2][3]
الخواص[عدل]
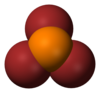
يوجد المركب في الشروط القياسية على شكل سائل عديم اللون، ويكون للفوسفور في هذا المركب في حالة أكسدة مقدارها +3، وللمركب بنية جزيئية هرمية ثلاثية. يمكن أن يتصرف المركب إما على شكل حمض لويس أو قاعدة لويس.
الاستخدامات[عدل]
يستخدم هذا المركب بشكل واسع في المختبرات الكيميائية عاملاً لإضافة البروم إلى المركبات العضوية في تفاعلات البرومة.[4] من أشهر الأمثلة التفاعل مع الكحولات للحصول على المشتقات البرومية:[5]
بشكل مشابه يتفاعل ثلاثي بروميد الفوسفور مع الأحماض الكربوكسيلية للحصول على بروميد الأسيل الموافق:
يفضل إجراء تفاعلات البرومة باستخدام هذا المركب على حمض الهيدروبروميك، وذلك من أجل تجنب تشكل الكاتيونات الكربونية؛ إذ يمكن حتى الحصول على بروميد النيوبنتيل من الكحول الموافق بمردود يبلغ 60%.[6]
مراجع[عدل]
- ^ ا ب ج PHOSPHORUS TRIBROMIDE (بالإنجليزية), QID:Q278487
- ^ J. F. Gay, R. N. Maxson "Phosphorus(III) Bromide" Inorganic Syntheses, 1947, vol. 2, 147ff. دُوِي:10.1002/9780470132333.ch43
- ^ Burton, T. M.؛ Degerping, E. F. (1940). "The Preparation of Acetyl Bromide". Journal of the American Chemical Society. ج. 62 ع. 1: 227. DOI:10.1021/ja01858a502.
- ^ Harrison, G. C.; Diehl, H.(1955)."β-Ethoxyethyl Bromide". Org. Synth.; Coll. Vol. 3: 370.
- ^ K. Peter, C. Vollhardt, N. E. Schore: Organische Chemie. 4. Auflage, Wiley-VCH Verlag, Weinheim 2005, S. 393 ff.
- ^ Wade, L. G. Jr. (2005). Organic Chemistry (ط. 6th). Upper Saddle River, NJ, USA: Pearson/Prentice Hall. ص. 477.
| ثلاثي بروميد الفسفور في المشاريع الشقيقة: | |
| |




