هيدريد ثلاثي بوتيل القصدير
| هيدريد ثلاثي بوتيل القصدير | |
|---|---|
 |
 |
| تسمية الاتحاد الدولي للكيمياء | |
Tributylstannane[1] |
|
| المعرفات | |
| رقم CAS | 688-73-3 |
| بوب كيم (PubChem) | 3032732 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | C12H28Sn |
| الكتلة المولية | 291.06 غ/مول |
| المظهر | سائل عديم اللون إلى أصفر |
| الكثافة | 1.10 غ/سم3 |
| نقطة الغليان | 80 °س |
| الذوبانية في الماء | يتفكك |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
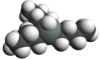
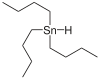
هيدريد ثلاثي بوتيل القصدير هو مركب قصدير عضوي يمكن كتابة صيغته الكيميائية على الشكل C4H9)3SnH)، ويكون في الشروط القياسية على شكل سائل عديم اللون إلى أصفر. يستخدم بشكل واسع في المختبرات الكيميائية للحصول على جذر ثلاثي بوتيل القصدير الذي يرمز له اختصاراً TBT.
التحضير[عدل]
يحضر المركب من اختزال أكسيد ثلاثي بوتيل القصدير باستخدام متعدد ميثيل هيدرو السيلوكسان:[4][5]
- 2"(MeSiH)" + (Bu3Sn)2O → "(Me2Si)2O" + 2 Bu3SnH
- (Bu3Sn)2O + 2/n (MeSi(H)O)n → 2 Bu3SnH + 1/n [(MeSiO)2O]n
الخواص[عدل]
يوجد المركب في الشروط القياسية من الضغط ودرجة الحرارة على شكل سائل عديم اللون إلى أصفر، وهو قابل للتقطير، لكنه حساس تجاه الماء والرطوبة الجوية إذ يتفكك في تفاعل حلمهة إلى أكسيد ثلاثي بوتيل القصدير.
الاستخدامات[عدل]
لمركب هيدريد ثلاثي بوتيل القصدير أهمية في الاصطناع العضوي، فهو يستخدم بمرافقة آزو مضاعف إيزوبوتيرونتريل AIBN أو بالإشعاع الضوئي من أجل تحويل الهاليدات العضوية (والمجموعات المتعلقة) إلى الهيدروكربونات الموافقة؛ وذلك وفق آلية تفاعل جذرية تتضمن الجذر الحر •Bu3Sn.[6][7]
اقرأ أيضاً[عدل]
المراجع[عدل]
- ^ "SnBu3H - PubChem Public Chemical Database". The PubChem Project. USA: National Center for Biotechnology Information. مؤرشف من الأصل في 2012-11-03.
- ^ أ ب ت Tri-n-butyltin (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Hayashi, K.; Iyoda, J.; Shiihara, I. "Reaction of organotin oxides, alkoxides and acyloxides with organosilicon hydrides. New preparative method of organotin hydrides " J. Organomet. Chem. 1967, 10, 81. دُوِي:10.1016/S0022-328X(00)81719-2
- ^ Jordi Tormo and Gregory C. Fu(2002)."Tributylstannane (Bu3SnH)-Catalyzed Barton-McCombie deoxygenation of Alcohols: 3-Deoxy-1,2:5,6-bis-O-(1-methylethyilidine)-α-D-ribo-hexafuranose". Org. Synth.78: 239.
- ^ OUP catalogue page, J. Clayden, N. Greeves, S. Warren and P. Wothers, in Organic Chemistry, 2000, OUP, Oxford, ch. 39, pp. 1040-1041. [وصلة مكسورة] نسخة محفوظة 04 يونيو 2008 على موقع واي باك مشين.
- ^ T. V. (Babu) RajanBabu, Philip C. Bulman Page, Benjamin R. Buckley, "Tri-n-butylstannane" Encyclopedia of Reagents for Organic Synthesis 2004, John Wiley & Sons. دُوِي:10.1002/047084289X.rt181.pub2
| هيدريد ثلاثي بوتيل القصدير في المشاريع الشقيقة: | |
| |

