فلوريد الزرنيخ الثلاثي
| فلوريد الزرنيخ الثلاثي | |
|---|---|
 |
 |
| الاسم النظامي (IUPAC) | |
Arsenic(III) fluoride |
|
| أسماء أخرى | |
Arsenic trifluoride, trifluoroarsane |
|
| المعرفات | |
| CAS | 7784-35-2 |
| بوب كيم | 24571 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | AsF3 |
| الكتلة المولية | 131.91 غ/مول |
| المظهر | سائل عديم اللون |
| الكثافة | 2.66 غ/سم3 |
| نقطة الانصهار | -6 °س |
| نقطة الغليان | 57 °س |
| الذوبانية في الماء | يتفكك |
| الذوبانية | الإيثانول والبنزين والإيثر الإيثيلي |
| المخاطر | |
| رمز الخطر وفق GHS |  |
| وصف الخطر وفق GHS | خطر |
| بيانات الخطر وفق GHS | H301, H311, H331 |
| بيانات وقائية وفق GHS | P261, P264, P270, P271, P280, P301+310, P302+352, P304+340, P311, P312, P321, P322, P330, P361 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
فلوريد الزرنيخ الثلاثي (أو ثلاثي فلوريد الزرنيخ) هو مركب كيميائي صيغته AsF3، ويوجد في الشروط القياسية على شكل سائل عديم اللون.
ينتمي المركب إلى مجموعة الفلوريدات، وهو سام مثل باقي مركبات الزرنيخ اللاعضوية.
التحضير
[عدل]يحضر المركب من تفاعل ثلاثي أكسيد الزرنيخ مع فلوريد الهيدروجين:[2]
أو مع حمض الفلوروكبريتيك:[3]
الخواص
[عدل]يوجد المركب في الشروط القياسية على شكل سائل عديم اللون، وهو يتحلمه عند التماس مع الماء؛[2] لكننه يمتزج مع المذيبات العضوية مثل الإيثانول والبنزين وثنائي إيثيل الإيثر.
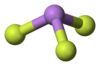
للمركب بنية جزيئية هرمية في الطور الغازي، والتي تلاحظ أيضاً في الطور الصلب.[2] يبلغ طول الرابطة As-F مقدار 170.6 بيكومتر، في حين أن زاوية الرابطة F-As-F تبلغ 96.2°.[4]
الاستخدامات
[عدل]يستخدم فلوريد الزرنيخ الثلاثي في فلورة الكلوريدات اللافلزية، ولكنه أقل فعالية في هذا الصدد من ثلاثي فلوريد الإثمد SbF3.[2]
المخاطر
[عدل]إن مركب فلوريد الزرنيخ الثلاثي سام جداً ومسرطن.[3]
مراجع
[عدل]- ^ ا ب ج ARSENIC TRIFLUORIDE (بالإنجليزية), QID:Q278487
- ^ ا ب ج د Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (بالإنجليزية) (2 ed.). Butterworth-Heinemann. ISBN:0-08-037941-9.
- ^ ا ب G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 197.
- ^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications (ردمك 0-19-855370-6)


