بومبيكول
| بومبيكول | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
(10E,12Z)-Hexadeca-10,12-dien-1-ol |
|
| المعرفات | |
| رقم CAS | 765-17-3 |
| بوب كيم (PubChem) | 445128 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C16H30O |
| كتلة مولية | 238.41 غ.مول−1 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
بومبيكول هو فرمون تطلقه أنثى دودة القز لجذب رفاقها. وهو أيضًا فرمون الجنس في عثة الحرير البري (بومبيكس ماندرينا).[1][2] اكتشفه أدولف بوتينانت في عام 1959 ، وكان أول فرمون يتم تمييزه كيميائيًا.[3]
ويمكن استخدام كميات دقيقة من هذا الفرمون لكل فدان من الأرض للتشويش على ذكور الحشرات حول موقع شركائها من الإناث. وبالتالي يمكن أن يكون بمثابة إغراء في المصائد لإزالة الحشرات بشكل فعال دون رش المحاصيل بكميات كبيرة من المبيدات. سمى بوتينانت المادة بعد الاسم اللاتيني للعثة بومبيكس موري.[4]
في الجسم الحي يبدو أن بومبيكول هو الرابط الطبيعي لبروتين ربط الفيرومون (BmorPBP) الذي يرافق الفيرومون إلى مستقبلات الفرمون.[5]
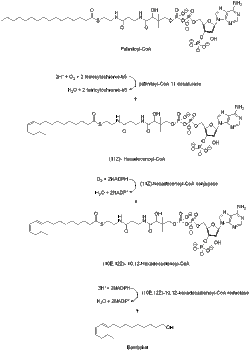
التركيب البيولوجي
[عدل]من المعروف أن بومبيكول مشتق من أسيتيل مرافق الإنزيم-أ عبر C-16 الدهنية أسيل بالميتويل CoA.[6]
يتم تحويل بالميتويل تميم الأنزيم أ إلى بومبيكول في خطوات تتضمن إزالة التشبع والتعديل الاختزالي لكربون الكربونيل. مقارنةً بالفيرومونات من النوع الأول ،[7] لا يحتاج التخليق الحيوي للبومبيكول إلى تقصير السلسلة أو أي نوع آخر من التعديل لمجموعة الهيدروكسيل الطرفية.
ينتج إنزيم ديساتوراسي (desaturase) المشفر بواسطة الجين (بمبغ ديسات 1:Bmpgdesat1) (Desat1) أحادي (11Z) -hexadecenoyl-CoA وكذلك diene (10E ، 12Z) -10،12-hexadecadienoyl-CoA. إن هذا الإنزيم هو الإنزيم الوحيد الضروري لتحفيز هاتين الخطوتين المتتاليتين لإزالة التشبع..[8]
تم العثور على سلائف بومبيكول أسيل (10E ، 12Z)-10، (12-هيكساديكادينات:12-hexadecadienoate) بشكل أساسي كإستر ثلاثي الجلسرين في قطرات الدهون السيتوبلازمية لخلايا الغدة الفرمون للعثة. وعندما تخرج الإناث البالغات من عذارىهن ، يبدأ الهرمون العصبي PBAN (الببتيد العصبي المنشط للتخليق الحيوي للفرمون) في إرسال إشارات إلى الأحداث التي تساعد في التحكم في تحلل الدهون في ثلاثي الجليسيرول المخزن ، وإطلاق (10E ، 12Z) -10،(12-هيكساديكادينات:12-hexadecadienoate) لتعديله الاختزالي النهائي .[9][10][11] آلية التحرر الدهني (10E،12Z)-10، (12-هيكساديكادينات:12-hexadecadienoate) من ثلاثي الجلسرين غير معروفة تمامًا ولكن تم تحديد الجينات المرشحة لترميز الليباز.[9][10]
المراجع
[عدل]- ^ Kuwahara، Yasumasa (1984). "Flight Time of Bombyx mandarina Males to a Pheromone Trap Baited with Bombykol". Applied Entomology and Zoology. ج. 19 ع. 3: 400–401. DOI:10.1303/aez.19.400.
- ^ Kuwahara، Yasumasa؛ Mori، Naoki؛ Yamada، Shigeki؛ Nemoto، Tadashi (1984). "Evaluation of Bombykol as the Sex Pheromone of Bombyx mandarina(Lepidoptera : Bombycidae)". Applied Entomology and Zoology. ج. 19 ع. 2: 265–267. DOI:10.1303/aez.19.265.
- ^ Butenandt، A.؛ Beckamnn, R.؛ Hecker, E. (1961). "Über den Sexuallockstoff des Seidenspinners .1. Der biologische Test und die Isolierung des reinen Sexuallockstoffes Bombykol". Hoppe-Seyler's Zeitschrift für Physiologische Chemie. ج. 324: 71–83. DOI:10.1515/bchm2.1961.324.1.71. PMID:13689417.
- ^ "Molecule of the Week". الجمعية الكيميائية الأمريكية. 2004. مؤرشف من الأصل في 2004-08-07. اطلع عليه بتاريخ 2013-03-02.
- ^ Leal، Walter S. (2005). "Pheromone Reception". في Schulz، Stefan (المحرر). The Chemistry of Pheromones and Other Semiochemicals II. Topics in Current Chemistry. Springer. ج. 240. ص. 1–36. DOI:10.1007/b98314. ISBN:9783540213086. اطلع عليه بتاريخ 2013-03-02.
- ^ Caspi et al, Nucleic Acids Research 42:D459-D471 2014.
- ^ Ando، T؛ Hase، T؛ Arima، R؛ Uchiyama، M (1988). "Biosynthetic pathway of bombykol, the sex pheromone of the female silkworm moth". Agricultural and Biological Chemistry. ج. 52 ع. 2: 473–478. DOI:10.1271/bbb1961.52.473.
- ^ Moto، K؛ Suzuki، MG؛ Hull، JJ؛ Kurata، R؛ Takahashi، S؛ Yamamoto، M؛ Okano، K؛ Imai، K؛ Ando، T؛ Matsumoto، S (2004). "Involvement of a bifunctional fatty-acyl desaturase in the biosynthesis of the silkmoth, Bombyx mori, sex pheromone". Proceedings of the National Academy of Sciences. ج. 101 ع. 23: 8631–6. Bibcode:2004PNAS..101.8631M. DOI:10.1073/pnas.0402056101. PMC:423246. PMID:15173596.
- ^ ا ب Zhang، SD؛ Li، X؛ Bin، Z؛ Du، MF؛ Yin، XM؛ An، SH (2014). "Molecular identification of a pancreatic lipase-like gene involved in sex pheromone biosynthesis of Bombyx mori". Insect Science. ج. 21 ع. 4: 459–68. DOI:10.1111/1744-7917.12053. PMID:23955937. S2CID:23364842.
- ^ ا ب Ohnishi، A؛ Kaji، M؛ Hashimoto، K؛ Matsumoto، S (2011). "Screening for the Genes Involved in Bombykol Biosynthesis: Identification and Functional Characterization of Bombyx mori Acyl Carrier Protein". Frontiers in Endocrinology. ج. 2: 92. DOI:10.3389/fendo.2011.00092. PMC:3355880. PMID:22649392.
- ^ Matsumoto، S؛ Ozawa، R؛ Uchiumi، K؛ Kurihara، M (1996). "Cell-free production of the silkworm sex pheromone bombykol". Bioscience, Biotechnology, and Biochemistry. ج. 60 ع. 2: 369–73. DOI:10.1271/bbb.60.369. PMID:9063992.
| بومبيكول في المشاريع الشقيقة: | |
| |

