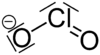
كلوريت
المظهر
| كلوريت | |
|---|---|
| الاسم النظامي (IUPAC) | |
كلوريت |
|
| المعرفات | |
| رقم CAS | 14998-27-7 |
| بوب كيم | 197148 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | -ClO2 |
| الكتلة المولية | 67.452 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
الكلوريت هو أيون صيغته -ClO2 وتسمى المركبات الحاوية على هذا الأيون في تركيبها باسم الكلوريتات. يحتوي هذا الأيون على الكلور في حالة الأكسدة +3؛ وتعد الكلوريتات أملاحاً مشتقة من حمض الكلوروز.
من أشهر الأمثلة على أملاح الكلوريتات مركب كلوريت الصوديوم NaClO2، والذي يحضر من تمرير غاز ثنائي أكسيد الكلور في محلول قلوي مؤلف من هيدروكسيد الصوديوم وبيروكسيد الهيدروجين.
الخواص
[عدل]تعد الكلوريتات أكثر ثباتية واستقراراً من حمض الكلوروز نفسه، وهي الأكثر شهرة من بين أملاح الهالوجينات ذات الصيغة HXO2.[3]
الاستخدمات
[عدل]يمكن الاستفادة من الخواص المؤكسدة لهذه الأملاح في عمليات التبييض في الصناعات النسيجية.[4]
مراجع
[عدل]- ^ ا ب CHLORITE (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier (ردمك 0-12-352651-5)
- ^ Otto-Albrecht Neumüller (Hrsg.): Römpp Lexikon Chemie Band 1: A–Cl. 8. neubearbeitete und erweiterte Auflage. Franckh'sche Verlagshandlung, Stuttgart 1979, ISBN 3-440-04511-0, S. 466.
في كومنز صور وملفات عن Chlorite ion.