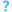راكدة بومانية: الفرق بين النسختين
| [نسخة منشورة] | [نسخة منشورة] |
ط بوت:التعريب V3.5 |
|||
| سطر 64: | سطر 64: | ||
== حدوث العدوى في قدامى المحاربين المصابين في العراق وأفغانستان == |
== حدوث العدوى في قدامى المحاربين المصابين في العراق وأفغانستان == |
||
يتعرض الجنود في [[العراق]] و[[أفغانستان]] لخطر الإصابات الناجمة عن إطلاق النار و[[العبوات الناسفة]]. وكان يعتقد في السابق أن العدوى تحدث بسبب التلوث بالراكدة البومانية في وقت الإصابة. وقد أظهرت دراسات لاحقة أنه على الرغم من أن الركدة البومانية قد تكون معزولة بشكل غير معتاد عن البيئة الطبيعية، فمن المرجح أن يتم اكتساب العدوى بشكل جزئي، ويرجع ذلك على الأرجح إلى قدرتها على العيش لفترات طويلة على الأسطح الاصطناعية والعديد من المرافق التي يتعرض الجنود المصابين لها خلال عملية إجلاء المصابين، حيث يتم نقل الجنود المصابين أولاً إلى المرافق من المستوى الأول بهدف استقرار حالاتهم. وبناءً على شدة الإصابة، يمكن نقل الجنود إلى مرفق من المستوى الثاني يتألف من فريق جراحي من أجل المزيد من الاستقرار. واعتمادا على الخدمات اللوجيستية للمحلية، قد يُنَقّل الجنود المصابون بين هذه المرافق عدة مرات قبل نقلهم إلى مستشفى رئيسي داخل منطقة القتال (المستوى الثالث). وبشكل عام بعد 1 - 3 أيام عندما يتم استقرار المرضى، يتم نقلهم عن طريق الجو إلى مرفق إقليمي (المستوى الرابع، حيث يتم أخيرا نقل الجنود المصابين إلى المستشفيات في بلدهم الأصلي لإعادة التأهيل والعلاج الإضافي.<ref>{{cite web|title=Army Medical Logistics|url=http://armypubs.army.mil/doctrine/DR_pubs/dr_a/pdf/fm4_02x1.pdf|work=FM 4-02.1|publisher=United States|accessdate=April 8, 2013|format=PDF|archive-url=https://web.archive.org/web/20130323025204/http://armypubs.army.mil/doctrine/DR_pubs/dr_a/pdf/fm4_02x1.pdf|archive-date=2013-03-23|dead-url=yes|df=}}</ref> ويبدو أن ذلك التعرض المتكرر للعديد من البيئات الطبية المختلفة هو السبب في أن عدوى الراكدة البومانية أصبحت شائعة بشكل متزايد، ومقاومتها للعديد من الأدوية هو عامل رئيسي في تعقيد علاج وإعادة تأهيل الجنود المصابين، مما أدى إلى المزيد من الوفيات.<ref name="MK O'Shea" /><ref>{{cite journal|last=Meghoo|first=CA|author2=Dennis, JW|author3= Tuman, C|author4= Fang, R|title=Diagnosis and management of evacuated casualties with cervical vascular injuries resulting from combat-related explosive blasts |journal=Journal of Vascular Surgery|date=May 2012|volume=55|issue=5|pages=1329–36; discussion 1336–7|pmid=22325667|doi=10.1016/j.jvs.2011.11.125}}</ref><ref>{{cite journal|last=Murray|first=CK|title=Epidemiology of infections associated with combat-related injuries in Iraq and Afghanistan |journal=The Journal of Trauma|date=March 2008|volume=64|issue=3 Suppl|pages=S232–8|pmid=18316967|doi=10.1097/ta.0b013e318163c3f5}}</ref> |
|||
== معدل الحدوث في المستشفيات == |
|||
يُشار إلى أن عدوى الراكدة البومانية على أنها عدوى انتهازية، وهي منتشرة بشكل كبير في المستشفيات، ولا تُشكل سوى القليل من المخاطر على الأفراد الأصحاء،<ref>{{cite web|title=''Acinetobacter'' in Healthcare Settings |url=https://www.cdc.gov/hai/organisms/acinetobacter.html|website=Centers for Disease Control and Prevention|publisher=US Department of Health and Human Services|accessdate=18 April 2017}}</ref> ومع ذلك، تشمل العوامل التي تزيد من مخاطر الإصابة: |
|||
* وجود ضعف في [[جهاز المناعة]] |
|||
* أمراض الرئة المزمنة |
|||
* [[داء السكري]] |
|||
* الإقامة المطولة في المستشفى |
|||
* المرض الذي يتطلب استخدام [[جهاز التنفس الصناعي]] في المستشفى |
|||
* وجود جرح مفتوح يعالج في المستشفى |
|||
* العلاجات التي تتطلب أجهزة توغلية، مثل [[قسطرة بولية|القسطرة البولية]] |
|||
ويمكن أن تنتشر الراكدة البومانية من خلال التلامس المباشر مع الأسطح والأجسام وبشرة الأشخاص الملوثين.<ref name="What Is Acinetobacter Baumannii"/> |
|||
ولقد تم توثيق استيراد البكتيريا إلى المستشفيات،<ref>{{cite journal|last=Jones|first=A|author2=Morgan, D|author3=Walsh, A|author4=Turton, J|author5=Livermore, D|author6=Pitt, T|author7=Green, A|author8=Gill, M|author9= Mortiboy, D|title=Importation of multidrug-resistant Acinetobacter spp infections with casualties from Iraq|journal=The Lancet Infectious Diseases|date=June 2006|volume=6|issue=6|pages=317–8|pmid=16728314|doi=10.1016/S1473-3099(06)70471-6}}</ref> حيث يتم إدخالها عادة إلى المستشفى من قِبَل مريض مستعمر. وبسبب قدرتها على البقاء على الأسطح الاصطناعية ومقاومة التجفيف، يمكن أن تبقى وربما تصيب مرضى جدد لبعض الوقت. ويُشتبه في أن نموها يُفضَل في المستشفيات بسبب الاستخدام المستمر للمضادات الحيوية من قبل المرضى في المستشفى.<ref>{{cite journal|last=Dijkshoorn|first=L|author2=Nemec, A|author3= Seifert, H|title=An increasing threat in hospitals: multidrug-resistant ''Acinetobacter baumannii'' |journal=Nature Reviews Microbiology|date=December 2007|volume=5|issue=12|pages=939–51|pmid=18007677|doi=10.1038/nrmicro1789}}</ref> ويمكن أن تنتشر عن طريق الاتصال الشخصي مع المريض أو الاتصال بالأسطح الملوثة،<ref>{{cite web|url=https://www.cdc.gov/HAI/organisms/acinetobacter.html|title=Acinetobacter in Healthcare Settings - HAI - CDC|author=|date=|website=www.cdc.gov|accessdate=2 April 2018}}</ref> كما يمكنها الدخول من خلال الجروح المفتوحة والقسطرة وأنابيب التنفس.<ref>Multidrug-Resistant Acinetobacter baumannii (MDRAB).” WHO Western Pacific Region, WPRO | WHO Western Pacific Region, 1 Nov. 2010, www.wpro.who.int/mediacentre/factsheets/fs_20101102/en/.</ref> وفي دراسة أجريت على وحدات الرعاية المركزة الأوروبية في عام 2009، وجد أن بكتيريا الراكدة البومانية مسؤولة عن 19.1٪ من حالات [[الالتهاب الرئوي]] المرتبط ب[[التنفس الصناعي]].<ref>{{cite journal|last=Koulenti|first=D|author2=Lisboa, T |author3=Brun-Buisson, C |author4=Krueger, W |author5=Macor, A |author6=Sole-Violan, J |author7=Diaz, E |author8=Topeli, A |author9=DeWaele, J |author10=Carneiro, A |author11=Martin-Loeches, I |author12=Armaganidis, A |author13=Rello, J |others=EU-VAP/CAP Study, Group|title=Spectrum of practice in the diagnosis of nosocomial pneumonia in patients requiring mechanical ventilation in European intensive care units |journal=Critical Care Medicine|date=August 2009|volume=37|issue=8|pages=2360–8|pmid=19531951|doi=10.1097/ccm.0b013e3181a037ac}}</ref> |
|||
{| class="wikitable" |
|||
|+ دراسات حالات مُسجَلَة |
|||
|- |
|||
|- |
|||
! البلد !! المرجع |
|||
|- |
|||
| [[استراليا]] || <ref>{{cite journal|last=Ng|first=J|author2=Gosbell, IB|author3= Kelly, JA|author4= Boyle, MJ|author5= Ferguson, JK|title=Cure of multiresistant ''Acinetobacter baumannii'' central nervous system infections with intraventricular or intrathecal colistin: case series and literature review |journal=The Journal of Antimicrobial Chemotherapy|date=November 2006|volume=58|issue=5|pages=1078–81|pmid=16916866|doi=10.1093/jac/dkl347}}</ref><ref>{{cite journal|last=Farrugia|first=DN|author2=Elbourne, LD|author3=Hassan, KA|author4=Eijkelkamp, BA|author5=Tetu, SG|author6=Brown, MH|author7=Shah, BS|author8=Peleg, AY|author9=Mabbutt, BC|author10= Paulsen, IT|title=The Complete Genome and Phenome of a Community-Acquired ''Acinetobacter baumannii''|journal=PLoS ONE|year=2013|volume=8|issue=3|pages=e58628|pmid=23527001|bibcode=2013PLoSO...858628F|doi=10.1371/journal.pone.0058628|pmc=3602452}} {{open access}}</ref> |
|||
|- |
|||
| [[البرازيل]] || <ref>{{cite journal|last=Werneck|first=JS|author2=Picão, RC|author3= Carvalhaes, CG|author4= Cardoso, JP|author5= Gales, AC|title=OXA-72-producing ''Acinetobacter baumannii'' in Brazil: a case report |journal=The Journal of Antimicrobial Chemotherapy|date=February 2011|volume=66|issue=2|pages=452–4|pmid=21131320|doi=10.1093/jac/dkq462}}</ref><ref>{{cite journal|last=Martins|first=N|author2=Martins, IS |author3=de Freitas, WV |author4=de Matos, JA |author5=Magalhães, AC |author6=Girão, VB |author7=Dias, RC |author8=de Souza, TC |author9=Pellegrino, FL |author10=Costa, LD |author11=Boasquevisque, CH |author12=Nouér, SA |author13=Riley, LW |author14=Santoro-Lopes, G |author15=Moreira, BM |title=Severe infection in a lung transplant recipient caused by donor-transmitted carbapenem-resistant ''Acinetobacter baumannii'' |journal=Transplant Infectious Disease |date=June 2012|volume=14|issue=3 |pages=316–20 |pmid=22168176|doi=10.1111/j.1399-3062.2011.00701.x |pmc=3307813}}</ref><ref>{{cite journal|last=Superti|first=SV|author2=Martins Dde, S|author3= Caierão, J|author4= Soares Fda, S|author5= Prochnow, T|author6= Zavascki, AP|title=Indications of carbapenem resistance evolution through heteroresistance as an intermediate stage in ''Acinetobacter baumannii'' after carbapenem administration |journal=Revista do Instituto de Medicina Tropical de Sao Paulo|date=March–April 2009|volume=51|issue=2|pages=111–3|pmid=19390741|doi=10.1590/s0036-46652009000200010}}</ref><ref>{{cite journal|last=Gionco|first=B|author2=Pelayo, JS|author3= Venancio, EJ|author4= Cayô, R|author5= Gales, AC|author6= Carrara-Marroni, FE|title=Detection of OXA-231, a new variant of blaOXA-143, in ''Acinetobacter baumannii'' from Brazil: a case report |journal=The Journal of Antimicrobial Chemotherapy|date=October 2012|volume=67|issue=10|pages=2531–2|pmid=22736746|doi=10.1093/jac/dks223}}</ref> |
|||
|- |
|||
| [[الصين]] || <ref>{{cite journal|last=Zhao|first=WS|author2=Liu, GY|author3= Mi, ZH|author4= Zhang, F|title=Coexistence of blaOXA-23 with armA and novel gyrA mutation in a pandrug-resistant ''Acinetobacter baumannii'' isolate from the blood of a patient with haematological disease in China |journal=The Journal of Hospital Infection|date=March 2011|volume=77|issue=3|pages=278–9|pmid=21281989|doi=10.1016/j.jhin.2010.11.006}}</ref><ref>{{cite journal|last=Xiao|first=SC|author2=Zhu, SH|author3= Xia, ZF|author4= Ma, B|author5= Cheng, DS|title=Successful treatment of a critical burn patient with obstinate hyperglycemia and septic shock from pan-drug-resistant strains |journal=Medical Science Monitor |date=November 2009|volume=15|issue=11|pages=CS163–5|pmid=19865060}}</ref><ref>{{cite journal|last=Wu|first=YC|author2=Hsieh, TC|author3=Sun, SS|author4=Wang, CH|author5=Yen, KY|author6=Lin, YY|author7= Kao, CH|title=Unexpected cloud-like lesion on gallium-67 scintigraphy: detection of subcutaneous abscess underneath the skin with normal appearance in a comatose patient in an intensive care setting |journal=The American Journal of the Medical Sciences|date=November 2009|volume=338|issue=5|pages=388|pmid=19770790|doi=10.1097/maj.0b013e3181a6dd36}}</ref><ref>{{cite journal|last=Duan|first=X|author2=Yang, L|author3= Xia, P|title=Septic arthritis of the knee caused by antibiotic-resistant ''Acinetobacter baumannii'' in a gout patient: a rare case report |journal=Archives of Orthopaedic and Trauma Surgery|date=March 2010|volume=130|issue=3|pages=381–4|pmid=19707778|doi=10.1007/s00402-009-0958-x}}</ref> |
|||
|- |
|||
| [[ألمانيا]] || <ref name="JA Wagner">{{cite journal|last=Wagner|first=JA|author2=Nenoff, P|author3= Handrick, W|author4= Renner, R|author5= Simon, J|author6= Treudler, R|title=Necrotizing fasciitis caused by ''Acinetobacter baumannii'' : A case report |language=German |journal=Der Hautarzt; Zeitschrift für Dermatologie, Venerologie, und verwandte Gebiete|date=February 2011|volume=62|issue=2|pages=128–30|pmid=20835812|doi=10.1007/s00105-010-1962-3}}</ref><ref name="JA Wagner" /><ref>{{cite journal|last=Aivazova|first=V|author2=Kainer, F|author3= Friese, K|author4= Mylonas, I|title=''Acinetobacter baumannii'' infection during pregnancy and puerperium |journal=Archives of Gynecology and Obstetrics|date=January 2010|volume=281|issue=1|pages=171–4|pmid=19462176|doi=10.1007/s00404-009-1107-z}}</ref><ref>{{cite journal|last=Schulte|first=B|author2=Goerke, C|author3=Weyrich, P|author4=Gröbner, S|author5=Bahrs, C|author6=Wolz, C|author7=Autenrieth, IB|author8= Borgmann, S|title=Clonal spread of meropenem-resistant ''Acinetobacter baumannii'' strains in hospitals in the Mediterranean region and transmission to South-west Germany |journal=The Journal of Hospital Infection|date=December 2005|volume=61|issue=4|pages=356–7|pmid=16213625|doi=10.1016/j.jhin.2005.05.009}}</ref> |
|||
|- |
|||
| [[الهند]] || <ref>{{cite journal|last=Piparsania|first=S|author2=Rajput, N|author3= Bhatambare, G|title=Intraventricular polymyxin B for the treatment of neonatal meningo-ventriculitis caused by multi-resistant ''Acinetobacter baumannii''--case report and review of literature |journal= [[The Turkish Journal of Pediatrics]] |date=September–October 2012|volume=54|issue=5|pages=548–54|pmid=23427525}}</ref><ref>{{cite journal|last=John|first=TM|author2=Jacob, CN|author3=Ittycheria, CC|author4=George, AM|author5=Jacob, AG|author6=Subramaniyam, S|author7=Puthiyaveettil, J|author8= Jayaprakash, R|title=Macrophage activation syndrome following ''Acinetobacter baumannii'' sepsis |journal= International Journal of Infectious Diseases |date=March 2012|volume=16|issue=3|pages=e223–4|pmid=22285540|doi=10.1016/j.ijid.2011.12.002}}</ref><ref>{{cite journal|last=Sharma|first=A|author2=Shariff, M|author3= Thukral, SS|author4= Shah, A|title=Chronic community-acquired Acinetobacter pneumonia that responded slowly to rifampicin in the anti-tuberculous regime |journal=The Journal of Infection|date=October 2005|volume=51|issue=3|pages=e149–52|pmid=16230195|doi=10.1016/j.jinf.2004.12.003}}</ref> |
|||
|- |
|||
| [[جنوب كوريا]] || <ref>{{cite journal|last=Jeong|first=HL|author2=Yeom, JS|author3=Park, JS|author4=Seo, JH|author5=Park, ES|author6=Lim, JY|author7=Park, CH|author8=Woo, HO|author9= Youn, HS|title=''Acinetobacter baumannii'' isolation in cerebrospinal fluid in a febrile neonate|journal=The Turkish journal of Pediatrics|date=July–August 2011|volume=53|issue=4|pages=445–7|pmid=21980849}}</ref><ref>{{cite journal|last=Hong|first=KB|author2=Oh, HS|author3=Song, JS|author4=Lim, JH|author5=Kang, DK|author6=Son, IS|author7=Park, JD|author8=Kim, EC|author9=Lee, HJ|author10= Choi, EH|title=Investigation and control of an outbreak of imipenem-resistant ''Acinetobacter baumannii'' Infection in a Pediatric Intensive Care Unit |journal=The Pediatric Infectious Disease Journal|date=July 2012|volume=31|issue=7|pages=685–90|pmid=22466324|doi=10.1097/inf.0b013e318256f3e6}}</ref><ref>{{cite journal|last=Lee|first=YK|author2=Kim, JK|author3= Oh, SE|author4= Lee, J|author5= Noh, JW|title=Successful antibiotic lock therapy in patients with refractory peritonitis |journal=Clinical Nephrology|date=December 2009|volume=72|issue=6|pages=488–91|pmid=19954727|doi=10.5414/cnp72488}}</ref><ref>{{cite journal|last=Lee|first=SY|author2=Lee, JW|author3= Jeong, DC|author4= Chung, SY|author5= Chung, DS|author6= Kang, JH|title=Multidrug-resistant Acinetobacter meningitis in a 3-year-old boy treated with i.v. colistin |journal=Pediatrics International |date=August 2008|volume=50|issue=4|pages=584–5|pmid=18937759|doi=10.1111/j.1442-200x.2008.02677.x}}</ref> |
|||
|- |
|||
| [[المملكة المتحدة]] || <ref>{{cite journal|last=Adams|first=D|author2=Yee, L|author3= Rimmer, JA|author4= Williams, R|author5= Martin, H|author6= Ovington, C|title=Investigation and management of an A. Baumannii outbreak in ICU |journal=British Journal of Nursing |date=February 2011|volume=20|issue=3|pages=140, 142, 144–7|pmid=21378633|doi=10.12968/bjon.2011.20.3.140}}</ref><ref>{{cite journal|last=Pencavel|first=TD|author2=Singh-Ranger, G|author3= Crinnion, JN|title=Conservative treatment of an early aortic graft infection due to Acinetobacter baumanii |journal=Annals of Vascular Surgery|date=May 2006|volume=20|issue=3|pages=415–7|pmid=16602028|doi=10.1007/s10016-006-9030-2}}</ref> |
|||
|- |
|||
| [[الولايات المتحدة]] || <ref>{{cite journal|last=Gusten|first=WM|author2=Hansen, EA|author3= Cunha, BA|title=''Acinetobacter baumannii'' pseudomeningitis |journal=Heart & Lung |date=January–February 2002|volume=31|issue=1|pages=76–8|pmid=11805753|doi=10.1067/mhl.2002.120258}}</ref><ref>{{cite journal|last=Fitzpatrick|first=MA|author2=Esterly, JS|author3= Postelnick, MJ|author4= Sutton, SH|title=Successful treatment of extensively drug-resistant ''Acinetobacter baumannii'' peritoneal dialysis peritonitis with intraperitoneal polymyxin B and ampicillin-sulbactam|journal=Annals of Pharmacotherapy|date=July–August 2012|volume=46|issue=7–8|pages=e17|pmid=22811349|doi=10.1345/aph.1r086}}</ref><ref>{{cite journal|last=Patel|first=JA|author2=Pacheco, SM|author3= Postelnick, M|author4= Sutton, S|title=Prolonged triple therapy for persistent multidrug-resistant ''Acinetobacter baumannii'' ventriculitis |journal=American Journal of Health-System Pharmacy |date=15 August 2011|volume=68|issue=16|pages=1527–31|pmid=21817084|doi=10.2146/ajhp100234}}</ref><ref>{{cite journal|last=Sullivan|first=DR|author2=Shields, J|author3= Netzer, G|title=Fatal case of multi-drug resistant ''Acinetobacter baumannii'' necrotizing fasciitis |journal=The American Surgeon|date=June 2010|volume=76|issue=6|pages=651–3|pmid=20583528}}</ref> |
|||
|} |
|||
وأظهرت دراسة إندونيسية عام 2013 أن عدوى [[حديثي الولادة]] ببكتيريا الراكدة البومانية ترجع إلى نفس سلالات البكتيريا الموجودة في المستشفى والتي قضوا بها أيامهم الأولى، وتم العثور على هذه السلالات على الأسطح الصلبة وكذلك على أيدي العاملين في المجال الطبي.<ref>{{cite journal |vauthors=Tjoa E, Moehario LH, Rukmana A, Rohsiswatmo R | year = 2013 | title = ''Acinetobacter baumannii'': Role in Blood Stream Infection in Neonatal Unit, Cipto Mangunkusumo Hospital, Jakarta, Indonesia | journal = International Journal of Microbiology | volume = 2013 | page = 180763 | doi = 10.1155/2013/180763 |pmid=24288538 |pmc=3830835}}</ref> |
|||
== انظر أيضًا == |
== انظر أيضًا == |
||
نسخة 18:55، 27 نوفمبر 2018
راكدة بومانية | |
|---|---|
| المرتبة التصنيفية | نوع |
| التصنيف العلمي | |
| النطاق: | الجراثيم |
| المملكة: | بكتيريا |
| الشعبة: | المتقلبات |
| الطائفة: | متقلبات غاما |
| الرتبة: | الزوافات |
| الفصيلة: | الموراكسيلية |
| الجنس: | الراكدة |
| النوع: | راكدة بومانية |
| الاسم العلمي | |
| Acinetobacter baumannii [1] Bouvet & Grimont، 1986 |
|
| تعديل مصدري - تعديل | |
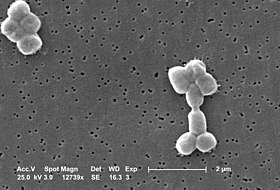
راكدة بومانية (الاسم العلمي:Acinetobacter baumannii) هي نوع من البكتيريا يتبع جنس الراكدة من الفصيلة الموراكسيلية[2] [3] . ومن أنواع البكتيريا الممرضة للإنسان، وهي بكتيريا لا هوائية سلبية الغرامي مقاومة للعديد من المضادات الحيوية ولذا فهي من الاصابات البكتيرية القاتلة وخصوصاً في إصابات المشافي.
تدخل هذه البكتيريا إلى جسم الإنسان عبر الجروح وأنابيب القسطرة وأنابيب التنفس، وتُصيب عادة المرضى ذوي المناعة المنخفضة وبإمكانها أن تنشئ مستعمرات غير خطيرة لدى الناس ذوي المناعة الطبيعية محولة إيَّأهم إلى ناقل خطير للمرض في حال كانوا من الكادر الطبي أو عمال المشافي. الإصابة بالأسنيتوباكتر بامانياي آخذة بالازدياد بشكل ملحوظ في المشافي في هذه الأيام، وهذا بسبب انها قادرة على العيش لخمسة أشهر على السطوح الغير ملموسة في حال توفر رطوبة مناسبة.
تصيب هذه البكتيريا المرضى بذات رئة شديدة وأحياناً قاتلة، وعلاجها يشكل تحدياً ومشكلة كبيرة في أغلب مشافي أوروبا والولايات المتحدة الأمريكية ويشكل الكاربابينيم الخط العلاجي الأول ويأتي بعده البوليميكسين والتيغيسيكلين والإمينوغليكوسيدات. وتجرى دراسات حالياً حول إنتاج بالع بكتيريا لمقاومة هذه البكتريا.
بروتين الغشاء الخارجي أ
يمكن أن يكون الالتصاق من العوامل الحاسمة في تحديد حدة البكتيريا، حيث تسمح القدرة على الارتباط بالخلايا المضيفة للبكتيريا بالتفاعل معها بطرق مختلفة، سواء عن طريق النظام الإفرازي الثالث في البكتيريا أو ببساطة من خلال التمسك بحركة السوائل السائدة. وقد ثبت أن بروتين الغشاء الخارجي (أ) يشارك في التصاق الراكدة البومانية إلى الخلايا الظهارية، مما يسمح للبكتيريا بغزو الخلايا من خلال آلية السوستة،[4] كما وُجِد أن البروتين يتوطن في ميتوكوندريا الخلايا الظهارية، ويسبب نخرها عن طريق تحفيز إنتاج أنواع الأكسجين التفاعلية.[5]
مقاومة المضادات الحيوية
جزر المقاومة AbaR
تتكون الجزر المرضية في البكتيريا، وهي هياكل وراثية شائعة نسبيا في مسببات الأمراض البكتيرية، من اثنين أو أكثر من الجينات المتجاورة التي تزيد من حدة الممرض. وقد تحتوي على جينات تشفر السموم أو تخثر الدم أو كما في تلك الحالة، تسمح للبكتيريا بمقاومة المضادات الحيوية. جزر المقاومة من نوع AbaR هي جزر نموذجية لمقاومة مضادات الراكدة البومانية مع اختلافات قد توجد في سلالة معينة. ويتكون كل منها من العمود الفقري للجينات القابلة للنقل التي تكون حوالي 16.3 كيلو بايت، مما يسهل نقل الجينات الأفقي. وتسمح الجينات القافزة بأخذ أجزاء من المواد الجينية من موضع ما في الجينوم ودمجها في موضع آخر، مما يجعل الانتقال الجيني الأفقي لهذه الجزر المسببة للأمراض المشابهة أكثر احتمالاً؛ لأنه عندما يتم أخذ مادة جينية بواسطة بكتيرة جديدة، تسمح الجينات القافزة للجزيرة الإمراضية بالاندماج في جينوم الكائنات الحية الدقيقة الجديدة. وفي هذه الحالة، يُمنَح الكائن الدقيق الجديد القدرة على مقاومة بعض المضادات الحيوية. وتحتوي AbaRs على العديد من الجينات لمقاومة المضادات الحيوية، وكلها محاطة بتتابعات الإدراج. وتوفر هذه الجينات مقاومة ضد الأمينوغليكوزيدات، وأمينوكليكليتول، والتتراسيكلين، والكلورامفينيكول.[6][7]
مضخات الإخراج
مضخات الإخراج هي عبارة عن آلات بروتينية تستخدم الطاقة لضخ المضادات الحيوية والجزيئات الصغيرة الأخرى التي تدخل في السيتوبلازم البكتيري والفضاء المحيطي خارج الخلية. ومن خلال ضخ المضادات الحيوية باستمرار خارج الخلية، يمكن للبكتيريا أن تزيد من تركيز المضاد الحيوي اللازم لقتلها أو تثبيط نموها عندما يكون الهدف من المضاد الحيوي العمل داخل البكتيريا. ومن المعروف أن الراكدة البومانية تمتلك مضختين ضخمتين رئيسيتين، مما يقلل من قابليتها لمضادات الميكروبات. وقد تبين أن أول جزيرة وهي AdeB هي المسؤولة عن مقاومة الأمينوغليكوزيد،[8] وثاني جزيرة AdeDE هي المسؤولة عن إخراج مجموعة واسعة من الركائز، بما في ذلك التتراسيكلين والكلورامفينيكول والكاربابينيمات المختلفة.[9]
الحمض النووي الريبي الصغير
الحمض النووي الريبوزي الميكروبي الصغير هو عبارة عن حمض نووي ريبوزي غير مشفر يقوم بتنظيم العمليات الخلوية المختلفة. وتم التحقق من صحة ثلاثة أنواع منه هي AbsR11 وAbsR25 وAbsR28 في سلالة MTCC 1425 (ATCC15308)، وهي سلالة (مقاومة للأدوية المتعددة) تُظهِر مقاومة لـ12 مضاد حيوي. ويمكن أن يلعب الحمض النووي الريبوزي من نوع AbsR25 دورًا في تنظيم المضخة الإخراجية ومقاومة الأدوية.[10]
بيتا لاكتاماز
لقد تم إثبات أن الراكدة البومانية تنتج على الأقل إنزيم بيتا لاكتاماز واحد، وهو إنزيم مسؤول عن شق حلقة اللاكتام ذات الأربع ذرات والمميزة للمضادات الحيوية المتعلقة بالبيتا لاكتام. وترتبط مضادات البيتا لاكتام هيكليا بالبنسلين، الذي يمنع تصنيع جدار الخلية البكتيرية. وشق حلقة اللاكتام يجعل هذه المضادات الحيوية غير ضارة للبكتيريا، وتم العثور على بيتا لاكتاماز OXA-23 محاطًا بمتتابعات الإدراج، مما يشير إلى أنه تم اكتسابها عن طريق نقل الجينات الأفقي.[11]
تشكيل البيوفيلم
قد لوحظت القدرة الظاهرية للراكدة البومانية على البقاء على الأسطح الاصطناعية لفترة طويلة من الزمن، مما يسمح لها بالعيش في بيئة المستشفى. ويعتقد أن ذلك يرجع إلى قدرتها على تشكيل الأغشية الحيوية (البيوفيلم).[12] وبالنسبة للعديد من البكتيريا المكونة للبيوفيلم، يتم توسط العملية بواسطة أسواط. وبالنسبة للراكدة البومانية، يبدو أن هذه العملية تتوسطها شعيرات. وقد تبين أن تعطيل الجينات المفترضة وجينات csuC وcsuE يثبط تشكيل الأغشية الحيوية،[13] كما تبين أن تشكيل الأغشية الحيوية يغير التمثيل الغذائي للكائنات الحية الدقيقة داخل البيوفيلم، وبالتالي تقليل حساسيتهم للمضادات الحيوية. وقد يكون ذلك بسبب وجود عدد أقل من العناصر المغذية داخل الغشاء الحيوي. ويمكن لعملية الأيض البطيئة أن تمنع البكتيريا من تناول مضاد حيوي أو أداء وظيفة حيوية بسرعة كافية لمضادات حيوية معينة ليكون لها تأثير. كما أنها توفر حاجزًا فعليًا ضد الجزيئات الكبيرة وقد تمنع جفاف البكتيريا.[14][15]
علامات وأعراض العدوى
الراكدة البومانية هي بكتيريا انتهازية تسبب مجموعة مختلفة الأمراض لكل منها أعراضها الخاصة، وبعض أنواع العدوى المحتملة تشمل:
- التهاب رئوي
- التهابات مجرى الدم
- التهاب السحايا
- التهابات الموقع الجراحي والجرح، بما في ذلك مرض أكل اللحم
- عدوى الجهاز البولي
غالبا لا يمكن تمييز أعراض عدوى الراكدة البومانية عن أنواع العدوى الانتهازية الأخرى التي تسببها بكتيريا انتهازية أخرى، بما في ذلك الكلبسيلة الرئوية والمكورة الرئوية.
ومن أعراض العدوى: الحمى، والقشعريرة، والطفح الجلدي، والارتباك و/أو الحالات العقلية المتغيرة، والألم عند التبول، والحاجة القوية للتبول بشكل متكرر، والحساسية للضوء الساطع، والغثيان (مع أو بدون القيء)، وآلام في العضلات والصدر، ومشاكل في التنفس، وسعال (مع أو بدون مخاط أصفر أو أخضر أو دموي).[16] وفي بعض الحالات، قد لا تظهر أية أعراض أو عدوى كما هو الحال مع استعمار جرح مفتوح أو موقع الرغامي.
العلاج
أصبح تحديد حساسية الدواء الخاص بالعدوى ضروريا لإنجاح العلاج؛ لأن معظم العدوى أصبحت الآن مقاومة للعديد من الأدوية. ويتم عادة علاج العدوى بالإيميبينيم أو ميروبينم، ولكن لوحظ ارتفاع مطرد في مقاومة الراكدة البومانية للكاربابينيم.[17] وبالتالي، فإن طرق العلاج غالبًا ما تعود إلى البوليميكسين، خاصة الكولستين.[18] ويعتبر الكوليستين الملاذ الأخير؛ لأنه غالبا ما يسبب تلف الكلى وغيرها من الآثار الجانبية الأخرى.[19] وتركز طرق الوقاية في المستشفيات على زيادة غسل اليدين وإجراءات التعقيم الأكثر جدية،[20] وتم علاج الراكدة البومانية مؤخرًا باستخدام العاثيات (الفيروسات المضادة للبكتيريا).[21]


حدوث العدوى في قدامى المحاربين المصابين في العراق وأفغانستان
يتعرض الجنود في العراق وأفغانستان لخطر الإصابات الناجمة عن إطلاق النار والعبوات الناسفة. وكان يعتقد في السابق أن العدوى تحدث بسبب التلوث بالراكدة البومانية في وقت الإصابة. وقد أظهرت دراسات لاحقة أنه على الرغم من أن الركدة البومانية قد تكون معزولة بشكل غير معتاد عن البيئة الطبيعية، فمن المرجح أن يتم اكتساب العدوى بشكل جزئي، ويرجع ذلك على الأرجح إلى قدرتها على العيش لفترات طويلة على الأسطح الاصطناعية والعديد من المرافق التي يتعرض الجنود المصابين لها خلال عملية إجلاء المصابين، حيث يتم نقل الجنود المصابين أولاً إلى المرافق من المستوى الأول بهدف استقرار حالاتهم. وبناءً على شدة الإصابة، يمكن نقل الجنود إلى مرفق من المستوى الثاني يتألف من فريق جراحي من أجل المزيد من الاستقرار. واعتمادا على الخدمات اللوجيستية للمحلية، قد يُنَقّل الجنود المصابون بين هذه المرافق عدة مرات قبل نقلهم إلى مستشفى رئيسي داخل منطقة القتال (المستوى الثالث). وبشكل عام بعد 1 - 3 أيام عندما يتم استقرار المرضى، يتم نقلهم عن طريق الجو إلى مرفق إقليمي (المستوى الرابع، حيث يتم أخيرا نقل الجنود المصابين إلى المستشفيات في بلدهم الأصلي لإعادة التأهيل والعلاج الإضافي.[22] ويبدو أن ذلك التعرض المتكرر للعديد من البيئات الطبية المختلفة هو السبب في أن عدوى الراكدة البومانية أصبحت شائعة بشكل متزايد، ومقاومتها للعديد من الأدوية هو عامل رئيسي في تعقيد علاج وإعادة تأهيل الجنود المصابين، مما أدى إلى المزيد من الوفيات.[23][24][25]
معدل الحدوث في المستشفيات
يُشار إلى أن عدوى الراكدة البومانية على أنها عدوى انتهازية، وهي منتشرة بشكل كبير في المستشفيات، ولا تُشكل سوى القليل من المخاطر على الأفراد الأصحاء،[26] ومع ذلك، تشمل العوامل التي تزيد من مخاطر الإصابة:
- وجود ضعف في جهاز المناعة
- أمراض الرئة المزمنة
- داء السكري
- الإقامة المطولة في المستشفى
- المرض الذي يتطلب استخدام جهاز التنفس الصناعي في المستشفى
- وجود جرح مفتوح يعالج في المستشفى
- العلاجات التي تتطلب أجهزة توغلية، مثل القسطرة البولية
ويمكن أن تنتشر الراكدة البومانية من خلال التلامس المباشر مع الأسطح والأجسام وبشرة الأشخاص الملوثين.[16]
ولقد تم توثيق استيراد البكتيريا إلى المستشفيات،[27] حيث يتم إدخالها عادة إلى المستشفى من قِبَل مريض مستعمر. وبسبب قدرتها على البقاء على الأسطح الاصطناعية ومقاومة التجفيف، يمكن أن تبقى وربما تصيب مرضى جدد لبعض الوقت. ويُشتبه في أن نموها يُفضَل في المستشفيات بسبب الاستخدام المستمر للمضادات الحيوية من قبل المرضى في المستشفى.[28] ويمكن أن تنتشر عن طريق الاتصال الشخصي مع المريض أو الاتصال بالأسطح الملوثة،[29] كما يمكنها الدخول من خلال الجروح المفتوحة والقسطرة وأنابيب التنفس.[30] وفي دراسة أجريت على وحدات الرعاية المركزة الأوروبية في عام 2009، وجد أن بكتيريا الراكدة البومانية مسؤولة عن 19.1٪ من حالات الالتهاب الرئوي المرتبط بالتنفس الصناعي.[31]
| البلد | المرجع |
|---|---|
| استراليا | [32][33] |
| البرازيل | [34][35][36][37] |
| الصين | [38][39][40][41] |
| ألمانيا | [42][42][43][44] |
| الهند | [45][46][47] |
| جنوب كوريا | [48][49][50][51] |
| المملكة المتحدة | [52][53] |
| الولايات المتحدة | [54][55][56][57] |
وأظهرت دراسة إندونيسية عام 2013 أن عدوى حديثي الولادة ببكتيريا الراكدة البومانية ترجع إلى نفس سلالات البكتيريا الموجودة في المستشفى والتي قضوا بها أيامهم الأولى، وتم العثور على هذه السلالات على الأسطح الصلبة وكذلك على أيدي العاملين في المجال الطبي.[58]
انظر أيضًا
وصلات خارجية
مراجع
- ^ "Species ''Acinetobacter baumannii''" (بالإنجليزية). LPSN. Retrieved 2020-03-31.
- ^ موقع تاكسونوميكون (بالإنكليزية) Taxonomicon راكدة بومانية تاريخ الولوج 10 أيار 2014 نسخة محفوظة 30 يونيو 2016 على موقع واي باك مشين.
- ^ قائمة أسماء بدائيات النوى مع جداول التعريف (بالإنكليزية) LPSN راكدة بومانية تاريخ الولوج 10 أيار 2014 نسخة محفوظة 06 يوليو 2017 على موقع واي باك مشين.
- ^ Choi، CH؛ Lee, JS؛ Lee, YC؛ Park, TI؛ Lee, JC (10 ديسمبر 2008). "Acinetobacter baumannii invades epithelial cells and outer membrane protein A mediates interactions with epithelial cells". BMC Microbiology. ج. 8: 216. DOI:10.1186/1471-2180-8-216. PMC:2615016. PMID:19068136.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Lee، JS؛ Choi, CH؛ Kim, JW؛ Lee, JC (يونيو 2010). "Acinetobacter baumannii outer membrane protein A induces dendritic cell death through mitochondrial targeting". Journal of Microbiology. ج. 48 ع. 3: 387–92. DOI:10.1007/s12275-010-0155-1. PMID:20571958.
- ^ Seputiene، V.؛ Povilonis, J.؛ Suziedeliene, E. (30 يناير 2012). "Novel Variants of AbaR Resistance Islands with a Common Backbone in Acinetobacter baumannii Isolates of European Clone II". Antimicrobial Agents and Chemotherapy. ج. 56 ع. 4: 1969–1973. DOI:10.1128/AAC.05678-11. PMC:3318354. PMID:22290980.
- ^ Post، V؛ White, PA؛ Hall, RM (يونيو 2010). "Evolution of AbaR-type genomic resistance islands in multiply antibiotic-resistant Acinetobacter baumannii". The Journal of Antimicrobial Chemotherapy. ج. 65 ع. 6: 1162–70. DOI:10.1093/jac/dkq095. PMID:20375036.
- ^ Magnet، S؛ Courvalin, P؛ Lambert, T (ديسمبر 2001). "Resistance-nodulation-cell division-type efflux pump involved in aminoglycoside resistance in Acinetobacter baumannii strain BM4454". Antimicrobial Agents and Chemotherapy. ج. 45 ع. 12: 3375–80. DOI:10.1128/aac.45.12.3375-3380.2001. PMC:90840. PMID:11709311.
- ^ Chau، SL؛ Chu, YW؛ Houang, ET (أكتوبر 2004). "Novel resistance-nodulation-cell division efflux system AdeDE in Acinetobacter genomic DNA group 3". Antimicrobial Agents and Chemotherapy. ج. 48 ع. 10: 4054–5. DOI:10.1128/aac.48.10.4054-4055.2004. PMC:521926. PMID:15388479.
- ^ Sharma، Rajnikant؛ Arya، Sankalp؛ Patil، Supriya Deepak؛ Sharma، Atin؛ Jain، Pradeep Kumar؛ Navani، Naveen Kumar؛ Pathania، Ranjana (1 يناير 2014). "Identification of novel regulatory small RNAs in Acinetobacter baumannii". PLoS One. ج. 9 ع. 4: e93833. Bibcode:2014PLoSO...993833S. DOI:10.1371/journal.pone.0093833. ISSN:1932-6203. PMC:3976366. PMID:24705412.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Higgins، PG؛ Pérez-Llarena, FJ؛ Zander, E؛ Fernández, A؛ Bou, G؛ Seifert, H (25 فبراير 2013). "OXA-235, a novel Class D Beta-Lactamase Involved in Resistance to Carbapenems in Acinetobacter baumannii". Antimicrobial Agents and Chemotherapy. ج. 57 ع. 5: 2121–6. DOI:10.1128/AAC.02413-12. PMC:3632948. PMID:23439638.
- ^ Espinal، P؛ Martí, S؛ Vila, J (يناير 2012). "Effect of biofilm formation on the survival of Acinetobacter baumannii on dry surfaces". The Journal of Hospital Infection. ج. 80 ع. 1: 56–60. DOI:10.1016/j.jhin.2011.08.013. PMID:21975219.
- ^ Tomaras، AP؛ Dorsey, CW؛ Edelmann, RE؛ Actis, LA (ديسمبر 2003). "Attachment to and biofilm formation on abiotic surfaces by Acinetobacter baumannii: involvement of a novel chaperone-usher pili assembly system". Microbiology. ج. 149 ع. Pt 12: 3473–84. DOI:10.1099/mic.0.26541-0. PMID:14663080.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعJ. Yeom - ^ Worthington، RJ؛ Richards, JJ؛ Melander, C (7 أكتوبر 2012). "Small molecule control of bacterial biofilms". Organic & Biomolecular Chemistry. ج. 10 ع. 37: 7457–74. DOI:10.1039/c2ob25835h. PMC:3431441. PMID:22733439.
- ^ أ ب "What Is Acinetobacter Baumannii?". Everyday Health. اطلع عليه بتاريخ 2017-04-18.
- ^ Su، CH؛ Wang، JT؛ Hsiung، CA؛ Chien، LJ؛ Chi، CL؛ Yu، HT؛ Chang، FY؛ Chang، SC (2012). "Increase of carbapenem-resistant Acinetobacter baumannii infection in acute care hospitals in Taiwan: Association with hospital antimicrobial usage". بلوس ون. ج. 7 ع. 5: e37788. Bibcode:2012PLoSO...737788S. DOI:10.1371/journal.pone.0037788. PMC:3357347. PMID:22629456.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|displayauthors=تم تجاهله يقترح استخدام|إظهار المؤلفين=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Abbo، A؛ Navon-Venezia، S؛ Hammer-Muntz، O؛ Krichali، T؛ Siegman-Igra، Y؛ Carmeli، Y (يناير 2005). "Multidrug-resistant Acinetobacter baumannii". Emerging Infectious Diseases. ج. 11 ع. 1: 22–9. DOI:10.3201/eid1101.040001. PMC:3294361. PMID:15705318.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|displayauthors=تم تجاهله يقترح استخدام|إظهار المؤلفين=(مساعدة) - ^ Spapen، H؛ Jacobs، R؛ Van Gorp، V؛ Troubleyn، J؛ Honoré، PM (25 مايو 2011). "Renal and neurological side effects of colistin in critically ill patients". Annals of Intensive Care. ج. 1 ع. 1: 14. DOI:10.1186/2110-5820-1-14. PMC:3224475. PMID:21906345.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|displayauthors=تم تجاهله يقترح استخدام|إظهار المؤلفين=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Acinetobacter in Healthcare Settings". CDC. اطلع عليه بتاريخ 2013-04-08.
- ^ "He was dying. Antibiotics weren't working. Then doctors tried a forgotten treatment". Mother Jones (بالإنجليزية الأمريكية). Retrieved 2018-05-17.
- ^ "Army Medical Logistics" (PDF). FM 4-02.1. United States. مؤرشف من الأصل (PDF) في 2013-03-23. اطلع عليه بتاريخ 2013-04-08.
{{استشهاد ويب}}: الوسيط غير المعروف|dead-url=تم تجاهله (مساعدة) - ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعMK O'Shea - ^ Meghoo، CA؛ Dennis, JW؛ Tuman, C؛ Fang, R (مايو 2012). "Diagnosis and management of evacuated casualties with cervical vascular injuries resulting from combat-related explosive blasts". Journal of Vascular Surgery. ج. 55 ع. 5: 1329–36, discussion 1336–7. DOI:10.1016/j.jvs.2011.11.125. PMID:22325667.
- ^ Murray، CK (مارس 2008). "Epidemiology of infections associated with combat-related injuries in Iraq and Afghanistan". The Journal of Trauma. ج. 64 ع. 3 Suppl: S232–8. DOI:10.1097/ta.0b013e318163c3f5. PMID:18316967.
- ^ "Acinetobacter in Healthcare Settings". Centers for Disease Control and Prevention. US Department of Health and Human Services. اطلع عليه بتاريخ 2017-04-18.
- ^ Jones، A؛ Morgan, D؛ Walsh, A؛ Turton, J؛ Livermore, D؛ Pitt, T؛ Green, A؛ Gill, M؛ Mortiboy, D (يونيو 2006). "Importation of multidrug-resistant Acinetobacter spp infections with casualties from Iraq". The Lancet Infectious Diseases. ج. 6 ع. 6: 317–8. DOI:10.1016/S1473-3099(06)70471-6. PMID:16728314.
- ^ Dijkshoorn، L؛ Nemec, A؛ Seifert, H (ديسمبر 2007). "An increasing threat in hospitals: multidrug-resistant Acinetobacter baumannii". Nature Reviews Microbiology. ج. 5 ع. 12: 939–51. DOI:10.1038/nrmicro1789. PMID:18007677.
- ^ "Acinetobacter in Healthcare Settings - HAI - CDC". www.cdc.gov. اطلع عليه بتاريخ 2018-04-02.
- ^ Multidrug-Resistant Acinetobacter baumannii (MDRAB).” WHO Western Pacific Region, WPRO | WHO Western Pacific Region, 1 Nov. 2010, www.wpro.who.int/mediacentre/factsheets/fs_20101102/en/.
- ^ Koulenti، D؛ Lisboa, T؛ Brun-Buisson, C؛ Krueger, W؛ Macor, A؛ Sole-Violan, J؛ Diaz, E؛ Topeli, A؛ DeWaele, J؛ Carneiro, A؛ Martin-Loeches, I؛ Armaganidis, A؛ Rello, J (أغسطس 2009). "Spectrum of practice in the diagnosis of nosocomial pneumonia in patients requiring mechanical ventilation in European intensive care units". Critical Care Medicine. EU-VAP/CAP Study, Group. ج. 37 ع. 8: 2360–8. DOI:10.1097/ccm.0b013e3181a037ac. PMID:19531951.
- ^ Ng، J؛ Gosbell, IB؛ Kelly, JA؛ Boyle, MJ؛ Ferguson, JK (نوفمبر 2006). "Cure of multiresistant Acinetobacter baumannii central nervous system infections with intraventricular or intrathecal colistin: case series and literature review". The Journal of Antimicrobial Chemotherapy. ج. 58 ع. 5: 1078–81. DOI:10.1093/jac/dkl347. PMID:16916866.
- ^ Farrugia، DN؛ Elbourne, LD؛ Hassan, KA؛ Eijkelkamp, BA؛ Tetu, SG؛ Brown, MH؛ Shah, BS؛ Peleg, AY؛ Mabbutt, BC؛ Paulsen, IT (2013). "The Complete Genome and Phenome of a Community-Acquired Acinetobacter baumannii". PLoS ONE. ج. 8 ع. 3: e58628. Bibcode:2013PLoSO...858628F. DOI:10.1371/journal.pone.0058628. PMC:3602452. PMID:23527001.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link)
- ^ Werneck، JS؛ Picão, RC؛ Carvalhaes, CG؛ Cardoso, JP؛ Gales, AC (فبراير 2011). "OXA-72-producing Acinetobacter baumannii in Brazil: a case report". The Journal of Antimicrobial Chemotherapy. ج. 66 ع. 2: 452–4. DOI:10.1093/jac/dkq462. PMID:21131320.
- ^ Martins، N؛ Martins, IS؛ de Freitas, WV؛ de Matos, JA؛ Magalhães, AC؛ Girão, VB؛ Dias, RC؛ de Souza, TC؛ Pellegrino, FL؛ Costa, LD؛ Boasquevisque, CH؛ Nouér, SA؛ Riley, LW؛ Santoro-Lopes, G؛ Moreira, BM (يونيو 2012). "Severe infection in a lung transplant recipient caused by donor-transmitted carbapenem-resistant Acinetobacter baumannii". Transplant Infectious Disease. ج. 14 ع. 3: 316–20. DOI:10.1111/j.1399-3062.2011.00701.x. PMC:3307813. PMID:22168176.
- ^ Superti، SV؛ Martins Dde, S؛ Caierão, J؛ Soares Fda, S؛ Prochnow, T؛ Zavascki, AP (مارس–أبريل 2009). "Indications of carbapenem resistance evolution through heteroresistance as an intermediate stage in Acinetobacter baumannii after carbapenem administration". Revista do Instituto de Medicina Tropical de Sao Paulo. ج. 51 ع. 2: 111–3. DOI:10.1590/s0036-46652009000200010. PMID:19390741.
- ^ Gionco، B؛ Pelayo, JS؛ Venancio, EJ؛ Cayô, R؛ Gales, AC؛ Carrara-Marroni, FE (أكتوبر 2012). "Detection of OXA-231, a new variant of blaOXA-143, in Acinetobacter baumannii from Brazil: a case report". The Journal of Antimicrobial Chemotherapy. ج. 67 ع. 10: 2531–2. DOI:10.1093/jac/dks223. PMID:22736746.
- ^ Zhao، WS؛ Liu, GY؛ Mi, ZH؛ Zhang, F (مارس 2011). "Coexistence of blaOXA-23 with armA and novel gyrA mutation in a pandrug-resistant Acinetobacter baumannii isolate from the blood of a patient with haematological disease in China". The Journal of Hospital Infection. ج. 77 ع. 3: 278–9. DOI:10.1016/j.jhin.2010.11.006. PMID:21281989.
- ^ Xiao، SC؛ Zhu, SH؛ Xia, ZF؛ Ma, B؛ Cheng, DS (نوفمبر 2009). "Successful treatment of a critical burn patient with obstinate hyperglycemia and septic shock from pan-drug-resistant strains". Medical Science Monitor. ج. 15 ع. 11: CS163–5. PMID:19865060.
- ^ Wu، YC؛ Hsieh, TC؛ Sun, SS؛ Wang, CH؛ Yen, KY؛ Lin, YY؛ Kao, CH (نوفمبر 2009). "Unexpected cloud-like lesion on gallium-67 scintigraphy: detection of subcutaneous abscess underneath the skin with normal appearance in a comatose patient in an intensive care setting". The American Journal of the Medical Sciences. ج. 338 ع. 5: 388. DOI:10.1097/maj.0b013e3181a6dd36. PMID:19770790.
- ^ Duan، X؛ Yang, L؛ Xia, P (مارس 2010). "Septic arthritis of the knee caused by antibiotic-resistant Acinetobacter baumannii in a gout patient: a rare case report". Archives of Orthopaedic and Trauma Surgery. ج. 130 ع. 3: 381–4. DOI:10.1007/s00402-009-0958-x. PMID:19707778.
- ^ أ ب Wagner, JA; Nenoff, P; Handrick, W; Renner, R; Simon, J; Treudler, R (Feb 2011). "Necrotizing fasciitis caused by Acinetobacter baumannii : A case report". Der Hautarzt; Zeitschrift für Dermatologie, Venerologie, und verwandte Gebiete (بالألمانية). 62 (2): 128–30. DOI:10.1007/s00105-010-1962-3. PMID:20835812.
- ^ Aivazova، V؛ Kainer, F؛ Friese, K؛ Mylonas, I (يناير 2010). "Acinetobacter baumannii infection during pregnancy and puerperium". Archives of Gynecology and Obstetrics. ج. 281 ع. 1: 171–4. DOI:10.1007/s00404-009-1107-z. PMID:19462176.
- ^ Schulte، B؛ Goerke, C؛ Weyrich, P؛ Gröbner, S؛ Bahrs, C؛ Wolz, C؛ Autenrieth, IB؛ Borgmann, S (ديسمبر 2005). "Clonal spread of meropenem-resistant Acinetobacter baumannii strains in hospitals in the Mediterranean region and transmission to South-west Germany". The Journal of Hospital Infection. ج. 61 ع. 4: 356–7. DOI:10.1016/j.jhin.2005.05.009. PMID:16213625.
- ^ Piparsania، S؛ Rajput, N؛ Bhatambare, G (سبتمبر–أكتوبر 2012). "Intraventricular polymyxin B for the treatment of neonatal meningo-ventriculitis caused by multi-resistant Acinetobacter baumannii--case report and review of literature". The Turkish Journal of Pediatrics. ج. 54 ع. 5: 548–54. PMID:23427525.
- ^ John، TM؛ Jacob, CN؛ Ittycheria, CC؛ George, AM؛ Jacob, AG؛ Subramaniyam, S؛ Puthiyaveettil, J؛ Jayaprakash, R (مارس 2012). "Macrophage activation syndrome following Acinetobacter baumannii sepsis". International Journal of Infectious Diseases. ج. 16 ع. 3: e223–4. DOI:10.1016/j.ijid.2011.12.002. PMID:22285540.
- ^ Sharma، A؛ Shariff, M؛ Thukral, SS؛ Shah, A (أكتوبر 2005). "Chronic community-acquired Acinetobacter pneumonia that responded slowly to rifampicin in the anti-tuberculous regime". The Journal of Infection. ج. 51 ع. 3: e149–52. DOI:10.1016/j.jinf.2004.12.003. PMID:16230195.
- ^ Jeong، HL؛ Yeom, JS؛ Park, JS؛ Seo, JH؛ Park, ES؛ Lim, JY؛ Park, CH؛ Woo, HO؛ Youn, HS (يوليو–أغسطس 2011). "Acinetobacter baumannii isolation in cerebrospinal fluid in a febrile neonate". The Turkish journal of Pediatrics. ج. 53 ع. 4: 445–7. PMID:21980849.
- ^ Hong، KB؛ Oh, HS؛ Song, JS؛ Lim, JH؛ Kang, DK؛ Son, IS؛ Park, JD؛ Kim, EC؛ Lee, HJ؛ Choi, EH (يوليو 2012). "Investigation and control of an outbreak of imipenem-resistant Acinetobacter baumannii Infection in a Pediatric Intensive Care Unit". The Pediatric Infectious Disease Journal. ج. 31 ع. 7: 685–90. DOI:10.1097/inf.0b013e318256f3e6. PMID:22466324.
- ^ Lee، YK؛ Kim, JK؛ Oh, SE؛ Lee, J؛ Noh, JW (ديسمبر 2009). "Successful antibiotic lock therapy in patients with refractory peritonitis". Clinical Nephrology. ج. 72 ع. 6: 488–91. DOI:10.5414/cnp72488. PMID:19954727.
- ^ Lee، SY؛ Lee, JW؛ Jeong, DC؛ Chung, SY؛ Chung, DS؛ Kang, JH (أغسطس 2008). "Multidrug-resistant Acinetobacter meningitis in a 3-year-old boy treated with i.v. colistin". Pediatrics International. ج. 50 ع. 4: 584–5. DOI:10.1111/j.1442-200x.2008.02677.x. PMID:18937759.
- ^ Adams، D؛ Yee, L؛ Rimmer, JA؛ Williams, R؛ Martin, H؛ Ovington, C (فبراير 2011). "Investigation and management of an A. Baumannii outbreak in ICU". British Journal of Nursing. ج. 20 ع. 3: 140, 142, 144–7. DOI:10.12968/bjon.2011.20.3.140. PMID:21378633.
- ^ Pencavel، TD؛ Singh-Ranger, G؛ Crinnion, JN (مايو 2006). "Conservative treatment of an early aortic graft infection due to Acinetobacter baumanii". Annals of Vascular Surgery. ج. 20 ع. 3: 415–7. DOI:10.1007/s10016-006-9030-2. PMID:16602028.
- ^ Gusten، WM؛ Hansen, EA؛ Cunha, BA (يناير–فبراير 2002). "Acinetobacter baumannii pseudomeningitis". Heart & Lung. ج. 31 ع. 1: 76–8. DOI:10.1067/mhl.2002.120258. PMID:11805753.
- ^ Fitzpatrick، MA؛ Esterly, JS؛ Postelnick, MJ؛ Sutton, SH (يوليو–أغسطس 2012). "Successful treatment of extensively drug-resistant Acinetobacter baumannii peritoneal dialysis peritonitis with intraperitoneal polymyxin B and ampicillin-sulbactam". Annals of Pharmacotherapy. ج. 46 ع. 7–8: e17. DOI:10.1345/aph.1r086. PMID:22811349.
- ^ Patel، JA؛ Pacheco, SM؛ Postelnick, M؛ Sutton, S (15 أغسطس 2011). "Prolonged triple therapy for persistent multidrug-resistant Acinetobacter baumannii ventriculitis". American Journal of Health-System Pharmacy. ج. 68 ع. 16: 1527–31. DOI:10.2146/ajhp100234. PMID:21817084.
- ^ Sullivan، DR؛ Shields, J؛ Netzer, G (يونيو 2010). "Fatal case of multi-drug resistant Acinetobacter baumannii necrotizing fasciitis". The American Surgeon. ج. 76 ع. 6: 651–3. PMID:20583528.
- ^ Tjoa E، Moehario LH، Rukmana A، Rohsiswatmo R (2013). "Acinetobacter baumannii: Role in Blood Stream Infection in Neonatal Unit, Cipto Mangunkusumo Hospital, Jakarta, Indonesia". International Journal of Microbiology. ج. 2013: 180763. DOI:10.1155/2013/180763. PMC:3830835. PMID:24288538.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link)
| في كومنز صور وملفات عن: راكدة بومانية |