أكسازول
| أكسازول | |
|---|---|
 |
 |
 |
 |
| الاسم النظامي (IUPAC) | |
1,3-oxazole |
|
| المعرفات | |
| رقم CAS | 288-42-6 |
| بوب كيم (PubChem) | 9255 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | C3H3NO |
| الكتلة المولية | 69.06 غ/مول |
| المظهر | سائل |
| الكثافة | 1.05 غ/سم3 |
| نقطة الانصهار | −84 °س |
| نقطة الغليان | 69–70 °س |
| حموضة (pKa) | 0.8 (للحمض المرافق) [3] |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
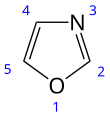
أكسازول هو مركب عضوي حلقي غير متجانس وغير مشبع له الصيغة الكيميائية C3H3NO، وينتمي إلى مجموعة الآزولات.
يتألف المركب بنيوياً من حلقة خماسية حاوية على ذرتين غير متجانستين، ذرة نتروجين وذرة أكسجين، يفصل بينهما ذرة كربون؛[4] بالإضافة إلى وجود رابطتين مضاعفتين؛ ويطلق على مشتقاته اسم أكسازولات. يوجد هناك متصاوغ للمركب، وهو إيزوكسازول.
التحضير[عدل]
يحضر أكسازول ومشتقاته بعدة طرق معروفة، منها اصطناع روبنسون-غابرييل Robinson–Gabriel synthesis واصطناع فيشر للأكسازول Fischer oxazole synthesis، بالإضافة إلى تفاعل فان لويزن Van Leusen reaction.
كما يمكن أن تتم عملية التحضير بطريقة أخرى انطلاقاً من مركبات أميدات البروبارجيل Propargyl؛ ففي واحدة من الدراسات،[5] تم تحضير الأكسازولات بأسلوب اصطناع القدر الواحد بإجراء تفاعل تكاثف بين أمينات البروبارجيل وكلوريد البنزويل، متبوعاً بتفاعل ازدواج سونوغاشيرا Sonogashira coupling للألكاين الطرفي، ثم بالمعالجة بمركب بارا-تولوين حمض السلفونيك (TsOH).
في طريقة أخرى يتم الانطلاق بالتفاعل بين مركبات نترو كلوريد البنزويل وإيزوسيانيد:[6]
أما الاصطناع الحيوي فيتم انطلاقاً من تفاعل تحلّق وأكسدة السيرين أو الثريونين.
الخواص[عدل]
يخضع الأكسازول للعديد من التفاعلات، منها تفاعل نزع بروتون مترافق مع فتح الحلقة إلى مركب إيزونتريل؛ وتفاعل استبدال عطري محب للإلكترونات بوجود مجموعات منشطة؛ وتفاعل استبدال عطري محب للنوى، بالإضافة إلى تفاعل ديلز-ألدر.
اقرا أيضاً[عدل]
المراجع[عدل]
- ^ أ ب ت OXAZOLE (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Zoltewicz, J. A. & Deady, L. W. Quaternization of heteroaromatic compounds. Quantitative aspects. Adv. Heterocycl. Chem. 22, 71-121 (1978).
- ^ Heterocyclic Chemistry TL Gilchrist, The Bath press 1985 ISBN 0-582-01421-2
- ^ A new consecutive three-component oxazole synthesis by an amidation–coupling–cycloisomerization (ACCI) sequence Eugen Merkul and Thomas J. J. Müller, Chem. Commun., 2006, 4817 - 4819, دُوِي:10.1039/b610839c
- ^ Fully Automated Continuous Flow Synthesis of 4,5-Disubstituted Oxazoles Marcus Baumann, Ian R. Baxendale, Steven V. Ley, Christoper D. Smith, and Geoffrey K. Tranmer, Org. Lett.; 2006; 8(23) pp 5231 - 5234; (Letter) دُوِي:10.1021/ol061975c
| في كومنز صور وملفات عن: أكسازول |



