بيناكولون
| بيناكولون | |
|---|---|
| الاسم النظامي (IUPAC) | |
3,3-Dimethyl-2-butanone |
|
| أسماء أخرى | |
t-Butyl methyl ketone |
|
| المعرفات | |
| رقم CAS | 75-97-8 |
| بوب كيم (PubChem) | 6416 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C6H12O |
| كتلة مولية | 100.16 غ.مول−1 |
| المظهر | Colorless liquid |
| الكثافة | 0.801 g cm−3 |
| نقطة الانصهار | -52[1] °س، خطأ في التعبير: علامة ترقيم لم نتعرف عليها «». °ك، خطأ في التعبير: علامة ترقيم لم نتعرف عليها «». °ف |
| نقطة الغليان | 103 to 106 °س، خطأ في التعبير: كلمة لم نتعرف عليها «to». °ك، خطأ في التعبير: كلمة لم نتعرف عليها «to». °ف |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| NFPA 704 |
|
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
بيناكولون (3,3-ثنائي ميثيل-2-بونانون) كيتون مهم في الكيمياء العضوية. وهو سائل عديم اللون ويمتاز برائحته التي تشبه رائحة النعناع أو الكمفور. يعد البيناكولون مادة بادئة لـ triazolylpinacolone المستخدم في صناعة مضاد الفطريات التريادمفون.
البيناكولون كيتون غير متناظر، ويمكن لمجموعة الألفا - مثيل أن تشارك في تفاعلات التكثيف، كما يمكن لمجموعة الكاربونيل أن تدخل في تفاعلاتها الاعتيادية (مثل الهدرجة، والإضافة الأمينية الاختزالية، الخ..).
التحضير[عدل]
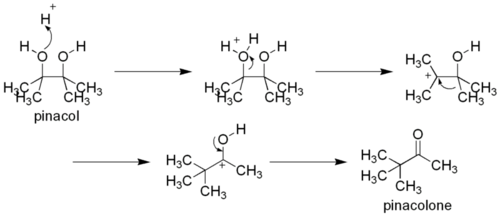
من أشهر طرق تحضير البيناكولون هي عملية إعادة ترتيب البيناكول، والتي تحدث عن طريق برتنة البيناكول (2,3-dimethylbutane-2,3-diol).[2]
يحضر البيناكولون صناعياً من التحلل المائي لـ 4,4,5-trimethyl-1,3-dioxane وهو ناتج تفاعل الآيزوبرين مع الفورمالديهايد فيما يدعى بتفاعل برنس. كما يحضّر من إضافة مجموعة الكيتون إلى حمض البيفاليك أو حمض الخليك أو الأسيتون على عامل مساعد من أكسيد الفلز.
يستخدم 3-Methylbutanal كمادة بادئة لتحضير 2,3-dimethyl-2-butene والذي يُحوَّل بدوره إلى البيناكولون. يمكن كذلك تحضير البيناكولون من 2-methy-2-butanol بعد مفاعلته مع كحول خماسي ذرات الكاربون.[3]
الاستخدامات[عدل]
تنتج كميات كبيرة من البيناكولون لاستخدامها في مضادات الفطريات ومضادات الأعشاب الضارة ومبيدات الحشرات.
المراجع[عدل]
- ^ Pinacolone | C6H12O | ChemSpider نسخة محفوظة 2016-05-08 في Wayback Machine
- ^ G. A. Hill and E. W. Flosdorf(1941)."Pinacolone". Org. Synth.; Coll. Vol. 1: 462.
- ^ Siegel، H؛ Eggersdorfer (2012). "Ketones". Ullman's Encyclopedia of Chemistry. 5. ج. 20 ع. 6. DOI:10.1002/14356007.a15_077.
{{استشهاد بدورية محكمة}}: الوسيط|تاريخ الوصولبحاجة لـ|مسار=(مساعدة)
| بيناكولون في المشاريع الشقيقة: | |
| |