أكاسيد الكوبالت والمنغنيز والنيكل والليثيوم
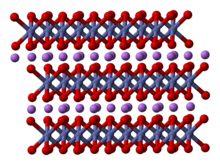
أكاسيد الكوبالت ليثيوم نيكل منغنيز (المختصرة Li-NMC أو LNMC أو NMC ) في بطاريات السيارات ؛ هي أكاسيد معدنية مختلطة من الليثيوم والنيكل والمنغنيز والكوبالت . لديهم الصيغة الكيميائية العامة LiNi x Mn y Co z O 2 . أهم المواد فيها لديهم تركيبة x + y + z قريبة من 1 ، مع كمية صغيرة من الليثيوم في موقع المعدن الانتقالي. في عينات NMC التجارية ، تحتوي التركيبة عادةً على أقل من 5٪ فائض من الليثيوم.[1][2] ترتبط المواد الهيكلية في هذه المجموعة ارتباطًا وثيقًا بأكسيد الليثيوم والكوبالت (III) (LiCoO 2 ) ولها هيكل متعدد الطبقات ولكنها تمتلك توزيعًا مثاليًا لشحنة Mn (IV) و Co (III) و Ni (II) بنسبة 1: 1: 1 . لمزيد من التركيبات الغنية بالنيكل يكون النيكل في حالة أكسدة أكثر للعمل على توازن الشحنة الكهربية . تعد مركمات NMCs من بين أهم مركمات تخزين أيونات الليثيوم في بطاريات أيونات الليثيوم. تستخدم على القطب الموجب الذي يعمل ككاثود (مهبط) أثناء التفريغ.

تلك البطاريات تستخدم لتشغيل السيارات الكهربائية ، فهي بطاريات كبيرة وعبارة عن مركمات تخزن الطاقة الكهربائية لتسيير سيارة كهربائية ثم يُعاد شحنها مرارا وتكرارا.
ومنها ما هو الصغير الذي يعمل في هاتف المحمول.
خصائصها[عدل]
والأهم من ذلك ، لأن الخاصية المفيدة لأكاسيد نوع NMC هي أن أكاسيد الليثيوم المختلطة هذه يمكنها ان تمنح أيونات ليثيوم و إلكترون ، ثم تكتسبهما ثانيا. عند شحن بطارية NMC ، يفرض الجهد الخارجي إطلاق الإلكترونات وبالتالي تحرير أيون Li + أيضًا. طبقا للتفاعل الكيميائي التالي:
التركيبة NMC مؤكسدة. وعند التفريغ ، يحدث التفاعل في الاتجاه المعاكس وفي نفس الوقت يطلق طاقة كهربائية. غالبًا ما يكون للمتغير في معادلة التفاعل القيمة الأولى عند تجميع الخلايا. والمتغير له قيمة أقل بكثير من وبالتالي أقل من واحد ، أي لا يمكنك استخراج كل الليثيوم من الأكسيد عند الجهد (الفولتية] الشائع للاستخدام. عادةً ما يقتصر جهد شحن بطاريات NMC على 4.2 فولت لمنع تحلل الإلكتروليت (الكهرل). وقد تعمل NMC نفسها أيضًا بجهد أعلى ، على سبيل المثال يتم تحديد أقصى جهد شحن قدره 4.8 فولت لمتغير واحد ، حيث يمكن تحقيق سعة 210 مللي أمبير / جرام .[3]
التاريخ[عدل]
يتم تمثيل كاثودات NMC المتكافئة كنقاط في المحلول الصلب بين الأعضاء النهائيين LiCoO2 و LiMnO2 و LiNiO2 . وهي مشتقة تاريخيًا من أعمال جون ب. غودينوف من عمله في عام 1980 على. [4][5] LiCoO2, وعمل Tsutomo Ohzuku على Li(NiMn)O2, واعمال أخري متعلقة بـ ل NaFeO2 . فيما يتعلق بالمقاييس المتكافئة stoichiometric NMCs تم نشر بحوث عن مواد NMC الغنية بالليثيوم لأول مرة في عام 1998 وهي هيكليًا تشبه أكسيد الليثيوم الكوبالت (III) (LiCoO 2 ) ولكنها استقرت مع وجود فائض من الليثيوم ، Li / NMC> 1.0 ، والتي تعتبر أنها سلسلة من المجالات النانوية تشبه Li2MnO3 من المواد. تم الإبلاغ عن هذه الكاثودات لأول مرة بواسطة CS Johnson و JT Vaughey و MM Thackeray و TE Bofinger و SA Hackney.[6] بالنسبة لكلا النوعين من كاثودات NMC يوجد نقل للشحنة الداخلية يؤكسد المنغنيز ويختزل كاتيونات النيكل ، بدلاً من أن تكون جميع الكاتيونات المعدنية الانتقالية ثلاثية التكافؤ. تساهم أكسدة الإلكترونين الاثنين للنيكل (II) عند الشحن في السعة العالية لمواد الكاثود NMC . في عام 2001 افترض Arumugam Manthiram أن الآلية التي تكوّن السعة العالية لكاثود أكسيد الطبقات هذه تنتج من انتقال يمكن فهمه بناءً على المواضع النسبية للمعدن في مستوى الطاقة 3d بالنسبة إلى قمة نطاق إلى الجزء العلوي من نطاق الأكسجين 2p.[7][8][9] تساعد هذه المشاهدة في تفسير السعة العالية لكاثودات NMC على النحو الوارد أعلاه 4.4 فولت (مقابل Li) كما وجد تزايد في السعة من أكسدة شبكة الأكسيد بدلاً من أكسدة الكاتيون.
في عام 2001 قدم كريستوفر جونسون ومايكل ثاكيراي وخليل أمين وجيكوك كيم براءة اختراع [10][11] لكاثودات الليثيوم نيكل منغنيز كوبالت الغنية (NMC) على أساس بنية Li 2 MnO 3 . في عام 2001 قدّم Zhonghua Lu و Jeff Dahn براءة اختراع [12] لفئة NMC لمواد القطب الموجب ، على أساس فكرة المحلول الصلب بين الأجزاء النهائيين.
نسب المعادن[عدل]
عدة مستويات مختلفة من النيكل ذات أهمية تجارية. يشار إلى النسبة بين المعادن الثلاثة بثلاثة أرقام. على سبيل المثال ، يتم اختصار LiNi 0.333 Mn 0.333 Co 0.333 O 2 إلى NMC111 أو NMC333 و LiNi 0.5 Mn 0.3 Co 0.2 O 2 إلى NMC532 (أو NCM523) و LiNi 0.6 Mn 0.2 Co 0.2 O 2 إلى NMC622 و LiNi 0.8 Mn 0.1 Co 0.1 O 2 إلى NMC811. في ضوء المشكلات المحتملة المتعلقة بمصادر الكوبالت فهناك اهتمام بزيادة مستوى النيكل ، على الرغم من أن هذا يقلل من الاستقرار الحراري.[13]
بينما يمكن استخدام كربونات الليثيوم أو هيدروكسيد الليثيوم لصنع NMC111 ، فإن هيدروكسيد الليثيوم ضروري لصنع NMC811 ، حيث تساعد درجة حرارة التوليف المنخفضة على التخفيف من التبادل فيموقع الليثيوم/ النيكل ، الذي يعزى إليه تقليل الأداء.[14]
استخدام أقطاب NMC[عدل]

توجد بطاريات NMC في معظم السيارات الكهربائية . تم تركيب بطاريات NMC في BMW ActiveE في 2011/2011 ، و في عام 2013 في BMW i8 .[15] تشمل السيارات الكهربائية المزودة ببطاريات NMC ، اعتبارًا من عام 2020: Audi e-tron GE و BAIC EU5 R550 و BMW i3 و BYD Yuan EV535 و Chevrolet Bolt و Hyundai Kona Electric و Jaguar I-Pace و Jiangling Motors JMC E200L و NIO ES6 و Nissan Leaf S Plus و Renault ZOE و Roewe Ei5 و VW e-Golf و VW ID.3.[16] لا يوجد سوى عدد قليل من مصنعي السيارات الكهربائية الذين لا يستخدمون NMC في بطاريات تشغيل السيارة التي تعمل بالكهرباء. الاستثناء الأكثر أهمية هو Tesla ، فهي تستخدم بطاريات NCA لسياراتها . في عام 2015 ، أعلن Elon Musk أن التخزين المنزلي لـTesla Powerwall يعتمد على NMC من أجل زيادة عدد دورات الشحن / والتفريغ على مدار عمر الوحدات.[17]
يستخدم NMC أيضًا للإلكترونيات المحمولة مثل الهواتف المحمولة / الهواتف الذكية وأجهزة الكمبيوتر المحمولة في معظم بطاريات pedelec.[18][19] بالنسبة لهذه التطبيقات ، لا تزال البطاريات التي تحتوي على أكسيد الكوبالت ليثيوم LCO مستخدمة بشكل حصري تقريبًا في عام 2008.[20] تطبيق آخر لبطاريات NMC هو محطات طاقة تخزين البطاريات . في كوريا على سبيل المثال ، تم تركيب نظامين للتخزين لـ NMC لتنظيم تردد التخزين في عام 2016: أحدهما بسعة 16 ميجاوات وطاقة 6 ميجاوات ساعة، والآخر بقدرة 24 ميجاوات و 9 ميجاوات ساعي.[21] في عام 2017/2018 ، تم تركيب وتشغيل بطارية بسعة تزيد عن 30 ميجاوات و 11 ميجاوات ساعة في نيومان في ولاية أستراليا الغربية .[22][23]
خصائص أقطاب NMC[عدل]
يبلغ الجهد الخلوي لبطاريات الليثيوم أيون بـ NMC بين 3.6–3.7 فولت.[24] اكتشف مانثيرام أن حدود قدرة كاثودات الأكسيد ذات الطبقات هذه ناتجة عن عدم الاستقرار الكيميائي الذي يمكن فهمه أنها
معتمدة على مستوى الطاقة 3d في ذرات المعادن بالنسبة إلى الجزء العلوي من نطاق مستوى الطاقة 2p للإكسجين.[7][25][9] كان لهذا الاكتشاف آثار كبيرة على التركيبة الممكنة عمليًا لبطاريات الليثيوم أيون ، فضلاً عن استقرارها من وجهة السلامة.
اقرأ أيضا[عدل]
المراجع[عدل]
- ^ Julien، Christian؛ Monger، Alain؛ Zaghib، Karim؛ Groult، Henri (يوليو 2016). "Optimization of Layered Cathode Materials for Lithium-Ion Batteries". Materials. ج. 9 ع. 7: 595. Bibcode:2016Mate....9..595J. DOI:10.3390/ma9070595. PMID:28773717.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Li، Xuemen؛ Colclasure، Andrew؛ Finegan، Donal؛ Ren، Dongsheng؛ Shi، Ying؛ Feng، Xuning؛ Cao، Lei؛ Yang، Yuan؛ Smith، Kandler (فبراير 2019). "Degradation Mechanisms of High Capacity 18650 Cells Containing Si-Graphite Anode and Nickel-Rich NMC Cathode". Electrochimica Acta. ج. 297: 1109–1120. DOI:10.1016/j.electacta.2018.11.194. OSTI:1491439.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعSigmaElSheet - ^ Mizushima، K.؛ Jones، P.C.؛ Wiseman، P.J.؛ Goodenough، J.B. (1980). "LixCoO2 (0<x<-1): A new cathode material for batteries of high energy density". Materials Research Bulletin. ج. 15 ع. 6: 783–789. DOI:10.1016/0025-5408(80)90012-4.
- ^ Breger، Julian؛ Dupre، Nicolas؛ Chupas، Peter؛ Lee، Peter؛ Proffen، Thomas؛ Parise، John؛ Grey، Clare (2005). "Short- and Long-Range Order in the Positive Electrode Material, Li(NiMn)0.5O2: A Joint X-ray and Neutron Diffraction, Pair Distribution Function Analysis and NMR Study". Journal of the American Chemical Society. ج. 127 ع. 20: 7529–7537. DOI:10.1021/ja050697u. PMID:15898804.
- ^ C. S. Johnson, J. T. Vaughey, M. M. Thackeray, T. E. Bofinger, and S. A. Hackney "Layered Lithium-Manganese Oxide Electrodes Derived from Rock-Salt LixMnyOz (x+y=z) Precursors" 194th Meeting of the Electrochemical Society, Boston, MA, Nov.1-6, (1998)
- ^ أ ب Chebiam، R. V.؛ Kannan، A. M.؛ Prado، F.؛ Manthiram، A. (2001). "Comparison of the chemical stability of the high energy density cathodes of lithium-ion batteries". Electrochemistry Communications. ج. 3 ع. 11: 624–627. DOI:10.1016/S1388-2481(01)00232-6.
- ^ Chebiam، R. V.؛ Prado، F.؛ Manthiram، A. (2001). "Soft Chemistry Synthesis and Characterization of Layered Li1−xNi1−yCoyO2−δ (0 ≤ x ≤ 1 and 0 ≤ y ≤ 1)". Chemistry of Materials. ج. 13 ع. 9: 2951–2957. DOI:10.1021/cm0102537.
- ^ أ ب Manthiram، Arumugam (2020). "A reflection on lithium-ion battery cathode chemistry". Nature Communications. ج. 11 ع. 1: 1550. Bibcode:2020NatCo..11.1550M. DOI:10.1038/s41467-020-15355-0. PMID:32214093.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ [1]
- ^ [2]
- ^ [3]
- ^ Sun، Xin؛ Luo، Xiaoli؛ Zhang، Zhan؛ Meng، Fanran؛ Yang، Jianxin (نوفمبر 2020). "Life cycle assessment of lithium nickel cobalt manganese oxide (NCM) batteries for electric passenger vehicles". Journal of Cleaner Production. ج. 273: 123006. DOI:10.1016/j.jclepro.2020.123006. مؤرشف من الأصل في 2023-01-12.
- ^ Zhao، Enyue؛ Fang، Lincan؛ Chen، Minmin؛ Chen، Dongfeng؛ Wang، Qingzhen؛ Hu، Zhongbo؛ Yan، Qing-Bo؛ Wu، Meimei؛ Xiao، Xiaoling (2017). "New insight into Li/Ni disorder in layered cathode materials for lithium ion batteries: a joint study of neutron diffraction, electrochemical kinetic analysis and first-principles calculations". Journal of Materials Chemistry A. ج. 5 ع. 4: 1679–1686. DOI:10.1039/C6TA08448F.
- ^ Apurba Sakti؛ Jeremy J. Michalek؛ Erica R.H. Fuchs؛ Jay F. Whitacre (1 يناير 2015)، "A techno-economic analysis and optimization of Li-ion batteries for light-duty passenger vehicle electrification" (PDF)، Journal of Power Sources، ج. 273، pp. 966–980، Bibcode:2015JPS...273..966S، DOI:10.1016/j.jpowsour.2014.09.078، مؤرشف من الأصل (PDF) في 2023-01-14، اطلع عليه بتاريخ 2020-02-23
- ^ Wangda Li؛ Evan M. Erickson؛ Arumugam Manthiram (يناير 2020)، "High-nickel layered oxide cathodes for lithium-based automotive batteries"، Nature Energy، Springer Nature، ج. 5، pp. 26–34، Bibcode:2020NatEn...5...26L، DOI:10.1038/s41560-019-0513-0، ISSN:2058-7546
- ^ Zachary Shahan (7 May 2015). "38,000 Tesla Powerwall Reservations In Under A Week (Tesla / Elon Musk Transcript)" (بالإنجليزية الأمريكية). Archived from the original on 2023-01-12.
- ^ "Batterie - Beschreibung von Batterietypen. Lithium-Ionen-Batterien" (بالألمانية). energieautark consulting gmbh. 27 Oct 2010.
Die meistverbreitteste Li-ionzelle auf dem Markt ist die Lithium-Nickel-Mangan-Kobalt-Oxid-Zelle (Li-NMC) mit einer Nominalspannung von 3.6 V je Zelle.
[وصلة مكسورة] - ^ Electrochemical Power Sources: Fundamentals, Systems, and Applications: Li-battery safety (ط. 1)، Amsterdam, Netherlands: Elsevier، 2018، p. 128، ISBN:978-0-444-64008-6، مؤرشف من الأصل في 2023-01-12، اطلع عليه بتاريخ 2020-02-23
- ^ Sébastien Patoux؛ Lucas Sannier؛ Hélène Lignier؛ Yvan Reynier؛ Carole Bourbon؛ Séverine Jouanneau؛ Frédéric Le Cras؛ Sébastien Martinet (مايو 2008)، "High voltage nickel manganese spinel oxides for Li-ion batteries"، Electrochimica Acta، ج. 53، ص. 4137–4145، DOI:10.1016/j.electacta.2007.12.054
- ^ Kokam (7 Mar 2016). "Kokam's 56 Megawatt Energy Storage Project Features World's Largest Lithium NMC Energy Storage System for Frequency Regulation" (بالإنجليزية). PR Newswire Association LLC. Archived from the original on 2023-01-12.
- ^ Giles Parkinson (12 Aug 2019). "Alinta sees sub 5-year payback for unsubsidised big battery at Newman" (بالإنجليزية الأسترالية). Archived from the original on 2023-01-12.
- ^ "Energy Storage Solution Provider" (PDF) (بالإنجليزية). Archived from the original (PDF) on 2020-02-23. Retrieved 2023-01-12.
- ^ "Automotive Lithium-Ion Batteries"، Johnson Matthey Technology Review، ج. 59، pp. 4–13، 2015، DOI:10.1595/205651315X685445، مؤرشف من الأصل في 2023-01-12
- ^ Chebiam، R. V.؛ Prado، F.؛ Manthiram، A. (2001). "Soft Chemistry Synthesis and Characterization of Layered Li1−xNi1−yCoyO2−δ (0 ≤ x ≤ 1 and 0 ≤ y ≤ 1)". Chemistry of Materials. ج. 13: 2951–2957. DOI:10.1021/cm0102537.
علامة <ref> بالاسم " Sakti2015 " المحددة في مجموعة <references> " " لا تحتوي على محتوى.
علامة <ref> بالاسم " Li2020 " المحددة في مجموعة <references> " " لا تحتوي على محتوى.
علامة <ref> بالاسم " Shahan2015 " المحددة في مجموعة <references> " " لا تحتوي على محتوى.
علامة <ref> بالاسم " Garche2018 " المحددة في مجموعة <references> " " لا تحتوي على محتوى.
علامة <ref> بالاسم " Patoux2008 " المحددة في مجموعة <references> " " لا تحتوي على محتوى.
علامة <ref> بالاسم " Kokam2016 " المحددة في مجموعة <references> " " لا تحتوي على محتوى.
علامة <ref> بالاسم " Parkinson " المحددة في مجموعة <references> " " لا تحتوي على محتوى.
علامة <ref> بالاسم " KokamPdf " المحددة في مجموعة <references> " " لا تحتوي على محتوى.
علامة <ref> بالاسم " Miller " المحددة في مجموعة <references> " " لا تحتوي على محتوى.



