نيكل
| |||||||||||||||||||||||||||||||||||||||||||||||||
| المظهر | |||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
رمادي فلزي ذو بريق ذهبي
| |||||||||||||||||||||||||||||||||||||||||||||||||
| الخواص العامة | |||||||||||||||||||||||||||||||||||||||||||||||||
| الاسم، العدد، الرمز | نيكل، 28، Ni | ||||||||||||||||||||||||||||||||||||||||||||||||
| تصنيف العنصر | فلز انتقالي | ||||||||||||||||||||||||||||||||||||||||||||||||
| المجموعة، الدورة، المستوى الفرعي | 10، 4، d | ||||||||||||||||||||||||||||||||||||||||||||||||
| الكتلة الذرية | 58.6934(4) غ·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||
| توزيع إلكتروني | Ar]; 3d8 4s2] | ||||||||||||||||||||||||||||||||||||||||||||||||
| توزيع الإلكترونات لكل غلاف تكافؤ | 2, 8, 17, 1 (صورة) | ||||||||||||||||||||||||||||||||||||||||||||||||
| الخواص الفيزيائية | |||||||||||||||||||||||||||||||||||||||||||||||||
| الطور | صلب | ||||||||||||||||||||||||||||||||||||||||||||||||
| الكثافة (عند درجة حرارة الغرفة) | 8.908 غ·سم−3 | ||||||||||||||||||||||||||||||||||||||||||||||||
| كثافة السائل عند نقطة الانصهار | 7.81 غ·سم−3 | ||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة الانصهار | 1728 ك، 1455 °س، 2651 °ف | ||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة الغليان | 3186 ك، 2913 °س، 5275 °ف | ||||||||||||||||||||||||||||||||||||||||||||||||
| حرارة الانصهار | 17.48 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||
| حرارة التبخر | 377.5 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||
| السعة الحرارية (عند 25 °س) | 26.07 جول·مول−1·كلفن−1 | ||||||||||||||||||||||||||||||||||||||||||||||||
| ضغط البخار | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| الخواص الذرية | |||||||||||||||||||||||||||||||||||||||||||||||||
| أرقام الأكسدة | 4
[1], -1 | ||||||||||||||||||||||||||||||||||||||||||||||||
| الكهرسلبية | 1.91 (مقياس باولنغ) | ||||||||||||||||||||||||||||||||||||||||||||||||
| طاقات التأين | الأول: 737.1 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||
| الثاني: 1753.0 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||||||
| الثالث: 3395 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر ذري | 124 بيكومتر | ||||||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر تساهمي | 4±124 بيكومتر | ||||||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر فان دير فالس | 163 بيكومتر | ||||||||||||||||||||||||||||||||||||||||||||||||
| خواص أخرى | |||||||||||||||||||||||||||||||||||||||||||||||||
| البنية البلورية | مكعب مركزي الوجه | ||||||||||||||||||||||||||||||||||||||||||||||||
| المغناطيسية | مغناطيسية حديدية | ||||||||||||||||||||||||||||||||||||||||||||||||
| مقاومة كهربائية | 69.3 نانوأوم·متر (20 °س) | ||||||||||||||||||||||||||||||||||||||||||||||||
| الناقلية الحرارية | 90.9 واط·متر−1·كلفن−1 (300 كلفن) | ||||||||||||||||||||||||||||||||||||||||||||||||
| التمدد الحراري | 13.4 ميكرومتر·متر−1·كلفن−1 (25 °س) | ||||||||||||||||||||||||||||||||||||||||||||||||
| سرعة الصوت (سلك رفيع) | (درجة حرارة الغرفة) 4900 متر·ثانية−1 | ||||||||||||||||||||||||||||||||||||||||||||||||
| معامل يونغ | 200 غيغاباسكال | ||||||||||||||||||||||||||||||||||||||||||||||||
| معامل القص | 76 غيغاباسكال | ||||||||||||||||||||||||||||||||||||||||||||||||
| معامل الحجم | 180 غيغاباسكال | ||||||||||||||||||||||||||||||||||||||||||||||||
| نسبة بواسون | 0.31 | ||||||||||||||||||||||||||||||||||||||||||||||||
| صلادة موس | 4.0 | ||||||||||||||||||||||||||||||||||||||||||||||||
| صلادة فيكرز | 638 ميغاباسكال | ||||||||||||||||||||||||||||||||||||||||||||||||
| صلادة برينل | 700 ميغاباسكال | ||||||||||||||||||||||||||||||||||||||||||||||||
| رقم CAS | 7440-02-0 | ||||||||||||||||||||||||||||||||||||||||||||||||
| النظائر الأكثر ثباتاً | |||||||||||||||||||||||||||||||||||||||||||||||||
| المقالة الرئيسية: نظائر النيكل | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
النيكل عنصرٌ كيميائي رمزه Ni وعدده الذرّي 28، وهو ينتمي إلى عناصر المستوى الفرعي d ويقع على رأس عناصر المجموعة العاشرة في الجدول الدوري؛ ويصنّف كيميائياً ضمن الفلزّات الانتقالية. النيكل فلزٌ أبيض فضّي بمظهرٍ ذهبيٍّ خفيفٍ، وهو أحد المواد المغناطيسية. لمسحوق النيكل النقي نشاط كيميائي جيّد؛ أمّا القطع كبيرة الحجم فهي بطيئة التفاعل في الظروف القياسية من الضغط ودرجة الحرارة، ويعود سبب ذلك إلى تشكّل طبقةٍ مُخَمّلةٍ من الأكسيد على السطح. لا يوجد النيكل في الطبيعة بشكله الحرّ إلّا نادراً، ولكنّه غالباً ما يكون مرتبطاً مع عناصرَ أخرى ضمن معادن مختلفة، وخاصة في طبقات الصخور فوق المافية. تكثر خامات النيكل في روسيا وكندا، وكذلك في جزر كاليدونيا الجديدة في المحيط الهادي. ينتج النيكل في الكون من عملية التخليق النووي في المستعرات العظمى؛ وهو يدخل في تركيب الحديد النيزكي والمستحصل من النيازك الحديدية، والتي كانت منتشرة على سطح الأرض في العصور التاريخية الأولى من عمر الأرض. يدخل النيكل أيضاً مع الحديد في تركيب اللبّ الداخلي والخارجي لباطن الأرض.
كان أكسل فريدريك كرونستيد أوّل من تمكّن من عزل فلزّ النيكل، وذلك في سنة 1751، ولكنه أخطأ في البداية وظنّه معدناً من معادن النحاس؛ ثمّ تمكّن بعد ذلك من تمييزه على أنّه عنصرٍ كيميائيٍّ جديد. تُشتَقّ تسمية هذا العنصر من الأساطير الجرمانية، إذ كان ينتشر بين عمال المناجم لفظ «نيكل» للإشارة إلى اسم عفريت، والذي كان يطلق على خامة من خامات النيكل والنحاس، والتي لم يكن ينتج عن صهرها فلزّ النحاس المنشود. استُخدِمَ النيكل منذ اكتشافه في طلي الحديد والنحاس الأصفر، وفي صناعة السبائك؛ كما يكثر استخدام النيكل في سكّ النقود المعدنية. للنيكل تطبيقاتٍ عمليّةٍ أخرى في مجال التحفيز الكيميائي، مثل نيكل راني، وفي صناعة بطّاريات المَرْكبات الكهربائية.
للنيكل دورٌ حيويٌ مهمٌ لبعض النباتات، إذ تحوي بعض الإنزيمات المهمة لها على النيكل في الموقع النشط. من جهةٍ أخرى، قد يسبّب تماس الجلد لدى البعض مع الأشياء المصنوعة من النيكل إلى حدوث حالة من التهاب الجلد التماسي التحسّسي، والمعروفة باسم «حساسية النيكل».
التاريخ وأصل التسمية
[عدل]
بسبب سهولة الخلط بين خامات النيكل وبين خامات الفضّة والنحاس، فلم تفهم خواص فلزّ النيكل فهماً كاملاً إلّا في العصور الحديثة نسبياً. مع ذلك، فإنّ النيكل المرافق لخامات النحاس والفضّة قد بُرْهِنَ على دخوله بنسبة عظمى تصل إلى 2% من تركيب قطع أثريّة تاريخيّة قديمة مصنوعة من البرونز، عثر عليها في سورية، وتعود إلى أقدم من 3500 ألف سنة قبل الميلاد.[2] كما تشير بعض النصوص الصينية القديمة إلى سبيكة من النحاس الأبيض، والتي كانت تعرف باسم بايتونغ [ط 1]، وهي تعرف حالياً باسم سبيكة «النيكل النحاسي» كبرونيكل [ط 2]، وكانت مستخدمةً حينها في عهود تتراوح بين 1700 إلى 1400 سنة قبل الميلاد. صُدِّرَ هذا النحاس الأبيض إلى دول أوروبا الغربية في بدايات القرن السابع عشر، ولكن لم يعرف أنّ تلك السبيكة كانت حاويةً على النيكل إلّا في سنة 1822.[3] وُجِدَ أيضاً أنّ نقوداً معدنية كانت قد سُكَّت من سبيكة النيكل النحاسي من الملوك البُخْتريين [ط 3]: أغاثوكليس [ط 4] وإيوثيديموس الثاني [ط 5] وبنتاليون [ط 6] في القرن الثاني قبل الميلاد، والتي غالباً كانت مُستقدَمةً من الصين.[4]
عُثِرَ في ألمانيا في فترة القرون الوسطى على معدن مصفَرّ في منطقة جبال الخام [ط 7]، والذي كان يشبه خام النحاس؛ إلّا أنّ عمال المناجم لم يتمكّنوا من استخراج النحاس من ذلك الخام، ممّا دفعهم إلى الاعتقاد بوجود قدرة خارقة تحول دون الحصول على مبتغاهم، لذلك أطلقوا اسم عفريت من الأساطير الجرمانية يدعى نيكل [ط 8] على اسم ذلك الخام، ليدعى حينها باسم Kupfernickel (كُبفرنيكل، حيث تعني كلمة Kupfer النحاس في اللغة الألمانية).[5]

يُعرَف هذا الخام حالياً باسم نيكلين [ط 9] (عُرف مسبقًا باسم نيكوليت[ط 10])؛ وهو يتكوّن كيميائياً من زرنيخيد النيكل. في سنة 1751 تمكّن البارون أكسل فريدريك كرونستيد [ط 11] في أثناء تجاربه لعزل النحاس من معدن كُبفرنيكل في منجم للكوبالت في السويد من الحصول على فلزّ أبيض، ليتبيّن له فيما بعد أنّه عنصر جديد، وأعلن اكتشافه وأطلق عليه اسم «نيكل»، نسبةً إلى أسطورة العفريت التي مَنَحَت الخام ذلك الاسم.[6] لا يزال اسم كُبفرنيكل مستخدماً في اللغة الألمانية، ولكن للإشارة إلى سبيكة النيكل النحاسي (كبرونيكل).[7]
كان خام كُبفرنيكل هو الوسيلة الوحيدة للحصول على النيكل حتّى بداية القرن التاسع عشر، ولكن منذ سنة 1824 أصبح من الممكن الحصول على هذا الفلزّ ناتجاً ثانوياً من عمليات استخراج خضاب أزرق الكوبالت [ط 12]؛ أمّا الإنتاج على صعيدٍ كبيرٍ فكان قد بدأ في النرويج في سنة 1848 من خامات معدن البيروتيت [ط 13] الغنيّة بالنيكل. ساهمت إضافة النيكل في عمليّات إنتاج الفولاذ في سنة 1889 إلى ازدياد الطلب العالمي عليه، وقد ساهم اكتشاف التوضّعات الرسوبية الغنيّة بالنيكل في جزر كاليدونيا الجديدة في تأمين حاجة السوق حتّى بدايات القرن العشرين، ثمّ تلاها اكتشاف كمّيّات كبيرة من خامات النيكل في كندا وروسيا وجنوب أفريقيا، بالشكل الذي أمّن حاجة السوق من هذا الفلزّ.[3]
الوفرة الطبيعية
[عدل]
يتركّز وجود النيكل على كوكب الأرض بمرافقة الحديد في تركيب اللبّ الداخلي [ط 15] والخارجي [ط 16] لباطن الأرض؛[8] وتقدّر نسبة الكسر الكتلي للنيكل في لبّ الأرض بقرابة 5%.[9] يدخل النيكل أيضاً في تركيب النيازك الحديدية [ط 17] وذلك على هيئة شكلين محدّدين من أشكال السبيكة مع الحديد، وهما الكاماسيت [ط 18] والتاينيت [ط 19]. تتراوح نسبة النيكل في الكاماسيت بين 5-10%، مع احتمالية وجود شوائب من الكوبالت أو الكربون؛ في حين أنّ محتوى النيكل في التاينيت يتراوح بين 20% إلى 65%.[10] اكتُشِفَ وجود النيكل في النيازك الحديدية أوّل مرّة سنة 1799 من العالم جوزيف لويس بروست [ط 20]، والذي كان حينها يحلّل عيّنات من النيازك الحديدية المُستَجْلَبَة من موقع كامبو دل ثيلو [ط 21] الأرجنتيني؛ وَوَجد أنّ نسبة النيكل فيها تصل إلى قرابة 10%.[11]
في الغلاف الصخري
[عدل]تبلغ وفرة النيكل في القشرة الأرضية مقدار 0.008%؛[وب-ألم 1] ومن النادر العثور عليه فيها بشكله الطبيعي الحرّ؛[وب-إنج 1] بل يوجد غالباً في القشرة الأرضية ضمن معادن مختلفة، وذلك في معدن البنتلانديت [ط 22] بمرافقة الكبريت والحديد؛ وفي معدن الميلريت [ط 23] بمرافقة الكبريت؛ وفي معدن النيكلين [ط 24] بمرافقة الزرنيخ.[وب-إنج 2] تُستخرَج خامات النيكل من طبقة اللاتيريت [ط 25]، والتي تنتشر فيها مزائج للنيكل مع فلزّات أخرى ضمن معادن مختلفة، وذلك مع الحديد مثلاً ضمن الليمونيت [ط 26]. كما يوجد النيكل في خام الغارنيريت [ط 27] النادر والمتوضّع في الصخور فوق المافية [ط 28] والحاوي على النيكل على هيئة سيليكات؛ والمؤلّف من معدن النبويت [ط 29] ومن معدن الوليمزيت [ط 30]؛ وكذلك في التوضّعات الكبريتيدية الصُهَاريّة [ط 31].[12] من معادن النيكل الأخرى كلّ من البنزنيت [ط 32] والأوارويت [ط 33]، وتلك أمثلةٌ على معادن نادرة، ولكنّها حاوية على النيكل بنسبة مرتفعة.[وب-إنج 3]
في الغلاف المائي
[عدل]عُثِرَ على كمّيّات كبيرة نسبياً من النيكل في أعماق المحيطات، وخاصّةً في منطقة تصدّع كليبرتون [ط 34] في المحيط الهادي، وذلك على هيئة عُقَيدَات متعدّدة الفلزّات [ط 35] المتوضّعة على أعماق تصل بين 3.5 إلى 6 كيلومتر في القاع.[13] تتألّف هذه العُقَيدات من عدّة عناصر أرضية نادرة [ط 36]، ويُقدّر أن يصل محتوى النيكل فيها إلى قرابة 1.7%.[14] مع تطوّر الأساليب والتقنيات العلمية والهندسية تقوم السلطة الدولية لقاع البحار [ط 37] بسنّ قوانين لوضع شروط ناظمة من أجل استخراج وجمع تلك العُقَيدات جمعاً يراعي الضوابط البيئية، ويتوافق مع أهداف التنمية المستدامة [ط 38] للأمم المتّحدة.[15]
الاستخراج
[عدل]| المرتبة | البلد | الإنتاج (مقدراً بالأطنان) |
|---|---|---|
| 1. | إندونيسيا | 606.000 |
| 2. | الفلبين | 345.000 |
| 3. | روسيا | 272.000 |
| 4. | كاليدونيا الجديدة (فرنسا) | 216.000 |
| 5. | كندا | 176.000 |
| 6. | أستراليا | 170.000 |
| 7. | الصين | 110.000 |
| 8. | البرازيل | 74.400 |
| 9. | كوبا | 51.000 |

تشير بعض التقديرات إلى أنّ النيكل يُعَدّن عالمياً بأكثر من حوالي 2.5 مليون طن سنوياً؛ ووفقاً لبيانات سنة 2020 تتصدّر إندونيسيا تلك الدول بإنتاج عالمي سنوي مقداره 760 ألف طن، ثمّ الفلبين بمقدار 320 ألف طن، ثمّ روسيا بمقدار 280 ألف طن، ثمّ كاليدونيا الجديدة بمقدار 200 ألف طن، ثمّ أستراليا بمقدار 170 ألف طن، ثمّ كندا بمقدار 150 ألف طن.[17] توجد توضّعات مهمّة لخامات النيكل في حوض سدبري [ط 39] في كندا، وفي مدينة نوريلسك [ط 40] وشبه جزيرة كولا [ط 41] في روسيا، وفي ولاية كوينزلاند [ط 42] في أستراليا، وفي مدينة موا في كوبا. إجمالاً تمتلك دولتا أستراليا وإندونيسيا أكبر احتياطيٍّ عالميٍّ من النيكل، وذلك بنسبةٍ تبلغ 43.6% من الاحتياطيّ العالميّ.[وب-إنج 5]
حتّى يكون استخراج النيكل مجدٍ اقتصادياً ينبغي أن يقع محتوى النيكل في الخامة بين 0.5-1%. تُستخرَج خامات النيكل عادةً إمّا من التوضّعات الكبريتيدية التقليدية، أو من تلك الموجودة في الطبقات اللاتيريتية؛ وهناك نزعة إلى استخراج خامات النيكل من الأخيرة على حساب الأولى؛ رغم ما يرافق ذلك من صعوبات تقنية، إذ يتطلب الاستخراج من الطبقات اللاتيريتية إجراء عملية تصويل حمضي مرتفع الضغط [ط 43].[18]
الإنتاج
[عدل]يُستَخلص فلزّ النيكل من خاماته تقليدياً وفق عمليات تتضمّن تحميص الخامة [ط 44] ثمّ الاختزال [ط 45]، ممّا يمكّن من الحصول على فلزٍّ بنقاوة أكبر من 75%. في تلك العمليّات الحرارية [ط 46] التقليدية تتعرّض خامات النيكل الكبريتيدية لدرجات حرارة مرتفعة، ممّا يؤدّي إلى الحصول على خليط كبريتيدي مصهور [ط 47]، والذي يخضع إلى عمليات تنقية [ط 48] لاحقة. أدّى التطوّر في عمليّات المعالجة المائية [ط 49] إلى الحصول على ناتج من النيكل ذي نقاوة مرتفعة نسبياً، وذلك عبر تركيز الخامات الكبريتيدية بعملية تعويم زَبَديّ [ط 50]، ثمّ تخضع لاحقاً إلى عمليّات صَهْرٍ حرارية.
ُُتُجرَى عمليّات الصَهْر وفق مراحل تدريجية من أجل فصل الفلزّات المرافقة، إذ للتخلّص من الحديد يُسخّن الخليط الكبريتيدي المصهور أوّلاً من أجل تحويل كبريتيد الحديد إلى أكسيد الحديد؛ ثمّ تضاف السيليكات وفحم الكوك لاحقاً من أجل الحصول على خَبَثٍ [ط 51] من سيليكات الحديد. أمّا النحاس فيُفصَل وفق عملية عملية شيريت غوردون [ط 52] بإضافة كبريتيد الهيدروجين وكبريتيد الصوديوم، ممّا يؤدّي إلى تشكيل كبريتيدات مضاعفة من النحاس والصوديوم سهلة الانصهار والفصل. بعد ذلك يُعرّض كبريتيد النيكل إلى الحرارة ويُحوّل إلى الأكسيد، والذي يُختَزل لاحقاً باستخدام فحم الكوك إلى فلز النيكل. يُنقّى فلزّ النيكل الناتج بعمليّات استخلاص كهربائي [ط 53] لاحقة.[19]
التنقية
[عدل]
- التحليل الكهربائي
لإجراء عمليّة التنقية يُوضَع النيكل الخام في خليّة تحليل كهربائي على المصعَد [ط 54]، أمّا على المهبط [ط 55] فتوضع صفيحةٌ من النيكل مرتفع النقاوة، في حين يُستخدَم كهرلٌ [ط 56] من أملاح النيكل.[19]
- عملية موند

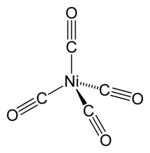
يُستَحصل على النيكل مرتفع النقاوة وفق عملية موند [ط 57]، وذلك بدرجة نقاوة تصل إلى 99.99%.[20] تُنسَب العملية إلى لودفيغ موند [ط 58]، والذي طوّرها أواخر القرن التاسع عشر. في هذه العملية يتفاعل النيكل مع أحادي أكسيد الكربون بوجود حفّاز من الكبريت عند درجة حرارة بين 40–80 °س، ليتشكّل مركّب كيميائي من رباعي كربونيل النيكل [ط 59]:
قد تتشكّل نواتج ثانوية من خماسي كربونيل الحديد [ط 60] أو من ثماني كربونيل ثنائي الكوبالت [ط 61]، ولكن يسهل فصلها عن الناتج الرئيسي.[21] يُمرّر رباعي كربونيل النيكل الناتج ضمن حجرة كبيرة عند درجات حرارة مرتفعة، الأمر الذي يؤدّي إلى تفكّكه وانطلاق غاز أحادي أكسيد الكربون والحصول على كُرَيّات [ط 62] من النيكل مرتفع النقاوة؛ أو يمكن بشكلٍ آخر أن تجرى عمليّة تفكك رباعي كربونيل النيكل في حجرة أصغر عند درجات حرارة تصل إلى 230 °س، ممّا يؤدّي إلى الحصول على مسحوق ناعم دقيق من النيكل مرتفع النقاوة.[22]
التحضير المخبري
[عدل]يمكن الحصول مخبرياً على كمّيّات صغيرة من النيكل بطرائق عديدة؛[23] منها:
- اختزال الأكسيد باستخدام الهيدروجين عند درجات حرارة تقع بين 150 °س إلى 250 °س:
- اختزال كلوريد النيكل الثنائي ضمن مستعلق في ثنائي إيثيل الإيثر باستخدام كاشف غرينيار [ط 63]؛ أو باستخدام الصوديوم:
- التفكّك الحراري لمركّب أكسالات النيكل [ط 64] بوجود الأكسجين:
النظائر
[عدل]يوجد إحدى وثلاثون نظيراً معروفاً للنيكل، والتي تتراوح أعدادها الكتلية بين 48 و78، منها خمسة نظائر مستقرّة وهي: نيكل-58 58Ni ونيكل-60 60Ni ونيكل-61 61Ni ونيكل-62 62Ni ونيكل-64 64Ni. أكثر هذه النظائر المستقرّة وفرةً طبيعيةً هو النظير نيكل-58، والذي يشكّل 68.077% من النيكل في الطبيعة، يليه النظير نيكل-60 بوفرة طبيعية مقدارها 26.22%.[وب-إنج 6] هنالك ستّة وعشرون نظيراً مشعّاً للنيكل، أطولها عمراً هو نيكل-59 59Ni والذي له عمر نصف 76,000 سنة، يليه النظير نيكل-63 63Ni بعمر نصف 100.1 سنة، والنظير نيكل-56 56Ni بعمر نصف 6.077 يوم؛ ولباقي نظائر النيكل المشعّة أعمار نصف أقلّ من 60 ساعة، ومعظمها دون 30 ثانية؛ مع العلم أنّه لا يوجد مصاوغ نووي [ط 65] لهذا العنصر.[24]
للنظير نيكل-62 62Ni أعلى قيمة وسطية لطاقة الترابط النووي [ط 66] لكلّ نُوَيّة [ط 67] من جميع نُوَيْدات [ط 68] العناصر الكيميائية المعروفة، وذلك بمقدار 8.7946 ميغاإلكترون-فولت/نُوَيّة [ط 69]؛[25][وب-إنج 7] وتلك قيمة أعلى من تلك التي لِنَظيرَي الحديد: حديد-56 56Fe وحديد-58 58Fe.[26] مع ذلك، فإنّ النيكل لا يعدّ أكثر عنصرٍ كيميائيٍّ ثقيلٍ وفرةً في الكون، وذلك يعود بسبب الانحلال الضوئي [ط 70] للنيكل داخل لبّ النجوم، وذلك يجعل الحديدَ أكثرَ وفرةً من النيكل بشكلٍ كبيرٍ.[26] يعدّ النظير نيكل-60 60Ni المستقرّ ناتجَ اضمحلالٍ للنُوَيدة المشعّة المنقرضة [ط 71] حديد-60 60Fe، والتي تضمحلّ بعمر نصف مقداره 2.6 مليون سنة. يَنتُج النظير المشعّ نيكل-56 56Ni في الكون من عملية احتراق السيليكون [ط 72] ويُطرَح بكمّيّات كبيرة من المستعرات العظمى من النوع Ia [ط 73]، ويشير شكل المنحنى الضوئي [ط 74] لتلك المستعرات العظمى في أعمار متوسطة إلى متأخرة إلى حدوث اضمحلال عن طريق التقاط إلكترون من النظير نيكل-56 متحوّلاً إلى كوبالت-56، والذي يضمحلّ بدوره إلى النظير حديد-56.[27] أمّا النظير، النيكل-59 59Ni، فهو نُوَيدة كونيّة [ط 75] مشعّة بعمر نصف مقداره 76 ألف سنة. يُستخدَم النظير نيكل-59 في جيوكيمياء النظائر، وذلك في التأريخ الإشعاعي من أجل تقدير عمر الأحجار النيزكية، ومن أجل معرفة الأصل الكوني للغبار في الجليد وفي الرواسب. من جهةٍ أخرى، وُجِدَ أيضاً أنّ للنظير المشعّ نيكل-78 عمر نصف مقداره 110 ميلي ثانية، ويُظَنّ أنّ له دوراً مهمّاً في التخليق النووي في المستعرات العظمى [ط 76] للعناصر الكيميائية الأثقل من الحديد.[وب-إنج 8] اكتُشِفَ النظير نيكل-48 48Ni سنة 1999، وهو أكثر نظيرِ لعنصرِ ثقيلِ غنىً بالبروتونات، فهو يمتلك 28 بروتوناً و20 نيوتروناً؛ وهو يمتلك عدداً سحريّاً مضاعفاً [ط 77] مثلما هو الحال في النظير نيكل-78 (28 بروتون و50 نيوترون).[وب-إنج 9] يوجد النظير نيكل-63 على هيئة شائبة في البُنَى الداعمة للمفاعلات النووية؛ وينتج من التقاط نيوترون [ط 78] من نيكل-62، ويُستخدَم من أجل الاستدلال والكشف عن اختبارات الأسلحة النووية.[28]
الخواص الفيزيائية
[عدل]
البنية الذرية
[عدل]يوجدد نمطان للتوزيع الإلكتروني داخل ذرّة النيكل، واللذان يَصِفَان ترتيب الإلكترونات داخل المدارات الذرّية؛ الأوّل: Ar]؛ 3d8 4s2] والثاني: Ar]؛ 3d9 4s1] (يشير [Ar] إلى التوزيع الإلكتروني في ذرّة الآرغون). هناك تقاربٌ كبيرٌ في حسابات السويّة الطاقية بين هَذَين التوزيعَين، إلّا أنّ يوجد خلافٌ في تحديد أيّهما الأقلّ طاقياً.[30] تُدرِجُ المراجع الكيميائية التوزيعَ الإلكتروني الأوّل للنيكل على الشاكلة Ar]؛ 3d8 4s2]؛[31] والذي يُكتَب أيضاً بشكلٍ شائعٍ على الشكل Ar]؛ 4s2 3d8]. [32] يتّفق هذا التوزيع مع قاعدة ماديلونغ [ط 82] في مبدأ أوفباو [ط 83] لترتيب المدارات الذرّية طاقياً، والذي يتنبّأ أنّ المدار 4s يُملَأ أوّلاً قبل المدار 3d؛ وذلك مثبتٌ عليه تجريبيّاً.[وب-إنج 10]
من جهةٍ أخرى، ونظراً للبنية الدقيقة [ط 84] السائدة في تركيب الذرّات، فإنّ التوزيع الإلكتروني للمدارَين 3d و 4s ينقسم بدوره إلى عدّة مستويات طاقيّة متعدّدة؛[وب-إنج 10] ممّا يؤدّي إلى حدوث تداخل بينها نظراً للتقارب بين المستويات الطاقية لذانك المدارَين؛ بالتالي فإنّه وفق حسابات الكيمياء النظرية يكون التوزيع الإلكتروني على الشكل الثاني Ar]؛ 3d9 4s1] أخفض طاقياً من الأوّل، لذلك يُدرَج هذا التوزيع الإلكتروني للنيكل أيضاً في مراجع الأبحاث الكيميائية.[30]
الخواص الفلزية
[عدل]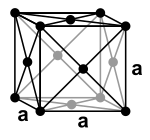
يوجد النيكل في الظروف القياسية من الضغط ودرجة الحرارة على هيئة فلزٍ ذي لون أبيض فضّي، مع وجود مًسْحَةٍ ذهبيّةٍ طفيفةٍ في حال الصقْل؛ وهو يُصنّف ضمن الفلزّات الثقيلة، إذ تبلغ كثافته مقدار 8.91 غ/سم3. يعدّ النيكل واحداً من أربعة عناصر، إلى جانب الحديد والكوبالت والغادولينيوم، تمتلك خواصاً مغناطيسية حديدية [ط 85] عند أو بالقرب من درجة حرارة الغرفة. تبلغ قيمة درجة حرارة كوري [ط 86] مقدار 354 °س،[33] أي أنّ النيكل يصبح لا مغناطيسياً فوق تلك الدرجة.[34] تترتّب البنية الذرّية للنيكل وفق نظامٍ بلّوريٍّ مكعّبٍ مركزيّ الوجه [ط 87]، وتبلغ فيه قيمة ثابت الشبكة البلّورية [ط 88] a مقدار 352.4 بيكومتر؛ مع وجود أربع وحدات صيغة [ط 89] في وحدة الخليّة [ط 90].[منشور-ألم 1]
النيكل فلزٌّ متوسّط الصلادة (تبلغ قيمة الصلادة وفق مقياس موس مقدار 3.8)، ولكنّه مطواع وقابل للسحب والطرق [ط 91]، كما أنّه قابل للصهر وللصقل؛ ويتميّز بأنّه موصلٌ جيّدٌ للكهرباء وناقلٌ جيّدٌ الحرارة.[7] تبلغ قيمة مقاومة الشدّ [ط 92] للنيكل المتوهّج بين 400–450 ميغاباسكال. إنّ قيمة مقاومة الانضغاط [ط 93] المرتفعة بمقدار 34 غيغاباسكال لا يمكن الوصول إليها في الظروف التجريبية للفلزات نظراً لتشكّل وحركة الانحرافات في البنية البلّورية؛ إلّا أنّها محقّقة في الجسيمات النانوية [ط 94] للنيكل.[35]
الخواص الكيميائية
[عدل]النيكل مستقرٌّ كيميائيّاً عند درجة حرارة الغرفة تجاه الرطوبة والماء والمحاليل القلويّة؛ أمّا الأحماض الممدّدة، مثل حمض الكبريتيك الممدّد، فتتفاعل مع النيكل ببطء، في حين تستطيع الأحماض المركّزة المؤكسدة، مثل حمض النتريك المركّز، أن تتفاعل مع سطح النيكل في البداية إلى أن تتشكّل طبقةٌ مُخَمّلةٌ من الأكسيد على السطح، والتي تقي باقي كتلة الفلزّ من التفاعل اللاحق.
يشكّل النيكل عدداً من المعقّدات التناسقية الملوّنة، ويكون العدد التناسقي فيها غالباً 4 أو 6؛ وتوجد تلك المعقّدات في ترتيبٍ هندسيٍّ جزيئيٍّ على نمط بنية جزيئية رباعية السطوح [ط 95] أو على نمط بنية جزيئية مستوية مربّعة [ط 96]؛ وتكون المعقّدات على النمط الأول رباعي السطوح ذات مغناطيسية مسايرة [ط 97]، أمّا النمط الثاني المستوي المربع فتكون فيه المعقّدات ذات مغناطيسية معاكسة [ط 98]؛ وفي عناصر المجموعة العاشرة لا تلاحظ هذه الظاهرة سوى عند النيكل، إذ أنّ البالاديوم الثنائي والبلاتين الثنائي يشكّلان معقداتٍ ذات بنية مستوية مربعة فقط.
المركبات الكيميائية بحالات الأكسدة المختلفة
[عدل]يمكن أن يوجد النيكل بعدّة حالات أكسدة، مثله مثل باقي الفلزّات الانتقالية، وهي تتراوح من -1 إلى +4، إذ يوجد النيكل في حالة الأكسدة 0 مثلاً في معقّداته التناسقية، مثلما هو الحال في مركّب رباعي كربونيل النيكل. وتعدّ حالة الأكسدة +2 الأكثر شيوعاً بين حالات الأكسدة المذكورة في كيمياء النيكل.
النيكل الثنائي
[عدل]
يشكّل النيكل الثنائي مع مختلف الأنيونات الشائعة عدداً معتبراً من المركّبات الكيميائية اللاعضوية، التي تتضمّن الكبريتيد NiS، والكبريتات NiSO4، النترات Ni(NO3)2 والكربونات NiCO3، والهيدروكسيد Ni(OH)2، بالإضافة إلى الهاليدات المعروفة من الفلوريد NiF2 والكلوريد NiCl2 والبروميد NiBr2 واليوديد NiI2. يعدّ كلوريد النيكل الثنائي مثالاً نمطياً على هاليدات النيكل الثنائي، وهو صلب أصفر اللون في شكله اللامائي، لكنّه يوجد غالباً في شكله المائي على هيئة سداسي هيدرات أخضر اللون، والذي يُستحصَل عند إذابة النيكل أو أكسيده في حمض الهيدروكلوريك. لكلوريد النيكل الثنائي اللامائي بنية بلّورية تتبع النظام البلّوري الثلاثي متساوي الأحرف [ط 99] وفق نمط يشبه تبلور كلوريد الكادميوم؛ في حين أنّ الشكل المائي سداسي الهيدرات يتبلور وفق نظامٍ بلّوري أحاديّ الميل [ط 100].[36]

يوجد أكسيد النيكل الثنائي NiO على هيئة مسحوق بلّوري أخضر اللون، ويُستخدَم في مجال صناعة الزجاج وتلوين السيراميك وصناعة الأقطاب الكهربائية، بالإضافة إلى استخدامه في مجال التحفيز الكيميائي في تفاعلات هدرجة المركّبات العضوية. من جهةٍ أخرى، يُستحصَل عادةً على كبريتات النيكل الثنائي بكمّيّات كبيرةٍ من حلّ وإذابة فلزّ النيكل في حمض الكبريتيك، ممّا يؤدّي إلى الحصول على بلّورات مُمَيّهة [ط 101] سداسية وسباعية الهيدرات؛ وعادةً ما يُستخدَم من أجل عمليّات الطلي الكهربائي بالنيكل [ط 102].[37] على العموم تميل أملاح النيكل الثنائي عند انحلالها في الماء إلى تشكيل معقّدات مائية 2+ [Ni(H2O)6] ذات لون أخضر.[38]
يشكّل النيكل الثنائي بعضاً من المعقّدات التناسقية وذلك مع رُبَيطاتٍ ضخمةٍ مثل ثنائي كلورو مضاعف (ثلاثي فينيل فوسفين) النيكل الثنائي [ط 103]؛ وكذلك الأمر مع رُبَيطات بسيطةٍ مثل الكلوريد في معقّد أنيون رباعي كلوريد النيكل الثنائي 2− [NiCl4] الأصفر؛ وكذلك مع ثنائي أمين الإيثيلين [ط 104] في معقّد 2+ [Ni(C2H4(NH2)2)] البنفسجي. يشكّل النيكل الثنائي أيضاً معقّداً تناسقياً مع رُبَيطة ثنائي ميثيل غليوكسيم [ط 105] ثنائيّة السنّ [ط 106]، وذلك في معقّد مضاعف (ثنائي ميثيل غليوكسيماتو) النيكل الثنائي [ط 107]، وهو معقّدٌ مستقرٌّ بسبب تشكّل روابط هيدروجينية تعمل على تثبيته؛ وله تطبيقات في الكشف التقليدي عن النيكل في الكيمياء التحليلية.[منشور-ألم 2]

تعدّ المعقّدات الأمينية مع رُبَيطات من الأمونيا من المعقّدات التناسقية المعروفة للنيكل الثنائي، وهي توجد إمّا على هيئة معقّد رباعي أمين النيكل الثنائي 2+ [Ni(NH3)4] الأزرق الفاتح؛ أو على هيئة معقّد سداسي أمين النيكل الثنائي 2+ [Ni(NH3)6] الأزرق الداكن إلى البنفسجي. تُستحصَل هذه المعقّدات من إضافة كمّيّات فائضةٍ من الأمونيا إلى ملح للنيكل الثنائي:[منشور-ألم 2]
أمّا المعقّدات السيانيدية فتُستحصَل عند إضافة سيانيد البوتاسيوم إلى محلولٍ ملحيٍّ للنيكل الثنائي، حيث يَنتجُ أوّلاً مركّب سيانيد النيكل الثنائي Ni(CN)2، والذي ينحلّ عند إضافة كمّيّاتٍ فائضةٍ من سيانيد البوتاسيوم بسبب تشكّل معقّد رباعي سيانو نيكلات البوتاسيوم [ط 108] الأصفر:[منشور-ألم 2]
من معقّدات النيكل الثنائي المعروفة أيضاً معقّد نيكلوسين [ط 109]، وهو مركّب نيكل عضوي ينتمي إلى مجموعة الميتالوسينات [ط 110] الشطيرية [ط 111]؛ إذ يتألّف النيكلوسين من مركز من أيون النيكل الثنائي المحصور بين وحدتين من أنيون حلقي البنتاديينيل [ط 112]، وهو يحوي على عشرين إلكتروناً في بنيته، والتي تأخذ فيها الحلقتان تصاوُغاً هندسياً مقارباً [ط 113].[39]
النيكل الثلاثي
[عدل]أشهر مركّبان للنيكل الثلاثي هما الأكسيد Ni2O3 وأكسيد الهيدروكسيد NiO(OH)، واللذان يجدان لهما تطبيقات في بطّاريات النيكل المختلفة. يُعثَر أيضاً على النيكل في حالة الأكسدة الثلاثية في بعض من المركّبات الكيميائية، منها مركّبات ثلاثي هالو فوسفينات النيكل الثلاثي [ط 114] Ni(PPh3)X3. [منشور-ألم 3] إلّا أنّ مركّبات النيكل الثلاثي غير مستقرّة على العموم، وتحتاج إلى تثبيت عبر الارتباط مع رُبَيطات مانحة للرابطة سيغما [ط 115] مثل الثيولات أو الفوسفينات العضوية [ط 116].[40]
حالات أكسدة أخرى
[عدل]تعدّ حالات الأكسدة الأخرى المتبقيّة للنيكل نادرةً وغير شائعة، وتوجد في أشكال معيّنة محدّدة، فالنيكل في حالة الأكسدة 0 (الصفري) يلاحظ في المعقّد رباعي كربونيل النيكل Ni(CO)4، وهو مركّب نيكل عضوي يوجد على هيئة سائل متطاير، والذي يتفكّك إلى النيكل عند تسخينه؛ وتُستغَلّ هذه الخاصّية في الحصول على شكل نقيٍّ من النيكل في عملية موند.[41] من المعقّدات الأخرى للنيكل في حالة الأكسدة الصفرية معقّد مضاعف (حلقي أوكتاديين) النيكل الصفري [ط 117] والمستخدم في مجال الاصطناع العضوي وكيمياء النيكل العضوية.[42] أمّا النيكل الأحادي فهو أيضاً غير شائع، وتوجد حالة الأكسدة هذه غالباً في المعقّدات التناسقية الحاوية على رابطة Ni-Ni، مثل معقّد K4[Ni2(CN)6] المُستحصَل من اختزال معقّد K2[Ni2(CN)6] باستخدام ملغمة صوديوم.[40] لا يعرف للنيكل الرباعي أيضاً إلّا عددٌ قليلٌ من المركّبات الكيميائية،[43][44] منها معقّدات تناسقية مع ربيطة الديكربوليد [ط 118] الضخمة (2-[C2B9H11]).[45][46]
التحليل الكيميائي
[عدل]

يمكن الكشف عن النيكل نوعياً وفق الوسائل التقليدية للكيمياء التحليلية عن طريق إجراء تفاعل تشكّل معقّد للنيكل الثنائي مع مركّب ثنائي ميثيل غليوكسيم. قبل إجراء تفاعل الكشف فإنّه عادةً ما تُرَسّب أملاح النيكل الثنائي من الوسط المائي عبر إضافة كبريتيد الأمونيوم، الأمر الذي يؤدّي إلى الحصول على راسبٍ أسودٍ من كبريتيد النيكل الثنائي، والذي يُرشَح ويُفصَل ثمّ يذاب في حمض النتريك للحصول على أيونات النيكل الثنائي المائية خضراء اللون. يجرى تفاعل الكشف النوعي مع ثنائي ميثيل غليوكسيم في وسطٍ قلويٍّ بإضافة هيدروكسيد الأمونيوم، ممّا يؤدّي إلى الحصول على راسب أحمر توتي من معقّد مضاعف (ثنائي ميثيل غليوكسيماتو) النيكل الثنائي.[منشور-ألم 4]
اعتماداً على تفاعل تشكّل هذا المعقّد فإنّه من الممكن وفق الوسائل التقليدية إجراء تحليل كمّي للنيكل الثنائي، وذلك مثلاً وفق أسلوب التحليل الوزني الكهربائي [ط 119] باستخدام أقطاب كهربائية من البلاتين؛ أو باستخدام أسلوب القياس الفولتي باستخدام قطب الزئبق المتقاطر [ط 120]. تُستخدَم حالياً وسائل التحليل الآلي الحديثة للكشف الكمّي عن النيكل، وذلك وفق تقنيات المطيافية الذرّية [ط 121] المختلفة، أو باستخدام تقنية مطيافية الكتلة المزوّدة ببلازما مقترنة بالحثّ [ط 122] على سبيل المثال؛ إذ تُمكّن هذه التقنيّات الحديثة من الحصول على نتائج للتحاليل حتى بكميّات نزرة.[منشور-ألم 5]
الدور الحيوي
[عدل]يصنّف النيكل ضمن المغذّيات الأساسية لبعض الكائنات الحيّة المجهرية والنباتات التي تحتاج إلى إنزيمات يوجد فيها هذا الفلز ضمن الموقع النشط الفعّال فيها؛[47] لذلك يلعب النيكل دوراً حيوياً مهمٍاً في البكتيريا والعتائق وكذلك الفطور.[48][49] يوجد عددٌ معتبرٌ من الأمثلة على الإنزيمات الحاوية على النيكل؛ منها إنزيم اليورياز [ط 123]، والذي يحفّز تفاعل حلمهة [ط 124] اليوريا ليشكّل الأمونيا والكربامات، وهو بالتالي ذو دورٍ حيويٍّ مهمٍّ؛[50][51] يوجد أيضاً نوعٌ من أنواع إنزيمات الهيدروجيناز [ط 125] المعتمدة على وجود النيكل والحديد في تركيبها، والمسؤولة عن تحفيز تفاعل أكسدة واختزال الهيدروجين الجزيئي إلى بروتونات وإلكترونات والعكس بالعكس.[48] يُذكَر أيضاً العامل المرافق F430 [ط 126]، والحاوي على النيكل ضمن رباعي بيرول [ط 127]، والموجود ضمن إنزيم ميثيل-مرافق الإنزيم M ريدوكتاز [ط 128] والذي يحفّز التشكل الحيوي للميثان.[52] يوجد أيضاً صنفٌ من إنزيمات هيدروجيناز أحادي أكسيد الكربون [ط 129] الحاوي على عناقيد تجميعيّة من ذرّات Fe-Ni-S في بنيته.[53] من إنزيمات النيكل أيضاً كلٌ من سوبر أكسيد ديسميوتاز [ط 130]؛[54] وغلايوكسيلاز [ط 131].[55]
لا يوجد دليلٌ قاطعٌ على أنّ النيكل من العناصر المغذّية الأساسية بالنسبة للإنسان، ولكن قد يكون النيكل ضرورياً بالنسبة للبكتريا الموجودة في الأمعاء الغليظة، وذلك بقيامه بدور مغذٍّ للمُعينَات الحيوية [ط 132].[56] لم تؤكّد الأكاديمية الوطنية للطبّ [ط 133] في الولايات المتّحدة الأمريكية أنّ النيكل من العناصر المغذّية الأساسية بالنسبة للإنسان، لذلك لم تضع لهذا العنصر قِيَماً للمدخول الكافي [ط 134] أو الكمّيّة المُوصى بتناولها [ط 135]؛ في حين أنّها وضعت الحدّ الأقصى للمدخول المقبول [ط 136] بمقدار 1000 ميكروغرام/اليوم على هيئة أملاح نيكل منحلّة؛ إذ أنّ ما يُمتصّ من النيكل يُطرَح في البول.[57] تعدّ أواني الطهو من المصادر التي قد يدخل فيها النيكل إلى الغذاء، وذلك من خلال عملية الرشح في أثناء الطهو؛ فقد وُجِدَ مثلاً أنّه بعد 10 عمليات طهو لصلصة الطماطم بذات الآنية المصنوعة من الفولاذ المقاوم للصدأ الحاوي على النيكل فقد رَشَحَ إليها مقدار 88 ميكروغرام من النيكل.[58]
الأثر البيئي
[عدل]يوجد النيكل عادةً بتراكيز منخفضة في الطبيعة؛ وهي لا تتجاوز 20 نانوغرام/م3 في الغلاف الجوّي؛ و100 مغ/كغ في التربة؛ و10 مغ/كغ في الغطاء النباتي؛ و10 ميكروغرام/ليتر في الماء العذب؛ و1 ميكروغرام/ليتر في ماء البحر.[59] يساهم النشاط البشري في رفع مستويات النيكل في الطبيعة؛ وذلك يتمثّل في عدّة أشكال، مثل رشوح النيكل من صنابير المياه المطليّة بالنيكل ممّا يؤدّي إلى تلوّث المياه والتربة؛ وكذلك طرح مخلّفات تعدين النيكل الصلبة من غير معالجة إلى الوسط البيئي، أو طرح أملاحه في مياه الصرف. من مصادر التعرّض الأخرى كلّ من حرق الوقود الأحفوري ودخان التبغ.[60]
الأهمية الاقتصادية
[عدل]سك النقود
[عدل]
شاع استخدام النيكل في سكّ النقود المعدنية منذ أواخر القرن الثامن عشر وأوائل القرن التاسع عشر؛ فعلى سبيل المثال سَكّتِ الإمبراطورية البريطانية سنة 1786 في مدينة برمنغهام نقوداً معدنيّة من النيكل من أجل إدارة التعاملات المالية في ماليزيا.[وب-ألم 2] أمّا في الولايات المتّحدة فتُستخدَم تسمية « نيكل » [ط 137] عبر تاريخها للإشارة إلى عددٍ من فئاتِ النقود المعدنية الحاوية على النيكل في تركيبها، مثل « سنت العقاب الطائر » [ط 138] المتدوال بين سنتي 1857–1858، و« سنت الرأس الهندي » [ط 139] المتداول بين سنتي 1859–1909، بالإضافة إلى « نيكل ثلاثة سنتات » [ط 140] المتداول بين سنتي 1865–1889. أمّا حالياً فتُستخدَم التسمية للإشارة إلى فئة خمسة سنتات التي لا تزال متداولةً حالياً، وهي تحوي على 25% من تركيبها من فلز النيكل و75% المتبقيّة من النحاس، وذلك يعادل وزناً مقدار 1.1 غرام بالنسبة للنيكل، ومقدار 3.75 غرام من النحاس. مع ارتفاع أسعار الفلزّات عالمياً منذ بداية القرن الحادي والعشرين فقد فاق الثمن الحقيقي لهذه القطعة النقدية مقدار قيمتها النقدية؛ ممّا جعلها هدفاً مغرياً للبعض، الذين بدأوا بصهرها والاتّجار بفلزَّي النيكل والنحاس لكسب مرابح مالية؛ الأمر الذي دفع دار السكّ الأمريكية [ط 141] إلى تجريم صهر وتصدير فئات النقود الأمريكية؛[وب-إنج 11] وفرضت غراماتٍ مالية قد تصل إلى 10 آلاف دولار أمريكي، وبالسجن لمدّة قد تصل إلى خمس سنوات.[وب-إنج 12] تجدر الإشارة إلى أنه في أثناء الحرب العالمية الثانية جرى سكّ هذه الفئة النقدية من غير إدخال النيكل في تركيبها، من أجل استخدام هذا الفلزّ في تطبيقات عسكرية.[5]
أدّى ارتفاع سعر النيكل عالمياً إلى التفكير بتأمين بديلٍ عن هذا الفلز في سكّ النقود المعدنية في مختلف أرجاء العالم، ولكنه لا يزال داخلاً مثلاً في تركيب نقود اليورو المعدنية من فئة 1 و2 يورو؛ وفي نقود الجنيه الإسترليني المعدنية من فئة 20 و50 بنس وكذلك 1 و2 جنيه إسترليني؛ وفي نقود الدولار الأمريكي المعدنية من فئة 5 و10 و25 و50 سنت وكذلك 1 دولار أمريكي.[وب-إنج 13] طرحت المملكة المتحدة تدريجياً منذ سنة 2012 نقوداً معدنية مصنوعة من الفولاذ المطلي بالنيكل لفئتي 5 و10 بنس، وهو ما حدا بالبعض إلى الاعتراض بسبب حساسيتهم تجاه النيكل.[وب-إنج 14]
القيمة السوقية
[عدل]ازداد سعر النيكل في السوق العالمية بكل مطّردٍ منذ بدايات القرن الحادي والعشرين، ففي شهر أبريل من سنة 2007 كان سعر هذا الفلز 52,300 دولار أمريكي/الطن.[وب-إنج 15] انخفض سعر الطن بعد ذلك بشكلٍ كبير، ووصل في سنة 2017 إلى سعر 11,000 دولار أمريكي/الطن.[وب-إنج 16] في أثناء الغزو الروسي لأوكرانيا في سنة 2022 زادت المخاوف بأنّ العقوبات على روسيا قد تؤدّي إلى ارتفاعٍ حادٍّ قصير الأجل [ط 142] في سعر النيكل في السوق العالمية، ممّا أدّى بالفعل إلى تضاعف سعر النيكل بأربع مرّات في مجرد يومَين، ليصل إلى 100,000 دولار أمريكي/الطن في شهر مارس من سنة 2022.[وب-إنج 17][وب-إنج 18] وفي تلك الفترة أيضاً ألغت بورصة لندن للمعادن [ط 143] عقوداً بقيمة 3.9 بليون دولار أمريكي، وعلّقت التداول التجاري بالنيكل لمدّة أكثر من أسبوع.[وب-إنج 19]
الاستخدامات
[عدل]
تنقسم تطبيقات النيكل الصناعية على النحو التالي: 68% في صناعة الفولاذ المقاوم للصدأ؛ 10% في صناعة السبائك اللاحديدية [ط 144]؛ 9% في مجال الطلي الكهربائي [ط 145]؛ 7% في مجال سبائك الفولاذ المختلفة؛ 3% في ورشات المسابك [ط 146]؛ و4% في استخدامات أخرى؛.[وب-إنج 20] وتلك تتضمّن صناعة البطّاريات بما فيها بطّاريات المَرْكَبات الكهربائية.[وب-إنج 21]
صناعة السبائك
[عدل]يدخل النيكل بشكلٍ واسعٍ وبارزٍ في صناعة عددٍ معتبرٍ من السبائك، إذ يساهم في تعزيز مقاومة الشدّ [ط 147] والمتانة [ط 148] وزيادة اللدونة [ط 149]. من أهمّ الفلزّات التي تُسبَك مع النيكل كلّ من الحديد والكروم والكوبالت والنحاس والألومنيوم، بالإضافة إلى الرصاص والذهب والفضّة. تعدّ سبيكة الفولاذ المقاوم للصدأ [ط 150] من سبائك النيكل المعروفة، بالإضافة إلى سبائك أخرى تتضمّن: سبيكة ألنيكو (من الألومنيوم والنيكل والكوبالت)؛ وسبيكة برمالوي [ط 151] (من النيكل والحديد)؛ وسبيكة إيلنفار [ط 152] (من الحديد والنيكل والكروم)؛ وسبيكة إنفار [ط 153] (من النيكل والحديد)؛ وكذلك سبيكة إنكونيل [ط 154] (من النيكل والكروم)؛ وسبيكة إنكولوي [ط 155] وسبيكة نيمونيك [ط 156] (وهي علامات تجارية لسبائك فائقة مقاومة للتآكل مؤلّفة من النيكل والكروم)؛ وكذلك سبيكة مونيل [ط 157] وسبيكة كونستانتان [ط 158] (من النيكل والنحاس).[19]
لسبائك النيكل تطبيقات مختلفة، فهي على العموم تتميّز بمقاومتها للتآكل والحرارة، لذا تُستخدَم مثلاً في صناعة العنفات الغازية [ط 159]. من جهةٍ أخرى تتميّز سبيكة كونستانتان بأنّ ذات مقاومة نوعية [ط 160] ثابتة ضمن مجال واسع من درجات الحرارة، لذا تجد لها استخدامات في صناعة المقاومات الكهربائية. أمّا سبيكة فضّة النيكل [ط 161] فهي مقاومة للتآكل بشكل كبير، وتُستخدَم في صناعة أدوات تناول الطعام؛ وسبيكة النيكل النحاسي تُستخدَم بشكلٍ كبيرٍ في سكّ النقود المعدنية. في حين تُستخدَم سبيكة نيكل راني [ط 162]، وهي علامة تجارية لسبيكة دقيقة الحبيبات من النيكل والألومنيوم، في مجال التحفيز الكيميائي وذلك بشكلٍ واسعٍ في تفاعلات الهدرجة [ط 163].[61]
متفرقات
[عدل]
يدخل النيكل ومركّباته وسبائكه في طيفٍ واسعٍ من التطبيقات المختلفة في مجالات الحياة اليومية؛ تتفاوت بين صناعة البطّاريات الكهربائية (مثل بطارية النيكل وهيدريد الفلز وبطارية النيكل والهيدروجين) وبين صناعة الخضب والطلي الكهربائي بالنيكل.[وب-إنج 22] إذ تُستخدَم مركّبات النيكل اللاعضوية خضباً لإضافة اللون الأخضر في صناعة الزجاج. أمّا فلزّ النيكل فكان يستخدم سابقاً في صناعة إطارات النظّارات. ونظراً لتمتّع النيكل بمقاومةٍ كيميائية تجاه الأحماض والقلويّات، فإنّه يُستخدَم في صناعة بعض التجهيزات المخبرية مثل البواتق [ط 165]. يُستخدَم أسلوب الطلي الكهربائي بالنيكل من أجل منع تآكل المشغولات المعدنية.[62] في حين تُستخدَم رغوة النيكل [ط 166] في صناعة أقطاب الانتشار الغازي [ط 167] في خلايا الوقود القلوية [ط 168].[63]
يُستخدَم النيكل مادّةً رابطةً [ط 169] في صناعة المنتَجات الصلدة المبنية على كربيد التنغستن، إذ يُضاف بنسبةٍ تتراوح بين 6-12% وزناً؛ ممّا يساهم في إضفاء خواص مغناطيسية على المنتَجات النهائية، بالإضافة إلى خواصَّ مقاومةٍ للتآكل؛ إلّا أن تلك المنتَجات ذات صلادة أقلّ من المنتَجات التي تستخدم الكوبالت مادّةً رابطةً فيها.[64] للنظير نيكل-63 63Ni عمر نصف مقداره 100.1 سنة، وهو يدخل في مجال الصناعات الإلكترونية في تركيب أجهزة كريترون [ط 170] إذ يعد مصدراً لانبعاث جسيمات بيتّا [ط 171] مرتفعة السرعة؛[وب-إنج 23] ويُستخدَم لذلك في تركيب مكشاف التقاط الإلكترون [ط 172] في أجهزة مطيافية الاستشراب الغازي [ط 173]؛ وتجرى دراساتٌ لاستخدامه مصدراً للطاقة في البطّاريات البيتافولتائية.[65][66]
المخاطر
[عدل]| نيكل | |
|---|---|
| المخاطر | |
| رمز الخطر وفق GHS |    |
| وصف الخطر وفق GHS | خطر |
| بيانات الخطر وفق GHS | H317, H351, H372, H402, H412 |
| بيانات وقائية وفق GHS | P201, P202, P260, P264, P270, P272, P273, P280, P302+352, P308+313, P333+313, P363, P405, P501 [وب-إنج 24] |
| NFPA 704 |
|
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
توجد أشكال عديدة للتعرّض لعنصر النيكل؛ ونظراً لكون هذا العنصر جوهرياً في غذاء النباتات، لذلك يمثّل الاستهلاك الفموي عبر تناول الغذاء مصدر تعرّضٍ طبيعيٍّ أساسيٍّ للنيكل.[67] بالرغم من ذلك، فإنّ النيكل يوجد عادةً بتراكيز منخفضة في الطبيعة؛ وما يتناوله الإنسان فإنّه يطرح يومياً مع البول أو البراز من غير امتصاص.[59] تصنّف مركّبات النيكل ضمن المسرطنات [ط 174]؛[68] وخاصّةً عند استنشاق أبخرتها،[69][70] وذلك وفق بيانات لدراسات تقييمية للحالة الصحّية للعمال الذين يتعرّضون لأبخرة مركّبات النيكل في أثناء عمليات التعدين؛[71] بالإضافة إلى دراسات داعمة لتجارب أجريت على الجرذان والفئران.[72][73] يمثّل مركّب رباعي كربونيل النيكل خاصّةً واحداً من مركّبات النيكل الخطرة، فخطورته تنبع من كونه غازاً سامّاً، وذلك من فلز النيكل بحدّ ذاته، ومن خطر انطلاق غاز أحادي أكسيد الكربون السام.[74]
يمثّل النيكل ومركّباته خطراً مهنياً؛[75] وخاصّةً على النسوة العاملات في مجال التعدين.[76] يمكن أن يتعرّض الإنسان إلى النيكل في مكان العمل عبر استنشاق الأبخرة أو الابتلاع أو التماس مع الجلد أو العين. في الولايات المتّحدة الأمريكية حدّدت إدارة السلامة والصحّة المهنية [ط 175] حدّ التعرّض المسموح [ط 176] به من النيكل في مكان العمل بمقدار 1 مغ/م3 ليوم عمل من ثمان ساعات؛ أمّا المعهد الوطني للسلامة والصحّة المهنية [ط 177] فوضع حدّ التعرّض الموصى به [ط 178] من النيكل بمقدار 0.015 مغ/م3؛ ويمثّل مقدار 10 مغ/م3 الحدّ الذي يسبّب خطورةً فوريةً للحياة أو الصحّة [ط 179].[وب-إنج 25]
قد يؤدّي التماس المباشر للجلد مع فلز النيكل عند البعض إلى حدوث نوعٍ من التهاب الجلد التماسيّ التحسّسيّ [ط 180]، والذي يُعرَف أيضاً تحت اسم «حساسية النيكل» [ط 181]؛[وب-إنج 26] وهي حالة شائعة الانتشار نسبياً.[77] إذ يكثر دخول النيكل في المجوهرات، وخاصّةً في صياغة الأقراط.[78] كما وجد في سنة 2002 أن نقود اليورو المعدنية من فئة 1 و2 يورو كانت حاويةً على تراكيز مرتفعة نسبياً من النيكل؛[79] ممّا أدّى إلى ظهور حالات من حساسية النيكل لدى البعض.[وب-إنج 14]
طالع أيضاً
[عدل]| نيكل في المشاريع الشقيقة: | |
| |
الهوامش
[عدل]- مصطلحات
- ^ baitong
- ^ Cupronickel
- ^ Bactrian kings
- ^ Agathocles of Bactria
- ^ Euthydemus II
- ^ Pantaleon
- ^ Erzgebirge
- ^ Nickel
- ^ nickeline
- ^ niccolite
- ^ Axel Fredrik Cronstedt
- ^ cobalt blue
- ^ pyrrhotite
- ^ Widmanstätten pattern
- ^ inner core
- ^ outer core
- ^ iron meteorites
- ^ Kamacite
- ^ Taenite
- ^ Joseph Louis Proust
- ^ Campo del Cielo
- ^ Pentlandite
- ^ Millerite
- ^ Nickeline
- ^ laterite
- ^ Limonite
- ^ Garnierite
- ^ Ultramafic rock
- ^ Népouite
- ^ Willemseite
- ^ magmatic sulfide deposits
- ^ Bunsenite
- ^ Awaruite
- ^ Clarion Clipperton Zone
- ^ polymetallic nodules
- ^ rare-earth metals
- ^ International Seabed Authority (ISA)
- ^ Sustainable Development Goals
- ^ Sudbury Basin
- ^ Norilsk
- ^ Kola Peninsula
- ^ Queensland
- ^ high pressure acid leaching
- ^ roasting
- ^ reduction
- ^ pyrometallurgical techniques
- ^ Matte
- ^ refining
- ^ hydrometallurgical techniques
- ^ Froth flotation
- ^ Slag
- ^ Sherritt-Gordon process
- ^ Electrorefining
- ^ Anode
- ^ Cathode
- ^ Electrolyte
- ^ Mond process
- ^ Ludwig Mond
- ^ Nickel tetracarbonyl
- ^ Iron pentacarbonyl
- ^ tetracobalt dodecacarbonyl
- ^ pellets
- ^ Grignard reagent
- ^ Nickel oxalate
- ^ Nuclear isomer
- ^ nuclear binding energy
- ^ Nucleon
- ^ Nuclide
- ^ MeV/nucleon
- ^ Photodisintegration
- ^ extinct radionuclide
- ^ silicon burning process
- ^ Type Ia supernova
- ^ light curve
- ^ Cosmogenic nuclide
- ^ supernova nucleosynthesis
- ^ doubly magic
- ^ neutron capture
- ^ Transmission electron microscopy
- ^ nanocrystal
- ^ single wall carbon nanotube
- ^ Madelung rule
- ^ Aufbau principle
- ^ fine structure
- ^ Ferromagnetism
- ^ Curie temperature
- ^ Face-centered cubic crystal system (fcc)
- ^ Lattice constant
- ^ Formula unit
- ^ Unit cell
- ^ malleable and ductile
- ^ Tensile strength
- ^ compressive strength
- ^ nanoparticles
- ^ Tetrahedral molecular geometry
- ^ Square planar molecular geometry
- ^ paramagnetic
- ^ diamagnetic
- ^ Trigonal crystal system
- ^ Monoclinic crystal system
- ^ hydrated
- ^ nickel electroplating
- ^ Dichlorobis(triphenylphosphine)nickel(II)
- ^ Ethylenediamine
- ^ Dimethylglyoxime
- ^ bidentate
- ^ Bis(dimethylglyoximato)nickel(II)
- ^ Potassium tetracyanonickelate(II)
- ^ Nickelocene
- ^ metallocenes
- ^ Sandwich compound
- ^ Cyclopentadienyl anion
- ^ Staggered conformation
- ^ Nickel(III) trihalophosphines
- ^ σ-donor ligands
- ^ Organophosphine
- ^ Bis(cyclooctadiene)nickel(0)
- ^ Dicarbollide
- ^ Electrogravimetry
- ^ dropping mercury electrode (DME)
- ^ Atomic spectroscopy
- ^ Inductively coupled plasma mass spectrometry (ICP-MS)
- ^ urease
- ^ hydrolysis
- ^ NiFe hydrogenase
- ^ cofactor F430
- ^ tetrapyrrole
- ^ methyl coenzyme M reductase
- ^ carbon monoxide dehydrogenase
- ^ superoxide dismutase
- ^ glyoxalase I
- ^ prebiotic
- ^ National Academy of Medicine (NAM)
- ^ Adequate Intakes (AIs)
- ^ Recommended Dietary Allowances (RDAs)
- ^ Tolerable Upper Intake Level (UL)
- ^ nickel
- ^ Flying Eagle cent
- ^ Indian Head cent
- ^ Three-cent nickel
- ^ United States Mint
- ^ short squeeze
- ^ London Metal Exchange
- ^ nonferrous alloys
- ^ electroplating
- ^ foundries
- ^ tensile strength
- ^ toughness
- ^ elastic limit
- ^ Stainless steel
- ^ Permalloy
- ^ Elinvar
- ^ Invar
- ^ Inconel
- ^ Incoloy
- ^ Nimonic
- ^ Monel
- ^ Constantan
- ^ Gas turbine
- ^ specific electrical resistance
- ^ Nickel silver
- ^ Raney nicke
- ^ hydrogenation reactions
- ^ Turboprop
- ^ Crucibles
- ^ Nickel foam
- ^ gas diffusion electrode
- ^ Alkaline fuel cell (AFC)
- ^ binder
- ^ krytron
- ^ beta particle emitter
- ^ electron capture detector (ECD)
- ^ Gas chromatography
- ^ carcinogens
- ^ Occupational Safety and Health Administration (OSHA)
- ^ permissible exposure limit (PEL)
- ^ National Institute for Occupational Safety and Health (NIOSH)
- ^ recommended exposure limit (REL)
- ^ IDLH
- ^ Allergic contact dermatitis
- ^ Nickel allergy
المراجع
[عدل]فهرس المراجع
[عدل]- المنشورات
- بالألمانية
- ^ Schubert (1974), p. 193–204.
- ^ ا ب ج Glöckner (1962), p. 103–107.
- ^ Jensen (1936), p. 265–281.
- ^ Schweda (2012), p. 87.
- ^ Feltkamp (1983), p. 351.
- بالإنكليزية
- ^ Carnes (2008), p. 290-294.
- ^ Rosenberg (1968), p. 1.
- ^ ا ب McNeil1990, p. 96–100.
- ^ Needham (1974), p. 237–250.
- ^ ا ب [a] Baldwin (1931a), p. 1749.
[b] Baldwin (1931b), p. 1954.
[c] Baldwin (1931c), p. 2325.
[d] Macdonald (1977), p. 888.
- ^ Weeks (1932), p. 22.
- ^ ا ب Rumble (2018), p. 104, 260.
- ^ Stixrude (1997), p. 24729-24739.
- ^ McDonough (2003), p. 559–577.
- ^ Rasmussen (1988), p. 107-112.
- ^ Calvo (2019), p. 118.
- ^ Minerals Center (2019), p. 112-113.
- ^ Minerals Center (2013), p. 108-109.
- ^ Mero (1977), p. 327–355.
- ^ Seabed Authority (2019), p. 7-35.
- ^ Minerals Center (2020), p. 112-113.
- ^ Minerals Center (2021), p. 112-114.
- ^ GUO (2011), p. 191.
- ^ ا ب ج Davis (2000), p. 7–13.
- ^ Mond (1890), p. 749–753.
- ^ Kerfoot (2000), p. 1.
- ^ Neikov (2009), p. 371.
- ^ Whaley (1957), p. 195–197.
- ^ Audi (2003), p. 3-128.
- ^ Shurtleff (1989), p. 522.
- ^ ا ب Fewell (1995), p. 653.
- ^ Pagel1997, p. 154–160.
- ^ Carboneau1995, p. 1-38.
- ^ Shiozawa2015, p. 15033.
- ^ ا ب Scerri (2007), p. 239-240.
- ^ Petrucci (2002), p. 950.
- ^ Miessler (1999), p. 38.
- ^ Zhu (2007), p. e301-e303.
- ^ Kittel1996, p. 449.
- ^ Sharma (2018), p. 4102.
- ^ Mizuno1961, p. 1574-1580.
- ^ Lascelles (2005), p. 1.
- ^ Aderonke (2019), p. 1-9.
- ^ Seiler1980, p. 2255–2260.
- ^ ا ب Housecroft (2008), p. 729.
- ^ Nature (1898), p. 63–64.
- ^ Wilke (1988), p. 185–206.
- ^ Camasso (2015), p. 1218–1220.
- ^ Baucom (1971), p. 6469–6475.
- ^ Spokoyny (2010), p. 5339–5343.
- ^ Warren (1967), p. 470–471.
- ^ Mulrooney (2003), p. 239–261.
- ^ ا ب Sydor (2013), p. 375–416.
- ^ Zamble (2017), p. 285.
- ^ Covacci (1999), p. 1328–1333.
- ^ Cox (2000), p. 443–448.
- ^ Ragsdale (2014), p. 125–145.
- ^ Wang (2014), p. 71-97.
- ^ Szilagyi (2004), p. 3018–3019.
- ^ Greig (2006), p. 217-223.
- ^ Zambelli (2013), p. 321–357.
- ^ Nutrition Board (2001), p. 521–529.
- ^ [a] Kamerud (2013), p. 9495–9501.
[b] Flint (1997), p. 115–126.
- ^ ا ب Rieuwerts (2015), p. 255.
- ^ Genchi (2020), p. 679.
- ^ Yang (2006), p. 1.
- ^ Mosallanejad (2016), p. 147–155.
- ^ Kharton (2011), p. 166.
- ^ Cheburaeva (1992), p. 423–425.
- ^ Uhm (2016), p. 773–777.
- ^ Bormashov (2018), p. 41–47.
- ^ Haber (2017), p. S1–S18.
- ^ IARC (2012), p. 169-218.
- ^ Cogliano (2011), p. 1827–1839.
- ^ Heim (2007), p. 126–137.
- ^ International Committee (1990), p. 1–82.
- ^ Toxicology Program (1996), p. 1–365.
- ^ Oller (2008), p. 262–275.
- ^ Barceloux (1999), p. 239–258.
- ^ Colditz (2015), vol. 2, p. 828–831.
- ^ [a] Vaktskjold (2006), p. 41–50.
[b] Vaktskjold (2007), p. 327–338.
[c] Vaktskjold (2008a), p. 99–115.
[d] Vaktskjold (2008b), p. 825–833.
- ^ Schnuch (2002), p. 32–39.
- ^ Thyssen (2007), p. 287–299.
- ^ Nestle (2002), p. 132.
- وب
- بالألمانية
- ^ "Häufigkeit in der Erdkruste". uniterra.de (بالألمانية). Archived from the original on 2020-02-21.
- ^ "nikkelen dubbele wapenstuiver Utrecht". nederlandsemunten (بالألمانية). Archived from the original on 2015-01-07. Retrieved 2023-08-09.
- بالإنكليزية
- ^ "Nickel: Nickel mineral information and data". Mindat.org (بالإنجليزية). Archived from the original on 2016-03-03. Retrieved 2023-08-08.
- ^ "Nickel & compounds: Overview". Department of Sustainability, Environment, Water, Population and Communities in Australia (بالإنجليزية). Archived from the original on 2011-12-08. Retrieved 2023-08-09.
- ^ "Mineral Species containing Nickel (Ni )". Webmineral (بالإنجليزية). Archived from the original on 2022-04-07. Retrieved 2023-08-08.
- ^ "Nichel Statistics" (PDF). U.S. Geological Survey (بالإنجليزية). 1 Apr 2014. Archived from the original (PDF) on 2014-08-12.
- ^ "Nickel reserves worldwide by country 2020". Statista (بالإنجليزية). Archived from the original on 2022-04-24. Retrieved 2023-08-11.
- ^ "Isotopes of the Element Nickel". Jefferson science associates (بالإنجليزية). Archived from the original on 2017-10-18. Retrieved 2023-08-10.
- ^ "Nuclear synthesis". Georgia State University (بالإنجليزية). Archived from the original on 2022-04-08. Retrieved 2023-08-10.
- ^ Castelvecchi, Davide (22 Apr 2005). "Atom Smashers Shed Light on Supernovae, Big Bang" (بالإنجليزية). Archived from the original on 2012-07-23.
- ^ W., P. (23 Oct 1999). "Twice-magic metal makes its debut – isotope of nickel". Science News (بالإنجليزية). Archived from the original on 2012-05-24.
- ^ ا ب "NIST Atomic Spectra Database Levels Form". NIST (بالإنجليزية). Archived from the original on 2011-03-20. Retrieved 2023-08-08.
- ^ "United States Mint Moves to Limit Exportation & Melting of Coins". United States Mint (بالإنجليزية). 14 Dec 2006. Archived from the original on 2006-05-27.
{{استشهاد ويب}}:|archive-date=/|archive-url=timestamp mismatch (help) - ^ "Prohibition on the Exportation, Melting, or Treatment of 5-Cent and One-Cent Coins". Federal Register (بالإنجليزية). 16 Apr 2007. Archived from the original on 2022-04-24. Retrieved 2023-08-09.
- ^ "Coin Specifications". United States Mint (بالإنجليزية). Archived from the original on 2022-05-06. Retrieved 2023-08-09.
- ^ ا ب Lacey, Anna (22 Jun 2013). "A bad penny? New coins and nickel allergy". BBC Health Check (بالإنجليزية). Archived from the original on 2013-08-07. Retrieved 2023-08-09.
- ^ "LME nickel price graphs". London Metal Exchange (بالإنجليزية). Archived from the original on 2009-09-28. Retrieved 2009-06-06.
{{استشهاد ويب}}:|archive-date=/|archive-url=timestamp mismatch (help) - ^ "London Metal Exchange". London Metal Exchange (بالإنجليزية). Archived from the original on 2017-09-20. Retrieved 2023-08-08.
- ^ Hume, Neil; Lockett, Hudson (8 Mar 2022). "LME introduces emergency measures as nickel hits $100,000 a tonne". Financial Times (بالإنجليزية). Archived from the original on 2022-03-27. Retrieved 2023-08-08.
- ^ Burton, Mark; Farchy, Jack; Cang, Alfred. "LME Halts Nickel Trading After Unprecedented 250% Spike". Bloomberg News (بالإنجليزية). Archived from the original on 2022-05-06. Retrieved 2022-03-08.
- ^ Farchy, Jack; Cang, Alfred; Burton, Mark (14 Mar 2022). "The 18 Minutes of Trading Chaos That Broke the Nickel Market". Bloomberg News (بالإنجليزية). Archived from the original on 2022-04-27. Retrieved 2023-08-09.
- ^ "First uses of nickel". Nickel Institute (بالإنجليزية). Archived from the original on 2017-09-21.
- ^ Treadgold, Tim (11 Aug 2019). "Gold Is Hot But Nickel Is Hotter As Demand Grows For Batteries In Electric Vehicles". Forbes (بالإنجليزية). Archived from the original on 2022-05-01. Retrieved 2023-08-09.
- ^ "Nickel Compounds – The Inside Story". Nickel Institute (بالإنجليزية). Archived from the original (PDF) on 2018-08-31.
- ^ "Silicon Investigations Krytron Pulse Power Switching Tubes". Silicon Investigations (بالإنجليزية). Archived from the original on 2011-07-06. Retrieved 2023-08-10.
{{استشهاد ويب}}:|archive-date=/|archive-url=timestamp mismatch (help) - ^ "Nickel". Sigma Aldrich (بالإنجليزية). Archived from the original on 2021-04-15. Retrieved 2023-08-13.
- ^ "CDC – NIOSH Pocket Guide to Chemical Hazards – Nickel metal and other compounds (as Ni)". CDC (بالإنجليزية). Archived from the original on 2017-07-18. Retrieved 2023-08-08.
- ^ Dow, Lea (3 Jun 2008). "Nickel Named 2008 Contact Allergen of the Year". Nickel Allergy Information (بالإنجليزية). Archived from the original on 2009-02-03.
معلومات المراجع الكاملة
[عدل]- الكتب
- الألمانية
- Wolfgang Glöckner (1962), Die Komplexverbindungen (بالألمانية), Köln: Aulis Verlag, OCLC:841171024, QID:Q121363324
- Hans Lüschen (1979). Die Namen der Steine: das Mineralreich im Spiegel der Sprache - mit einem Wörterbuch, enthaltend über 1300 Namen von Mineralien, Gesteinen, Edelsteinen, Fabel- und Zaubersteinen (بالألمانية) (2nd ed.). Thun: Q114675722. ISBN:978-3-7225-6265-0. OCLC:6356236. OL:4189181M. QID:Q121359108.
- Herbert Feltkamp; Peter Fuchs; Heinz Sucker, eds. (1983). Pharmazeutische Qualitätskontrolle (بالألمانية). Stuttgart: Q58644684. ISBN:978-3-13-611501-5. OCLC:14535063. QID:Q121461684.
- Eberhard Schweda; Gerhart Jander (2012). Jander/Blasius - Anorganische Chemie II: quantitative Analyse und Präparate (بالألمانية) (16th ed.). Stuttgart: S. Hirzel Verlag. ISBN:978-3-7776-2133-3. OCLC:762070580. QID:Q121438588.
- الإنجليزية
- Samuel J. Rosenberg (1968), Nickel and its alloys (PDF) (بالإنجليزية), Washington, D.C.: National Institute of Standards and Technology, OCLC:271046165, QID:Q121349068
- Joseph Needham (1974). Science and civilisation in China (بالإنجليزية). Cambridge: Cambridge University Press. ISBN:978-0-521-08571-7. OCLC:652409197. OL:7731599M. QID:Q121352782.
- Ian McNeil, ed. (1990). An Encyclopedia of the history of technology (بالإنجليزية). London: Routledge. ISBN:978-0-415-01306-2. OCLC:1158874922. OL:18352382M. QID:Q121351885.
- Charles Kittel (1996). Introduction to Solid State Physics (بالإنجليزية) (7th ed.). New York City: Wiley. ISBN:978-0-471-11181-8. OCLC:473472310. OL:786207M. QID:Q121344702.
- B. E. J. Pagel (1997). Nucleosynthesis and chemical evolution of galaxies (بالإنجليزية). Cambridge: Cambridge University Press. ISBN:978-0-521-55061-1. OCLC:36461636. OL:660608M. QID:Q121435234.
- Gary L. Miessler; Donald Arthur Tarr (1999). Inorganic chemistry (بالإنجليزية). Upper Saddle River: Prentice Hall. ISBN:978-0-13-841891-5. OCLC:39379369. OL:369303M. QID:Q121437603.
- Davis, Joseph R. (2000). Nickel, cobalt, and their alloys (بالإنجليزية). Russell Township: ASM International. ISBN:978-0-87170-685-0. OL:6793133M. QID:Q121423064.
- Scerri, Eric R. (2007). The periodic table: its story and its significance (بالإنجليزية). Oxford: Oxford University Press. ISBN:978-0-19-530573-9. OCLC:122340314. OL:26406596M. QID:Q121436635.
- Catherine E. Housecroft; A. G. Sharpe (2008). Inorganic chemistry (بالإنجليزية) (3rd ed.). Harlow: Pearson plc. ISBN:978-0-13-175553-6. OCLC:228102552. OL:22769942M. QID:Q121423495.
- Ralph H. Petrucci; William S. Harwood; F. Geoffrey Herring (2002). General chemistry: Principles and Modern Applications (بالإنجليزية) (8th ed.). Upper Saddle River: Prentice Hall. ISBN:978-0-13-014329-7. OCLC:46872308. OL:3946457M. QID:Q121437115.
- Oleg D. Neikov, ed. (2009). Handbook of Non-Ferrous Metal Powder: Technologies and Applications (بالإنجليزية). Amsterdam: Elsevier BV. ISBN:978-0-08-055940-7. OCLC:633685081. OL:34432988M. QID:Q121421423.
- Vladislav Kharton, ed. (2011). Handbook of Solid state electrochemistry: Electrodes, interfaces and ceramic membranes (بالإنجليزية). Weinheim: Wiley-VCH. Vol. 2. ISBN:978-3-527-32638-9. OCLC:880314201. OL:25190592M. QID:Q121461947.
- Graham Colditz, ed. (2015). The SAGE Encyclopedia of Cancer and Society (بالإنجليزية) (2nd ed.). Thousand Oaks: SAGE Publishing. DOI:10.4135/9781483345758. ISBN:978-1-4833-4573-4. OCLC:920521078. OL:28558450M. QID:Q121363648.
- John Rieuwerts (2015). The elements of environmental pollution (بالإنجليزية). London: Routledge, Taylor & Francis. ISBN:978-0-415-85919-6. OCLC:886492996. OL:28146790M. QID:Q121438681.
- Deborah B. Zamble; Magdalena Rowinska-Zyrek; Henryk Kozłowski, eds. (2017). The Biological Chemistry of Nickel (بالإنجليزية). Cambridge: Royal Society of Chemistry. ISBN:978-1-78262-498-1. OCLC:1007052796. OL:29341269M. QID:Q121436547.
- John R. Rumble; David R. Lide, Jr.; Thomas J. Bruno, eds. (2018). CRC handbook of chemistry and physics: ready-reference book of chemical and physical data (بالإنجليزية) (99th ed.). Boca Raton: CRC Press. ISBN:978-1-138-56163-2. OCLC:1043763515. OL:27842487M. QID:Q121365869.
- الإسبانية
- Miguel Calvo (2019). Construyendo la tabla periódica (بالإسبانية). Zaragoza: Prames. ISBN:978-84-8321-908-9. OCLC:1122719318. OL:29692567M. QID:Q69632156.
- الدوريات المُحكَّمة
- الألمانية
- K. A. Jensen (1936). "Zur Stereochemie des koordinativ vierwertigen Nickels". Zeitschrift für anorganische und allgemeine Chemie (بالألمانية). 229 (3): 265–281. DOI:10.1002/ZAAC.19362290304. ISSN:0044-2313. OCLC:5156761570. QID:Q56057850.
- K. Schubert (1974). "Ein Modell für die Kristallstrukturen der chemischen Elemente". Q27714162 (بالألمانية). 30 (1): 193–204. DOI:10.1107/S0567740874002469. ISSN:0567-7408. OCLC:5153433049. QID:Q54013592.
- الإنجليزية
- Ludwig Mond; Carl Langer; Friedrich Quincke (1890). "L.—Action of carbon monoxide on nickel". Journal of the Chemical Society. Transactions (بالإنجليزية). 57: 749–753. DOI:10.1039/CT8905700749. ISSN:0368-1645. OCLC:4658901911. QID:Q55867261.
- "The Extraction of Nickel from its Ores by the Mond Process". Nature (بالإنجليزية). 59 (1516): 63–64. 1898. Bibcode:1898Natur..59...63.. DOI:10.1038/059063A0. ISSN:1476-4687. OCLC:5842256909. QID:Q30049011.
- William H. Baldwin (1931). "The story of Nickel. I. How "Old Nick's" gnomes were outwitted". Journal of Chemical Education (بالإنجليزية). 8 (9): 1749. DOI:10.1021/ED008P1749. ISSN:0021-9584. OCLC:4666615165. QID:Q55897560.
- William H. Baldwin (1931). "The story of Nickel. Part II. Nickel comes of age". Journal of Chemical Education (بالإنجليزية). 8 (10): 1954. DOI:10.1021/ED008P1954. ISSN:0021-9584. OCLC:4666615548. QID:Q56057854.
- William H. Baldwin (1931). "The story of nickel. Part III. Ore, matte, and metal". Journal of Chemical Education (بالإنجليزية). 8 (12): 2325. DOI:10.1021/ED008P2325. ISSN:0021-9584. OCLC:4666615407. QID:Q56057855.
- Mary Elvira Weeks (1932). "The discovery of the elements. III. Some eighteenth-century metals". Journal of Chemical Education (بالإنجليزية). 9 (1): 22. DOI:10.1021/ED009P22. ISSN:0021-9584. OCLC:4666616687. QID:Q55872208.
- T. P. Whaley; C. C. Chappelow Jr. (1957). "Nickel Powder". Inorganic Syntheses (بالإنجليزية). 5. ISSN:0073-8077. QID:Q121422936.
- Mizuno, Joji (1961). "The Crystal Structure of Nickel Chloride Hexahydrate, NiCl2\cdot6H2O". Journal of the Physical Society of Japan (بالإنجليزية). 16 (6): 1574–1580. Bibcode:1961JPSJ...16.1574M. DOI:10.1143/JPSJ.16.1574. ISSN:0031-9015. OCLC:5175200367. QID:Q121315836.
- Leslie F. Warren; M. Frederick. Hawthorne (1967). "(3)-1,2-Dicarbollyl Complexes of Nickel(III) and Nickel(IV)". Journal of the American Chemical Society (بالإنجليزية). 89 (2): 470–471. DOI:10.1021/JA00978A065. ISSN:0002-7863. OCLC:4665440991. QID:Q56057852.
- Everett I. Baucom; Russell S. Drago (1971). "Nickel(II) and nickel(IV) complexes of 2,6-diacetylpyridine dioxime". Journal of the American Chemical Society (بالإنجليزية). 93 (24): 6469–6475. DOI:10.1021/JA00753A022. ISSN:0002-7863. OCLC:4665466620. QID:Q56057853.
- Agnes Margaret Macdonald, ed. (1977). Chambers twentieth century dictionary: with supplement (بالإنجليزية). Edinburgh: W. and R. Chambers. ISBN:978-0-550-10226-3. OCLC:16366777. OL:22475131M. QID:Q121357038.
- John L. Mero (1977). "Economic Aspects of Nodule Mining". Elsevier Oceanography Series (بالإنجليزية). 15: 327–355. DOI:10.1016/S0422-9894(08)71025-0. ISSN:0422-9894. OCLC:4922441478. QID:Q121297994.
- P. Seiler; J. D. Dunitz (1980). "The structure of nickelocene at room temperature and at 101 K". Acta Crystallographica (بالإنجليزية). B36: 2255–2260. DOI:10.1107/S0567740880008539. ISSN:0365-110X. OCLC:5153206743. QID:Q121410211.
- Kaare L. Rasmussen; John T. Wasson (1988). "Trace Element Partitioning between Taenite and Kamacite; Relationship to the Cooling Rates of Iron Meteorites". Meteoritics (بالإنجليزية). 23 (2): 107–112. Bibcode:1988Metic..23..107R. DOI:10.1111/J.1945-5100.1988.TB00905.X. ISSN:0026-1114. OCLC:5156691782. QID:Q56057849.
- Günther Wilke (1988). "Contributions to Organo-Nickel Chemistry". Angewandte Chemie International Edition (بالإنجليزية). 27 (1): 185–206. DOI:10.1002/ANIE.198801851. ISSN:1433-7851. OCLC:5153012710. QID:Q59486325.
- Richard Shurtleff; Edward Derringh (1989). "The most tightly bound nucleus". American Journal of Physics (بالإنجليزية). 57 (6): 552–552. Bibcode:1989AmJPh..57..552S. DOI:10.1119/1.15970. ISSN:0002-9505. OCLC:4434510201. QID:Q59702406.
- R. F. Cheburaeva; I. N. Chaporova; T. I. Krasina (1992). "Structure and properties of tungsten carbide hard alloys with an alloyed nickel binder". Powder Metallurgy and Metal Ceramics (بالإنجليزية). 31 (5): 423–425. DOI:10.1007/BF00796252. ISSN:1068-1302. OCLC:5656041635. QID:Q56057856.
- M. P. Fewell (1995). "The atomic nuclide with the highest mean binding energy". American Journal of Physics (بالإنجليزية). 63 (7): 653–658. DOI:10.1119/1.17828. ISSN:0002-9505. OCLC:203257819. QID:Q29012255.
- Flint GN; Packirisamy S (1997). "Purity of food cooked in stainless steel utensils". Food Additives and Contaminants (بالإنجليزية). 14 (2): 115–126. DOI:10.1080/02652039709374506. ISSN:0265-203X. OCLC:117492774. PMID:9102344. QID:Q34421526.
- Lars Stixrude; Evgeny Wasserman; Ronald E. Cohen (1997). "Composition and temperature of Earth's inner core". Journal of Geophysical Research (بالإنجليزية). 102 (B11): 24729–24739. Bibcode:1997JGR...10224729S. DOI:10.1029/97JB02125. ISSN:0148-0227. OCLC:5152077095. QID:Q29040115.
- Barceloux DG (1999). "Nickel". Journal of Toxicology: Clinical Toxicology (بالإنجليزية). 37 (2): 239–258. DOI:10.1081/CLT-100102423. ISSN:0731-3810. OCLC:7777342478. PMID:10382559. QID:Q33670258.
- Covacci A; Rappuoli R (1999). "Helicobacter pylori virulence and genetic geography". Science (بالإنجليزية). 284 (5418): 1328–1333. DOI:10.1126/SCIENCE.284.5418.1328. ISSN:0036-8075. OCLC:120175051. PMID:10334982. QID:Q33639332.
- G M Cox; J Mukherjee; G T Cole; A Casadevall; J R Perfect (2000). "Urease as a virulence factor in experimental cryptococcosis". Infection and Immunity (بالإنجليزية). 68 (2): 443–448. DOI:10.1128/IAI.68.2.443-448.2000. ISSN:0019-9567. OCLC:122214534. PMC:97161. PMID:10639402. QID:Q33886908.
- Derek G. E. Kerfoot (2000). "Nickel". Ullmann's Encyclopedia of Industrial Chemistry (بالإنجليزية). DOI:10.1002/14356007.A17_157. OCLC:8682098516. QID:Q54006804.
- A Schnuch; W Uter; J Geier; O Gefeller (2002). "Epidemiology of contact allergy: an estimation of morbidity employing the clinical epidemiology and drug-utilization research (CE-DUR) approach". Contact Dermatitis (بالإنجليزية). 47 (1): 32–39. DOI:10.1034/J.1600-0536.2002.470107.X. ISSN:0105-1873. OCLC:5153694390. PMID:12225411. QID:Q34842501.
- Markus O Speidel (2002). "Metallurgy: high nickel release from 1- and 2-euro coins". Nature (بالإنجليزية). 419 (6903): 132. DOI:10.1038/419132A. ISSN:1476-4687. OCLC:112454151. PMID:12226655. QID:Q34149208.
- G. Audi; O. Bersillon; J. Blachot; A.H. Wapstra (2003). "The Nubase evaluation of nuclear and decay properties". Nuclear Physics A (بالإنجليزية). 729 (1): 3–128. Bibcode:2003NuPhA.729....3A. DOI:10.1016/J.NUCLPHYSA.2003.11.001. ISSN:1873-1554. QID:Q28111992.
- W.F. McDonough (2003), Compositional Model for the Earth's Core (بالإنجليزية), vol. 2, pp. 547–568, Bibcode:2003TrGeo...2..547M, DOI:10.1016/B0-08-043751-6/02015-6, OCLC:7327695679, QID:Q55951843
- Scott B Mulrooney; Robert P Hausinger (2003). "Nickel uptake and utilization by microorganisms". FEMS Microbiology Reviews (بالإنجليزية). 27 (2–3): 239–261. DOI:10.1016/S0168-6445(03)00042-1. ISSN:0168-6445. OCLC:5155998618. PMID:12829270. QID:Q35164022.
- Robert K Szilagyi; Edward I Solomon (2004). "S K-edge X-ray absorption spectroscopic investigation of the Ni-containing superoxide dismutase active site: new structural insight into the mechanism". Journal of the American Chemical Society (بالإنجليزية). 126 (10): 3018–3019. DOI:10.1021/JA039106V. ISSN:0002-7863. OCLC:112264310. PMID:15012109. QID:Q34304404.
- Keith Lascelles; Lindsay G. Morgan; David Nicholls; Detmar Beyersmann (2005). "Nickel Compounds". Ullmann's Encyclopedia of Industrial Chemistry (بالإنجليزية). DOI:10.1002/14356007.A17_235.PUB2. OCLC:8682091498. QID:Q30053728.
- Neil Greig; Susan Wyllie; Tim J Vickers; Alan H Fairlamb (2006). "Trypanothione-dependent glyoxalase I in Trypanosoma cruzi". Biochemical Journal (بالإنجليزية). 400 (2): 217–23. DOI:10.1042/BJ20060882. ISSN:0264-6021. OCLC:110054774. PMC:1652828. PMID:16958620. QID:Q24682276.
- Jon Oyvind Odland; Ljudmila Vasiljevna Talykova; Valerij Petrovitsj Chashchin; Evert Nieboer; Yngvar Thomassen; Jon Øyvind Odland (2006). "Genital malformations in newborns of female nickel-refinery workers". Scandinavian Journal of Work, Environment & Health (بالإنجليزية). 32 (1): 41–50. DOI:10.5271/SJWEH.975. ISSN:0355-3140. OCLC:108720642. PMID:16539171. QID:Q51815223.
- Teng-Kuei Yang; Dong-Sheng Lee; Julia Haas (2006). "Raney Nickel". Encyclopedia of Reagents for Organic Synthesis (بالإنجليزية). DOI:10.1002/047084289X.RR001.PUB2. ISBN:978-0-470-84289-8. OCLC:8682062126. QID:Q57256370.
- Katherine E Heim; Hudson K Bates; Rusty E Rush; Adriana R Oller (2007). "Oral carcinogenicity study with nickel sulfate hexahydrate in Fischer 344 rats". Toxicology and Applied Pharmacology (بالإنجليزية). 224 (2): 126–137. DOI:10.1016/J.TAAP.2007.06.024. ISSN:0041-008X. OCLC:173990637. PMID:17692353. QID:Q51742411.
- Jacob Pontoppidan Thyssen; Allan Linneberg; Torkil Menné; Jeanne Duus Johansen (2007). "The epidemiology of contact allergy in the general population--prevalence and main findings". Contact Dermatitis (بالإنجليزية). 57 (5): 287–299. DOI:10.1111/J.1600-0536.2007.01220.X. ISSN:0105-1873. OCLC:5153727335. PMID:17937743. QID:Q34007584.
- Arild Vaktskjold; Ljudmila Vasiljevna Talykova; Valerij Petrovitsj Chashchin; Jon Oyvind Odland; Evert Nieboer (2007). "Small-for-gestational-age newborns of female refinery workers exposed to nickel". International Journal of Occupational Medicine and Environmental Health (بالإنجليزية). 20 (4): 327–338. DOI:10.2478/V10001-007-0034-0. ISSN:1232-1087. OCLC:264367873. PMID:18165195. S2CID:1439478. QID:Q51721211.
- Ying Zhu; Ping Yu; Xiaofeng Jin; Ding-sheng Wang (2007). "Curie temperature of body-centered-tetragonal Ni". Journal of Magnetism and Magnetic Materials (بالإنجليزية). 310 (2): e301–e303. DOI:10.1016/J.JMMM.2006.10.240. ISSN:0304-8853. OCLC:5900809482. QID:Q56611144.
- Colin Nuckolls; Michael Steigerwald (2008). "A stable tetraalkyl complex of nickel(IV)". Angewandte Chemie International Edition (بالإنجليزية). 48 (2): 290–294. DOI:10.1002/ANIE.200804435. ISSN:1433-7851. OCLC:5153759218. PMID:19021174. QID:Q34884701.
- Adriana R Oller; Daniel T Kirkpatrick; Ann Radovsky; Hudson K Bates (2008). "Inhalation carcinogenicity study with nickel metal powder in Wistar rats". Toxicology and Applied Pharmacology (بالإنجليزية). 233 (2): 262–275. DOI:10.1016/J.TAAP.2008.08.017. ISSN:0041-008X. OCLC:276445905. PMID:18822311. QID:Q55050665.
- Arild Vaktskjold; Ljudmila V Talykova; Valerij P Chashchin; Jon Ø Odland; Evert Nieboer (2008). "Spontaneous abortions among nickel-exposed female refinery workers". International Journal of Environmental Health Research (بالإنجليزية). 18 (2): 99–115. DOI:10.1080/09603120701498295. ISSN:0960-3123. OCLC:264128471. PMID:18365800. QID:Q45017905.
- Vaktskjold Arild; Talykova Ljudmila Vasiljevna; Chashchin Valerij Petrovitsj; Odland Jon Öyvind; Nieboer Evert (2008). "Maternal nickel exposure and congenital musculoskeletal defects". American Journal of Industrial Medicine (بالإنجليزية). 51 (11): 825–833. DOI:10.1002/AJIM.20609. ISSN:0271-3586. OCLC:5153631031. PMID:18655106. QID:Q44733225.
- Alexander M Spokoyny; Omar K Farha; Charles W Machan; Chunxing She; Charlotte L Stern; Tobin J Marks; Joseph T Hupp; Chad A Mirkin (2010). "Electronic tuning of nickel-based bis(dicarbollide) redox shuttles in dye-sensitized solar cells". Angewandte Chemie International Edition (بالإنجليزية). 49 (31): 5339–5343. DOI:10.1002/ANIE.201002181. ISSN:1433-7851. OCLC:652035000. PMID:20586090. QID:Q34123203.
- Vincent James Cogliano; Robert Baan; Kurt Straif; et al. (2011). "Preventable exposures associated with human cancers". Journal of the National Cancer Institute (بالإنجليزية). 103 (24): 1827–39. DOI:10.1093/JNCI/DJR483. ISSN:0027-8874. OCLC:776241441. PMC:3243677. PMID:22158127. QID:Q28255126.
- Xue-yi GUO; Wen-tang SHI; Dong LI; Qing-hua TIAN (2011). "Leaching behavior of metals from limonitic laterite ore by high pressure acid leaching". Nonferrous Metals Society of China Transactions (بالإنجليزية). 21 (1): 191–195. DOI:10.1016/S1003-6326(11)60698-5. ISSN:1003-6326. OCLC:4931762672. QID:Q56611143.
- Kristin L Kamerud; Kevin A Hobbie; Kim A Anderson (2013). "Stainless steel leaches nickel and chromium into foods during cooking". Journal of Agricultural and Food Chemistry (بالإنجليزية). 61 (39): 9495–9501. DOI:10.1021/JF402400V. ISSN:0021-8561. OCLC:5534278818. PMC:4284091. PMID:23984718. QID:Q34367168.
- Andrew M Sydor; Deborah B Zamble (2013). "Nickel metallomics: general themes guiding nickel homeostasis". Metal ions in life sciences (بالإنجليزية). 12: 375–416. DOI:10.1007/978-94-007-5561-1_11. ISSN:1559-0836. OCLC:5533657327. PMID:23595678. QID:Q38099790.
- Barbara Zambelli; Stefano Ciurli (2013). "Nickel and human health". Metal ions in life sciences (بالإنجليزية). 13: 321–357. DOI:10.1007/978-94-007-7500-8_10. ISSN:1559-0836. OCLC:5679767631. PMID:24470096. QID:Q38182483.
- Stephen W Ragsdale (2014). "Biochemistry of methyl-coenzyme M reductase: the nickel metalloenzyme that catalyzes the final step in synthesis and the first step in anaerobic oxidation of the greenhouse gas methane". Metal ions in life sciences (بالإنجليزية). 14: 125–145. DOI:10.1007/978-94-017-9269-1_6. ISSN:1559-0836. OCLC:5702524088. PMID:25416393. QID:Q38270456.
- Vincent C.-C. Wang; Stephen W. Ragsdale; Fraser A. Armstrong (2014). "Investigations of the efficient electrocatalytic interconversions of carbon dioxide and carbon monoxide by nickel-containing carbon monoxide dehydrogenases". Metal ions in life sciences (بالإنجليزية). 14: 71–97. DOI:10.1007/978-94-017-9269-1_4. ISSN:1559-0836. OCLC:5701513120. PMC:4261625. PMID:25416391. QID:Q26825963.
- Nicole M Camasso; Melanie S. Sanford (2015). "Design, synthesis, and carbon-heteroatom coupling reactions of organometallic nickel(IV) complexes". Science (بالإنجليزية). 347 (6227): 1218–1220. CiteSeerX:10.1.1.897.9273. DOI:10.1126/SCIENCE.AAA4526. ISSN:0036-8075. PMID:25766226. S2CID:206634533. QID:Q34466914.
- Hidetsugu Shiozawa; Antonio Briones-Leon; Oleg Domanov; et al. (2015). "Nickel clusters embedded in carbon nanotubes as high performance magnets". Scientific Reports (بالإنجليزية). 5: 15033. DOI:10.1038/SREP15033. ISSN:2045-2322. OCLC:5893999610. PMC:4602218. PMID:26459370. QID:Q34497762.
- Young Rang Uhm; Byoung Gun Choi,; Jong Bum Kim; Dong-Hyuk Jeong; Kwang Jae Son (2016). "Study of a Betavoltaic Battery Using Electroplated Nickel-63 on Nickel Foil as a Power Source". Nuclear Engineering and Technology (بالإنجليزية). 48 (3): 773–777. DOI:10.1016/J.NET.2016.01.010. ISSN:1738-5733. OCLC:6780148638. QID:Q121422972.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: علامات ترقيم زائدة (link) - M. H. Mosallanejad; A. Shafyei; S. Akhavan (2016). "Simultaneous co-deposition of SiC and CNT into the Ni coating". Canadian Metallurgical Quarterly (بالإنجليزية). 55 (2): 147–155. DOI:10.1080/00084433.2016.1150406. ISSN:0008-4433. OCLC:6685400428. QID:Q121365906.
- Lynne T. Haber; Hudson K Bates; Bruce C Allen; Melissa J Vincent; Adriana R Oller (2017). "Derivation of an oral toxicity reference value for nickel". Regulatory Toxicology and Pharmacology (بالإنجليزية). 87 Suppl 1: S1–S18. DOI:10.1016/J.YRTPH.2017.03.011. ISSN:0273-2300. OCLC:7061118472. PMID:28300623. QID:Q38903738.
- V.S. Bormashov; S.Yu. Troschiev; S.A. Tarelkin; et al. (2018). "High power density nuclear battery prototype based on diamond Schottky diodes". Diamond and Related Materials (بالإنجليزية). 84: 41–47. Bibcode:2018DRM....84...41B. DOI:10.1016/J.DIAMOND.2018.03.006. ISSN:0925-9635. OCLC:7998019027. QID:Q121412757.
- A Sharma; J Hickman; Gazit Nimrod; E Rabkin; Y Mishin (2018). "Nickel nanoparticles set a new record of strength". Nature Communications (بالإنجليزية). 9 (1): 4102. Bibcode:2018NatCo...9.4102S. DOI:10.1038/S41467-018-06575-6. ISSN:2041-1723. OCLC:7865052134. PMC:6173750. PMID:30291239. QID:Q57022688.
- Aderonke AV; Dede AH; Oluwatobi AI; Stephen NE (2019). "A Review on the Metal Complex of Nickel (Ii) Salicylhydroxamic Acid and its Aniline Adduct". Journal of Translational Science and Research (بالإنجليزية). 2 (1): 1–9. DOI:10.24966/TSR-6899/100006. OCLC:8874833804. S2CID:212626015. QID:Q121367967.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - Giuseppe Genchi; Alessia Carocci; Graziantonio Lauria; Maria Stefania Sinicropi; Alessia Catalano (2020). "Nickel: Human Health and Environmental Toxicology". International Journal of Environmental Research and Public Health (بالإنجليزية). 17 (3): 679. DOI:10.3390/IJERPH17030679. ISSN:1660-4601. OCLC:8516727830. PMC:7037090. PMID:31973020. QID:Q92881191.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link)
- التقارير
- الإنجليزية
- International Committee on Nickel Carcinogenesis in Man (1990). "Report of the International Committee on Nickel Carcinogenesis in Man". Scandinavian Journal of Work, Environment & Health (بالإنجليزية). 16 (1 Spec No): 1–82. DOI:10.5271/SJWEH.1813. ISSN:0355-3140. OCLC:21575268. PMID:2185539. QID:Q64410831.
- Carboneau, M L; Adams, J P (1995). "Nickel-63". National Low-Level Waste Management Program Radionuclide Report Series (بالإنجليزية). 10. DOI:10.2172/31669. OCLC:4433535421. OSTI:31669. QID:Q121433850.
- National Toxicology Program (1996). "NTP Toxicology and Carcinogenesis Studies of Nickel Oxide (CAS No. 1313-99-1) in F344 Rats and B6C3F1 Mice (Inhalation Studies)". National Toxicology Program technical report series (بالإنجليزية). 451: 1–381. ISSN:0888-8051. OCLC:6922400012. PMID:12594524. QID:Q53452786.
- Food and Nutrition Board (2001). DRI, dietary reference intakes for vitamin A, vitamin K, arsenic, boron, chromium, copper, iodine, iron, manganese, molybdenum, nickel, silicon, vanadium, and zinc: a report of the Panel on Micronutrients subcommittees on Upper Reference of Nutrients and of Interpretation and Uses of Dietary Reference Intakes, and the Standing Committee on the Scientific Evaluation of the Dietary Reference intakes (بالإنجليزية). Washington, D.C.: National Academies Press. ISBN:978-0-309-07279-3. OCLC:316869508. OL:18175272M. QID:Q121423528.
- International Agency for Research on Cancer (2012). Arsenic, metals, fibres, and dusts: A review of human carcinogens (PDF). IARC monographs on the evaluation of carcinogenic risks to humans. Supplement (بالإنجليزية). Lyon, Geneva: World Health Organization. Vol. 100 C. ISBN:978-92-832-1320-8. OCLC:779856914. OL:25977153M. QID:Q121461471.
- National Minerals Information Center (2013). Mineral commodity summaries 2013 (PDF). Mineral Commodity Summaries (بالإنجليزية). Reston: United States Geological Survey. DOI:10.3133/MINERAL2013. ISBN:978-1-4113-3548-6. OCLC:8160801247. OL:50672573M. QID:Q121387587.
- National Minerals Information Center (2019). Mineral Commodity Summaries 2019 (PDF). Mineral Commodity Summaries (بالإنجليزية). Reston: United States Geological Survey. DOI:10.3133/70202434. ISBN:978-1-4113-4283-5. OCLC:1204139162. OL:30682681M. QID:Q61974213.
- International Seabed Authority (2019), Strategic Plan 2019-2023 (PDF) (بالإنجليزية), QID:Q121408312
- National Minerals Information Center (2020). Mineral Commodity Summaries 2020 (PDF). Mineral Commodity Summaries (بالإنجليزية). Reston: United States Geological Survey. ISBN:978-1-4113-4362-7. OL:29889957M. QID:Q121410496.
- National Minerals Information Center (2021). Mineral Commodity Summaries 2021 (PDF). Mineral Commodity Summaries (بالإنجليزية). Reston: United States Geological Survey. DOI:10.3133/MCS2021. ISBN:978-1-4113-4398-6. OL:38892806M. QID:Q121368379.
| H | He | |||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||




![{\displaystyle {\ce {NiC2O4 ->[T][] Ni + 2 CO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4f5ac7119d30ce593cf99675097e91e39e33a04d)
![{\displaystyle {\ce {NiSO4 + 4NH4+ + 4OH- -> [Ni(NH3)4]SO4 + 4H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fed711e628c3ba92046eb178a459488074a035c9)
![{\displaystyle {\ce {Ni(CN)2 + 2KCN -> K2[Ni(CN)4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7a2b8181f20f5d9ad99c2900689b699739283d0d)
