ثلاثي أكسيد ثنائي الهيدروجين
| ثلاثي أكسيد ثنائي الهيدروجين | |
|---|---|
| الاسم النظامي (IUPAC) | |
Trioxidane |
|
| أسماء أخرى | |
ثلاثي أكسيد ثنائي الهيدروجين |
|
| المعرفات | |
| رقم CAS | 14699-99-1 |
| بوب كيم (PubChem) | 166717 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | H2O3 |
| الكتلة المولية | 50.01 غ/مول |
| المظهر | غير ثابت في الظروف القياسية |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
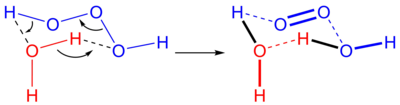
ثلاثي أكسيد ثنائي الهيدروجين (كما يعرف باسم تريوكسيدان) عبارة عن مركب كيميائي له الصيغة H2O3 والذي يمكن كتابته على الشكل HOOOH. هذا المركب غير ثابت ويتفكك في الظروف العادية من الضغط ودرجة الحرارة. يصنف هذا المركب على أنه أكسيد للهيدروجين.
الخصائص[عدل]
يتفكك مركب ثلاثي أكسيد ثنائي الهيدروجين H2O3 إلى الماء والأكسجين.
إن التفاعل العكسي أي إضافة الأكسجين للماء لا يؤدي إلى حدوث تفاعل.
يظهر مركب ثلاثي أكسيد ثنائي الهيدروجين خواص حمضية أقوى منها لفوق أكسيد الهيدروجين، حيث يتفكك إلى البروتون H+ وOOOH-.[3]
التحضير[عدل]
يتشكل ثلاثي أكسيد ثنائي الهيدروجين بكميات صغيرة من تفاعل الأوزون مع فوق أكسيد الهيدروجين. بشكل آخر يمكن تحضير هذا المركب من تفاعل الأوزون مع مركبات عضوية اختزالية عند درجات حرارة منخفضة بوجود مذيبات عضوية كما يحدث في عملية أنثراكينون. كما يمكن تحضير المركب من تفكك ثلاثي أكسيد المركبات العضوية.(ROOOH).[4]
في بعض الأوساط الحيوية، يمكن للأوزون أن يؤدي إلى تشكل ثلاثي أكسيد ثنائي الهيدروجين.[5]
البنية[عدل]
إن التحاليل الطيفية للمركب تظهر أن لثلاثي أكسيد ثنائي الهيدروجين بنية خطية منكسرة H-O-O-O-H، تكون فيها طول الرابطة O-O في مركب ثلاثي أكسيد ثنائي الهيدروجين (142.8 بيكومتر) أقصر منها في فوق اكسيد الهيدروجين (146.4 بيكومتر). يمكن أن يوجد أشكال ثنائية وثلاثية من المركب.
المراجع[عدل]
- ^ ا ب ج trioxidanexxx (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01xxx، 1 سبتمبر 2020، QID:Q98915402
- ^ Kohsuke Suma, Yoshihiro Sumiyoshi, and Yasuki Endo (2005). "The Rotational Spectrum and Structure of HOOOH". J. Am. Chem. Soc. ج. 127 ع. 43: 14998–14999. DOI:10.1021/ja0556530. PMID:16248618. مؤرشف من الأصل في 2013-05-23.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Božo Plesničar (2005). "Progress in the Chemistry of Dihydrogen Trioxide (HOOOH)" (PDF). Acta Chim. Slov. ج. 52: 1–12. اطلع عليه بتاريخ 2012-04-23.[وصلة مكسورة]
- ^ Paul T. Nyffeler, Nicholas A. Boyle, Laxman Eltepu, Chi-Huey Wong, Albert Eschenmoser, Richard A. Lerner, Paul Wentworth Jr. (2004). "Dihydrogen Trioxide (HOOOH) Is Generated during the Thermal Reaction between Hydrogen Peroxide and Ozone". Angewandte Chemie International Edition. ج. 43 ع. 35: 4656–4659. DOI:10.1002/anie.200460457. PMID:15317003.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)
| ثلاثي أكسيد ثنائي الهيدروجين في المشاريع الشقيقة: | |
| |