غليكوز أمينوغليكان
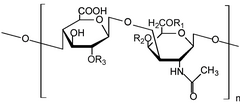

الغليكوز أمينوغليكانات (بالإنجليزية: Glycosaminoglycans)[1] أو عديدات السكاريد المخاطية (بالإنجليزية: mucopolysaccharides)[2] هو عديد سكاريد طويل غير متفرع يتكون من وحدات سكر ثنائي متكررة.
الوحدات المتكررة (باستثناء الكيراتان) تتكون من سكر أميني (مثل ن-أسيتيل غلوكوزامين أو ن-أسيتيل غالاكتوزامين) مع حمض يورونيك (مثل حمض الغلوكورونيك أو حمض الإيدورونيك) أو غلاكتوز.[3]
الغليكوز أميوغليكانات شديدة القطبية ومنجذبة للماء لذلك فهي مفيدة للجسم حيث أنها تمتص الصدمات ومادة مزلقة.
الإنتاج[عدل]
تتنوع مركبات الغليكوز أمينوغليكان (GAGs) بشكل كبير من حيث الكتلة الجزيئية، والسكر الثنائي في بنيتها، والكبريتات. السبب هو أن اصطناعها لا يتم بالقولبة مثل البروتينات أو الحموض النووية، بل يتغير باستمرار بواسطة الإنزيمات المعالجة.[4][5]
تُصنف مركبات الغليكوز أمينوغليكان ضمن أربع مجموعات بحسب بنية السكاكر الثنائية الأساسية. يُصطنع الهيبارين/ سلفات الهيباران (HSGAG) وسلفات الكوندرويتين/ سلفات الديرماتان (CSGAGs) في جهاز غولجي، إذ تتعدل النوى البروتينية المصنعة في الشبكة الإندوبلازمية الخشنة بعد الترجمة بالغلكزة المرتبطة بـ O بواسطة إنزيمات الغليكوزيل ترانسفيراز لتشكل البروتيوغليكانات. قد تعدل سلفات الكيراتان النوى البروتينية من خلال الغلكزة المرتبطة بـ N أو الغلكزة المرتبطة بـ O للبروتيوغليكان. الصنف الرابع من GAGs هو حمض الهيالورونيك، يُصطنع عبر إنزيم السينثاز الغشائي المدمج الذي ينتج على الفور سلسلة ثنائية سكاريد طويلة.
الوظيفة[عدل]
CSGAGs[عدل]
يتوضع الهيبارين الداخلي ويُخزن ضمن حبيبات إفرازية في الخلايا البدينة. يتبرتن الهيستامين الموجود ضمن الحبيبات (H2A2+) في درجة الحموضة داخل الحبيبات (5.2-6.0)، بالتالي يُعتقد أن الهيبارين، ذا الشحنة السالبة القوية، يحافظ على التوازن الإلكتروستاتيكي ويخزن الهستامين. سريريًا، يُعطى الهيبارين كمضاد للتخثر، ويعد أيضًا خط العلاج الأول للأمراض الانصمامية الخثارية. يؤدي سلفات الهيباران عددًا من الأنشطة والوظائف البيولوجية، بما في ذلك التصاق الخلايا، تنظيم نمو الخلايا وتكاثرها، عمليات النمو، ارتباط ليباز البروتين الشحمي على السطح الخلوي مع البروتينات الأخرى، تولّد الأوعية، الغزو الفيروسي والنقائل الورمية.[6][7]
تتفاعل CSGAGs مع البروتينات الرابطة للهيبارين، وبالتحديد تفاعلات سلفات الديرماتان مع عوامل نمو الأرومة الليفية FGF-2 وFGF-7 التي تلعب دورًا في تكاثر الخلايا والتئام الجروح. بينما تنشط التفاعلات مع عامل نمو الخلايا الكبدية/ عامل الانتثار (HGF/SF) مسار التأشير HGF/SF من خلال مستقبله. تعد CASGAGs مهمة في توفير الدعم والالتصاق في العظام والجلد والغضاريف. من المعروف أن CSGAGs تلعب دورًا في الوظائف البيولوجية الأخرى التي تشمل تثبيط نمو المحاوير العصبية وتجديدها في أثناء نمو الجهاز العصبي المركزي، ولها دور في نمو الدماغ، ونشاط تكوين الاستطالات العصبية، والعدوى بالعوامل الممرضة.[8][9][10]
سلفات الكيراتان[عدل]
إحدى الوظائف الرئيسية للفئة الثالثة من GAGs، سلفات الكيراتان، هي الحفاظ على إماهة الأنسجة. يوجد سلفات الكيراتان في العظام والغضاريف وقرنية العين. داخل القرنية الطبيعية، تكون سلفات الديرماتان مميهة بالكامل بينما سلفات الكيراتان مميهة بشكل جزئي فقط ما يشير إلى أن سلفات الكيراتان قد تتصرف كمحلول دارئ للإماهة. في الحالات المرضية مثل حثل البقعة والقرنية، تتغير مستويات GAGs مثل سلفات الكيراتان، يُعتقد أن فقدان الرطوبة داخل سدى القرنية هو سبب ضبابية القرنية، وهذا يدعم الفرضية القائمة منذ زمن طويل وهي أن شفافية القرنية تعتمد على مستويات مناسبة من سلفات الكيراتان. توجد سلفات الكيراتان في العديد من الأنسجة الأخرى إلى جانب القرنية، فمن المعروف أنها تنظم عملية التصاق البلاعم، وتشكل حواجز أمام نمو المحاوير العصبية، وتنظم عملية انغراس الأجنة في بطانة الرحم أثناء دورات الحيض، وتؤثر على حركية الخلايا البطانية في القرنية. باختصار، تلعب سلفات الكيراتان دور عامل مضاد للالتصاق، ما يوحي بوظائف مهمة جدًا في حركية الخلية وارتباطها والعمليات البيولوجية المحتملة الأخرى.[11][12]
سلفات الديرماتان[عدل]
يؤدي سلفات الديرماتان وظائفه في الجلد والأوتار والأوعية الدموية وصمامات القلب.[11]
حمض الهيالورونيك[عدل]
حمض الهيالورونيك هو أحد المكونات الرئيسية للأنسجة والسوائل الزليلية، وهو المادة الأساسية في الأنسجة الضامة الأخرى. يربط حمض الهيالورونيك الخلايا ببعضها البعض، ويزلق المفاصل، ويساعد في الحفاظ على شكل كرة العين. مرونة ولزوجة حمض الهيالورونيك تجعله مثاليًا لتزليق المفاصل والأسطح التي تتحرك فوق بعضها البعض، مثل الغضاريف. يكون محلول حمض الهيالورونيك تحت ضغط القص المنخفض ذا لزوجة أعلى بكثير منها تحت ضغط القص العالي. الهيالورونيداز، هو إنزيم تنتجه خلايا الدم البيضاء وخلايا الحيوانات المنوية وبعض البكتيريا، يحطم حمض الهيالورونيك، فيصبح المحلول أكثر سيولة.[13]
الأمثلة[عدل]
طالع أيضا[عدل]
المصادر[عدل]
- ^ "glycosaminoglycan" في معجم دورلاند الطبي
- ^ "mucopolysaccharide" في معجم دورلاند الطبي
- ^ Esko، Jeffrey D؛ Kimata، Koji؛ Lindahl، Ulf (2009). "Chapter 16: Proteoglycans and Sulfated Glycosaminoglycans". Essentials of Glycobiology. Cold Spring Harbor Laboratory Press. ISBN:0879695595.
- ^ Sasisekharan، Ram؛ Raman، Rahul؛ Prabhakar، Vikas (أغسطس 2006). "Glycomics Approach to Structure-Function Relationships of Glycosaminoglycans". Annual Review of Biomedical Engineering. ج. 8 ع. 1: 181–231. DOI:10.1146/annurev.bioeng.8.061505.095745. PMID:16834555.
- ^ Caligur, Vicki (2008). "Glycosaminoglycan Sulfation and Signaling". مؤرشف من الأصل في 2019-10-19. اطلع عليه بتاريخ 2012-11-25.
- ^ Rodén، L. (1989). Lane، DA (المحرر). Heparin: Chemical and Biological Properties, Clinical Applications. CRC Press, Inc. ص. 1.
- ^ Jin L، Abrahams JP، Skinner R، Petitou M، Pike RN، Carrell RW (1997). "The anticoagulant activation of antithrombin by heparin". Proceedings of the National Academy of Sciences of the United States of America. ج. 94 ع. 26: 14683–8. Bibcode:1997PNAS...9414683J. DOI:10.1073/pnas.94.26.14683. PMC:25092. PMID:9405673.
- ^ Sugahara K، Mikami T، Uyama T، Mizuguchi S، Nomura K، Kitagawa H (2003). "Recent advances in the structural biology of chondroitin sulfate and dermatan sulfate". Current Opinion in Structural Biology. ج. 13 ع. 5: 612–620. DOI:10.1016/j.sbi.2003.09.011. PMID:14568617.
- ^ Trowbridge JM، Gallo RL (2002). "Dermatan sulfate: new functions from an old glycosaminoglycan". Glycobiology. ج. 12 ع. 9: 117R–125R. DOI:10.1093/glycob/cwf066. PMID:12213784.
- ^ Rabenstein DL. (2002). "Heparin and heparan sulfate: structure and function". Natural Product Reports. ج. 19 ع. 3: 312–331. DOI:10.1039/B100916H. PMID:12137280.
- ^ أ ب Tortora, Gerard J. (31 ديسمبر 2013). Principles of anatomy & physiology. Derrickson, Bryan (ط. 14th). Danvers, MA. ISBN:978-1-118-34500-9. OCLC:871018672.
{{استشهاد بكتاب}}: صيانة الاستشهاد: مكان بدون ناشر (link) - ^ Funderburgh, JL. (2000). "Keratan sulfate: structure, biosynthesis, and function". Glycobiology. ج. 10 ع. 10: 951–8. DOI:10.1093/glycob/10.10.951. PMID:11030741.
- ^ Laurent TC، Laurent UB، Fraser JR (1996). "The structure and function of hyaluronan: An overview". Immunology and Cell Biology. ج. 74 ع. 2: A1-7. DOI:10.1038/icb.1996.32. PMID:8724014.
| في كومنز صور وملفات عن: غليكوز أمينوغليكان |
