نظام (تحريك حراري)

النظام في الثرموديناميك (والتي تعد من أقسام الفيزياء والكيمياء وعدد من فروع الهندسة) هو نظام محدود الحجم (غاز، أو سائل، أو مواد صلبة، أو خليط منها) نجري عليه مشاهداتنا ويتميز بحالة متوازنة للطاقة. ينطبق ذلك على نظام مغلق، أي لا يحدث تبادل للحرارة أو الإشعاع أو تبادل لمواد بين النظام والوسط المحيط به - هذا بخلاف «النظام المفتوح» فيكون في حالة تبادل مع الوسط المحيط ويجري بينهما تبادل للمواد أو الحرارة.
في حالة النظام المغلق نهتم بدراسة تغيرات الطاقة والحرارة والشغل التي تخرج من حدود النظام، وتغير بذلك الطاقة الداخلية وحالة النظام. وفي حالة النظام المعزول لا يوجد تبادل من أي نوع مع الوسط المحيط؛ أي أن الطاقة الكلية للنظام تبقى ثابتة لا تتغير.

أنظمة الترموديناميكا معهودة لنا في حياتنا اليومية، فعندما نركب سيارة يقوم محرك الاحتراق الداخلي بتحريكنا عن طريق حرق البنزين وتحويل الطاقة الحرارية إلى طاقة حركة (شغل). وإذا شئنا السفر بالقطار قامت الآلة البخارية أو محرك ديزل بتحريك القطار، وإذا استغنينا عن القطار وأردنا السفر بالطائرة قامت المحركات النفاثة بالارتفاع بنا والسفر في الجو، وغيرها وغيرها. كلها محركات نزودها بالوقود المناسب ونجني منها شغلا (حركة). هذا الفرع من الفيزياء والكيمياء يختص بتلك الدراسات بغرض رفع كفاءة الآلات التي تخدمنا بما فيها جميع أنواع محطات توليد الكهرباء، والمحركات والبطاريات والمراكم وغيرها، مما يعود علينا بحفض استهلاك الوقود وخفض مصروفاته.
النظام المفتوح[عدل]
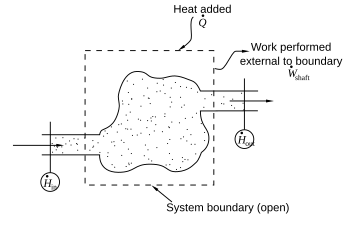
في النظام المفتوح يتبادل النظام مع الجو المحيط طاقة ومواد. ومثال على النظام المفتوح تتم فيه عملية دورية هو التوربين. فعند تشغيله يقوم سيل ثابت من مواد (ماء / أو بخار / أو غاز) بتحريكه. في تلك الحالة تبقى حالة السيل الداخل وحالة السيل الخارج ثابتتين ويتغير السيل فقط في داخل النظام. يدخل وسط التشغيل مضغوطا في التوربين ويخرج منه متمددا، ويدور التوربين ويشغل آلة أو يدير مولد كهربائي وينتج تيارا كهربائيا، ويسمى ذلك «شغل تقني»؛ ويمكن وصفه بالمعادلة:
هذا تعريف شامل للشغل W الذي يرمز له في الإنجليزية بـ Work ؛ وما يهمنا في المقام الأول هو الجزء الأول الذي نتعامل معه في مختبراتنا العلمية وفي حياتنا العملية. أما المعادلة الشمولية فهي تشمل أيضا نوعين آخرين من الطاقة وهي طاقة خارجية E وطاقة تفكك W diss ,(مثل تفكك ملح في سائل)، وكلاهما حالة خاصة.
إذن:
- ( التغير في الطاقات الخارجية، وطاقة التفكك W diss ، تلك حالات خاصة نستطيع اهمالها في مناقشتنا الحالية.)
ويهمنا «الشغل التقني» W بتعريفات مختلفة، فهو الجزء الذي نكتسبه من محرك احتراق داخلي أو محرك بخاري أو من محطة قوى كهربائية، ومقداره هو:
- الذي يشمل حاصل ضرب الحجم في تغير الضغط.
عندما يعمل محرك سيارة مثلا فإن انفجار غاز البنزين واحتراقه في أسطوانة المحرك يجعل غاز الاحتراق يتمدد فيدفع المكبس. ومع تناوب عمليات الاحتراق في أسطوانة المحرك يتحرك المكبس وذراعه إلى الخلف ثم إلى الأمام وهكذا، وعن طريق الذراع المفصلي تتحول تلك الحركة الخطية إلى حركة دائرية، فنقول أن المحرك يدور. ثم عن طريق صندوق التروس تنتقل حركة دوران المحور إلى العجلات وتسير السيارة.
في حالة تدوير توربين بخاري بواسطة ضغط بخار الماء، المبدأ هو نفس المبدأ؛ يدخل بخار الماء تحت ضغط شديد في قلب التوربين فتدور زعانف التوربين وتدير محور التوربين، ونستفيد من تلك الحركة الدورانية بأشكال عديدة وينتج شغلا. بجانب هذا الشغل ينشا عند مدخل التوربين ومخرجه شغل إزاحي. فإذا كانت كتلة بخار الماء عند المدخل بالحجم وعند المخرج بالحجم , يكون الشغل الإزاحي عند المدخل وعند المخرج
يشكل كلا الشغلين الإزاحيين جزءا من انثالبية H السيل الداخل والسيل الخارج بالإضافة إلى الطاقة الداخلية U:
تلك هي معادلة الإنثالبي (أو المحتوى الحراري) للنظام، والمحتوى الحراري H يمكن أن يتحول جزء منه إلى شغل p. dV (حركة) والباقي يبقى مخزونا في النظام، ويعرف بالحرارة الداخلية أو الطاقة الداخلية U .
وفي الصورة المبينة للنظام المفتوح open system وهي تمثل محرك الاحتراق الداخلي نجد أن النظام مرة يكون مفتوحا ومرة مغلقا على التوالي. ولكن يمكن اعتبار النظام نظام مفتوحا عبر مدة طويلة من الزمن، إذ أن المحرك يطرد الغاز العادم إلى الهواء، وهذا الغاز العادم يحمل معه جزءا من الحرارة، لا نستفيد منها. .
النظام المغلق[عدل]
في النظام المغلق لا تخرج منه مادة. ولكن يمكن فيه دخول أو خروج حرارة أو شغل. ومن أنواع الشغل يمكن أن تكون:
- شغل تغير الحجم عكوسي نؤديه على النظام، وهذا يسمى أحيانا شغل حجمي. من الامثلة الموجودة في الجدول نجد: ضغط الغاز في الأسطوانة بواسطة المكبس بدون احتكاك. وحيث أنه في المعادلة نجد التغير في الحجم سالب الإشارة يكون الشغل المؤدى على النظام موجب الإشارة.
- شغل مشتت. ومثال له المروحة في غرفة أو جهاز التدفئة الكهربائي في غرفة محدودة الحجم. يخرج من حدود النظام شغل يتشتت من الغرفة. كما أن الشغل الناشئ عن احتكاك المكبس بالأسطوانة ينتمي إلى تلك الطاقة الداخلة الغير عكوسية.
ونظرا لأن الطاقة لا تنشأ من نفسها ولا تنعدم طبقا ل القانون الأول للديناميكا الحرارية تتزايد الطاقة الداخلية في النظام بمقدار الطاقة الداخلة إليه من الخارج. ويمكن وصف توازن الطاقة للنظام المغلق المستقر بالمعادلة:
- حيث الرقم 1 يعني الحالة الأولى للنظام، والرقم 2 الحالة النهائية للنظام.
مع
والمؤشران 1 و 2 في المعادلة يؤشران إلى الحالة الابتدائية والحالة النهائية على التوالي، كما يعني المؤشر 1,2 المسلك من 1 إلى 2.
وكما ذكر أعلاه: تعني W diss طاقة التفكك (ويمكن إهمالها)، و W v وهو الشغل التقني الناتج من الألة حيث V تدل على الشعل الناتج من التغير في حجم النظام أو من التغير في ضغط النظام . وفي حالة تغير الطاقة الخارجية للنظام سواء كانت طاقة الوضع (بسبب صعود النظام أو هبوطه تحت تأثير جاذبية الأرض) و/أو طاقة الحركة (حيث يمكن للنظام أن يكون في حالة حركة، مثل تجربة نبنيها على متن قطار يسير)، يصبح توازن الطاقات للنظام المغلق (طبقا للقانون الأول للديناميكا الحرارية):
ملحوظة 1 : الجزء الثالث من المعادلة إلى اليمين الذي يحتوي على g (وهي عجلة الجاذبية) يعطي اختلاف طاقة الوضع للنظام بتغير الارتفاع عن سطح الأرض. في العادة لا نأخذ هذا الجزء في الاعتبار عند التعامل مع نظام مغلق.
ملحوظة 2 : الجزء الرابع من المعادلة إلى اليمين الذي يحتوي على تغير سرعة النظام من c1 إلى c2 يعطي تغير طاقة الحركة للنظام، وعادة لا نـأخذ تلك المؤثرات في الحسبان عند دراسة نظام مغلق، لأننا نجري تجاربنا عادة في مختبر ثابت لا يتحرك ومن النادر أن نقوم بتجربة في مختبر موجود في عربة قطار.
بناء على تلك الملحوظتين يمكننا اختصار معادلة توازن الطاقات لتكون:
وهي المعادلة المعهودة لنا والتي تقول أن التغير في الطاقة الداخلية U للنظام تساوي مجموع الحرارة Q والشغل W الناشئة منه أو المعطاة له.
النظام المعزول[عدل]
النظام المعزول هو نظام مغلق، لا يحدث فيه تبادل طاقة مع الخارج (المثال 4 في القائمة). ولا يستحق النظام المعزول المثالي الدراسة باستفاضة حيث أن جميع الأجزاء في معادلة توازن الطاقات تختفي وتصبح صفرا. .[1][2][3][4][5]
مثال دورة كارنو[عدل]
{مقالة رئيسية: دورة كارنو}
تبين مقالة دورة كارنو الرسم التوضيحي للأسطوانة والمكبس التي استخدمها كارنو لتوضيح آلته المثالية، ونرمز لدورة كارنو هنا بالرسوم والرموز المعتادة لنا:

في هذا الشكل يظهر «وسيط الشغل» الذي قد يكون بخارا أو سائلا يمكن تسخينه بحرارة QH فيُنتج شغلا ميكانيكيا W. في عام 1824 افترض سادي كارنو في رسالته «أفكار حول القوة الحركية للنار» أن يكون الوسط أي مادة قابلة للتمدد مثل بخار الماء أو بخار الكحول أو بخار الزئبق أو غاز أو الهواء وغيرها. ومع أنه في ذلك العصر ظهرت عدة آلات متغيرة التصميم، إلا أنها كانت جميعها تحتوي على غلاية، يتم فيها تسخين الماء QH حتى الغليان بواسطة فرن، وكان QC ماء بارد يسيل في مكثف موضوع على الآلة. وكان الشغل الناتج W عبارة عن حركة مكبس الذي يُدير محورا، فيمكن بذلك إدارة قرصا أو بكرة تعمل على رفع المياه من المناجم. وقام كارنو آنذاك بتعريف الشغل بأنه «رفع ثقل إلى ارتفاع معين».
انظر أيضا[عدل]
- دورة كارنو
- كفاءة تحويل الطاقة
- بقاء الطاقة
- ديناميكا حرارية
- القانون الثاني للترموديناميك
- ترموديناميكا كيميائية
- دورة رانكن
- كفاءة حرارية
- دورة حركة حرارية
- فضاء الطور
- توازن ترموديناميكي
- طاقة حرة ثرموديناميكية
- ترموديناميكا كيميائية
المراجع[عدل]
- ^ I.M.Kolesnikov؛ V.A.Vinokurov؛ S.I.Kolesnikov (2001). Thermodynamics of Spontaneous and Non-Spontaneous Processes. Nova science Publishers. ص. 136. ISBN:1-56072-904-X. مؤرشف من الأصل في 2014-06-27.
- ^ "A System and Its Surroundings". ChemWiki. University of California - Davis. مؤرشف من الأصل في 3 فبراير 2016. اطلع عليه بتاريخ May 2012.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ "Hyperphysics". The Department of Physics and Astronomy of Georgia State University. مؤرشف من الأصل في 15 يناير 2019. اطلع عليه بتاريخ May 2012.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Bryan Sanctuary. "Open, Closed and Isolated Systems in Physical Chemistry,". Foundations of Quantum Mechanics and Physical Chemistry. McGill University (Montreal). مؤرشف من الأصل في 3 مايو 2019. اطلع عليه بتاريخ May 2012.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Material and Energy Balances for Engineers and Environmentalists (PDF). Imperial College Press. ص. 7. مؤرشف من الأصل (PDF) في 15 أغسطس 2009. اطلع عليه بتاريخ May 2012.
{{استشهاد بكتاب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة)
| نظام في المشاريع الشقيقة: | |
















