داء الليشمانيات الجلدي
| داء الليشمانيات الجلدي | |
|---|---|
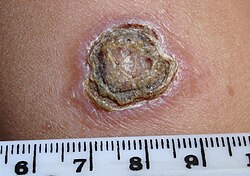 قرحة داء الليشمانيات الجلدي عند طفل من الشرق الأوسط.
| |
| معلومات عامة | |
| الاختصاص | أمراض معدية |
| من أنواع | مرض جلدي نادر ، ومرض جلدي، وداء الليشمانيات، ومرض |
| الأسباب | |
| الأسباب | ليشمانيا، وليشمانيا مدارية ، وليشمانية أثيوبية، وليشمانيا برازيلية |
| طريقة انتقال العامل المسبب للمرض | عبر البعوض |
| المظهر السريري | |
| الأعراض | حطاطة، وقرحة جلدية، وندبة |
| الإدارة | |
| أدوية | |
| تعديل مصدري - تعديل | |
داء الليشمانيات الجلدي (يُسَمَّى بِالعَامِّيَّةِ: المُسْتَكْوِيَةُ[1][2] أو البداة[1] أو الأبدة[2] أو الآكِلَةُ[1] أو المُحْتَفِرَةُ[2] أو الأخت[1][2]) (بالإنجليزية: cutaneous leishmaniasis) أشيع أشكال داء الليشمانيات، وهو مجموعة أمراض يسببها طفيلي وحيد الخلية من جنس الليشمانيا، حيث يمكن لنحو عشرين نوعاً من هذا الطفيلي أن تسبب المرض عند الإنسان، أغلبها، باستثناء المرض الناجم عن الليشمانيا المدارية، أمراض حيوانية المنشأ. ينتقل هذا المرض بواسطة لدغ حشرات من أسرة الفواصد تنتمي إلى جنس الفاصدة في العالم القديم وجنس اللوتزومية في العالم الجديد.
التسميات المحلية[عدل]
التسميات المحلية لداء الليشمانيات الجلدي عديدة حسب مناطق توطن المرض، منها قرحة الشرق وحبّة حلب[3] وحبة السنة[4] وحبة بسكرة[5] وقرحة بغداد، والأخت في شبه الجزيرة العربية[6] (في العالم القديم)، ومرض الأنديز[7] أو إسبونديا في العالم الجديد.
العلامات والأعراض[عدل]
داء الليشمانيا الجلدي التالي لمرض الكلازار (عقبولة الداء الأسود PKDL)[عدل]
ينجم داء الليشمانيا الجلدي التالي لمرض الكلازار [الإنجليزية] (PKDL) عن الإصابة بمرض الكلازار الذي قد يظهر على جلد الأفراد المصابين بعد فترة يمكن أن تصل إلى 20 عامًا من علاجهم جزئيًا أو عدم علاجهم أو حتى لدى هؤلاء الأفراد الذين يمكن القول إنه شفوا منهُ على النحو الكافي والملائم.[8][9] ففي السودان، يمكن أن يظهر هذا المرض في حوالي %60 من الحالات التي خضعت للعلاج. ويظهر هذا المرض في صورة بقع جلدية ناقصة التصبغ أو حطاطات أو عقيدات أو احمرار بالجلد في منطقة الوجه. وعلى الرغم من أي كائن حي يسبب الإصابة بمرض الكلازار يمكنه أن يسبب الإصابة بداء PKDL، فإنه من الشائع ارتباط الإصابة به بطفيل الليشمانيا الدونوفانية الذي يسبب أنماطًا مختلفة من المرض في كل من الهند والسودان. ففي النمط الذي يظهر به المرض في الهند، تكبر العقيدات بمرور الوقت وتشكل بقعًا أو لطعًا دهنيةً كبيرةً، لكنها نادرًا ما تتقرح، لكن بالنسبة للعقيدات التي تتكون في النمط الذي يظهر في أفريقيا، فإنها غالبًا ما تتقرح كلما تقدمت مراحل المرض بمرور الوقت. ويشيع امتداد تأثير هذا المرض ليشمل الأعصاب في أفريقيا، لكن هذا الأمر نادر الحدوث في شبة القارة الهندية.[10] وقد تبين من خلال دراسة هذا المرض في إطار علم الأنسجة أن هناك مجموعة متنوعة من الخلايا الالتهابية المزمنة؛ والتي يمكن أن تتمثل في خلايا بلعمية أو في أورام حبيبية ظهارية.[11] ولا يعتبر تركيز الطفيليات ثابتًا في كل الدراسات المتعلقة بهذا الشأن، الأمر الذي ربما يعكس انخفاض درجة حساسية أساليب التشخيص التي كانت مستخدمة من قبل.
يتضمن منهج التشخيص الحالي: 1- الكشف عن وجود الطفيليات من خلال الفحص الميكروسكوبي، سواء عن طريق فحص مستنبتات طفيلية أو التلقيح الحيواني في المعمل، 2- التشخيص المناعي لمستضدات الطفيليات، 3- الكشف عن الحمض النووي DNA للطفيل في النسيج الحيوي المصاب. وتتمتع وسائل التشخيص الأحدث المعتمدة على تقنية تفاعل البلمرة التسلسلي (PCR) بدرجة حساسية ودقة أعلى. وقد تم الإعلان عن ظهور حالات إصابة بداء PKDL لدى أفراد مصابين بفيروس نقص المناعة البشرية المعروف باسم HIV اختصارًا[12] وقد يمثل ذلك مشكلةً في المستقبل.
ويستخدم صوديوم الستيبوجلوكونات (SSG) بمفرده أو مع دواء الريفامبيسين لعلاج داء PKDL لفترة علاج طويلة قد تمتد إلى 4 أشهر. وربما يكون الخضوع للعلاج موضع جدل خاصةً وأن فترة العلاج طويلة.
داء الليشمانيا الجلدي المخاطي[عدل]
يعتبر داء الليشمانيا الجلدي المخاطي أكثر أنواع داء الليشمانيا الجلدي إثارةً للخوف نظرًا لأنه ينتج آفات مدمرة ومشوهة في الوجه. وفي الأغلب يكون السبب فيها هو طفيل الليشمانيا البرازيلية، لكن هناك حالات نادرة تم رصدها والتي يرجع السبب في حدوثها إلى طفيل الليشمانيا الأثيوبية.
ويعالج داء الليشمانيا الجلدي المخاطي على فترات طويلة (تصل إلى 30 يومًا) من العلاج بجرعات كبيرة (20 ملليجرام/كيلوجرام) من الأنتيمونيات خماسية التكافؤ. وقد لا ينجح العلاج في نحو %42 من حالات الإصابة.[13] وحتى في حالات المرضى الذين يبدو ظاهريًا أنهم قد شفوا من المرض، قد تعاود حوالي %19 منهم الإصابة بالمرض مرةً أخرى.[14] وجرب العديد من أشكال المزج بين الأدوية التي تحتوي على عوامل منظمة للمناعة، مثل إعطاء مزيج من دواء البنتوكسيفللين (مثبط العامل المنخر للورم ألفا) ومركب الأنتيموني خماسي التكافؤ بجرعات كبيرة لمدة 30 يومًا على عدد محدود من المرضى (23 مريضًا) من البرازيل خضعوا لدراسات عشوائية مضبوطة باستخدام الدواء الوهمي حول تأثير هذا المزيج الدوائي، وقد شفيت نسبة 90% منهم، كما تراجعت الفترة اللازمة للعلاج، وهي النتيجة التي ينبغي تفسيرها ودراستها بحرص في ضوء الحدود الأساسية للدراسات محدودة النطاق.[15] وكانت إحدى الدراسات محدودة النطاق السابقة (التي أجريت على 12 مريضًا)، مع إضافة كريم الإيموكويمود للمزيج السابق، قد أظهرت نتائج مبشرة[16] والتي لا يزال من الضروري التحقق منها من خلال تجارب ذات نطاق أوسع.
الفيسيولوجيا المرضية[عدل]

ينتقل البروماستيجوت، الطور المعدي من طفيل الليشمانيا، إلى جلد الإنسان عن طريق لدغة ذبابة الرمل. بعدها، يهاجم طفيل الليشمانيا الخلايا البلعمية في الإنسان ويتكاثر داخلها.
تظهر آفة حمراء بارزة في مكان لدغة الذبابة (غالبًا في غضون أسابيع أو ربما بعد سنوات من اللدغة). بعد ذلك، تتقرح الآفة وقد تصيبها عدوى بكتيرية ثانوية. في أنواع عديدة من طفيل الليشمانيا، (على سبيل المثال، طفيل الليشمانيا الكبيرة) عادةً ما تشفى الآفة بشكل تلقائي، ولكنها تترك ندوبًا ضامرةً مكانها. وفي بعض الأنواع الأخرى (مثل طفيل الليشمانيا البرازيلية) ربما تشفى الآفة تلقائيًا مع ترك آثار ندبة مكانها، لكنها تعاود الظهور مجددًا في مكان آخر من الجسم (خاصةً الآفات الناتجة عن الإصابة بداء الليشمانيا المخاطي المدمر). وقد تشفى آفات الأنواع الأخرى من الليشمانيا تلقائيًا، ثم تعاود الظهور مرةً أخرى في صورة آفات ملحقة حول مكان الآفة الأصلية، أو على امتداد مسار التصريف الليمفاوي.
تسبب بعض أنواع طفيل الليشمانيا داء الليشمانيا الجلدي (مثل طفيل الليشمانيا الكبيرة وطفيل الليشمانيا المدارية)، بينما تسبب بعض الأنواع الأخرى داء الليشمانيا الحشوي (مثل طفيل الليشمانيا الطفلية وطفيل الليشمانيا الدونوفانية)، على الرغم من أن البحث الناشئ (بسبب ارتفاع معدلات انتشار الإصابة التي تمتد من دول الغرب المتقدمة وحتى الشعوب القبلية) يظهر عدم وجود حدود واضحة وفاصلة بين هذه الأنواع.[17]
التشخيص[عدل]

يعتمد التشخيص على المظهر المميز للآفات البارزة التي تغطيها قشرة ولم تُعالج والتي يمكن أن تتقرح وتصيبها عدوى ثانوية من كائنات حية مثل بكتيريا المكورات العنقودية الذهبية، لدى شخص قد عاد من منطقة يستوطن بها المرض. ويتمثل المعيار الأمثل للتشخيص في تقنية تفاعل البلمرة التسلسلي المعروفة باسم PCR اختصارًا.[18]
العلاج[عدل]
لا توجد أدلة مؤكدة على أن هناك علاجًا مثاليًا لداء الليشمانيات الجلدي. فطرق العلاج المناسبة لأحد أشكال داء الليشمانيات قد تكون غير مناسبة لأنواع أخرى منه. وعلى نحو مثالي، ينبغي بذل كل جهد ممكن من أجل تحديد أنواع طفيل الليشمانيا من خلال التقنيات الجزيئية (تقنية PCR) قبل البدء في علاج أي منها. وفي إطار أية دولة نامية، عادةً ما يكون هناك نوع واحد فقط من الطفيل منتشرًا في كل إقليم أو مدينة بها، لذلك ليس من الضروري غالبًا تصنيف كل عدوى طفيلية.
- طفيل الليشمانيا الكبيرة
- تعتبر حالات العدوى بالليشمانيا الكبيرة عادةً من الحالات التي تشفى تلقائيًا ولا تتطلب علاجًا، لكن هناك تقارير عديدة عن وجود حالات إصابة خطيرة سببها طفيل الليشمانيا الكبيرة في أفغانستان.
وفي المملكة العربية السعودية، ثبتت فاعلية الفلوكونازول في تسريع الشفاء من خلال تناول 200 مغ منه يوميًا عن طريق الفم لمدة ستة أسابيع[19]
- الليشمانيا البرازيلية
- يعتبر العلاج باستخدام مركبات الأنتموان خماسي التكافؤ أو الأمفوتريسين ضروريًا في حالة الإصابة بعدوى بالليشمانيا البرازيلية بسبب احتمال أن يتسبب في تكون آفات مخاطية جلدية مشوهة للوجه.
- الليشمانيا الطفلية
- تسبب الليشمانيا الطفلية الإصابة بداء الليشمانيات الجلدي في جنوب فرنسا.[20]
هناك طرق علاج جديدة بدواء الميلتيفوسين الذي يتم تناوله عن طريق الفم (إمبافيدو) والذي قد أوضحت تجارب سريرية عديدة فاعليته وأمنه في علاج كلٍ من داء الليشمانيات الحشوي وداء الليشمانيات الجلدي. وتظهر دراسات أجريت مؤخرًا في بوليفيا ارتفاع معدل الشفاء من داء الليشمانيات الجلدي المخاطي في حالة استخدام دواء الميلتيفوسين. بالإضافة إلى ذلك، أظهرت دراسات مقارنة ضد الأنتيمونيات خماسية التكافؤ في إيران وباكستان تحقق معدل شفاء عالٍ من كل من طفيلي الليشمانيا الكبيرة والليشمانيا المدارية في حالة استخدام الدواء نفسه. وقد تم تسجيل هذا الدواء في العديد من دول أمريكا اللاتينية (مثل كولومبيا)، وكذلك في ألمانيا، موطن شركة «زينتاريس جي إم بي إتش» المصنعة للدواء. وفي أكتوبر 2006، تم منح الدواء وضع الدواء اليتيم (orphan drug)، أو الدواء المستخدم لعلاج الأمراض أو الحالات المرضية النادرة، من قبل إدارة الأغذية والأدوية الأمريكية. وبوجه عام، فإن هذا الدواء يتميز بآثار جانبية طفيفة مقارنة ببقية الأدوية الأخرى. وتتمثل الآثار الجانبية الأساسية له في حدوث اضطرابات هضمية خلال اليومين الأولين من العلاج، الأمر الذي لا يؤثر مطلقًا على فاعلية الدواء.
ومن الشائع حدوث إصابة بعدوى بكتيرية ثانوية (خاصة العدوى بالعنقودية الذهبية) وقد يتطلب علاجها استخدام المضادات الحيوية. وللأسف، قد يخطئ الأطباء غير المعتادين على مواجهة حالات الإصابة بداء الليشمانيات الجلدي في تشخيص الآفة، بحيث يعتبرونها عدوى بكتيرية عادية (خاصةً بعد عزل بكتيريا العنقودية الذهبية من عينات الجلد التي يتم أخذها لإجراء فحص بكتيري) ويغيب عن أذهانهم احتمال أن تكون إصابة بداء الليشمانيات.
الانتشار الوبائي للمرض[عدل]
يعتبر داء الليشمانيا الجلدي من الأمراض المستوطنة في أجزاء عديدة من العالم. لحوالي 20 نوعًا من أنواع طفيل الليشمانيا المختلفة القدرة على إصابة الإنسان بالعدوى. ويرتبط انتشار داء الليشمانيا الجلدي ارتباطًا وثيقًا بالتوزيع الجغرافي؛ حيث يمكن أن تنتشر الإصابة بداء الليشمانيا الجلدي بين المناطق الجغرافية المختلفة بمعدلات مختلفة لتمتد لقرى تبعد حتى بمقدار 15 ميلاً عن مركز الإصابة.
بالإضافة إلى ذلك، ترتبط بعض أنواع طفيل الليشمانيا بوجود الإنسان، ولذلك فهي تنتشر في المدن (مثل طفيل الليشمانيا المدارية)، بينما ترتبط بعض الأنواع الأخرى عادة بدرجة أكبر بأنواع من الحيوانات، ومن ثم تعتبر من الطفيليات حيوانية المصدر (مثل طفيل الليشمانيا الكبيرة). وهناك بعض أنواع الطفيليات التي يمكن أن تعتبر عادةً من الطفيليات حيوانية المصدر (مثل طفيل الليشمانيا البنامية)، والتي ربما تتحول إلى أمراض تصيب الإنسان بشكل رئيسي.[21]
ولقد كانت هناك حالات إصابة بداء الليشمانيا الجلدي منتشرة بين الجنود العائدين من أفغانستان.[22]
المراجع[عدل]
- ^ أ ب ت ث أسماء الأمراض ومواضع الكي الأكثر شهرة في الطب الشعبي في منطقة الخليج. (تاريخ الاطلاع: 2 يونيو 2019) نسخة محفوظة 02 أكتوبر 2018 على موقع واي باك مشين.
- ^ أ ب ت ث مرض «اللشمانيا» يسجل أعلى معدلات الإصابة بـ 534 حالة في القصيم نسخة محفوظة 2 أكتوبر 2018 على موقع واي باك مشين.. موقع جريدة الشرق السعودية، العدد 187 بتاريخ 8 يونيو 2012. (تاريخ الاطلاع: 2 يونيو 2019) "نسخة مؤرشفة". مؤرشف من الأصل في 2018-10-02. اطلع عليه بتاريخ 2019-06-02.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ T. Canaan (1929). "The oriental boil: An epidemiological study in Palestine". Transactions of the Royal Society of Tropical Medicine and Hygiene. ج. 23 ع. 1: 89–94. DOI:10.1016/S0035-9203(29)90903-2.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|quotes=تم تجاهله (مساعدة) - ^ Russell A. (1756). The natural history of Aleppo, and parts adjacent. London: Printed for A. Millar. ص. M1 page 262.
- ^ Hoare C.A. (1938). "Early discoveries regarding the parasite of oriental sore". Transactions of the Royal Society of Tropical Medicine and Hygiene. ج. 32 ع. 1: 67–92. DOI:10.1016/S0035-9203(38)90097-5.
- ^ Peters W. (1988). "«The little sister» -- a tale of Arabia". Transactions of the Royal Society of Tropical Medicine and Hygiene. ج. 82 ع. 2: 179–84. DOI:10.1016/0035-9203(88)90400-2. مؤرشف من الأصل في 2020-01-26.
- ^ World Health Organization/TDR (2009). Leishmaniasis: background information. Retrieved 2009-05-02. نسخة محفوظة 14 مارس 2018 على موقع واي باك مشين.
- ^ Banerjee N (1973). "Role of I.M.A. during natural calamities and national emergencies". Journal of the Indian Medical Association. ج. 61 ع. 11: 477–81. PMID:4600129.
- ^ Rathi SK, Pandhi RK, Chopra P, Khanna N (2005). "Post-kala-azar dermal leishmaniasis: a histopathological study". Indian journal of dermatology, venereology and leprology. ج. 71 ع. 4: 250–3. DOI:10.4103/0378-6323.16616. PMID:16394433.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Salotra P, Singh R (2006). "Challenges in the diagnosis of post kala-azar dermal leishmaniasis". Indian J. Med. Res. ج. 123 ع. 3: 295–310. PMID:16778312.
- ^ Singh N, Ramesh V, Arora VK, Bhatia A, Kubba A, Ramam M (1998). "Nodular post-kala-azar dermal leishmaniasis: a distinct histopathological entity". J. Cutan. Pathol. ج. 25 ع. 2: 95–9. DOI:10.1111/j.1600-0560.1998.tb01696.x. PMID:9521498.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Stark D, Pett S, Marriott D, Harkness J (2006). "Post-kala-azar dermal leishmaniasis due to Leishmania infantum in a human immunodeficiency virus type 1-infected patient". J. Clin. Microbiol. ج. 44 ع. 3: 1178–80. DOI:10.1128/JCM.44.3.1178-1180.2006. PMC:1393159. PMID:16517925.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Franke ED, Wignall FS, Cruz ME؛ وآخرون (1990). "Efficacy and toxicity of sodium stibogluconate for mucosal leishmaniasis". Ann Intern Med. ج. 113 ع. 12: 934–40. PMID:2173461.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Netto EM, Marsden PD, Llanos-Cuentas EA؛ وآخرون (1990). "Long-term follow-up of patients with Leishmania (Viannia) braziliensis infection and treated with glucantime". Trans R Soc Trop Med Hyg. ج. 84 ع. 3: 367–70. DOI:10.1016/0035-9203(90)90321-5. PMID:2260171.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Ojha R.P.؛ Cervantes، D؛ Fischbach، LA؛ وآخرون (2007). "Oral pentoxifylline and pentavalent antimony for treatment of leishmaniasis: promising but inconclusive evidence of superiority, compared with antimony monotherapy". Clin. Infect. Dis. ج. 45 ع. 8: 1104. DOI:10.1086/521938. PMID:17879933.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة) - ^ Arevalo I.؛ وآخرون (2001). "Successful treatment of drug-resistant cutaneous leishmaniasis in humans by use of imiquimod, an immunomodulator". Clin. Infect. Dis. ج. 33 ع. 11: 1847–51. DOI:10.1086/324161. PMID:11692295.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة) - ^ "Cutaneous leishmaniasis". Wikipedia (بالإنجليزية). 16 Feb 2022. Archived from the original on 2022-03-15.
- ^ Reithinger R & Dujardin J-C (2007). "Molecular diagnosis of leishmaniasis: current status and future applications". J Clin Microbiol. ج. 45 ع. 1: 21–25. DOI:10.1128/JCM.02029-06. PMC:1828971. PMID:17093038.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Alrajhi AA, Ibrahim EA, De Vol EB؛ وآخرون (2002). "Fluconazole for the treatment of cutaneous leishmaniasis caused by Leishmania major". N Engl J Med. ج. 346 ع. 12: 891–95. DOI:10.1056/NEJMoa011882. PMID:11907288. مؤرشف من الأصل في 2009-06-06.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Pratlong F.؛ وآخرون (2004). "Isoenzymatic analysis of 712 strains of Leishmania infantum in the south of France and relationship of enzymatic polymorphism to clinical and epidemiological features". Journal of Clinical Microbiology. ج. 42 ع. 9: 4077–82. DOI:10.1128/jcm.42.9.4077-4082.2004. PMC:516332. PMID:15364993.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة) - ^ Vergel C, Palacios R, Cadena H؛ وآخرون (2006). "Evidence for Leishmania (Viannia) parasites in the skin and blood of patients before and after treatment". J Infect Dis. ج. 194 ع. 4: 503–511. DOI:10.1086/505583. PMID:16845635.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Canadian soldiers bring back Old World disease". مؤرشف من الأصل في 2018-09-28.[وصلة مكسورة]
| في كومنز صور وملفات عن: داء الليشمانيات الجلدي |
