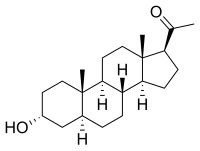
ألوبريجنانولون
| ألوبريجنانولون | |
|---|---|
| الاسم النظامي (IUPAC) | |
1-(3-hydroxy-10,13-dimethyl- |
|
| أسماء أخرى | |
3α,5α-Tetrahydroprogesterone |
|
| المعرفات | |
| رقم CAS | 516-54-1 |
| بوب كيم (PubChem) | 262961 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| الصيغة الجزيئية | C21H34O2 |
| الكتلة المولية | 318.49 g/mol |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
ألوبريجنانولون يعرف أيضاً باسم 3α-هيدروكسي-5α-بريجنان-20-واحد أو 3α,5α-تيتراهيدروبروجستيرون (3α,5α-THP) هو بريجنان مثبط ذاتي للستيروئيدات العصبية،[1] يتم تصنيع ألوبريجنانولون من البروجستيرون وهو وسيط إيجابي تبادلي قوي لعمل حمض غاما أمينوبيوتريك (غابا) على مستقبلات غابا،[1] ويمتلك ألوبريجنانولون تأثيرات ممائلة لتلك التي تسببها الوسائط الإيجابية التبادلية الأخرى مثل البنزوديازيبينات ومن هذه التأثيرات أنه مضاد للقلق، ومهدئ، وله نشاط مضاد للتشنجات.[1]
يمارس ألوبريجنانولون الذي يتم إفرازه ذاتياً داخل الجسم دوراً عصبياً محورياً عن طريق صقل مستقبلات غابا وتحوير عمل بعض البدائل الإيجابية ومحفزات مستقبلات غابا،[2] ويعد المشتق من هذه المادة 21-تيتراهيدروديأوكسي كورتيكوستيرون مثبطاً ذاتياً لعمل الإستيروئيدات وله خصائص متشابهة جداً مع خصائص ألوبريجنانولون ،وتم وضع النظير 3β-ميثيل لألوبريجنانولون و جاناكزولون تحت التطوير لعلاج الصرع وبعض الحالات الأخرى مثل إضطراب ما بعد الصدمة.[1]
التصنيع[عدل]
يبدأ تصنيع ألوبريجنانولون في المخ بتحويل هرمون البروجستيرون إلى 5α-دايهيدروبروجستيرون بواسطة الإنزيم 5α-ريدكتيز من النوع 1، ثم بعد ذلك يقوم 3α-هيدروكسي ستيرويد ديهيدروجينيز بتحويل ذلك المركب الوسطي إلى ألوبريجنانولون،[1] يتم تصنيع ألوبريجنانولون في المخ بواسطة الخلايا العصبية الهرمية والقشرية والخلايا شبه الهرمية في قاع وجوانب اللوزة.[3]
هناك إرتباط وثيق بين القلق، والإكتئاب،[4] وإضطراب ما بعد الصدمة مع إنخفاض مستوى ألوبريجنانولون في السائل النخاعي (المخي شوكي)، وبالمثل فإنه غالباً ما يتم النظر إلى الإضطرابات المزاجية والعجز الجنسي على أنها آثار جانبية لمثبطات إنزيم 5α-ريدكتيز مثل فيناسترايد، ويُعتقد أنها نتيجة جزئية للتدخل في إنتاج ألوبريجنانولون.[5][6]
آلية العمل[عدل]
يعمل ألوبريجنانولون كوسيط إيجابي تبادلي قوي للغاية على مستقبلات غابا،.[1] كما يعمل ألوبريجنانولون مثل جميع مثبطات الستيرويدات العصبية الأخرى مثل تيتراهيدروديأوكسي كورتيكوستيرون على تحوير جميع مستقبلات الغابا إيجابياً والتي تحتوي على الوحدات الفرعية δ، وتُظهر تلك المستقبلات التي تحتوي وحدات δ أعظم تقوية للخلايا العصبية.[1] ووجدوا كذلك أن ألوبريجنانولون يعمل كوسيط إيجابي تبادلي على مستقبلات غابا-ρ على الرغم من الآثار المترتبة على هذا العمل مازالت غير واضحة،[7][8] وبالإضافة إلى العمل على مستقبلات غابا فإنه يعمل مثل البروجستيرون كوسيط بدائلي سلبي على مستقبلات أستيل كولين النيكوتينية،[9] ويبدو أنه يعمل أيضاً كوسيط بدائلي سلبي للمستقبلات (5-HT3)،[10] وجنباً إلى جنب مع مثبطات الستيرويدات العصبية الأخرى يبدو أن تأثير ألوبريجنانولون ضعيف جداً يكاد يكون معدوم على البوابات الأيونية الأخرى مثل مستقبلات ن-ميثيل-د-أسبارتات (NMDA)، ومستقبلات(α-أمينو-3-هيدروكسي-5-ميثيل-4-أيزوكزول بروبيونيك أسيد)، ومستقبلات الكينين، ومستقبلات الجلايسين.[11]
وخلافاً لهرمون البروجستيرون فإن ألوبريجنانولون غير نشط على مستقبلات البروجستيرون النووية[11] ومع ذلك فيمكن أن تتم أكسدته داخل الخلية إلى 5α-دايهيدروبروجستيرون والذي يحفز مستقبلات البروجستيرون الخلوية ووفقاً لذلك يبدو أن ألوبريجنانولون له تأثير غير مباشر على مستقبلات البروجستيرون النووية يشبه تأثير البروجستيرون.[12] ويالإضافة إلى هذا وجدوا مؤخراً أن ألوبريجنانولون له تأثير تحفيزي على مستقبلات البروجستيرون في الأغشية ويتضمن ذلك مستقبلات δ ومستقبلات α ومستقبلات β، ووجدوا أيضاً ان نشاط ألوبريحنانولون على هذه المستقبلات أقوى من نشاطه على مستقبلات غابا،[13][14] ربما يرتبط عمل ألوبريجنانولون على هذه المستقبلات جزئياً مع خصائصه المضادة للغدد التناسلية والحامية للأعصاب،[13][15] ويتشابه ألوبريجنانولون مع البروجستيرون أيضاً في أنه يعمل كمنشط لمستقبلات بريغنان x.[11][16]
على غرار العديد من الوسائط الإيجابية التبادلية الأخرى التي تعمل على مستقبلات غابا وجدوا أن ألوبريجنانولون يعمل كمثبط لقنوات الكالسيوم الكهربية من النوع L [17] ويتضمن ذلك الوحدات الفرعية α1،[18] ومع ذلك فقد تم تحديد أقل تركيز لألوبريجنانولون في الدم لكي يكون قادراً على تثبيط قنوات الكالسيوم بحوالي 3 ميكرومتر (3000 نانومتر) وهذا التركيز أكبر بكثير من التركيز الذي يفرزه المخ البشري الطبيعي والذي يقدر بحوالي 5 نانومتر،[18] ولذلك فإنه من غير المحتمل أن يتم تثبيط قنوات الكالسيوم بواسطة ألوبريجنانون الذي يتم تصنيعه داخل الجسم فقط.[18][19]
الوظائف[عدل]
يمتلك ألوبريجنانولون مجموعة واسعة من التأثيرات مثل أنه مضاد للإكتئاب، ومضاد للقلق، ويقلل الإجهاد، ويعطي شعور بالسعادة،[20] وتحسين التصرف الإجتماعي،[21] ومضاد للعدوانية،[22] ومهدئ، ومنوم،[23] ومحفز للنشاط الجنسي،,[21] ومسكن للألم،[24] ومضاد للتشنجات، وله آثار عصبية، كما يؤدي إلى حدوث إضطرابات الذاكرة والإدراك.[1]
ويبدو أن التغيرات في مستويات ألوبريجنالون في الدم تلعب دوراً هاماً في فيزيولوجيا المزاج، والقلق، ومتلازمة ما قبل الحيض، وصرع الحيض، وبعض الحالات العصبية الأخرى.[25][26][27]
يمكن أن تؤدي زيادة مستويات ألوبريجنانولون إلى تأثيرات عكسية بما في ذلك سوء الحالة المزاجية، والقلق، والتهيج، والعدوانية.[28][29][30] ويبدو أن هذه التأثيرات تحدث بسبب أن التركيزات المنخفضة أو المعتدلة (بمعدل 1.5-2 نانومتر ألوبريجنانولون) تثبط نشاك مستقبلات غابا بينما يؤدي الزيادة أو النقصان في ذلك التركيز إلى إثارتها،[28][29] ويبدو أن هذا تأثير مشترك بين جميع الوسائط التبادلية على مستقبلات غابا،[25][30] ووفقاً لهذا فإن التناول الحاد لجرعات منخفضة من البروجستيرون (الذي بدوره يرفع مستويات ألوبريجنانولون) له آثار سلبية على الحالة المزاجية بينما المستويات المعتدلة لها تأثير محايد.[31]
التطبيقات العلاجية[عدل]
يتميز ألوبريجنانولون وغيره من الستيرويدات العصبية بفترة نصف عمر صغيرة جداً ولهذا لم يسعى العلماء في إستخدامه لأغراض علاجية، وبدلاً من ذلك قاموا بتصنيع النظائر مع تحسين الملامح العلاجية مثل جاناكزولون الذي تم تصنيعه وفحصه بدقة. ومع ذلك فإن تناول البروحستيرون الخارجي مثل الجرعات القليلة منه عن طريق الفم يزيد من مستويات ألوبريجنانولون في الجسم،[32] ولذلك فمن المقترح وصف جرعات صغيرة من البروحستيرون عن طريق الفم كعلاج مساعد لألوبريجنانولون.[32] ونتيجة لذلك فهناك بعض الإهتمام باستخدام البروجستيرون لعلاج الصرع الحيضي،[33] فضلاً عن غيرها من الحالات المصاحبة للدورة الشهرية والمرتبطة بالستيرويدات العصبية.
انظر أيضا[عدل]
وصلات خارجية[عدل]
- Herd، MB؛ Belelli، D؛ Lambert، JJ (2007). Neurosteroid modulation of synaptic and extrasynaptic GABA(A) receptors. Pharmacol. Ther. 116(1):20-34. DOI:10.1016/j.pharmthera.2007.03.007.
= مراجع[عدل]
- ^ أ ب ت ث ج ح خ د Reddy DS (2010). "Neurosteroids: endogenous role in the human brain and therapeutic potentials". Prog. Brain Res. ج. 186: 113–37. DOI:10.1016/B978-0-444-53630-3.00008-7. PMC:3139029. PMID:21094889.
- ^ Pinna، G؛ Uzunova، V؛ Matsumoto، K؛ Puia، G؛ Mienville، J. -M؛ Costa، E؛ Guidotti، A (1 مارس 2000). "Brain allopregnanolone regulates the potency of the GABAA receptor agonist muscimol". Neuropharmacology. ج. 39 ع. 3: 440–448. DOI:10.1016/S0028-3908(99)00149-5. مؤرشف من الأصل في 2019-07-27.
- ^ Agís-Balboa, Roberto C.; Pinna, Graziano; Zhubi, Adrian; Maloku, Ekrem; Veldic, Marin; Costa, Erminio; Guidotti, Alessandro (26 Sep 2006). "Characterization of brain neurons that express enzymes mediating neurosteroid biosynthesis". Proceedings of the National Academy of Sciences (بالإنجليزية). 103 (39): 14602–14607. DOI:10.1073/pnas.0606544103. ISSN:0027-8424. PMC:1600006. PMID:16984997. Archived from the original on 2019-12-15. Retrieved 2020-05-26.
- ^ Uzunova, V.; Sheline, Y.; Davis, J. M.; Rasmusson, A.; Uzunov, D. P.; Costa, E.; Guidotti, A. (17 Mar 1998). "Increase in the cerebrospinal fluid content of neurosteroids in patients with unipolar major depression who are receiving fluoxetine or fluvoxamine". Proceedings of the National Academy of Sciences (بالإنجليزية). 95 (6): 3239–3244. DOI:10.1073/pnas.95.6.3239. ISSN:0027-8424. PMC:19726. PMID:9501247. Archived from the original on 2020-05-26. Retrieved 2020-05-26.
- ^ "Decreased Cerebrospinal Fluid Allopregnanolone Levels in Women with Posttraumatic Stress Disorder - Biological Psychiatry". www.biologicalpsychiatryjournal.com. مؤرشف من الأصل في 2020-03-03. اطلع عليه بتاريخ 2016-01-26.
- ^ Römer B، Gass P (ديسمبر 2010). "Finasteride-induced depression: new insights into possible pathomechanisms". J Cosmet Dermatol. ج. 9 ع. 4: 331–2. DOI:10.1111/j.1473-2165.2010.00533.x. PMID:21122055.
- ^ Morris KD، Moorefield CN، Amin J (أكتوبر 1999). "Differential modulation of the gamma-aminobutyric acid type C receptor by neuroactive steroids". Mol. Pharmacol. ج. 56 ع. 4: 752–9. PMID:10496958.
- ^ Li W، Jin X، Covey DF، Steinbach JH (أكتوبر 2007). "Neuroactive steroids and human recombinant rho1 GABAC receptors". J. Pharmacol. Exp. Ther. ج. 323 ع. 1: 236–47. DOI:10.1124/jpet.107.127365. PMID:17636008.
- ^ Bullock AE، Clark AL، Grady SR، وآخرون (يونيو 1997). "Neurosteroids modulate nicotinic receptor function in mouse striatal and thalamic synaptosomes". J. Neurochem. ج. 68 ع. 6: 2412–23. DOI:10.1046/j.1471-4159.1997.68062412.x. PMID:9166735.
- ^ Wetzel CH، Hermann B، Behl C، وآخرون (سبتمبر 1998). "Functional antagonism of gonadal steroids at the 5-hydroxytryptamine type 3 receptor". Mol. Endocrinol. ج. 12 ع. 9: 1441–51. DOI:10.1210/mend.12.9.0163. PMID:9731711.
- ^ أ ب ت Mellon SH (أكتوبر 2007). "Neurosteroid regulation of central nervous system development". Pharmacol. Ther. ج. 116 ع. 1: 107–24. DOI:10.1016/j.pharmthera.2007.04.011. PMC:2386997. PMID:17651807. مؤرشف من الأصل في 2019-12-16.
- ^ Rupprecht R، Reul JM، Trapp T، وآخرون (سبتمبر 1993). "Progesterone receptor-mediated effects of neuroactive steroids". Neuron. ج. 11 ع. 3: 523–30. DOI:10.1016/0896-6273(93)90156-l. PMID:8398145.
- ^ أ ب Thomas P، Pang Y (2012). "Membrane progesterone receptors: evidence for neuroprotective, neurosteroid signaling and neuroendocrine functions in neuronal cells". Neuroendocrinology. ج. 96 ع. 2: 162–71. DOI:10.1159/000339822. PMC:3489003. PMID:22687885.
- ^ Pang Y، Dong J، Thomas P (يناير 2013). "Characterization, neurosteroid binding and brain distribution of human membrane progesterone receptors δ and {epsilon} (mPRδ and mPR{epsilon}) and mPRδ involvement in neurosteroid inhibition of apoptosis". Endocrinology. ج. 154 ع. 1: 283–95. DOI:10.1210/en.2012-1772. PMC:3529379. PMID:23161870.
- ^ Sleiter N، Pang Y، Park C، وآخرون (أغسطس 2009). "Progesterone receptor A (PRA) and PRB-independent effects of progesterone on gonadotropin-releasing hormone release". Endocrinology. ج. 150 ع. 8: 3833–44. DOI:10.1210/en.2008-0774. PMC:2717864. PMID:19423765.
- ^ Lamba V، Yasuda K، Lamba JK، وآخرون (سبتمبر 2004). "PXR (NR1I2): splice variants in human tissues, including brain, and identification of neurosteroids and nicotine as PXR activators". Toxicol. Appl. Pharmacol. ج. 199 ع. 3: 251–65. DOI:10.1016/j.taap.2003.12.027. PMID:15364541.
- ^ Hu AQ، Wang ZM، Lan DM، وآخرون (يوليو 2007). "Inhibition of evoked glutamate release by neurosteroid allopregnanolone via inhibition of L-type calcium channels in rat medial prefrontal cortex". Neuropsychopharmacology. ج. 32 ع. 7: 1477–89. DOI:10.1038/sj.npp.1301261. PMID:17151597.
- ^ أ ب ت Earl DE، Tietz EI (أبريل 2011). "Inhibition of recombinant L-type voltage-gated calcium channels by positive allosteric modulators of GABAA receptors". J. Pharmacol. Exp. Ther. ج. 337 ع. 1: 301–11. DOI:10.1124/jpet.110.178244. PMC:3063747. PMID:21262851.
- ^ Keitel V، Görg B، Bidmon HJ، وآخرون (نوفمبر 2010). "The bile acid receptor TGR5 (Gpbar-1) acts as a neurosteroid receptor in brain". Glia. ج. 58 ع. 15: 1794–805. DOI:10.1002/glia.21049. PMID:20665558.
- ^ Rougé-Pont F، Mayo W، Marinelli M، Gingras M، Le Moal M، Piazza PV (يوليو 2002). "The neurosteroid allopregnanolone increases dopamine release and dopaminergic response to morphine in the rat nucleus accumbens". Eur. J. Neurosci. ج. 16 ع. 1: 169–73. DOI:10.1046/j.1460-9568.2002.02084.x. PMID:12153544.
- ^ أ ب Frye CA (ديسمبر 2009). "Neurosteroids' effects and mechanisms for social, cognitive, emotional, and physical functions". Psychoneuroendocrinology. 34 Suppl 1: S143–61. DOI:10.1016/j.psyneuen.2009.07.005. PMC:2898141. PMID:19656632. مؤرشف من الأصل في 2018-07-30.
- ^ Pinna G، Costa E، Guidotti A (فبراير 2005). "Changes in brain testosterone and allopregnanolone biosynthesis elicit aggressive behavior". Proc. Natl. Acad. Sci. U.S.A. ج. 102 ع. 6: 2135–40. DOI:10.1073/pnas.0409643102. PMC:548579. PMID:15677716.
- ^ Terán-Pérez G، Arana-Lechuga Y، Esqueda-León E، Santana-Miranda R، Rojas-Zamorano JÁ، Velázquez Moctezuma J (أكتوبر 2012). "Steroid hormones and sleep regulation". Mini Rev Med Chem. ج. 12 ع. 11: 1040–8. DOI:10.2174/138955712802762167. PMID:23092405. مؤرشف من الأصل في 2019-06-24.
- ^ Patte-Mensah C، Meyer L، Taleb O، Mensah-Nyagan AG (فبراير 2014). "Potential role of allopregnanolone for a safe and effective therapy of neuropathic pain". Prog. Neurobiol. ج. 113: 70–8. DOI:10.1016/j.pneurobio.2013.07.004. PMID:23948490.
- ^ أ ب Bäckström T، Andersson A، Andreé L، وآخرون (ديسمبر 2003). "Pathogenesis in menstrual cycle-linked CNS disorders". Ann. N. Y. Acad. Sci. ج. 1007: 42–53. DOI:10.1196/annals.1286.005. PMID:14993039.
- ^ Guille C، Spencer S، Cavus I، Epperson CN (يوليو 2008). "The role of sex steroids in catamenial epilepsy and premenstrual dysphoric disorder: implications for diagnosis and treatment". Epilepsy Behav. ج. 13 ع. 1: 12–24. DOI:10.1016/j.yebeh.2008.02.004. PMC:4112568. PMID:18346939.
- ^ Finocchi C، Ferrari M (مايو 2011). "Female reproductive steroids and neuronal excitability". Neurol. Sci. 32 Suppl 1: S31–5. DOI:10.1007/s10072-011-0532-5. PMID:21533709.
- ^ أ ب Bäckström T، Haage D، Löfgren M، وآخرون (سبتمبر 2011). "Paradoxical effects of GABA-A modulators may explain sex steroid induced negative mood symptoms in some persons". Neuroscience. ج. 191: 46–54. DOI:10.1016/j.neuroscience.2011.03.061. PMID:21600269.
- ^ أ ب Andréen L، Nyberg S، Turkmen S، van Wingen G، Fernández G، Bäckström T (سبتمبر 2009). "Sex steroid induced negative mood may be explained by the paradoxical effect mediated by GABAA modulators". Psychoneuroendocrinology. ج. 34 ع. 8: 1121–32. DOI:10.1016/j.psyneuen.2009.02.003. PMID:19272715.
- ^ أ ب Bäckström T، Bixo M، Johansson M، وآخرون (فبراير 2014). "Allopregnanolone and mood disorders". Prog. Neurobiol. ج. 113: 88–94. DOI:10.1016/j.pneurobio.2013.07.005. PMID:23978486.
- ^ Andréen L، Sundström-Poromaa I، Bixo M، Nyberg S، Bäckström T (أغسطس 2006). "Allopregnanolone concentration and mood--a bimodal association in postmenopausal women treated with oral progesterone". Psychopharmacology (Berl.). ج. 187 ع. 2: 209–21. DOI:10.1007/s00213-006-0417-0. PMID:16724185.
- ^ أ ب Andréen L، Spigset O، Andersson A، Nyberg S، Bäckström T (يونيو 2006). "Pharmacokinetics of progesterone and its metabolites allopregnanolone and pregnanolone after oral administration of low-dose progesterone". Maturitas. ج. 54 ع. 3: 238–44. DOI:10.1016/j.maturitas.2005.11.005. PMID:16406399.
- ^ Orrin Devinsky؛ Steven Schachter؛ Steven Pacia (1 يناير 2005). Complementary and Alternative Therapies for Epilepsy. Demos Medical Publishing. ص. 378–. مؤرشف من الأصل في 2014-06-20.
| ألوبريجنانولون في المشاريع الشقيقة: | |
| |