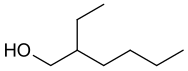
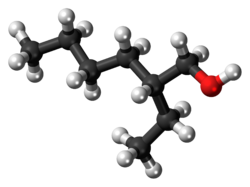
2-إيثيل هكسانول
| 2-إيثيل هكسانول | |
|---|---|
| اعتبارات علاجية | |
| معرّفات | |
| CAS | 104-76-7 |
| بوب كيم | CID 7720 |
| ECHA InfoCard ID | 100.002.941 |
| كيم سبايدر | 7434 |
| المكون الفريد | XZV7TAA77P |
| كيوتو | C02498 |
| ChEBI | CHEBI:16011 |
| ChEMBL | CHEMBL31637 |
| بيانات كيميائية | |
| الصيغة الكيميائية | C8H18O |
| الكتلة الجزيئية | 833 غرام لكل مول |
| بيانات فيزيائية | |
| نقطة الانصهار | -76 °C (-105 °F) |
| تعديل مصدري - تعديل | |
ثنائي إيثيل هكسانول هو كحول كيرالي يحتوي على ثمانية ذرات كربون، وهو عبارة عن سائل عديم اللون شحيح الذوبان في الماء، ولكنه قابل للذوبان بشكل جيد في معظم المذيبات العضوية. يتم إنتاج كحول ثنائي الإيثيل هكسانول عالميّاً على نطاق واسع (بمعدل يزيد عن 2،000،000،000 كيلوغرام سنويّاً) بهدف استخدامه في العديد من التطبيقات مثل صناعة المذيبات، والمنكهات، والعطور، كما يُستخدم كمادة اوليّة في إنتاج مواد كيميائية أخرى مثل المرطبات، والملدنات.[1] يُوجد ثنائي الإيثيل هكسانول في النباتات، والفواكه، والنبيذ.[2][3] تتميّز رائحة كحول ثنائي الإيثيل هكسانول بكونها ترابية ثقيلة ذات نكهة وردية قليلاً في حالة المصاوغ المرآتي R و"عطريّة زهريّة ذات نكهة حلوة خفيفة بفي حالة لمصاوغ المرآتي S.[4][5]
التسمية
[عدل]يُشار إلى مركب 2-إيثيل هكسانول ومشتقاته بشكل شائع في المجالات الصناعيّة بالتسمية (أيزوأوكتانول) ومشتقاتها التي تتضمن الأيزوأوكتيل، بيد أنّ اتفاقيات الاتحاد الدولي للكيمياء البحتة والتطبيقية للتسمية تشترط أنه من الأصوب أن ينطبق هذا الاسم على تصاوغ آخر من مركبات الأوكتانول هو 6-ميثيل الهبتان 1-ول.[6] فهرست خدمة المستخلصات الكيميائية أيضًا المسمى أيزوأوكتانول على أنه 6-ميثيل الهبتان 1-ول.
الخصائص
[عدل]يساعد تفرع ذرات الكربون في جزيء ثنائي الإيثيل هكسانول على منع التبلّر. تتأثر مركبات إسترات ثنائي الإيثيل هكسانول بشكل مماثل، وجميعها مركبات ذات تطايريّة منخفضة، ولها خصائص مطرّية نظرًا لأن ثنائي الإيثيل هكسانول عبارة عن كحول دهني.
التطبيقات
[عدل]يستخدم ثنائي الإيثيل هكسانول بشكل شائع كمذيب منخفض التطاير، ويمكن استخدامه أيضًا كمعزز للرقم السيتاني عند التفاعل مع حمض النيتريك، كما يستخدم في التفاعل مع الإبيكلوروهيدرين وهيدروكسيد الصوديوم لإنتاج إيثر الغليسيديل للجزيء الذي يستخدم كمخفف إيبوكسي تفاعلي في مختلف تطبيقات الطلاء والمواد اللاصقة ومانعات التسرب. يمكن استخدامه في تطوير الصور وإنتاج المطاط واستخراج النفط والغاز.[7]
تُعتبر إسترات ثنائي الإيثيل هكسانول أساساً لبعض التطبيقات الصناعيّة مثل في إنتاج الملدنات ومواد التشحيم، حيث يساعد وجودها على تقليل اللزوجة وخفض نقاط التجمد.
يشيع استخدام مركب فثالات مضاعف ثنائي إيثيل الهكسيل في إنتاج مادّة البولي فينيل كلوريد أو الكلوريد متعدد الفينيل، يُعتبر مركب ثلاثي ترايستر تريس (ثنائي إيثيل هكسيل) تريميليت ملدّناً شائع الاستخدام، ويتم إنتاجه عن طريق أسترة ثلاثة جزيئات من ثنائي إيثيل هكسانول لكل حمض ثلاثي ألانتيكريد.
الإنتاج صناعيّاً
[عدل]يتم إنتاج ثنائي الإيثيل هكسانول صناعيًا عن طريق التكاثف الألدولي لمركبات ألدهيد البوتان، ثمّ هدرجة الهيدروكسي ألدهيد الناتج. يُصنّع نحو 2500000 طنّاً من ثنائي إيثيل الهكسانول سنويّاً باستخدام هذه الطريقة.[8][9]

ويمكن الحصول على مركبات ألدهيد البوتان (ن-بيوتانول) من خلال تفاعل أوكسو للبروبيلين كعمل قائم بذاته، أو كخطوة أولى في عمليّة متكاملة. تُنتج معظم تلك العمليّات مركبات ن-بيوتانول، وإيزوبيوتانول إلى جانب مركب ثنائي الإيثيل هكسانول. يشار أحيانًا إلى الكحوليات المحضّرة باستخدام هذه الطريقة باسم كحولات أوكسو. تشبه هذه العملية إلى حد كبير عملية تفاعل غيربت، والتي يمكن إنتاجه من خلالها أيضًا.[10]
الآثار على الصحة العامة للإنسان والحيوان
[عدل]يظهر مركب 2-إيثيل الهكسانول سمّية منخفضة في النماذج الحيوانية، وتتراوح الجرعة المميتة منه ما بين 2-3 غرام/كيلوغرام في الفئران. كما وُجد أن مركبات 2-إيثيل الهكسانول العضوية المتطايرة تتسبّب في بعض المشكلات الصحية التي ترتبط بجودة الهواء الداخليّ، مثل تهيج الجهاز التنفسي. ينبعث 2-إيثيل هكسانول في الهواء من خلال أرضيات البولي فينيل كلوريد المركبة على الخرسانة التي لم تُجفّف بشكل صحيح.[11][12]
وُجد أيضًا أن هناك علاقة وثيقة بين مركب 2-إيثيل الهكسانول وزيادة حدوث تشوهات الهيكل العظمي في الأجنة، أو ما يُعرف بتسمّم النمو. ويُعتقد أن هذا ناتج عن عملية التمثيل الغذائي لمركب 2-إيثيل الهكسانول، والتي يتحوّل خلالها إلى حمض 2-إيثيل الهكسانويك عن طريق أكسدة الكحول الأساسيّ.[13][14] وقد ثبت أن حمض 2-إيثيل الهكسانويك والمواد المماثلة مثل حمض الفالبرويك تلعب دوراً في حدوث التشوهات الخلقية.[15][16][17][18][19]
المراجع
[عدل]- ^ Helmut Bahrmann؛ Heinz-Dieter Hahn؛ Dieter Mayer (2005). "2-Ethylhexanol". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a10_137. ISBN:978-3527306732.
- ^ Fan، Wenlai؛ Qian، Michael C. (2006). "Characterization of Aroma Compounds of Chinese "Wuliangye" and "Jiannanchun" Liquors by Aroma Extract Dilution Analysis". Journal of Agricultural and Food Chemistry. ج. 54 ع. 7: 2695–2704. DOI:10.1021/jf052635t. PMID:16569063.
- ^ Mayuoni-Kirshinbaum، Lina؛ Tietel، Zipora؛ Porat، Ron؛ Ulrich، Detlef (2012). "Identification of aroma-active compounds in 'wonderful' pomegranate fruit using solvent-assisted flavour evaporation and headspace solid-phase micro-extraction methods". European Food Research and Technology. ج. 235 ع. 2: 277–283. DOI:10.1007/s00217-012-1757-0. S2CID:97102092.
- ^ Klaus Rettinger؛ Christian Burschka؛ Peter Scheeben؛ Heike Fuchs؛ Armin Mosandl (1991). "Chiral 2-alkylbranched acids, esters and alcohols. Preparation and stereospecific flavour evaluation" (PDF). Tetrahedron: Asymmetry. ج. 2 ع. 10: 965–968. DOI:10.1016/S0957-4166(00)86137-6. مؤرشف من الأصل (PDF) في 2021-11-04.
- ^ McGinty، D.؛ Scognamiglio، J.؛ Letizia، C.S.؛ Api، A.M. (2010). "Fragrance material review on 2-ethyl-1-hexanol". Food and Chemical Toxicology. ج. 48: S115–S129. DOI:10.1016/j.fct.2010.05.042. PMID:20659633.
- ^ "Rule A-2. Saturated Branched-chain Compounds and Univalent Radicals (ACYCLIC HYDROCARBONS)". www.acdlabs.com. مؤرشف من الأصل في 2021-08-30.
- ^ "Product Spotlight: 2-Ethylhexanol". 12 ديسمبر 2019. مؤرشف من الأصل في 2021-04-14.
- ^ C. Kohlpaintner؛ M. Schulte؛ J. Falbe؛ P. Lappe؛ J. Weber (2008). "Aldehydes, Aliphatic". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a01_321.pub2. ISBN:978-3527306732.
- ^ Ashford’s Dictionary of Industrial Chemicals, Third edition, 2011, page 4180-4181.
- ^ Miller، Robert؛ Bennett، George (يناير 1961). "Producing 2-Ethylhexanol by the Guerbet Reaction". Industrial & Engineering Chemistry. ج. 53 ع. 1: 33–36. DOI:10.1021/ie50613a027.
- ^ Ernstgård، L.؛ Norbäck، D. (2010). "Acute effects of exposure to 1 mg/m(3) of vaporized 2-ethyl-1-hexanol in humans". Indoor Air. ج. 20 ع. 2: 168–75. DOI:10.1111/j.1600-0668.2009.00638.x. PMID:20409194.
- ^ Hildenbrand، S.؛ Wodarz، R. (2009). "Biomonitoring of the di(2-ethylhexyl) phthalate metabolites mono(2-ethyl-5-hydroxyhexyl) phthalate and mono(2-ethyl-5-oxohexyl) phthalate in children and adults during the course of time and seasons". International Journal of Hygiene and Environmental Health. ج. 212 ع. 6: 679–84. DOI:10.1016/j.ijheh.2009.06.003. PMID:19615938.
- ^ Deisinger, PJ, Boatman, RJ, Guest, D (15 Mar 2009). "Metabolism of 2-ethylhexanol administered orally and dermally to the female Fischer-344 rat". hero.epa.gov (بالإنجليزية). Archived from the original on 2021-11-22. Retrieved 2021-04-09.
{{استشهاد ويب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Eastman Kodak Company, Eastman Kodak (15 Mar 2009). "Pharmacokinetic studies with 2-ethylhexanol in the female fischer 344 rat (final report) with attachments and cover letter dated 050791". hero.epa.gov (بالإنجليزية). Archived from the original on 2021-11-22. Retrieved 2021-04-09.
- ^ Pennanen، Sirpa؛ Tuovinen، Kai؛ Huuskonen، Hannele؛ Komulainen، Hannu (1992). "The developmental toxicity of 2-ethylhexanoic acid in Wistar rats". Fundamental and Applied Toxicology. ج. 19 ع. 4: 505–511. DOI:10.1016/0272-0590(92)90088-Y. PMID:1426708. مؤرشف من الأصل في 2021-11-22.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|بواسطة=تم تجاهله يقترح استخدام|عبر=(مساعدة)صيانة الاستشهاد: التاريخ والسنة (link) - ^ "2-Ethylhexanoic acid". ACGIH. مؤرشف من الأصل في 2021-11-22. اطلع عليه بتاريخ 2021-04-09.
- ^ "Annex 1 Background Document to the Opinion proposing harmonised classification and labelling at EU level of 2-Ethylhexanoic acid and its salts, with the exception of those specified elsewhere in this Annex". European Chemicals Agency. 2020. مؤرشف من الأصل في 2021-11-22. اطلع عليه بتاريخ 2021-04-09.
- ^ "Valproic Acid". The American Society of Health-System Pharmacists. مؤرشف من الأصل في 2017-07-31. اطلع عليه بتاريخ 2015-10-23.
- ^ "Valproate banned without the pregnancy prevention programme". GOV.UK. مؤرشف من الأصل في 2021-10-27. اطلع عليه بتاريخ 2018-04-26.