خلية جذعية سرطانية
| خلية جذعية سرطانية | |
|---|---|
| تفاصيل | |
| تعديل مصدري - تعديل |
الخلايا الجذعية السرطانية (بالإنجليزية: neoplastic stem cells) هي خلايا سرطانية (توجد داخل الأورام الخبيثة أو سرطانات الدم) تمتلك جميع خصائص الخلية الجذعية السليمة، ولا سيما القدرة على التمايز إلى جميع أنواع الخلايا الموجودة في العينة السرطانية. ولذلك، فإن الخلايا الجذعية السرطانية هي خلايا مولدة للورم (مكونة للورم)، في مقابل غيرها من الخلايا السرطانية غير المكونة للورم. ويمكن أن تولد الخلايا الجذعية السرطانية الأورام من خلال عمليات التجديد الذاتي التي تقوم بها الخلية الجذعية وتمايزها إلى أنواع عديدة من الخلايا الأخرى. يفترض أن تدوم مثل هذه الخلايا في الأورام في شكل تجمع خلوي متميز وتسبب الانتكاس وانتشار المرض، وذلك عن طريق تحفيز تكوين أورام جديدة. ومن ثم، فإن تطوير علاجات نوعية تستهدف الخلايا الجذعية السرطانية يعطي الأمل في تحسين حياة مرضى السرطان وتعايشهم مع المرض، وخاصةً أولئك الذين يعانون من مرض انتشاري.
جدير بالذكر أن طرق علاج السرطان الحالية تم تطوير معظمها بناءً على نموذج حيواني، حيث تم اعتبار العلاجات القادرة على تحفيز انكماش الورم وتقلصه من الأساليب العلاجية الفعالة. ومع ذلك، لا يمكن أن تمثل الحيوانات نموذجًا كاملاً للأمراض التي تصيب الإنسان. وعلى وجه الخصوص، في نماذج الفئران التي لا يتجاوز عمرها عامين، يكون من الصعب للغاية دراسة انتكاس الورم.
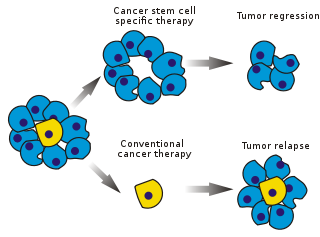
كثيرًا ما تُختبر فعالية علاجات السرطان، في مراحله الأولى، من خلال تقدير الجزء المزال من كتلة الورم (القتل الجزئي للورم). ونظرًا لأن الخلايا الجذعية السرطانية ستشكل نسبة ضئيلة جدًا من الورم، فهذا لا يستدعي بالضرورة اختيار الأدوية التي تستهدف خصيصًا الخلايا الجذعية. تشير بعض النظريات إلى أن العلاج الكيماوي التقليدي يقتل الخلايا المتمايزة التي تشكل جسم الورم وغير القادرة على توليد خلايا جديدة. في حين أن مجموعة من الخلايا الجذعية السرطانية، التي تسبب الأورام، يمكن أن تظل كما هي دون أن يؤثر فيها العلاج الكيماوي وتتسبب في انتكاس المرض.
الدليل على وجود الخلايا الجذعية السرطانية[عدل]

إن حقيقة وجود الخلايا الجذعية السرطانية موضوع مختلف فيه في الأبحاث الطبية، وذلك لأن العديد من الدراسات لم تنجح في اكتشاف أوجه التشابه والاختلاف بين أنسجة الخلايا الجذعية السليمة والخلايا الجذعية السرطانية.[1] يجب أن تكون الخلايا السرطانية قادرة على التكاثر والتجدد الذاتي المستمر حتى تتمكن من عمل الطفرات المتعددة اللازمة لعملية التسرطن وحتى تدعم نمو الورم بما أن الخلايا المتمايزة لا تستطيع الانقسام إلى أجل غير مسمى (حيث إن انقسامها مقيد بما يسمى حد هايفليك).[بحاجة لمصدر] ومع ذلك، هناك خلاف حول ما إذا كانت مثل هذه الخلايا المتمايزة تمثل أقلية في الورم أم لا. وإذا اشتملت معظم خلايا الورم على خصائص الخلايا الجذعية، فليس هناك ما يدفع إلى التركيز على مجموعة خلوية ثانوية بعينها. هذا بالإضافة إلى وجود خلاف حول الخلية الأصلية التي نشأت عنها الخلايا الجذعية السرطانية - ما إذا كانت نشأت عن الخلايا الجذعية التي فقدت القدرة على تنظيم عملية التكاثر أو عن المجموعة الأكثر تمايزًا من الخلايا السليفة (progenitor cells) التي اكتسبت القدرة على التجدد الذاتي (وهو أمر مرتبط بمسألة المرونة التكيفية (plasticity) للخلية الجذعية).
وقد تم نشر أول دليل قاطع على وجود الخلايا الجذعية السرطانية في عام 1997 في المجلة الطبية طب الطبيعة. قام الباحثان بونيه وديك[2] بعزل مجموعة ثانوية من الخلايا المصابة باللوكيميا التي تظهر بها الواسمة السطحية CD34، ولكنها تفتقر إلى الواسمة CD38. وقد أثبت الباحثان أن المجموعة الخلوية الثانوية CD34+/CD38- قادرة على تكوين أورام سرطانية في فئران التجارب المصابة بمرض السكر ونقص المناعة والمعروفة باسم NOD/SCID وهي فئران تشبه أنسجتها أنسجة المصدر الذي أخذت منه العينة.[3]
في تجارب أبحاث السرطان، يتم في بعض الأحيان حقن خلايا مصابة بورم في حيوان تجارب لتكوين ورم سرطاني بداخله. ويتم بعد ذلك متابعة تقدم المرض في مرحلة مبكرة ويمكن اختبار قدرة الأدوية الجديدة على القضاء عليه. ومع ذلك، فإن تكوين ورم فعال يحتاج إلى حقن الآلاف بل عشرات الآلاف من الخلايا. وكالمعتاد، تم إرجاع سبب ذلك إلى ضعف مناهج البحث (ذلك حيث إن الخلايا الورمية تفقد ما بها من حيوية أثناء عملية النقل) أو الأهمية البالغة للبيئة المحيطة الدقيقة وهي المحيط البيوكيميائي للخلايا التي تم حقنها. ويجادل مؤيدو نموذج الخلية الجذعية السرطانية بأن جزءًا صغيرًا فقط من الخلايا التي تم حقنها - الخلايا الجذعية السرطانية - بإمكانها تكوين ورم. في سرطان الدم النخاعي الحاد الذي يصيب الإنسان، يكون تواتر هذه الخلايا أقل من 1 لكل 10,000.[2]
تأتي أدلة أخرى على وجود الخلايا الجذعية السرطانية من علم الأنسجة وهو العلم الذي يختص بدراسة تركيب أنسجة الأورام. هناك الكثير من الأورام التي تكون غير متجانسة على الإطلاق وتحتوي على العديد من أنواع الخلايا التي يكون مصدرها العضو العائل. وعادةً ما تحتفظ الأورام بعدم تجانسها عن طريق انتشارها أو انتقالها إلى أماكن أخرى غير مصابة في الجسم. وهذا يدل على أن الخلية التي أنتجت هذه الأورام لديها القدرة على تكوين أنواع عديدة من الخلايا. بعبارة أخرى، فإنها خلية متعددة القدرات، وهي سمة أصيلة في الخلايا الجذعية.[2]
دعا وجود الخلايا الجذعية لدى مرضى اللوكيميا إلى إجراء المزيد من البحوث عن أنواع السرطان الأخرى. وقد تم مؤخرًا العثور على الخلايا الجذعية السرطانية في العديد من الأورام الصلبة، بما في ذلك:
- سرطان المخ[4]
- سرطان الثدي[5]
- سرطان القولون[6]
- سرطان المبيض[7]
- سرطان البنكرياس[8]
- سرطان البروستاتا[9][10]
أهمية الخلايا الجذعية السرطانية[عدل]
إن اكتشاف مصدر الخلايا السرطانية ليس مهمًا فقط لنجاح العلاج، ولكن إذا لم تنجح العلاجات الحالية للسرطان في تدمير الخلايا الجذعية السرطانية جيدًا، فإن الورم سيظهر مرة أخرى. هذا بالإضافة إلى إمكانية ألا يقضي العلاج الكيماوي، مثلاً، تمامًا على الخلايا الجذعية السرطانية المقاومة له. وبناءً عليه، فإن الورم الذي سيتكون بعد ذلك يحتمل بدرجة كبيرة أن يكون هو الآخر مقاومًا للعلاج الكيماوي. وإذا تم الكشف عن الورم السرطاني في وقت مبكر كفاية، فيمكن القضاء على نسبة كبيرة منه ومنعه من الظهور مرة أخرى بطرق العلاج التقليدية. ولكن كلما ازداد حجم الورم، ازدادت صعوبة إزالته دون مواجهة مقاومة منه وترك ما يكفي في الجسم لإعادة ظهوره مرة أخرى.
يمكن أن تتسبب بعض علاجات السرطان إلى جانب العلاج الكيماوي، مثل دواء باكليتاكسيل المستخدم في علاج سرطان المبيض (سرطان عادةً ما يُكتشف في مراحل متأخرة) في رفض الجسم الاستجابة إلى العلاج الكيماوي (تنتكس 55-75% من الحالات بعد أقل من عامين[11]). ويحتمل أن تكون هذه العلاجات تفعل ذلك عن طريق تدمير الخلايا السرطانية سريعة التأثر بالدواء (يستهدف خلايا CD44 الإيجابية، وهي سمة ارتبطت بزيادة مدة بقاء بعض سرطانات المبيض) ويترك تلك الخلايا التي لم تتأثر بدواء باكليتاكسيل (خلايا CD44 السلبية) لتنمو من جديد، وذلك حتى بعد إزالة أكثر من ثلث إجمالي حجم الورم.[12] ومع ذلك، فإن هناك دراسات تبين كيف يمكن استخدام دواء باكليتاكسيل مع لجائن أخرى للتأثير على خلايا CD44 الإيجابية.[13] وبينما أصبح دواء باكليتاكسيل مؤخرًا لا يستطيع وحده علاج مرض السرطان، فإنه فعال في إطالة عمر المرضى.[11]
النماذج الميكانيكية والرياضية[عدل]
متى تم وضع فرضيات طرق علاج السرطان، أصبح من الممكن وضع نماذج الرياضيات الحيوية التنبؤية،[14] بناءً على طريقة الحيز الخلوي على سبيل المثال. على سبيل المثال، يمكن معرفة معدلات نمو الخلايا الشاذة من نظيراتها السليمة من خلال معامل طفرات محددة. وقد تم توظيف مثل هذا النموذج للتنبؤ بأن تضرر الخلايا الناضجة بشكل مستمر يزيد من فرصة تكوين خلايا جديدة شاذة، وبالتالي خطر الإصابة بالسرطان.[15] ومع ذلك، فإنه ينبغي القيام بالكثير من الأبحاث قبل تحديد الفعالية الإكلينيكية لهذه النماذج.[16]
أصل الخلايا الجذعية السرطانية[عدل]
ما زال أصل الخلايا الجذعية السرطانية مجالاً للبحث المستمر. وقد تم تشكيل العديد من المجموعات داخل المجتمع العلمي للنظر في هذه المسألة، ومن المحتمل أن تكون عدة إجابات صحيحة، وذلك بناءً على نوع الورم والنمط الظاهري له. جدير بالذكر أنه سوف يثار فارق واحد مهم في كثير من الأحيان وهو أن خلية المنشأ للورم لا يمكن أن توضيحها باستخدام الخلية الجذعية السرطانية كنموذج. ويرجع السبب في ذلك إلى أن الخلايا الجذعية السرطانية معزولة عن أورام المرحلة الأخيرة. ولذلك، فإن وصف الخلية الجذعية السرطانية بأنها خلية المنشأ كثيرًا ما يكون ادعاءً غير دقيق، على الرغم من أن الخلية الجذعية السرطانية قادرة على بدء تكوين ورم جديد.
مع هذا التوضيح المذكور، فإن العديد من النظريات تحدد أصل الخلايا الجذعية السرطانية. وباختصار، قد تكون الخلايا الجذعية السرطانية: طفرات في خلايا جذعية متطورة أو خلايا سليفة متطورة أو طفرات في خلايا جذعية بالغة أو خلايا سليفة بالغة أو خلايا طفرية تكتسب صفات الخلايا الجذعية. كثيرًا ما تركز هذه النظريات على خلية المنشأ للورم ومن ثم ينبغي التعامل معها بشيء من الحذر والشك.
يفضل بعض الباحثين النظرية التي تقول إن علة تكوين الخلية الجذعية السرطانية هي حدوث طفرة في مجموعات الأعشاش البيئية للخلايا الجذعية أثناء تكونها. ويستلزم التطور المنطقي لهذه النظرية أن تتعرض هذه المجموعات الجذعية لطفرات ثم تنتشر إلى حد أن تتشارك في الطفرة العديد من الخلايا المتحدرة من الخلايا الجذعية الطفرية. وتصبح هذه الخلايا الجذعية الابنة أقرب ما تكون إلى أن تتحول إلى أورام، وبما أن هناك الكثير منها، تزيد احتمالات تسبب الطفرة في تكون سرطان.[17]
توجد نظرية أخرى تربط بين الخلايا الجذعية البالغة وتكون الأورام. ويرتبط ذلك في معظم الأحيان بالأنسجة التي يرتفع معدل تجديد خلاياها (مثل، أنسجة الجلد أو الأمعاء). في هذه الأنسجة، كان يُفترض منذ فترة طويلة أن تكون الخلايا الجذعية مسئولة عن تكوين الورم. ويعتبر ذلك نتيجة منطقية لعمليات الانقسام الخلوي المتكررة لهذه الخلايا الجذعية (مقارنةً بمعظم الخلايا الجذعية البالغة)، بالإضافة إلى العمر المديد للخلايا الجذعية البالغة. ويساعد هذا التركيب في إيجاد مجموعة من الظروف المثالية لتتراكم الطفرات، مع العلم أن تراكم الطفرات هو العامل الأساسي الذي يؤدي إلى بداية السرطان في الجسم. وعلى الرغم من الدعم المنطقي لتلك لنظرية، فإنه في الآونة الأخيرة فقط ظهر دليل على أن هذا الارتباط يمثل ظاهرة فعلية. ومن المهم الأخذ في الاعتبار أنه نظرًا للطبيعة غير المتجانسة للدليل على وجود الخلايا الجذعية السرطانية، فمن المحتمل أن يتكون أي نوع سرطان من أصل بديل.
كثيرًا ما يبزغ احتمال ثالث وهو إمكانية إلغاء تمايز الخلايا الطفرية لدرجة أن تكتسب هذه الخلايا خصائص الخلية الجذعية. ويستخدم هذا الاحتمال كثيرًا كبديل محتمل لأية خلية منشأ محددة؛ حيث إنه يشير إلى أن أية خلية يمكن أن تصبح خلية جذعية سرطانية.
يوجد مفهوم آخر متعلق بهذه المسألة وهو مفهوم السلسلة الهرمية للورم. يدعي هذا المفهوم أن الورم عبارة عن مجموعة غير متجانسة من الخلايا الطفرية التي تشترك جميعًا في بعض الطفرات، ولكنها ستختلف في أنماط ظاهرية معينة. في هذا النموذج، يتكون الورم من عدة أنواع من الخلايا الجذعية، يعد أحدها الأمثل لبيئة بعينها بينما يمثل العديد منها بدائل أقل نجاحًا. ويمكن لهذه البدائل الثانوية أن تصبح أكثر نجاحًا في بعض البيئات وتسمح للورم بالتكيف مع بيئته، بما في ذلك الطرق التي يمكن معالجة الأورام بها. وإذا كان هذا الوضع صحيحًا، فإن له انعكاسات خطيرة على واقعية طرق العلاج النوعية للخلية الجذعية السرطانية.[18] بداخل نموذج السلسلة الهرمية للورم، سيكون صعبًا للغاية تحديد أصل الخلية الجذعية السرطانية.
تأثير الخلايا الجذعية السرطانية على علاج السرطان[عدل]
إن وجود الخلايا الجذعية السرطانية له تأثيرات عدة على طرق علاج السرطان في المستقبل. وتشمل هذه التأثيرات تعيين المرض ووضع أهداف علاجية انتقائية ومنع انتشار المرض وتحديد استراتيجيات جديدة للتدخل العلاجي.
إن الخلايا الجذعية الجسدية السليمة تقاوم بطبيعتها أدوية العلاج الكيماوي (chemotherapeutic agents)؛ حيث إن لديها مضخات متعددة (مثل، مقاومة الأدوية المتعددة MDR) تقوم بضخ الأدوية ويقوم الحمض النووي DNA بتجديد البروتينات، بالإضافة إلى أن معدل تجديد الخلايا لديها بطئ (أدوية العلاج الكيماوي تستهدف بصورة طبيعية الخلايا سريعة التكاثر)[بحاجة لمصدر]. إن الخلايا الجذعية السرطانية التي تحولت من خلايا جذعية سليمة يمكن أيضًا أن تنتج بروتينات تعمل على زيادة مقاومتها لأدوية العلاج الكيماوي. تقوم هذه الخلايا الجذعية السرطانية التي ما زالت على قيد الحياة بإعادة تكوين الورم؛ مما يسبب حدوث انتكاس. من خلال الاستهداف الانتقائي للخلايا الجذعية السرطانية، سيصبح من الممكن علاج المرضى الذين يعانون من أورام عدوانية وغير قابلة للاستئصال، فضلاً عن منع الورم من الانتشار في الجسم. تشير الفرضية العلمية إلى أنه بعدما يتم القضاء على الخلية الجذعية السرطانية، فإن السرطان سيتقهقر بسبب التمايز الخلوي و/أو موت الخلية[بحاجة لمصدر]. ولم يتضح بعد النسبة التي تمثلها الخلايا الجذعية السرطانية من خلايا الورم، وبالتالي ضرورة القضاء عليها.[19]
قدم عدد من الدراسات أبحاثًا في إمكانية تحديد واسمات معينة يمكن أن تميز الخلايا الجذعية السرطانية من كتلة الورم (وكذلك من الخلايا الجذعية السليمة).[5] هذا بالإضافة إلى البحث في التوقيعات البروتيومية والجينومية للورم[بحاجة لمصدر]. وفي عام 2009، اكتشف العلماء مركبًا، وهو السالينوميسين، الذي يقلل بشكل انتقائي نسبة الخلايا الجذعية السرطانية في الثدي لدى فئران التجارب، وذلك أفضل 100 مرة من الباكليتاكسيل المستخدم بكثرة كأحد أدوية العلاج الكيماوي للسرطانات.[20]
المسارات الخلوية[عدل]
من المؤكد أن تصميم أدوية جديدة لعلاج الخلايا الجذعية السرطانية سيتطلب فهم الآليات الخلوية التي تنظم عملية تكاثر الخلية. وقد حدثت الإنجازات الأولى في هذا المجال في الخلايا الجذعية المولدة للدم ونظيراتها المتحولة في سرطان الدم، وهو المرض الذي تمت دراسة أصل الخلايا الجذعية السرطانية جيدًا من أجله. وقد أصبح من الواضح الآن أن الخلايا الجذعية في العديد من أعضاء الجسم تتشارك المسارات الخلوية نفسها، كما في حالة سرطان الدم الناتج عن الخلايا الجذعية المكونة للدم.
بالإضافة إلى ذلك، فإن خلية جذعية سليمة يمكن أن تتحول إلى خلية جذعية سرطانية عن طريق اختلال تنظيم تكاثرها ومسارات التمايز التي تتحكم بها أو عن طريق تحفيز نشاط البروتينات الورمية.
جين Bmi-1[عدل]
تم اكتشاف جين Bmi-1 من مجموعة polycomb المسئول عن تعطيل استنساخ الخلايا باعتباره جين ورمي عادي ينشط في الورم اللمفي[21] وثبت مؤخرًا أنه ينظم تكاثر الخلايا الجذعية المكونة للدم على وجه التحديد.[22] كما اتضح دور جين Bmi-1 في الخلايا الجذعية العصبية.[23] ويبدو أن مسار هذا الجين يكون نشطًا في الخلايا الجذعية السرطانية في أورام المخ لدى الأطفال.[24]
جين Notch[عدل]
كان مسار جين Notch يُعرف لعلماء أحياء النمو منذ عقود مضت. وقد ثبت الآن أن دوره في السيطرة على تكاثر الخلية الجذعية يمتد لأنواع متعددة من الخلايا، بما في ذلك الخلايا الجذعية المكونة للدم والخلايا الجذعية العصبية والخلايا الجذعية الثديية.[25] جدير بالذكر أن مسار Notch يعمل كجينات ورمية في أورام الثدي[26] والأورام الأخرى.
جينا القنفذ الصوتي وWnt[عدل]
إن هذين المسارين يعملان كمسارات منظمة للخلية الجذعية.[27] وعادة ما يزداد نشاط مساري القنفذ الصوتي (SHH) وWnt بشدة في الأورام، كما أنهما ضروريان لنمو الورم. ومع ذلك، فإن عوامل استنتساخ جين Gli التي ينظمها بروتين القنفذ الصوتي تستمد اسمها من الأورام الدبقية (gliomas) حيث يتم تعبيرها عادةً عند مستويات عالية. والجدير بالذكر أنه يوجد قدر من التداخل بين المسارين وعادةً ما ينشطان معًا.[28] وهذا مجرد اتجاه وليس قاعدة ثابتة. على سبيل المثال، في سرطان القولون تظهر إشارة المسار القنفذي مقاومة لمسار Wnt.
إن محصرات مسار القنفذ الصوتي متوفرة، مثل السايكلوبامين. ويوجد أيضًا نوع جديد من السايكلوبامين قابل للذوبان في الماء يمكن أن يكون أكثر فعالية في علاج السرطان. وهناك أيضًا مركب ديميثيلامينو بارثينولين (DMAPT) القابل للذوبان في الماء والمشتق من مركب بارثينوليد (يسبب ضغط التعرض للمواد المؤكسدة ويوقف إرسال إشارات العامل النووي كابا بي (NF-kB))[29] لعلاج سرطان الدم النخاعي الحاد وربما يستخدم أيضًا في علاج سرطان العظام وسرطان البروستاتا. وقد بدأت تجربة إكلينيكية لمركب ديميثيلامينو بارثينولين في إنجلترا في أواخر عام 2007 أو عام 2008. علاوةً على ذلك، بدأ مؤخرًا إدخال دواء إيميتيلستات أو (GRN163L) في التجارب التي تستهدف الخلايا الجذعية السرطانية في سرطان العظم المعروف باسم المايلوما (myeloma). إذا كان من الممكن القضاء على الخلية الجذعية السرطانية، إذن من الممكن الشفاء من السرطان إذا لم تكن هناك المزيد من الخلايا الجذعية السرطانية لتقوم بتكوين سرطان مرة أخرى. وأخيرًا، فإن إنزيم التيلوميراز مؤهل ليكون موضوع دراسة في علم وظائف الخلية الجذعية السرطانية.[30]
اقرأ أيضا[عدل]
المراجع[عدل]
- ^ Gupta PB, Chaffer CL, Weinberg RA (2009). "Cancer stem cells: mirage or reality?". Nat Med. ج. 15 ع. 9: 1010–2. DOI:10.1038/nm0909-1010. PMID:19734877.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ أ ب ت Bonnet D, جون ديك (1997). "Human acute myeloid leukemia is organized as a hierarchy that originates from a primitive hematopoietic cell". Nature medicine. ج. 3 ع. 7: 730–7. DOI:10.1038/nm0797-730. PMID:9212098.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة) - ^ Matsui W, Huff CA, Wang Q, Malehorn MT, Barber J, Tanhehco Y, Smith BD, Civin CI, Jones RJ (2004). "Characterization of clonogenic multiple myeloma cells". Blood. ج. 103 ع. 6: 2332–6. DOI:10.1182/blood-2003-09-3064. PMID:14630803.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Singh SK, Clarke ID, Terasaki M, Bonn VE, Hawkins C, Squire J, Dirks PB (2003). "Identification of a cancer stem cell in human brain tumors". Cancer research. ج. 63 ع. 18: 5821–8. PMID:14522905. مؤرشف من الأصل في 2010-05-28.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ أ ب Al-Hajj M, Wicha MS, Benito-Hernandez A, Morrison SJ, Clarke MF (2003). "Prospective identification of tumorigenic breast cancer cells". Proceedings of the National Academy of Sciences of the United States of America. ج. 100 ع. 7: 3983–8. DOI:10.1073/pnas.0530291100. PMC:153034. PMID:12629218.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ O'Brien CA, Pollett A, Gallinger S, Dick JE (2007). "A human colon cancer cell capable of initiating tumour growth in immunodeficient mice". Nature. ج. 445 ع. 7123: 106–10. DOI:10.1038/nature05372. PMID:17122772.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Zhang S, Balch C, Chan MW, Lai HC, Matei D, Schilder JM, Yan PS, Huang TH, Nephew KP (2008). "Identification and characterization of ovarian cancer-initiating cells from primary human tumors". Cancer research. ج. 68 ع. 11: 4311–20. DOI:10.1158/0008-5472.CAN-08-0364. PMC:2553722. PMID:18519691.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Li C, Heidt DG, Dalerba P, Burant CF, Zhang L, Adsay V, Wicha M, Clarke MF, Simeone DM (2007). "Identification of pancreatic cancer stem cells". Cancer research. ج. 67 ع. 3: 1030–7. DOI:10.1158/0008-5472.CAN-06-2030. PMID:17283135.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Maitland NJ, Collins AT (2008). "Prostate cancer stem cells: a new target for therapy". J. Clin. Oncol. ج. 26 ع. 17: 2862–70. DOI:10.1200/JCO.2007.15.1472. PMID:18539965.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة) - ^ Lang Sh, Frame F, Collins A (2009). "Prostate cancer stem cells". J. Pathol. ج. 217 ع. 2: 299–306. DOI:10.1002/path.2478. PMC:2673349. PMID:19040209.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ أ ب معهد المملكة المتحدة الوطني للصحة والتميز العيادي Full guidance on the use of paclitaxel in the treatment of ovarian cancer, 22 January 2003. [وصلة مكسورة] نسخة محفوظة 16 فبراير 2012 على موقع واي باك مشين.
- ^ Mor, G. Yale Medical School. تقديم بيانات غير منشورة في جامعة ميزوري بكلية الطب في مدينة كنساس. Jan 7, 2008.
- ^ Auzenne E, Ghosh SC, Khodadadian M, Rivera B, Farquhar D, Price RE, Ravoori M, Kundra V, Freedman RS, Klostergaard J (2007). "Hyaluronic acid-paclitaxel: antitumor efficacy against CD44(+) human ovarian carcinoma xenografts". Neoplasia (New York, N.Y.). ج. 9 ع. 6: 479–86. PMC:1899257. PMID:17603630. مؤرشف من الأصل في 2012-03-11.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Preziosi, Luigi (2003). Cancer Modelling and Simulation. Boca Raton: CRC Press.
- ^ Ganguly R, Puri IK (2006). "Mathematical model for the cancer stem cell hypothesis". Cell proliferation. ج. 39 ع. 1: 3–14. DOI:10.1111/j.1365-2184.2006.00369.x. PMID:16426418.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة) - ^ Ganguly R, Puri IK (2007). "Mathematical model for chemotherapeutic drug efficacy in arresting tumour growth based on the cancer stem cell hypothesis". Cell proliferation. ج. 40 ع. 3: 338–354. DOI:10.1111/j.1365-2184.2007.00434.x. PMID:17531079.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة) - ^ Wang Y, Yang J, Zheng H, Tomasek GJ, Zhang P, McKeever PE, Lee EY, Zhu Y (2009). "Expression of mutant p53 proteins implicates a lineage relationship between neural stem cells and malignant astrocytic glioma in a murine model". Cancer Cell. ج. 15 ع. 6: 514–26. DOI:10.1016/j.ccr.2009.04.001. PMC:2721466. PMID:19477430.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Clarke MF, Dick JE, Dirks PB, Eaves CJ, Jamieson CH, Jones DL, Visvader J, Weissman IL, Wahl GM (2006). "Cancer stem cells--perspectives on current status and future directions: AACR Workshop on cancer stem cells". Cancer research. ج. 66 ع. 19: 9339–44. DOI:10.1158/0008-5472.CAN-06-3126. PMID:16990346.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Cancer stem cells: Invitation to a second round". مؤرشف من الأصل في 2011-09-13.
- ^ "Cell - Identification of Selective Inhibitors of Cancer Stem Cells by High-Throughput Screening". مؤرشف من الأصل في 2013-10-29.
- ^ Haupt Y, Bath ML, Harris AW, Adams JM (1993). "bmi-1 transgene induces lymphomas and collaborates with myc in tumorigenesis". Oncogene. ج. 8 ع. 11: 3161–4. PMID:8414519.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Park IK, Qian D, Kiel M, Becker MW, Pihalja M, Weissman IL, Morrison SJ, Clarke MF (2003). "Bmi-1 is required for maintenance of adult self-renewing haematopoietic stem cells". Nature. ج. 423 ع. 6937: 302–5. DOI:10.1038/nature01587. PMID:12714971.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Molofsky AV, Pardal R, Iwashita T, Park IK, Clarke MF, Morrison SJ (2003). "Bmi-1 dependence distinguishes neural stem cell self-renewal from progenitor proliferation". Nature. ج. 425 ع. 6961: 962–7. DOI:10.1038/nature02060. PMC:2614897. PMID:14574365.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Hemmati HD, Nakano I, Lazareff JA, Masterman-Smith M, Geschwind DH, Bronner-Fraser M, Kornblum HI (2003). "Cancerous stem cells can arise from pediatric brain tumors". Proceedings of the National Academy of Sciences of the United States of America. ج. 100 ع. 25: 15178–83. DOI:10.1073/pnas.2036535100. PMC:299944. PMID:14645703.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Dontu G, Jackson KW, McNicholas E, Kawamura MJ, Abdallah WM, Wicha MS (2004). "Role of Notch signaling in cell-fate determination of human mammary stem/progenitor cells". Breast cancer research : BCR. ج. 6 ع. 6: R605–15. DOI:10.1186/bcr920. PMC:1064073. PMID:15535842.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Diévart A, Beaulieu N, Jolicoeur P (1999). "Involvement of Notch1 in the development of mouse mammary tumors". Oncogene. ج. 18 ع. 44: 5973–81. DOI:10.1038/sj.onc.1202991. PMID:10557086.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Beachy PA, Karhadkar SS, Berman DM (2004). "Tissue repair and stem cell renewal in carcinogenesis". Nature. ج. 432 ع. 7015: 324–31. DOI:10.1038/nature03100. PMID:15549094.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Zhou BP, Hung MC (2005). "Wnt, hedgehog and snail: sister pathways that control by GSK-3beta and beta-Trcp in the regulation of metastasis". Cell cycle (Georgetown, Tex.). ج. 4 ع. 6: 772–6. PMID:15917668. مؤرشف من الأصل في 2020-01-26.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|شهر=تم تجاهله يقترح استخدام|تاريخ=(مساعدة) - ^ She M, Chen X (2009). "Targeting signal pathways active in cancer stem cells to overcome drug resistance". Chin J Lung Cancer. ج. 12: 3–7. DOI:10.3779/j.issn.1009-3419.2009.01.001. مؤرشف من الأصل في 2019-12-14.
- ^ Bollmann FM. The many faces of telomerase: emerging extratelomeric effects. Bioessays. 2008 Aug;30(8):728-32.ببمد: 18623070
مصادر أخرى[عدل]
- Polyak K, Weinberg RA. Transitions between epithelial and mesenchymal states: acquisition of malignant and stem cell traits. Nat Rev Cancer. 2009 Apr;9(4):265-73.ببمد: 19262571
- Sánchez-García I, Vicente-Dueñas C, Cobaleda C. The theoretical basis of cancer-stem-cell-based therapeutics of cancer: can it be put into practice? Bioessays. 2007 Dec;29(12):1269-80.ببمد: 18022789
- Gao JX. Cancer stem cells: the lessons from pre-cancerous stem cells.J Cell Mol Med. 2008 Jan-Feb;12(1):67-96. ببمد: 18053092
- Chen L, Shen R, Ye Y, Pu XA, Liu X, Duan W, Wen J, Zimmerer J, Wang Y, Liu Y, Lasky LC, Heerema NA, Perrotti D, Ozato K, Kuramochi-Miyagawa S, Nakano T, Yates AJ, Carson WE 3rd, Lin H, Barsky SH, Gao JX.Precancerous stem cells have the potential for both benign and malignant differentiation.PLoS One. 2007 Mar 14;2(3):e293.ببمد: 17355942
وصلات خارجية[عدل]
- Cancer Stem Cell News مدونة أخبار عن الخلايا الجذعية السرطانية تهتم بنشر أحدث الأبحاث والمقالات المتاحة مجانًا
- Exploring the role of cancer stem cells in radioresistance جزء مقتطف من مقال كتبه كل من Michael Baumann وMechthild Krause وRichard Hill، في إطار "Nat Rev Cancer" 2008(Jul); 8(7):545-54
- "A Tumor's Lifeblood", Jessica Gorman, CR magazine, Summer 2006
- "Cancer Stem Cell Scientific Literature Review", UMDNJ Stem Cell Research and Regenerative Medicine، June 17, 2006
- "Stem cells may cause some forms of bone cancer", News-Medical.Net، December 7, 2005
- "The Bad Seed: Rare stem cells appear to drive cancers", Science News Online، March 20, 2004
- "The Real Problem in Breast Tumors: Cancer Stem Cells", Genome News Network، March 7, 2003
