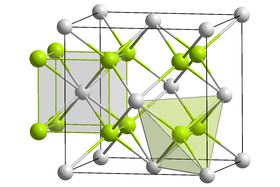
كربيد البيريليوم
| كربيد البيريليوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
Beryllium carbide |
|
| المعرفات | |
| رقم CAS | 506-66-1 |
| بوب كيم (PubChem) | 68173 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | Be2C |
| الكتلة المولية | 30.04 غ/مول |
| المظهر | بلورات صفراء محمرّة |
| الكثافة | 1.9 غ/سم3 عند 20 °س |
| نقطة الانصهار | 2100 °س يتفكك |
| الذوبانية في الماء | يتفكك |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
كربيد البيريليوم مركب كيميائي له الصيغة Be2C، ويكون على شكل بلورات صفراء محمرّة.
التحضير
يمكن تحضير كربيد البيريليوم من التفاعل المباشر للعناصر المكوّنة، وهي الكربون والبيريليوم.[2] عند درجة حرارة تبلغ 900 °س يحدث تفاعل ناشر للحرارة يقوم برفع درجة حرارة المزيج إلى 1400 °س.[3]
كما يمكن تحضير المركب من تفاعل اختزال أكسيد البيريليوم بالفحم عند درجات حرارة مرتفعة.[4]
يمكن في التفاعل الأخير أن يتشكل أحادي أكسيد الكربون كناتج ثانوي عند درجات الحرارة المرتفعة،[5] كما في التفاعل التالي:
الخواص
إن كربيد البيريليوم عبارة عن مادة بلورية صلبة ذات لون أصفر محمر، والتي تتبلور وفق النظام البلّوري المكعّب. عند التماس مع الماء يتفكك المركب بتفاعل حلمهة، ويتشكل هيدروكسيد البيريليوم و غاز الميثان.[4]
بما أن هيدروكسيد البيريليوم من المركبات المذبذبة، فإن التفاعل يتسرّع بوجود هيدروكسيدات قلوية بسبب تشكّل أملاح البيريلات المنحلّة في الوسط.[6]
بالتالي يكون التفاعل الإجمالي:
تتفاعل الهالوجينات مع كربيد البيريليوم عند درجات حرارة مرتفعة، حيث تتشكل الهاليدات الموافقة بالإضافة إلى الكربون، كما هو الحال مع الفلور في التفاعل التالي:
احتياطات الأمان
إن البيريليوم ومركباته الكيميائية هي مواد سامّة ومسرطنة، حيث يمكن أن تسبب مرض التسمم بالبيريليوم. لذا ينبغي أخذ الحيطة والحذر عند التعامل مع هذه المركبات.
المراجع
- ^ أ ب ت Beryllium carbide (بالإنجليزية), QID:Q278487
- ^ Dale L. Perry, Sidney L. Phillips: Handbook of inorganic compounds. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 62 .
- ^ Kenneth A. Walsh: "Beryllium chemistry and Processing", ASM International (2009). p. 117
- ^ أ ب C. L. Parsons: "The Chemistry and Literature of Beryllium", Chemical Publishing (1909), p. 26. النص نسخة محفوظة 05 مارس 2017 على موقع واي باك مشين.
- ^ K. Motzfeld: "Equilibrium of the Reaction between Beryllium Oxide and Carbon to Give Beryllium Carbide" in Acta Chemica Scandinavica 1964, 18, p. 495-503. دُوِي:10.3891/acta.chem.scand.18-0495
- ^ Vorlesungsskriptum: "Chemie der Metalle", Universität Freiburg(بالألمانية) نسخة محفوظة 24 سبتمبر 2017 على موقع واي باك مشين.