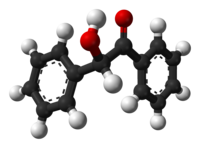
بنزوين
| بنزوين | |
|---|---|
| الاسم النظامي (IUPAC) | |
2-hydroxy-1,2-di(phenyl)ethanone |
|
| أسماء أخرى | |
2-hydroxy-2-phenylacetophenone, 2-hydroxy-1,2-diphenylethanone, desyl alcohol, bitter almond oil camphor |
|
| المعرفات | |
| رقم CAS | 119-53-9 |
| بوب كيم (PubChem) | 8400 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C14H12O2 |
| كتلة مولية | 212.24 غ.مول−1 |
| المظهر | off-white crystals |
| الكثافة | 1.31 g/cm3 |
| نقطة الانصهار | 132–137 °C |
| نقطة الغليان | 344 °C |
| الذوبانية في الماء | Slightly Soluble |
| الذوبانية في كلور | Soluble |
| المخاطر | |
| NFPA 704 |
|
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
البَنْزُوين[1] هو مركب عضوي صيغته الكيميائية PhCH(OH)C(O)Ph وهو كيتون هيدروكسيلي، مرتبط بمجموعتي فينيل. يكون البنزوين على هيئة بلورات ذات لون أبيض فاتح، وله رائحة خفيفة تشبه رائحة الكافور. وينتج البنزوين من البنزلديهيد في تكاثف البنزوين، وهو مركب متماكب ضوئياً ويتواجد على شكل زوجين متخايلين، (R) بنزوين، و(S) بنزوين.
ولا يدخل البنزوين في تكوين الراتينج بنزويني المستخرج من الأشجار البنزوينية (الأصطركيات) حيث أن المادة المكونة لها هي حمض البنزويك.
التاريخ
[عدل]ورد ذكر البنزوين لأول مرة سنة 1832 عن طريق يوستوس فون ليبيغ وفريدرش فولر في أبحاثهما المتعلقة بزيت اللوز المر، وهو بنزلديهيد مع كمية قليلة من حمض الهيدروسيانيك[2] أما الإنتاج المحفز بواسطة تكاثف البنزوين فقد طوره نيكولاي زينين أثناء تواجده مع ليبيغ.[3][4]
الاستخدامات
[عدل]يستخدم البنزوين بشكل اساسي كمادة بادئة لإنتاج البنزل، وهو بادئ ضوئي[5]، وتسير عملية التحول عن طريق التأكسد العضوي باستخدام أيون النحاس الثنائي[6]، أو حمض النتريك، أو الأوكسون. وقد أجري هذا التفاعل في إحدى الدراسات باستخدام الأكسجين الجوي وقاعدة ألومينا في ثنائي كلورو الميثان.[7]
التحضير
[عدل]يحضر البنزوين بواسطة البنزلديهيد بواسطة تكاثف البنزوين.[6]
روابط خارجية
[عدل]Benzoin synthesis, Organic Syntheses, Coll. Vol. 1, p. 94 (1941); Vol. 1, p. 33 (1921)
المراجع
[عدل]- ^ سمير إسماعيل الحلو (1999)، القاموس الجديد للنباتات الطبية: أكثر من 2000 نبات بأسمائها العربية والإنجليزية واللاتينية (بالعربية والإنجليزية واللاتينية) (ط. 1)، جدة: دار المنارة، ص. 63، OCLC:1158805225، QID:Q117357050
- ^ Wöhler, Liebig؛ Liebig (1832). "Untersuchungen über das Radikal der Benzoesäure". Annalen der Pharmacie. ج. 3 ع. 3: 249–282. DOI:10.1002/jlac.18320030302.
- ^ N. Zinin (1839). "Beiträge zur Kenntniss einiger Verbindungen aus der Benzoylreihe". Annalen der Pharmacie. ج. 31 ع. 3: 329–332. DOI:10.1002/jlac.18390310312.
- ^ N. Zinin (1840). "Ueber einige Zersetzungsprodukte des Bittermandelöls". Annalen der Pharmacie. ج. 34 ع. 2: 186–192. DOI:10.1002/jlac.18400340205.
- ^ Hardo Siegel, Manfred Eggersdorfer "Ketones" in Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, 2002 by Wiley-VCH, Wienheim. دُوِي:10.1002/14356007.a15_077
- ^ ا ب Clarke, H. T.; Dreger.E. E.(1941)."Benzil". Org. Synth.; Coll. Vol. 1: 87.
- ^ Konstantinos Skobridis, Vassiliki Theodorou, Edwin Weber (2006). "A very simple and chemoselective air oxidation of benzoins to benzils using alumina". Arkivoc. 06-1798JP: 102–106. مؤرشف من الأصل في 2020-03-26.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)
| في كومنز صور وملفات عن: بنزوين |