حمى الروماتزم: الفرق بين النسختين
| [نسخة منشورة] | [نسخة منشورة] |
ط استرجاع تعديلات 2003:45:4E56:8925:24C6:2FB5:4167:BC9D (نقاش) حتى آخر نسخة بواسطة [[م... وسمان: تحرير من المحمول تعديل ويب محمول |
تطوير محتوى المقال القديم |
||
| سطر 1: | سطر 1: | ||
{{Infobox disease |
{{Infobox disease |
||
| Name = |
| Name = حُمّى الروماتزم |
||
| Image = Streptococcus_pyogenes_01.jpg |
| Image = Streptococcus_pyogenes_01.jpg |
||
| Caption = بكتيريا ''[[Streptococcus pyogenes|السبحية المقيحة]]'' (صبغ بابنهايم) هي المحفز لإحداث حمى الروماتزم. |
| Caption = بكتيريا ''[[Streptococcus pyogenes|السبحية المقيحة]]'' (صبغ بابنهايم) هي المحفز لإحداث حمى الروماتزم. |
||
| سطر 15: | سطر 15: | ||
| eMedicine_mult = {{eMedicine2|med|2922}} {{eMedicine2|emerg|509}} {{eMedicine2|ped|2006}} |
| eMedicine_mult = {{eMedicine2|med|2922}} {{eMedicine2|emerg|509}} {{eMedicine2|ped|2006}} |
||
| MeshID = D012213}} |
| MeshID = D012213}} |
||
'''حمى الروماتيزم'''، أو مايعرف بحمى رماتيزميه حاده، هي مرض التهابي يصيب [[القلب]]، [[المفاصل]]، [[الجلد]]، و[[المخ]].<ref name=Lancet2012/> تبدأ علامات المرض عادة بعد اسبوعين الى اربع اسابيع من التهاب بلعومي.<ref name=Lee2012>{{cite journal|last1=Lee|first1=KY|last2=Rhim|first2=JW|last3=Kang|first3=JH|title=Kawasaki disease: laboratory findings and an immunopathogenesis on the premise of a "protein homeostasis system".|journal=Yonsei medical journal|date=March 2012|volume=53|issue=2|pages=262–75|pmid=22318812|doi=10.3349/ymj.2012.53.2.262}}</ref> ومن اعراضه وعلاماته الحرارة، وألم في عدة مفاصل، وحركات عضلية لا ارادية، وعلامة مميزة الا انها غير شائعة وهي [[طفح جلدي]] غير حاك تسمى حُمامى هامشيّة. يصاب القلب في اكثر من نصف هذه الحالات. تلف دائم لصمامات القلب أو ما يعرف بداء القلب الروماتيزمي يحدث عادة بعد عدة نوبات وقد يحدث التلف في حالات خاصة بعد نوبة حادة واحدة من الحمى الروماتيزمية، ويمكن ان تسبب هذه الصمامات المعطوبة احتشاء في عضلة القلب، وتزيد من خطورة حدوث [[رجفان اذيني]] والتهاب في الصمامات.<ref name=Lancet2012/> |
|||
حمى الروماتيزم الحاده تحدث بعد التهاب بلعومي ببكتبريا تسمى بكتريا عقديه مقيِّحه.<ref name=Lancet2012/> اذا لم يعالج هذا الالتهاب، فإن الحمى الروماتيزميه الحادة تحدث في ٣٪ من الاشخاص.<ref>{{cite book|last1=Ashby|first1=Carol Turkington, Bonnie Lee|title=The encyclopedia of infectious diseases|date=2007|publisher=Facts On File|location=New York|isbn=9780816075072|page=292|edition=3rd|url=https://books.google.ca/books?id=4Xlyaipv3dIC&pg=PA292}}</ref> يُعتَقَد ان المرض يحدث بسبب انتاج اجسام مضادة ضد انسجة جسم المريض نفسه. بعض الناس بسبب جيناتهم معرضين اكثر للاصابه بالمرض عندما يتعرضون لهذه البكتيريا. ومن العوامل الاخرى التي تزيد من خطورة الاصابه بالمرض سوء التغذيه والفقر.<ref name=Lancet2012/> أما تشخيص حمى الروماتيزم فتتضمن وجود الاعراض والعلامات بالاضافه الى دليل على عدوى بالبكتيريا العقديه مؤخرا.<ref>{{cite web|title=Rheumatic Fever 1997 Case Definition|url=http://wwwn.cdc.gov/NNDSS/script/casedef.aspx?CondYrID=823&DatePub=1/1/1997%2012:00:00%20AM|website=cdc.gov|accessdate=19 February 2015|date=3 February 2015}}</ref> |
|||
'''حمى الروماتزم'''<ref>قاموس المورد، البعلبكي، بيروت، لبنان.</ref><ref>المعجم الطبي الموحد</ref> أو '''الحمى الرثوية''' أو '''الحمى الروماتزمية''' [[مرض]] [[التهاب|التهابي]] يحدث بعد اصابة الإنسان ب[[التهاب اللوزتين]] ناتج من [[عدوى بكتيريا مكورة سبحية من المجموعة أ]] |
|||
نتيجة لردة فعل [[جهاز المناعة]] ضد هذه ال[[بكتيريا]] فيبدأ [[الجسم المضاد]] يستهدف [[عضلة القلب]] والمفاصل لوجود تشابه في التركيب بين البكتيريا وهذه الأنسجة.كما تُعرف '''الحمى الروماتيزمية'''' أيضاً بالحمى الروماتيزمية الحادة وهي التهاب يمكن أن يؤثر على القلب و المفاصل و الجلد و الدماغ. يتطور المرض عادةً من اسبوعين إلى أربعة أسابيع بعد الإصابة بالتهاب الحلق. وتتضمن الأعراض الحرارة و الآم المفاصل المتعددة و حركة العضلات اللاإرادية وطفح جلدي غير مألوف مصحوب بحكة ويعرف بإسم حُمامى هامشية. و يؤثر القلب في نصف الحالات بالإضافة إلى تلف مزمن في صمامات القلب ويعرف بإسم مرض القلب الروماتيزمي و ذلك يحدث غالباً بعد الإصابات المتكررة بالحمى الروماتيزمية الحادة و لكن احياناً قد يحدث بعد حالة واحدة. و يؤدي تلف الصمامات إلى فشل القلب. ايضاً تزيد الصمامات غير الطبيعية من خطر اصابة الشخص بالرجفان الأذيني و إصابة الصمامات. وقد تحدث الحمى الروماتيزمية الحادة بعد إصابة الحلق ببكتيريا العقدية المقيحة. تحدث الحمى الروماتيزمية الحادة إذا لم تعالج لتصيب ثلاثة في المئة من الناس. ويُعتقد أن الألية الكامنة تؤثر على انتاج اجسام مضادة لمحاربة أنسجة الشخص نفسه. بعض الناس اكثر عرضةً للإصابة بالمرض عند التعرض للبكتيريا وذلك بسبب جيناتهم الوراثية، و تشمل عوامل الخطر الأخرى سوء التغذية و الفقر أيضاً. و غالباً ما يتم تشخيص الحمى الروماتيزمية الحادة بناءً على ظهور علامات و أعراض في التركيبة مع الأدلة على وجود الإلتهابات العقدية في الآونة الأخيرة. علاج الأشخاص المصابين بالتهاب الحلق بالمضادات الحيوية مثل الأنسولين ليقلل من خطر إصابتهم بالحمى الروماتيزمية الحادة. ويشمل ذلك غالباً فحص الناس المُصابة بالتهاب الحلق الذي قد لا يكون متاحاً في العالم النامي. و تضمن التدابير الوقائية تحسين مرافق الصرف الصحي. في بعض الأحيان ويُنصح الأشخاص المصابين بالحمى الروماتيزمية الحادة و مرض القلب الروماتيزمي بإستخدام المضادات الحيوية لفترات طويلة. العودة التدريجية إلى الأنشطة الطبيعية قد يتبعها نوبة. ويكون العلاج أكثر صعوبة عند تطور مرض القلب الروماتيزمي. كما يتطلب احياناً جراحة استبدال الصمام أواصلاحة. و فيما عدا ذلك يتم علاج المضاعفات وفقاً لطبيعتها. يُصاب حوالي 325 ألف طفل سنوياً بالحمى الروماتيزمية الحادة, أي حوالي 18 مليون نسمة مصابين حالياً بمرض القلب الروماتيزمية. تتراوح أعمار المصابين بالحمى الروماتيزمية الحادة بين 5 سنوات الى 14 سنة, 20% من الهجوم لأول مرة يحدث لدى البالغين. ويعد هذا المرض أكثر شيوعاً في الدول النامية و بين السكان الأصليين في الدول النامية. أدى ذلك الى وفاة 275ألف شخص في عام 2013مُنخفضاً بذلك عن عام 1990 حيث أدى إلى وفاة 374 ألف شخص. كما تحدث أغلب حالات الوفاة في الدول النامية, حيث أن 12.5% من الأشخاص المصابين محتمل موتهم في كل عام. و يُعتقد أن وصف الحالة في كتابات أبقراط يعود تاريخها إلى ما لا يقل عن خمسة قرون قبل الميلاد. سُمي هذا المرض بذلك الاسم لأن أعراضه تتشابه مع تلك الإضطرابات الروماتيزمية. |
|||
معالجة الناس المصابين بالتهاب بلعومي ببكتيريا عقديه بالمضادات الحيويه مثل [[البنسيلين]] تقلل من خطورة الاصابه بالحمى الروماتيزميه.<ref>{{cite journal|last1=Spinks|first1=A|last2=Glasziou|first2=PP|last3=Del Mar|first3=CB|title=Antibiotics for sore throat.|journal=The Cochrane database of systematic reviews|date=5 November 2013|volume=11|pages=CD000023|pmid=24190439|doi=10.1002/14651858.CD000023.pub4}}</ref> يحدث عادة فحص للبكتيريا العقدية في المرضى المصابين بالتهاب الحلق، ويمكن ان لا يتواجد هذا الفحص في الدول النامية، ومن الأساليب الاخرى للوقايه من هذا المرض هو تحسين الصرف الصحي. ينصح في بعض الأحيان لمرضى الحمى الرماتيزميه وداء القلب الروماتيزمي بمدة طويله من العلاج بالمضادات الحيويه. يعود المريض الى ممارسة حياته الطبيعيه تدريجيا بعد نوبة المرض. لكن عندما يتطور المرض الى مرحلة داء القلب الروماتيزمي يصبح العلاج اكثر صعوبة. ويمكن ان يحتاج العلاج الى تصليح او حتى استبدال للصمام. وتعالج المضاعفات وفقا لطبيعتها.<ref name=Lancet2012/> |
|||
يصاب ٣٢٥,٠٠٠ طفل سنويا بالحمى الرماتيزميه، ويوجد حاليا ١٨ مليون شخص مصاب بداء القلب الرماتيزمي. عادة يصاب الاطفال بالحمى الرماتيزميه بين عمر ٥ و ١٤ سنه،<ref name=Lancet2012/> 20% من الحالات تحدث لديهم النوبة الأولى بعد سن البلوغ .<ref name=Robbins>{{Cite book | last1 = Kumar | first1 = Vinay | last2 = Abbas | first2 = Abul K | last3 = Fausto | first3 = Nelson | last4 = Mitchell | first4 = Richard N | year = 2007 | title = Robbins Basic Pathology | edition = 8th | publisher = Saunders Elsevier | pages = 403–6 | isbn = 978-1-4160-2973-1}}</ref> ينتشر المرض غالبا في الدول النامية وبين السكان الاصليين في الدول المتطورة.<ref name=Lancet2012>{{cite journal|last1=Marijon|first1=E|last2=Mirabel|first2=M|last3=Celermajer|first3=DS|last4=Jouven|first4=X|title=Rheumatic heart disease.|journal=Lancet|date=10 March 2012|volume=379|issue=9819|pages=953–64|pmid=22405798|doi=10.1016/S0140-6736(11)61171-9}}</ref> حيث بلغ عدد الوفيات٢7٥,٠٠٠ في سنه ٢٠١٣ مقارنة ب ٣٧٤,٠٠٠ في سنة ١٩٩٠.<ref name=GDB2013>{{cite journal|last1=GBD 2013 Mortality and Causes of Death|first1=Collaborators|title=Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013.|journal=Lancet|date=17 December 2014|pmid=25530442|doi=10.1016/S0140-6736(14)61682-2|volume=385|issue=9963|pages=117–171|pmc=4340604}}</ref> اغلب الوفيات كانت في الدول النامية حيث سجلت نسبة الوفاة ١٢.٥٪ سنويا من المجموع الكلي للمصابين بهذا المرض في هذه الدول.<ref name=Lancet2012/> ويعود تاريخ المرض الى القرن الخامس قبل الميلاد كما تبين في سجلات ابوقراط.<ref>{{cite journal|last1=Quinn|first1=RW|title=Did scarlet fever and rheumatic fever exist in Hippocrates' time?|journal=Reviews of infectious diseases|date=1991|volume=13|issue=6|pages=1243–4|pmid=1775859|doi=10.1093/clinids/13.6.1243}}</ref> وتعود تسميت المرض الى اعراضه التي تتشابه مع اعراض امراض الروماتيزم.<ref>{{DorlandsDict |nine/000956569|rheumatic fever}}</ref> |
|||
== الأعراض == |
|||
== الأعراض والعلامات == |
|||
- تظهر الآعراض عادة بين سن 5-15 سنة |
|||
[[ملف:Pos strep.JPG|تصغير|يسار|حالة مصابة بعقديات الحلق مع نضحات لوزتين في شخص عمره 16 سنه. ]] |
|||
تبدا علامات المرض عادة بعد اسبوعين الى اربع اسابيع من التهاب بلعومي.<ref name=Lee2012/> وتتضمن الاعراض:حرارة، الم في عدة مفاصل و تتغير المفاصل المصابة مع مرور الوقت، حركات عضليه لا اراديه، وعلامة مميزه الا انها غير شائعة وهي طفح جلدي غير حاك تسمى حُمامى هامشيّة. يصاب القلب في اكثر من نصف هذه الحالات. وتسبب تلف دائم ل[[صمامات القلب]]، يعرف ب داء القلب الروماتيزمي، يحدث عادة بعد عدة نوبات، ويمكن ان يحدث في حالات خاصة بعد نوبة حمى روماتيزميه حاده واحده. ويمكن ان تسبب هذه الصمامات المعطوبة احتشاء في [[عضلة القلب]]، وتزيد من خطورة حدوث [[رجفان اذيني]] والتهاب في الصمامات.<ref name=Lancet2012/> |
|||
=== أخرى === |
|||
-التهاب المفاصل وخاصة رسغ القدم والركبتين ورسغا الذراعين والكوعين وتصبح المفاصل المصابة متورمة وساخنة وتسبب الألم للمصاب حينما تلمس أو تحرك. |
|||
* الم في البطن |
|||
* نزيف من الانف |
|||
== الفزيولوجيا المرضيه == |
|||
الحمى الروماتيزميه مرض يصيب جمييع اجهزه الجسم، حيث تصيب الانسجه الضامه المحيطه بالشريان، وتحدث بعد عدوى غير معالجه ببكتيريا عقديه بلعوميه محلله ذاتA بيتا. يُعتقد ان المرض يحدث بسبب اجسام مضاده تفاعليه متصالبه , وهذا النوع من التفاعل هو النوع الثاني من الحساسية المفرطة ويسمى التمويه الجزيئي. عادة تبقى [[الخلايا البائية|الخلايا المناعية البائية]] (B cells) نشطة على السطح دون تحفيزها من قبل [[الخلايا التائية]] (T cells ) . خلال عدوى العقديات, الخلايا الناضجه المظهره للمستضد مثل خلايا B تظهر مولد الضد لخلايا CD4- T التي تتمايز الى خلايا T2 المساعده. خلايا T2 المساعده تحفز خلايا B لتصبح خلايا بلازميه والتي بدورها تنتج اجسام مضاده ضد الجدار الخلوي للعقديات. ولكن الاجسام المضاده يمكن ان تتفاعل ضد بطانه القلب والمفاصل,<ref>{{cite book | last1 = Abbas | first1 = Abul K. | last2 = Lichtman | first2 = Andrew H. | last3 = Baker | first3 = David L. | title = Basic immunology: functions and disorders of the immune system | edition = 2 | publisher = Elsevier Saunders | year = 2004 | location = Philadelphia, Pennsylvania | isbn = 978-1-4160-2403-3|display-authors=etal}}</ref> منتجة اعراض الحمى الروماتيزميه. |
|||
للبكتيريا العقديه المقيحه جدار خلوي مكون من حزم من [[البوليمر]] التي تحتوي على بروتين M والذي يعتبر مستضد للغايه. تعمل الاجسام المضاده الناتجه من جهاز المناعه ضد بروتين M تفاعل مناعي ضد بروتين الليف العضلي القلبي مايوسن،<ref>{{cite journal |vauthors=Faé KC, da Silva DD, Oshiro SE, etal |title=Mimicry in recognition of cardiac myosin peptides by heart-intralesional T cell clones from rheumatic heart disease |journal=J. Immunol. |volume=176 |issue=9 |pages=5662–70 |date=May 2006 |pmid=16622036 |doi= 10.4049/jimmunol.176.9.5662|url=http://www.jimmunol.org/cgi/pmidlookup?view=long&pmid=16622036}}</ref> و غلايكوجين عضلات القلب, وخلايا [[العضلات الملساء]] للشرايين، مما يحفز اطلاق السايتوكاينات وتدمير الانسجه. لكن التفاعل المناعي المتصالب الوحيد المثبت هو مع الانسجه الضامه المحيطه بالاوعيه. هذا الالتهاب يحدث من خلال اتصال مباشر بين الخلايا المتممه و مستقبل Fc مما يحفز استجلاب للنيوتروفيل (العدلات) والخلايا الاكوله. اجسام آشوف المميزه، مكونه من كولاجين ايوزينوفيلي منتفخ محاط بخلايا ليمفيه وخلايا اكوله ويمكن رؤيته باستخدام المجهر الضوئي. من الممكن ان تتحول الخلايا الاكوله الاكبر الى خلايا انتيشو او خلايا آشوف ضخمه. الضرر الصمامي المتسبب من الروماتزم الحاد ممكن ان يتضمن ايضا [[مناعه خلويه]], تتضمن افات الصمام بشكل رئيسي خلايا T المساعده وخلايا اكوله. <ref name=RobbinsPath>{{cite book |author=Cotran, Ramzi S.; Kumar, Vinay; Fausto, Nelson; Nelso Fausto; Robbins, Stanley L.; Abbas, Abul K. |title=Robbins and Cotran pathologic basis of disease |publisher=Elsevier Saunders |location=St. Louis, Mo |year=2005 |pages= |isbn=0-7216-0187-1 |url=http://www.robbinspathology.com/ |oclc= |doi= |accessdate=}}</ref> |
|||
-التهاب القلب الشامل: حدوث التهاب في كل طبقات [[القلب]]، وظهور [[جسم آشوف|أجسام آشوف]]، مما يؤدي إلى التشوه الوظيفي في كل من عضلة القلب وصماماته خصوصا [[صمام تاجي|الصمام التاجي]] و[[صمام أبهري|الصمام الأبهري]] الذي يؤدي لصعوبه في التنفس وزياده ضربات القلب. |
|||
في الحمى الروماتيزميه، هذه الافات يمكن ان تتواجد في اي طبقه من طبقات القلب, ولذلك سميت التهاب القلب الشامل. يمكن ان يسبب الالتهاب ارتشاح مصل فبيريني تاموري توصف بانها تأمور الخبز والزبدة والتي عاده تنتهي دون اي اثار. اشراك بطانه القلب ينتج اجمالا نخر شبه فبريني و تكوين ثآليل على طول خط اغلاق الصمام القلب اليساري. ينتج من الترسيب ثآليل, ولكن ينتج تسميك غير متساوي من الافات التحت الشغاف تسمى لويحات ماكاليوم. |
|||
- طفح جلدي واحمرار |
|||
=== داء القلب الروماتيزمي === |
|||
- وبعض الحركات اللاراديه في اليدين والوجه |
|||
[[ملف:Rheum.heart.disease.jpeg|تصغير|يسار|الفسيولوجيا المرضيه للحمى الروماتيزميه ]] |
|||
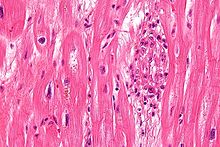
[[ملف:Rheumatic heart disease - 3a - very high mag.jpg|تصغير|يسار|صورة مجهرية لاجسام آشوف (يمين الصوره) كما تكون في حمى القلب الروماتيزمي. صبغة H&E.]] |
|||
داء القلب الروماتيزمي المزمن يتميز بنوبات متكرره من الالتهاب و الترميم الليفي. التغيرات الأساسية التي تحدث للصمامات تتضمن تسميك لشرفات الصمام، التحام في الصواري، وتسميك وتقصير في الاربطه الوتريه.<ref name=RobbinsPath/> تَحدُث نتيجه تفاعل مناعي ذاتي ضد بكتريا عقديه محلله نوع A بيتا تسبب تدمير للصمامات<ref>{{cite journal|pmid=14170842|year=1964|last1=Kaplan|first1=MH|last2=Bolande|first2=R|last3=Rakita|first3=L|last4=Blair|first4=J|title=Presence of Bound Immunoglobulins and Complement in the Myocardium in Acute Rheumatic Fever. Association with Cardiac Failure|volume=271|pages=637–45|doi=10.1056/NEJM196409242711301|journal=The New England Journal of Medicine|issue=13}}</ref> . ينتج من التليف والتندب لشرفات الصمام، الصواري، والشرفات اعاقات تسبب تضيق او قَلَس للصمامات.<ref name="essential">{{cite book|editor-first=Clive|editor-last=Rosendorff|first=Edmund A. W|last=Brice|first2=Patrick J.|last2=Commerford|year=2005|chapter=Rheumatic Fever and Valvular Heart Disease|title=Essential Cardiology: Principles and Practice|location=Totowa, New Jersey|publisher=Humana Press|pages=545–563|isbn=978-1-59259-918-9|doi=10.1007/978-1-59259-918-9_30}}</ref> يطلق على الالتهاب الناتج من الحمى الروماتيزميه – عادة يحدث خلال فتره الطفوله - التهاب الصمام الروماتيزمي. ويكون نصف مرضى الحمى الروماتيزميه مصابين بالتهاب بطانه الصمام. ومعظم نسبة المراضة والوفيات المتعلقة بالحمى الروماتيزمية سببها التدمير الذي تحدثه الحمى الروماتيزميه لانسجة [[صمامات القلب]].<ref name="essential" /> إنّ آلية تطور المرض لداء القلب الروماتيزمي معقده وغير مفهومه بشكل كامل، لكن من المعلوم انها تتضمن التمويه الجزيئي والقابيليه الجينيه التي تؤدي الى تفاعل مناعي ذاتي. |
|||
التمويه الجزيئي يحدث عندما تتشارك الحواتم بين مولد الضد للمُضيف ومولد الضد للبكتيريا.<ref>{{cite journal|pmid=16455580|year=2006|last1=Guilherme|first1=L|last2=Kalil|first2=J|last3=Cunningham|first3=M|title=Molecular mimicry in the autoimmune pathogenesis of rheumatic heart disease|volume=39|issue=1|pages=31–9|doi=10.1080/08916930500484674|journal=Autoimmunity}}</ref> يسبب هذا تفاعل مناعي ذاتي ضد الانسجه الاصليه في القلب التي يتم التعرف عليها بالخطا كاجسام غريبه نتيجه التفاعليه المتصالبه للاجسام المضاده التي تتكون نتيجه الحواتم المشتركه. تكون بطانه الصمامات هي المكان الرئيسي للدمار الناتج من الخلايا الليمفيه. وتعتبر خلاياCD4 T هي الخلايا الرئيسيه المؤثره في داء القلب الروماتيزمي. <ref>{{cite journal|pmid=2786783|year=1989|last1=Kemeny|first1=E|last2=Grieve|first2=T|last3=Marcus|first3=R|last4=Sareli|first4=P|last5=Zabriskie|first5=JB|title=Identification of mononuclear cells and T cell subsets in rheumatic valvulitis|volume=52|issue=2|pages=225–37|journal=Clinical immunology and immunopathology|doi=10.1016/0090-1229(89)90174-8}}</ref> تبدأ عمليه تحفيز خلايا T عاده باظهار مولدات الضد للبكتيريا العقديه A. في داء القلب الروماتيزمي، يسبب التمويه الجزيئي تحفيز غير صحيح لخلايا T والتي بدورها تُحفّز خلايا B التي تبدا بانتاج اجسام مضاده خاصة لمولدات ضد ذاتيه. وهذا ينتج استجابة مناعية ضد انسجة القلب التي تم التعرف عليها على اساس انها اجسام غريبه. تزيد الصمامات الروماتيزميه من استعراض VCAM-1 على سطح الخلية وهو بروتين يساعد على التصاق الخلايا الليمفيه.<ref name="Roberts">{{cite journal|pmid=11133385|year=2001|last1=Roberts|first1=S|last2=Kosanke|first2=S|last3=Terrence Dunn|first3=S|last4=Jankelow|first4=D|last5=Duran|first5=CM|last6=Cunningham|first6=MW|title=Pathogenic mechanisms in rheumatic carditis: Focus on valvular endothelium|volume=183|issue=3|pages=507–11|doi=10.1086/318076|journal=The Journal of infectious diseases}}</ref> وتتم اعاده تنظيم VCAM-1 بعد ارتباطها ببطانه الصمام عن طريق اجسام مضاده خاصة لمولدات ضد ذاتيه ناتجه بسبب التمويه الجزيئي بين بروتينات الشخص ومولدات الضد للبكتيريا العقديه A، وهذا يؤدي الى التهابات وندوبات في الصمام تُلاحظ في التهاب الصمام الروماتيزمي، والتي تحدث عاده بسبب ارتشاح لخلايا T CD4.<ref name="Roberts"/> |
|||
==علامات وأعراض أخرى== |
|||
بينما تبقى القابليه الجينيه غير واضحه، وجدت بعض العوامل الجينيه التي تزيد من القابليه للتفاعل المناعي المتصالب في الحمى الروماتيزميه. اما العامل الرئيسي المساهم هو النوع الثاني من الجزيء MHC ، الموجود على الخلايا الليمفيه والخلايا المقدمه لمولد الضد، خاصه أليل DR, DQ على الكروموسوم البشري ٦.<ref name="Stanevicha">{{cite journal|pmc=333411|year=2003|last1=Stanevicha|first1=V|last2=Eglite|first2=J|last3=Sochnevs|first3=A|last4=Gardovska|first4=D|last5=Zavadska|first5=D|last6=Shantere|first6=R|title=HLA class II associations with rheumatic heart disease among clinically homogeneous patients in children in Latvia|volume=5|issue=6|pages=R340–R346|doi=10.1186/ar1000| journal=[[Arthritis Research & Therapy]] |pmid=14680508}}</ref> ويزيد اتحاد أليلات معينه من التفاعل المناعي المتصالب في داء القلب الروماتيزمي. مستضد الكريات البيضاء البشري النوع الثاني (HLA class II) أليل DR7 (HLA-DR7) غالبا لها ارتباط بداء القلب الروماتيزمي، واتحادها مع أليلات معينه من DQ لها ارتباط ظاهري لنشوء الضرر الصمامي.<ref name="Stanevicha"/> العمليه التي من خلالها تزيد جزيئات MHC- II قابليه المُضيف للتفاعل المناعي التصالبي في الحمى الروماتيزميه غير معروفه، لكن من المحتمل ان لها علاقه بدور جزيء HLA في تقدمة مولد الضد لمستقبلات خلايا T، وهذا يحفز العمليه المناعيه. ووجد ايضا على كروموسوم رقم ٦ سايتوكاين TNF-a الذي له علاقه بداء القلب الروماتيزمي.<ref name="Stanevicha"/> ويفاقم الظهورعالي المستوى ل TNF-a من التهاب الانسجه الصماميه وهذا يساهم في تطور داء القلب الروماتيزمي. مانوز بايندينغ ليكتين MBL هو بروتين التهابي يستخدم في التعرف على مسبب المرض. وتوجد مغايرات مختلفه من مواقع جين MBL2 على الحمض النووي لها علاقه بداء القلب الروماتيزمي. فالتضيق في الصمام التاجي الناتج من داء القلب الروماتيزمي له ارتباط ب MBL2 أليل التي تنسخ كميات كبيره من MBL.<ref>{{cite journal|pmid=18602696|year=2008|last1=Schafranski|first1=MD|last2=Pereira Ferrari|first2=L|last3=Scherner|first3=D|last4=Torres|first4=R|last5=Jensenius|first5=JC|last6=De Messias-Reason|first6=IJ|title=High-producing MBL2 genotypes increase the risk of acute and chronic carditis in patients with history of rheumatic fever|volume=45|issue=14|pages=3827–31|doi=10.1016/j.molimm.2008.05.013|journal=Molecular immunology}}</ref> اما القَلَس في الصمام الابهري في مرضى داء القلب الروماتيزمي له ارتباط ب MBL2 أليل التي تنسخ كميات قليله من MBL.<ref>{{cite journal|pmc=2446618|year=2008|last1=Ramasawmy|first1=R|last2=Spina|first2=GS|last3=Fae|first3=KC|last4=Pereira|first4=AC|last5=Nisihara|first5=R|last6=Messias Reason|first6=IJ|last7=Grinberg|first7=M|last8=Tarasoutchi|first8=F|last9=Kalil|first9=J|title=Association of Mannose-Binding Lectin Gene Polymorphism but Not of Mannose-Binding Serine Protease 2 with Chronic Severe Aortic Regurgitation of Rheumatic Etiology|volume=15|issue=6|pages=932–936|doi=10.1128/CVI.00324-07|journal=Clinical and Vaccine Immunology : CVI|last10=Guilherme|first10=L.|pmid=18400978}}</ref> وتم فحص جينات اخرى لفهم اكثر لتعقيدات التفاعليات المناعيه المتصالبه في داء القلب الروماتيزمي. |
|||
* ألم في البطن |
|||
== التشخيص == |
|||
* نزيف الأنف |
|||
[[ملف:Rheumatic_heart_disease%2C_gross_pathology_20G0013_lores.jpg|تصغير|يسار|حمى الروماتيزم في جثه مشرحة مع خصائص مميزه (تسميك للصمام التاجي و تسميك الحبال الوتريه القلبيه و تضخيم بطانه البطين الايسر). ]] |
|||
* يسبق الإصابة العقدية : الحمى القرمزية، ارتفاع antistreptolysin 0 أو غيرها من الأضداد العقدية، أو الزرع الإيجابي للبلعوم. |
|||
نُشِرَ مقياس جونز المعدل لاول مره في عام ١٩٤٤ بواسطه ت. دوكيت جونز،(دكتور في الطب MD ) .<ref>{{cite journal | last = Jones | first = T Duckett |title=The diagnosis of rheumatic fever |journal=[[Journal of the American Medical Association|JAMA]] |volume=126 |issue= 8|pages=481–4 |year= 1944 | doi= 10.1001/jama.1944.02850430015005}}</ref> وكان يراجع دوريا من خلال جمعيه القلب الامريكيه بالتعاون مع مجموعات اخرى.<ref>{{cite journal | last =Ferrieri | first = P |title=Proceedings of the Jones Criteria workshop | journal = Circulation | volume=106 |issue=19 |pages=2521–3 |year=2002 |pmid=12417554 |doi = 10.1161/01.CIR.0000037745.65929.FA |url=http://circ.ahajournals.org/cgi/content/full/106/19/2521?ck=nck | publisher =Jones Criteria Working Group | last2 =Jones Criteria Working | first2 =Group}}</ref> واعتمادا على مقياس جونز المعدل، يتم تشخيص الحمى الروماتيزمية من خلال وجود اثنتين من المعايير الرئيسية، او معيار رئيسي واحد ومعيارين ثانويين، مع وجود دليل على التهاب ببكتيريا عقدية: من خلال ارتفاع معيار ضد الحالّة العِقْدِيّة O او انزيم DNAase.<ref name =Robbins/> يستثنى من ذلك رقص سيدنهام والتهاب القلب الخامل، حيث تعتبر كل واحده منهن بنفسها اشاره الى الحمى الروماتيزميه.<ref>{{cite web |url= http://www.emedicine.com/emerg/topic509.htm | work = eMedicine | title = Rheumatic Fever | first = Steven J | last = Parrillo | publisher = DO, FACOEP, FACEP | accessdate =14 July 2007}}</ref><ref>{{cite journal | title= Guidelines for the diagnosis of rheumatic fever. Jones Criteria, 1992 update | publisher = Special Writing Group of the Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease of the Council on Cardiovascular Disease in the Young of the American Heart Association |journal=JAMA |volume=268 |issue=15 |pages= 2069–73 | year = 1992 |pmid=1404745 |doi = 10.1001/jama.268.15.2069}}</ref><ref>{{cite journal|first=Anita|last= Saxena | title =Diagnosis of rheumatic fever: Current status of Jones criteria and role of echocardiography|journal = Indian Journal of Pediatrics | volume =67|issue=4|pages=283–6|year=2000|pmid=11129913|doi= 10.1007/BF02758174}}</ref> نشرت مقاله في ابريل ٢٠١٣ في الجريدة الهنديه للابحاث الطبية صرحت ان ابحاث مخطط صدى القلب و دوبلر E,D، رغم وجود تحفظات على منافعهم, ساهمت بشكل كبير في تشخيص مرض داء القلب الروماتيزمي، مما يرجح عدم كفايه مقياس جونز ١٩٩٢. وشخصت ابحاث E,D التهابا للقلب مصابين بحمى الروماتيزم الحادة ، وبالمثل عند متابعه مرضى [[حمى الروماتزم|حمى الروماتيزم]] ممن اتوا في البدايه برقص سيدنهام وحدها.<ref>{{cite journal|pmc=3724245|year=2013|last1=Kumar|first1=RK|last2=Tandon|first2=R|title=Rheumatic fever & rheumatic heart disease: The last 50 years|volume=137|issue=4|pages=643–658|journal=The Indian Journal of Medical Research|pmid=23703332}}</ref> |
|||
<ref>\^ a b Ed Boon, Davidson's General Practice of Medicine, 20th edition. P. 617. |
|||
ومن العلامات السابقه لعدوى العقديات: [[حمى قرمزية]] مؤخرا، ارتفاع عيار مستضد الحاله العقديه O او عيار اجسام مضاده ضد عقديه اخرى، او موجبية زراعه الحلق.<ref name="davidson617"/> |
|||
</ref> |
|||
يتطور المرض عادةً من اسبوعين إلى أربعة أسابيع بعد الإصابة بالتهاب الحلق. وتتضمن الأعراض الحرارة و الآم المفاصل المتعددة و حركة العضلات اللاإرادية وطفح جلدي غير مألوف مصحوب بحكة ويعرف بإسم حُمامى هامشية. و يؤثر القلب في نصف الحالات بالإضافة إلى تلف مزمن في صمامات القلب ويعرف بإسم مرض القلب الروماتيزمي و ذلك يحدث غالباً بعد الإصابات المتكررة بالحمى الروماتيزمية الحادة و لكن احياناً قد يحدث بعد حالة واحدة. و يؤدي تلف الصمامات إلى فشل القلب. ايضاً تزيد الصمامات غير الطبيعية من خطر اصابة الشخص بالرجفان الأذيني و إصابة الصمامات. |
|||
=== المعايير الرئيسية === |
|||
''''''أمراض القلب الروماتيزمي:'''''' |
|||
* [[التهاب المفاصل]]: التهاب مؤقت متنقل في المفاصل الكبرى، عاده يبدا في الساق وينتقل الى الاعلى. |
|||
* [[التهاب القلب]]: التهاب في [[عضلة القلب]] ( myocarditis) تظهر ك[[فشل القلب الاحتقاني]] مع ضيق في التنفس، او التهاب غلاف القلب مع احتكاك، او نفخه قلبيه جديده. |
|||
* عقيدات تحت جلديه: تجاميع صلبةغير مؤلمة من الالياف فوق العظام او الاربطه. عاده تظهر خلف الرسغ، خارج الكوع، و على مقدمة الركبه. |
|||
* حمامى هامشيه: طفح جلدي محمر طويل المدى يبدا في الجذع او الذراع على شكل بقع، تنتشر الى الخارج وتُمسح من الداخل لتشكل حلقه، تستمر بالانتشار لتتحد مع حلقات اخرى، لتكون شكل حيه، تنتشر إلى الوجه وتسوء مع الحراره. |
|||
* رقص سيدنهام: سلسله من الحركات السريعه المميزه لا يتأثر بها الوجه والذراعين. تحدث في اخر اوقات المرض على الاقل ثلاث اشهر من بدايه العدوى. |
|||
=== المعايير الثانوية === |
|||
تتميز أمراض القلب الروماتيزمي المزمن بالإلتهاب المتكرر الليفيني، وتشمل الكاردينال التشريحية التغييرات في سماكة نشرة الصمام و ذوبان الصواري و سماكة الحبال الوترية و تقصيرها . و هو ناتج عن ردة فعل المناعة الذاتية اتجاه العقديات الإنحلالية للمجموعة A-B و التي ينتج عنها ضرر الصمامات , كما يؤدي تلف وجرح نشرات الصمام و انقاط الالتقاء و تداخل الشرفات إلى تشوهات يمكن أن تؤدي إلى ضيق الصمام أو ارتجاعه، فالإلتهابات الناجمة عن مرض الحمى الروماتيزمية عادةً ما تكون خلال مرحلة الطفولة و يشار إليها بالتهاب الصمام الروماتيزمي، فحوالي نصف المرضى المصابين بالحمى الروماتيزمية الحادة قد تتطور حالاتهم إلى التهاب البطانة التي تبطن الصمامات، فتسبب الحمى الروماتيزمية معظم الأمراض و الوفيات كما أن لها آثار مدمرة على نسيج صمام القلب.و أسباب أمراض القلب الروماتيزمية معقدة و غير واضحة تماماً، و لكن من المعروف أن المحاكاة الجزيئية والوراثية قد تؤدي إلى ردات فعل المناعية الذاتية، فتحدث المحاكاة الجزيئية عندما يتم تقاسم الحواتم بين مُستضدات المضيف و مستضدات GAS، وهذا يسبب ردة فعل مناعية ذاتية مضادة لأنسجة القلب، وبسبب التفاعل المتبادل للأجسام المضادة الناتجة من التقاسم الحاتمة فتُعرّف بشكل خاطىء بأنها "خارجية"، فموقع البطانة الصمامية معروف بتضمنه للأضرار الناتجة من اللمفاويات، وتعتبر الخلايا التائية CD4+ من أهم الخلايا المسببة لرد الفعل المناعي الذاتي لأنسجة القلب في مرض القلب الروماتيزمي، وعادةً ما يتم تنشيط الخلايا التائية بواسطة عرض مستضدات GAS، فنتائج المحاكاة الجزئية غير صحيحة في تنشيط الخلايا التائية، كما يمكن للخلايا التائية الليمفاوية تنشيط الخلايا البيضاء في الدم والتي ستبدأ في انتاج الأجسام المضادة الذاتية في مرض القلب الروماتيزمي، وهذا يجعل ردة الفعل المناعية تشن هجوماً ضد الأنسجة في القلب و التي تخطأ في التعرف عليها كالأسباب المرضية، وتستخرج الصمامات الروماتيزمية السوائل المتزايدة من VCAM-1، كما يعد البروتين أداة للإلتصاق بالخلايا اللمفاوية، وتتولد الأجسام المضادة الذاتية بالمحاكاة الجزيئية بين بروتينات الإنسان و مستضدات GAS لتنضيم VCAM-1 بعد ربط البطانة الصمامية، وهذا يؤدي إلى التهاب و ندب في الصمامات و يُلاحظ ذلك في التهاب الصمام الروماتيزمي , كما يرجع ذلك أساساً إلى خلية التسلل CD4+T. و قد تم العثور على عدد قليل من العوامل الوراثية لزيادة حساسية ردود فعل المناعة الذاتية في مرض القلب الروماتيزمي في حين أن الآليات الوراثية لا تزال غير واضحة، وتتكون الطبقة الثانية من الجزيئات MHC و هي من المكونات المساهمة والمهيمنة و توجد في الخلايا الليمفاوية و الخلايا العارضة للمستضد و تحديداً في الأليلات DR و DQ على الكروموسوم البشري السادس وتظهر مجموعات معينة من الأليل لزيادة حساسية المناعة الذاتية في مرض القلب الروماتيزمي, و مضاد الكريات البيضاء البشرية HLA من الدرجة الثانية للأليل DR7 , و غالباً ما يكون HLA-DR7 مرتبط مع مرض القلب الروماتيزمي, و على ما يبدو أن الجمع بينها و بين بعض الأليلات DQ يرتبط مع تطور الضرر الصمامي. فآلية الجزيئات من الدرجة الثانية MHC لزيادة حساسية العائل لردود المناعة الذاتية في مرض القلب الروماتاتيزمي غير معروفة, و لكن من المُرجح أن ترتبط بالدور الذي تلعبه جزيئات HLA في تقديم المستضدات لمستقبلات الخلايا التائية مما يثير رد الفعل المناعي. كما عُثر على الكروموسوم البشري السادس الخلوي TNF-α و الذي يرتبط أيضاً مع مرض القلب الروماتيزمي. فقد تتفاقم المستويات العالية من TNF-α التهاب الأنسجة الصمامي, و تُساهم في إنشاء مرض القلب الروماتيزمي. كتين ملزم المانوز MBL هو بروتين التهابي يساهم في التعرف على العوامل المُسببة للأمراض. و ترتبط الأنواع المختلفة من مناطق الجينات MBL2 في مرض القلب الروماتيزمي. |
|||
* حراره ٣٨.٢-٣٨.٩ س ( 100,8 – 102,0 ف ) |
|||
فمرض القلب الروماتيزمي ناجم عن ضيق الصمام التاجي و الذي يرتبط بترميز أليلات MBL2 لإنتاج عالي من MBL. فقلس الصمام الأبهري لدى المرضى المصابين بمرض القلب الروماتيزمي مرتبط بأليلات MBL2 المختلفة التي تتحول لإنتاج منخفض من MBL .كما يجري التحقيق في الجينات الأخرى لفهم تعقيدات ردود الفعل المناعة الذاتية التي تحدث في مرض القلب الروماتيزمي. و تم نشر تعديل معايير جونز لأول مرة في عام 1944 من قبل T. Duckett جونز، MD.و تم تنقيحها بشكل دوري بواسطة جمعية القلب الأمريكية و ذلك بالتعاون مع مجموعات أخرى. |
|||
* الم [[مفاصل]]: الم في المفاصل بدون انتفاخ ( لا يتم احتسابها اذا كان التهاب المفاصل المتعدد موجود من ضمن المعايير الرئيسية) |
|||
* ارتفاع سرعه تثفل [[كريات الدم الحمر]] او البروتين المتفاعل C |
|||
* ارتفاع الكريات البيض |
|||
* خصائص مميزه في [[تخطيط القلب]] تشير لتوقف القلب، مثل استطوال فتره PR<ref name="davidson617">Ed Boon, Davidson's General Practice of Medicine, 20th edition. P. 617.</ref><ref>{{cite web | url = http://www.utmb.edu/pedi_ed/CORE/Cardiology/page_40.htm | title = Rheumatic Fever | accessdate = 6 August 2011 | last = Aly | first = Ashraf | year = 2008 | work = Core Concepts of Pediatrics | publisher = University of Texas}}</ref> ( لا تحتسب اذا كان التهاب القلب من ضمن المعايير الرئيسية) |
|||
* نوبات قديمه من الحمى الروماتيزميه او مرض قلبي خامل |
|||
حمى الروماتيزم في جثه مشرحة مع خصائص مميزه (تسميك للصمام التاجي و تسميك الحبال الوتريه القلبيه و تضخيم بطانه البطين الايسر). |
|||
== الوقاية == |
|||
''''''التشخيص:'''''' |
|||
الوقايه من تكرار المرض يتم من خلال استئصال العدوى الحاده واعطاء مضادات حيويه وقائيه. تقترح جمعيه القلب الامريكيه المحافظه على صحة الاسنان، واعطاء [[مضادات حيوية|مضادات حيويه]] وقائيه على المدى البعيد للاشخاص المعروفين بالتهاب الشغاف الجرثومي، او زراعه قلب، او لديهم صمام قلب صناعي، او انواع من عيوب قلبيه خلقيه.<ref name="aha">{{cite web|title=What About My Child and Rheumatic Fever?|url=http://www.heart.org/idc/groups/heart-public/@wcm/@hcm/documents/downloadable/ucm_300321.pdf|publisher=American Heart Association|accessdate=23 February 2014|format=PDF}}</ref> |
|||
ووفقا لمعايير جونز المنقحة يمكن أن يتم تشخيص الحمى الروماتيزمية عندما يتواجد معيارين رئيسيين، أو معيار رئيسي بالإضافة إلى وجود معيارين صغيرين فرعيين جنبا إلى جنب مع دليل الإصابة بعدوى بالبكتيريا العنقودية: ارتفاع الحالة العقدية عيار صفر أو الحمض النووي،و الإستثناءات هي الرقاص (مرض عصبي ) و تراخي القلب، وكل منها يمكن أن يشير إلى الحمى الروماتيزمية. ففي أبريل عام 2013 عند مراجعة المقالة في المجلة الهندية للأبحاث الطبية ذُكر أن تخطيط صدى القلب و دراسة ودوبلر (E & D)، و بالرغم من بعض التحفظات حول فائدتها، إلا أنها اظهرت العبء الهائل لأمراض القلب الروماتيزمية، و ذلك يشير إلى عدم كفاية معايير جونز 1992. و قد أظهرت دراسات (E & D) أن التهاب القلب السريري للمرضى المصابون بالحمى الروماتيزمية الحادة و المتابعة للمرضى الذين يعانون من أمراض القلب الروماتيزمي قد يعرض في البداية على أنها حالات وحيدة من مرض رقاص سيدنهام. و تشمل علامات وجود عدوى بالبكتيريا العقدية السابقة: الحمى القرمزية الجديدة أو رفع الحالة العقدية أو الأجسام المضادة لعيار العقدية أو ضيق الحنجرة . |
|||
[[ملف:Pos strep.JPG|تصغير|يسار|حالة التهاب في الحلق لطفل يبلغ من العمر 16 عاماً]] |
|||
''''''المعايير الرئيسية:'''''' |
|||
-'''''التهاب المفاصل:''''' هو التهاب مؤقت , متنقل من المفاصل الكبيرة، وعادة ما يبدأ في الساقين و ينتقل للأعلى. |
|||
-'''''التهاب القلب:''''' هو التهاب عضلة القلب و يمكن أن يعبر عنها بفشل القلب الاحتقاني مع ضيق في التنفس و التهاب التامور مع الاحتكاك أو نفخة قلبية جديدة. |
|||
-'''''العقيدات تحت الجلد:''''' هو ألم و مجموعات ثابتة من ألياف الكولاجين التي تكسو العظام أو الأوتار، و تظهر عادةً في الجزء الخلفي من المعصم و الكوع الخارجي والجزء الأمامي من الركبة. |
|||
-'''''حمامى هامشية:'''''هو طفح جلدي محمر طويل الأمد و يبدأ على الجذع والذراعين كبقع، وينتشر هذا الطفح بشكل واضح في الوسط على شكل حلقات تستمر في الإنتشار والإلتحام مع الحلقات الأخرى لتصبح في نهاية المطاف كمظهر الثعابين. و ينتشر هذا الطفح عادةٌ على الوجه و يسوء مع الحرارة. |
|||
-'''''مرض رقاص سيدنهام (رقص سانت فيتوس):''''' هي سلسلة من الحركات السريعة دون قصد تحدث في الوجه و الذراع. و يمكن حدوثة في وقت متأخر جداً من هذا المرض و بعد مدة ثلاثة أشهر على الأقل من بداية العدوى. |
|||
''''''المعايير الصغرى:'''''' |
|||
-'''''الحمى''''' (٣٨،٢ - ٣٨،٩ درجة مئوية) |
|||
-'''''ألم مفصلي:''''' و هو ألم المفاصل من دون تورم (لا يمكن إدراجه ضمن التهاب المفاصل الموجود كسبب رئيسي) |
|||
-'''''ارتفاع معدل الترسيب أو البروتين المتفاعل C.''''' |
|||
-'''''زيادة عدد كريات الدم البيضاء.''''' |
|||
-'''''تظهر ملامح احصار القلب''''' من خلال التخطيط الكهربائي للقلب مثل مرحلة PR لفترة طويلة |
|||
(لا يمكن إدراجه ضمن التهاب المفاصل الموجود كسبب رئيسي) |
|||
-'''''المرحلة السابقة من الحمى الروماتيزمية و مرض القلب النشط.''''' |
|||
''''''الوقاية:'''''' |
|||
يتحقيق منع رجوع ظهور المرض مرةً أخرى عن طريق القضاء على العدوى الحادة والوقاية بالمضادات الحيوية. فتقترح جمعية القلب الأمريكية المحافظة على صحة الأسنان . و الأشخاص الذين لديهم تاريخ عائلي في الإصابة بالتهاب الشغاف البكتيري أو زراعة القلب أو صمامات القلب الاصطناعية، أو "بعض أنواع العيوب الخلقية في القلب" قد يرغبون في الوقاية طويلة الأمد عن طريق استخدام المضادات الحيوية. |
|||
== العلاج == |
== العلاج == |
||
ان معالجه الحمى الرروماتيزميه تتجه نحو تقليل الالتهاب بعلاجات ضد الالتهاب مثل اسبيرين او كورتيكوستيرويد. والاشخاص الذين أثبتت الزراعة إصابتهم بعقديات الحلق يجب معالجتهم بالمضادات الحيويه. يعتبر الاسبيرين هو الدواء الافضل ويجب ان يعطى في جرعات عاليه ١٠٠مغ/كغ/يوم. يجب متابعه الاعراض الجانبيه مثل التهاب المعده، وتسمم بالساليسايلات. في الاطفال والمراهقين استخدام الاسبيرين والمنتجات المحتويه على الاسبيرين لها علاقة بمتلازمة ريز، وهي حاله خطرة ومميته .يجب ان يوضع بالحسبان الاخطار، والفوائد، والعلاجات البديله عند استخدام الاسبيرين والمنتجات المحتويه على الاسبيرين في الاطفال والمراهقين. يستخدم [[الايبوبروفين]] للالم وعدم الارتياح والكورتيكوستيرويد للالتهابات المتوسطه والشديده في الحمى الروماتيزميه للاطفال والمراهقين. اما استخدام الستيرويد فيبقى للحالات التي يوجد فيها دليل على اصابه القلب. استخدام الستيرويد يمكن ان يمنع الندوبات المستقبليه للانسجه ويمكن ان يمنع حدوث مضاعفات مثل [[التضيق التاجي]]. وتعطى حقنه شهريا من بينسلسن طويل المدى لمده خمس سنوات لمرضى تعرضو لنوبه واحده من الحمى الروماتيزميه. اما اذا كان هناك دليل على التهاب القلب، فان مدة العلاج قد تطول ل٤٠ سنه ومن الاساسيات للعلاج في الحمى الروماتيزميه استمراريه استخدام مضادات حيويه بجرعات قليله ( مثل [[البنسلين]]، سلفاديازين، ايريثرومايسين) لمنع حدوث التكرار. |
|||
=== التطعيم === |
|||
في عام 1876 تم اكتشاف الآثار المفيدة لدواء الصفصافين (salicin) الذي يستخرج من شجرة الصفصاف بصورة خلات الصفصافيك Acetylsalicylic Acid ويعتبر [[الأسبرين]] أيضا من أكبر الأدوية أثرا لعلاج أعراض الحمى الرثوية كالحرارة والانتفاخات الجلدية والالتهابات المفاصل. |
|||
حاليا لا يوجد مطعوم للبكتيريا العقديه المقيحه، ولكن يوجد ابحاث لتطوير هذا المطعوم. تتضمن الصعوبات في ايجاد مطعوم الانواع المختلفه من البكتيريا العقديه المقيحه في الطبيعه وضروره وجود عدد كبير من الناس ووقت كثير لمحاولات صناعته بامان وكفاءه عاليه.<ref>{{cite web|title=Initiative for Vaccine Research (IVR) - Group A Streptococcus|url=http://www.who.int/vaccine_research/diseases/soa_bacterial/en/index3.html|publisher=World Health Organization|accessdate=15 June 2012}}</ref> |
|||
و يعطى المريض [[كورتيزون|الكورتيزون]] أحياناً أيضا في محاولة لتقليل التغيرات الالتهابية في القلب وبهذا يقل الدمار الذي يحدث للصمامات القلبية. |
|||
- التقليل من الملح في الغذاء |
|||
- الراحة التامة |
|||
لإدارة الحمى الروماتيزمية يجب الحد من الإلتهاب و ذلك باستخدام مضاد الإلتهابات مثل الأسبرين وكورتيكوستيرويد. و يجب علاج بكتيريا الحلق بالمضادات الحيوية. فالأسبرين هو الدواء الأفضل ويجب أن يُعطى على جرعات عالية من 100 ملغ / كغ / يومياً. كما ينبغي على الفرد ملاحظة الآثار الجانبية مثل تسمم المعدة و الساليسيلات. و يستخدم الأطفال والمراهقين الأسبرين والمنتجات المحتوية على الأسبرين التي يمكن أن تترافق مع متلازمة راي وهي حالة خطيرة ومميتة. |
|||
فيجب النظر دائما في مخاطرالأسبرين والمنتجات المحتوية على الأسبرين وفوائده والعلاجات البديلة له عند إعطائه الأطفال والمراهقين، كما ينبغي استخدام الإيبوبروفين لتخفيف الألم والإنزعاج والستيروئيدات القشرية و ذلك لتعديل التفاعلات الإلتهابية الحادة التي تظهرها الحمى الروماتيزمية لدى الأطفال والمراهقين. و يُحفظ الأسترويد للحالات التي يوجد فيها دليل على إكتناف القلب، ويتم استخدام المنشطات التي تمنع من ازدياد تندب الأنسجة و تمنع من تطوير العقابيل مثل تضيق الصمام التاجي، فيجب أن يعطى المرضى الذين يعانون من نوبة واحدة من الحمى الروماتيزمية حقن شهرية من البنسلين طويلة المفعول لمدة خمس سنوات، وقد تطول مدة العلاج إلى 40 سنة إذا كان هناك دليل على الإصابة بالتهاب القلب. ويشمل آخر جزء مهم في علاج الحمى الروماتيزمية استخدام جرعة منخفضة من المضادات الحيوية (مثل البنسلين، سلفاديازين، أو الاريثروميسين) و ذلك لمنع تكرار حدوثها. |
|||
== الوقاية == |
|||
يتضمن العلاج آخذ جرعات من [[البنسلين]] لمده خمسة سنوات أو لغاية سن 21 سنة. |
|||
'''اللقاح:''' |
|||
إلى الآن لم تتوفر أي لقاحات للحماية من الإصابة المقيحة بالرغم من انه كانت تجرى بحوث لصنع لقاح لهذا المرض .وتكمن صعوبة عمل اللقاح في المجموعات الكبيرة لسلالات S المقيحة الموجودة في البيئة و كما تحتاج التجارب المناسبة للسلامة وفاعلية اللقاح إلى الكثير من الوقت وأعداد كبيرة من الناس. |
|||
''''''العدوى:'''''' |
|||
ثقافة الناس الإيجابية يجب أن تعالج العقدية المُقيحة يالبنسلين طالما أن الحساسية غير موجودة. |
|||
و لن يغير هذا العلاج مسار المرض المزمن. فببنزاثين بنزيل بنسلين هو العلاج الأنسب للحمى الروماتيزمية السريري الذي جاء في دليل أكسفورد للطب . |
|||
''''''الإلتهاب:'''''' |
|||
غالباً ما تُستخدم الستيروئيدات القشرية لدعم هذا النقص كما أن الساليسيلات مخففة للألم. |
|||
=== العدوى === |
|||
''''''فشل القلب:'''''' |
|||
الاشخاص موجبيي الزراعه للعقديات المقيحه يجب علاجهم بالبنسلين مادامت الحساسيه للدواء غير موجوده. هذا العلاج لن يغير مسار المرض الحاد. ان افضل العلاجات الموجوده في كتب اوكسفورد (Oxford Handbook of Clinical Medicine) للحمى الروماتيزميه هو بينزاثين بينزيل بينيسلين. |
|||
=== الالتهاب === |
|||
يعاني بعض المرضى من التهاب القلب الذي يظهر كفشل القلب الاحتقاني، ويتطلب العلاج المعتاد لفشل القلب: مثبطات ACE و مدرات البول و حاصرات بيتا والديجوكسين، فعلى عكس فشل القلب الطبيعي يستجيب فشل القلب الروماتيزمية جيداً للالقشرية. |
|||
يستخدم عاده الكورتيكوستيرويد، ولكن لا يوجد دليل قوي لاثبات ذلك. <ref name=Lancet2012/> ويستخدم الساليساليت لتخفيف الالم. |
|||
=== فشل القلب === |
|||
بعض الاشخاص يصابون بالتهاب قلبي قوي تظهر اعراضه على شكل فشل قلب احتقاني. وهذا يحتاج الى الادويه المستخدمه عاده في [[فشل القلب]]: مثبطات ACE، [[مدر بول|مدرات بول]]، مُحْصِر بيتا، ديجوكسين. على العكس من فشل القلب العادي، فان فشل القلب الروماتيزمي يستجيب جيدا للكورتيكوستيرويد. |
|||
== الاوبئه == |
|||
''''''علم الأوبئة:'''''' |
|||
[[ملف:Rheumatic heart disease world map - DALY - WHO2004.svg|تصغير|يسار|العمر بالسنوات مصحح باحتساب مدد العجز لحمى القلب الروماتيزمي لكل 100.000 مواطن في 2004. <ref>{{cite web |url= http://www.who.int/healthinfo/global_burden_disease/estimates_country/en/ | title = WHO Disease and injury country estimates | year= 2009 | work = World Health Organization |accessdate=11 November 2009}}</ref>]] |
|||
حمى الروماتيزم منتشره عالميا ومسؤوله عن حالات كثيره لدمار [[صمامات القلب]].كان عدد الوفيات عالميا في ٢٠١٠ بسببها ٣٤٥.٠٠٠ مقارنه ب ٤٦٣.٠٠٠ في عام١٩٩٠.<ref name=Loz2012>{{cite journal|last=Lozano|first=R|title=Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010|journal=Lancet|date=15 December 2012|volume=380|issue=9859|pages=2095–128|pmid=23245604|doi=10.1016/S0140-6736(12)61728-0|last2=Naghavi|first2=M|last3=Foreman|first3=K|last4=Lim|first4=S|last5=Shibuya|first5=K|last6=Aboyans|first6=V|last7=Abraham|first7=J|last8=Adair|first8=T|last9=Aggarwal|first9=R|first10=Stephanie Y|first11=Mohammad A|first12=Miriam|first13=H Ross|first14=Laurie M|first15=Kathryn G|first16=Charles|first17=Larry M|first18=Suzanne|first19=David H|first20=Michelle L|first21=Emelia J|first22=Derrick|first23=Kavi|first24=Boris|first25=Aref Bin|first26=Gretchen|first27=Fiona|first28=Ian|first29=Soufiane|first30=Chiara}}</ref> |
|||
في الدول الغربيه، اصبحت نادره منذ ستينيات القرن العشرين، ربما نتيجه انتشار استخدام المضادات الحيويه لمعالجه عدوى العقديات. بينما اصبحت اقل بكثير في الولايات المتحده منذ بداية القرن العشرين و لكان هناك عدة حالات تفشي للمرض منذ ١٩٨٠.على الرغم من ان المرض يحدث نادرا، الا انه مرض خطير وله نسبه وفيات من ٢-٥٪.<ref>{{Cite journal | url = http://www.nlm.nih.gov/medlineplus/ency/article/003940.htm | publisher = NLM/NIH | title = Medline Plus Medical Encyclopedia | contribution = Rheumatic fever | postscript = <!-- Bot inserted parameter. Either remove it; or change its value to "." for the cite to end in a ".", as necessary. -->{{inconsistent citations}}}}.</ref> |
|||
الحمى الروماتيزميه اساسا تصيب الاطفال بين الاعمار ٥-١٧ سنه، وتحدث تقريبا بعد ٢٠ يوم من التهاب الحلق. ولا تكون هناك اي اعراض بسبب عدوى البكتيريا العقيدية في ثلث الحالات. |
|||
نسبه تطور الحمى الروماتيزميه في الاشخاص المصابين بعدوى عقديه غير معالجه يتوقع ان تكون٣٪. ونسبه اعاده حدوثها مع عدوى متكرره غير معالجه تزداد ل(تقريبا٥٠٪).<ref>{{cite book | last =Porth | first = Carol |title=Essentials of pathophysiology: concepts of altered health states | publisher =Lippincott Williams & Wilkins |location=Hagerstown, MD |year=2007 | isbn= 0-7817-7087-4}}</ref> وتكون نسبه الحدوث اقل بكثير في الاشخاص المستخدمين للمضادات الحيويه للعلاج. اما الاشخاص الذين اصيبوا بحمى روماتيزميه لديهم القابليه لحدوث نوبات احتدام مع تكرار العدوى بالعقديات. |
|||
تكرار الحمى الروماتيزميه نوعا ما شائع في غياب استمرار اخد جرعات صغيره من [[المضادات الحيوية]]، خصوصا في اول ثلاث الى خمس سنين بعد اول حادثه. المضاعفات التي تصيب القلب قد تكون على المدى الطويل خطيره، خصوصا اذا كان الصمام قد اصيب. |
|||
الباقين على قيد الحياه من الحمى الروماتيزميه عاده يجب ان ياخدوا بينسلين لمنع عدوى العقديات التي من المحتمل ان تؤدي الى حالات اخرى من الحمى الروماتيزميه القاتله. |
|||
== المراجع == |
|||
{{مراجع|2}} |
|||
==وصلات خارجية== |
|||
الحمى الروماتيزمية شائعة في جميع أنحاء العالم، ومسؤولةً عن العديد من حالات صمامات القلب التالفة . فقدت أدت الحمى إلى 345،000 حالة وفاة على مستوى العالم اعتباراً من عام 2010 ، بانخفاض من 463،000 في عام 1990. وأصبح من النادر نسبيا في الدول الغربية منذ عام ١٩٦٠، وربما يرجع ذلك إلى الاستخدام واسع النطاق للمضادات الحيوية لعلاج الالتهابات العقديات.في حين كانت النسبة أقل شيوعا بكثير في الولايات المتحدة منذ بداية القرن العشرين و كان تفشي المرض أقل منذ عام 1980. فعلى الرغم من أن المرض نادراً ما يحدث، إلا أنه أمر خطير ويبلغ معدل حالات الوفاة من 2% إلى 5% ، وتؤثر الحمى الروماتيزمية في المقام الأول على الأطفال الذين تتراوح أعمارهم بين 5 و 17 سنة، ويحدث تقريبا بعد 20 يوماً من الإصابة بالتهاب الحلق. قد لاتسبب العدوى بالبكتيريا الكامنة أي أعراض ولكنها تصيب ثلث الحالات، ويقدر معدل تطور مرض الحمى الروماتزمية عند الأشخاص المصابين بعدوى بكتيريا غير المعالجة ليصل إلى 3٪. تتكرر الإصابة بالعدوى الغير معالجة اللاحقة بكثرة أي (حوالي 50٪). معدل تطور المرض أقل بكثير لدى الأشخاص الذين تلقوا العلاج عن طريق المضادات الحيوية، والأشخاص الذين يعانون من الحمى الروماتيزمية لديهم ميل لتطور وتفجر الإلتهابات البكتيرية المتكررة، إن الإصابة المتكررة بالحمى الروماتيزمية هو أمر شائع نسبياً في ظل غياب الجرعة المنخفضة من المضادات الحيوية ، وخاصةً خلال أول ثلاث أو خمس سنوات بعد الإصابة الأولى، وقد تكون مضاعفات القلب معقدة وحادة على المدى الطويل خصوصا ًإذا شاركتها الصمامات. و في كثير من الأحيان يكون الناجون من مرض الحمى الروماتزمية قد تناولوا البنسلين لمنع العدوى بالبكتريا العنقودية و التي ربما تؤدي إلى حالة أخرى من حالات الحمى الروماتيزمية و يمكن أن تكون قاتلة. |
|||
* [http://heartcenter.seattlechildrens.org/conditions_treated/rheumatic_heart_disease.asp Rheumatic fever information] from Seattle Children's Hospital Heart Center |
|||
*Jones major criteria, [http://www.lifehugger.com/moc/289/rheumatic-fever-diagnosis-jones-major-criteria Mnemonic] |
|||
*[http://www.world-heart-federation.org/what-we-do/rheumatic-heart-disease-network Rheumatic Heart Disease Network] |
|||
==المراجع== |
|||
{{مراجع}} |
|||
{{أمراض القلب}} |
{{أمراض القلب}} |
||
نسخة 22:55، 27 يناير 2016
| حُمّى الروماتزم | |
|---|---|
 بكتيريا السبحية المقيحة (صبغ بابنهايم) هي المحفز لإحداث حمى الروماتزم.
| |
| معلومات عامة | |
| الاختصاص | طب القلب |
| من أنواع | خمج جرثومي، ومرض |
| الإدارة | |
| أدوية | |
| تعديل مصدري - تعديل | |
حمى الروماتيزم، أو مايعرف بحمى رماتيزميه حاده، هي مرض التهابي يصيب القلب، المفاصل، الجلد، والمخ.[1] تبدأ علامات المرض عادة بعد اسبوعين الى اربع اسابيع من التهاب بلعومي.[2] ومن اعراضه وعلاماته الحرارة، وألم في عدة مفاصل، وحركات عضلية لا ارادية، وعلامة مميزة الا انها غير شائعة وهي طفح جلدي غير حاك تسمى حُمامى هامشيّة. يصاب القلب في اكثر من نصف هذه الحالات. تلف دائم لصمامات القلب أو ما يعرف بداء القلب الروماتيزمي يحدث عادة بعد عدة نوبات وقد يحدث التلف في حالات خاصة بعد نوبة حادة واحدة من الحمى الروماتيزمية، ويمكن ان تسبب هذه الصمامات المعطوبة احتشاء في عضلة القلب، وتزيد من خطورة حدوث رجفان اذيني والتهاب في الصمامات.[1]
حمى الروماتيزم الحاده تحدث بعد التهاب بلعومي ببكتبريا تسمى بكتريا عقديه مقيِّحه.[1] اذا لم يعالج هذا الالتهاب، فإن الحمى الروماتيزميه الحادة تحدث في ٣٪ من الاشخاص.[3] يُعتَقَد ان المرض يحدث بسبب انتاج اجسام مضادة ضد انسجة جسم المريض نفسه. بعض الناس بسبب جيناتهم معرضين اكثر للاصابه بالمرض عندما يتعرضون لهذه البكتيريا. ومن العوامل الاخرى التي تزيد من خطورة الاصابه بالمرض سوء التغذيه والفقر.[1] أما تشخيص حمى الروماتيزم فتتضمن وجود الاعراض والعلامات بالاضافه الى دليل على عدوى بالبكتيريا العقديه مؤخرا.[4]
معالجة الناس المصابين بالتهاب بلعومي ببكتيريا عقديه بالمضادات الحيويه مثل البنسيلين تقلل من خطورة الاصابه بالحمى الروماتيزميه.[5] يحدث عادة فحص للبكتيريا العقدية في المرضى المصابين بالتهاب الحلق، ويمكن ان لا يتواجد هذا الفحص في الدول النامية، ومن الأساليب الاخرى للوقايه من هذا المرض هو تحسين الصرف الصحي. ينصح في بعض الأحيان لمرضى الحمى الرماتيزميه وداء القلب الروماتيزمي بمدة طويله من العلاج بالمضادات الحيويه. يعود المريض الى ممارسة حياته الطبيعيه تدريجيا بعد نوبة المرض. لكن عندما يتطور المرض الى مرحلة داء القلب الروماتيزمي يصبح العلاج اكثر صعوبة. ويمكن ان يحتاج العلاج الى تصليح او حتى استبدال للصمام. وتعالج المضاعفات وفقا لطبيعتها.[1]
يصاب ٣٢٥,٠٠٠ طفل سنويا بالحمى الرماتيزميه، ويوجد حاليا ١٨ مليون شخص مصاب بداء القلب الرماتيزمي. عادة يصاب الاطفال بالحمى الرماتيزميه بين عمر ٥ و ١٤ سنه،[1] 20% من الحالات تحدث لديهم النوبة الأولى بعد سن البلوغ .[6] ينتشر المرض غالبا في الدول النامية وبين السكان الاصليين في الدول المتطورة.[1] حيث بلغ عدد الوفيات٢7٥,٠٠٠ في سنه ٢٠١٣ مقارنة ب ٣٧٤,٠٠٠ في سنة ١٩٩٠.[7] اغلب الوفيات كانت في الدول النامية حيث سجلت نسبة الوفاة ١٢.٥٪ سنويا من المجموع الكلي للمصابين بهذا المرض في هذه الدول.[1] ويعود تاريخ المرض الى القرن الخامس قبل الميلاد كما تبين في سجلات ابوقراط.[8] وتعود تسميت المرض الى اعراضه التي تتشابه مع اعراض امراض الروماتيزم.[9]
الأعراض والعلامات

تبدا علامات المرض عادة بعد اسبوعين الى اربع اسابيع من التهاب بلعومي.[2] وتتضمن الاعراض:حرارة، الم في عدة مفاصل و تتغير المفاصل المصابة مع مرور الوقت، حركات عضليه لا اراديه، وعلامة مميزه الا انها غير شائعة وهي طفح جلدي غير حاك تسمى حُمامى هامشيّة. يصاب القلب في اكثر من نصف هذه الحالات. وتسبب تلف دائم لصمامات القلب، يعرف ب داء القلب الروماتيزمي، يحدث عادة بعد عدة نوبات، ويمكن ان يحدث في حالات خاصة بعد نوبة حمى روماتيزميه حاده واحده. ويمكن ان تسبب هذه الصمامات المعطوبة احتشاء في عضلة القلب، وتزيد من خطورة حدوث رجفان اذيني والتهاب في الصمامات.[1]
أخرى
- الم في البطن
- نزيف من الانف
الفزيولوجيا المرضيه
الحمى الروماتيزميه مرض يصيب جمييع اجهزه الجسم، حيث تصيب الانسجه الضامه المحيطه بالشريان، وتحدث بعد عدوى غير معالجه ببكتيريا عقديه بلعوميه محلله ذاتA بيتا. يُعتقد ان المرض يحدث بسبب اجسام مضاده تفاعليه متصالبه , وهذا النوع من التفاعل هو النوع الثاني من الحساسية المفرطة ويسمى التمويه الجزيئي. عادة تبقى الخلايا المناعية البائية (B cells) نشطة على السطح دون تحفيزها من قبل الخلايا التائية (T cells ) . خلال عدوى العقديات, الخلايا الناضجه المظهره للمستضد مثل خلايا B تظهر مولد الضد لخلايا CD4- T التي تتمايز الى خلايا T2 المساعده. خلايا T2 المساعده تحفز خلايا B لتصبح خلايا بلازميه والتي بدورها تنتج اجسام مضاده ضد الجدار الخلوي للعقديات. ولكن الاجسام المضاده يمكن ان تتفاعل ضد بطانه القلب والمفاصل,[10] منتجة اعراض الحمى الروماتيزميه.
للبكتيريا العقديه المقيحه جدار خلوي مكون من حزم من البوليمر التي تحتوي على بروتين M والذي يعتبر مستضد للغايه. تعمل الاجسام المضاده الناتجه من جهاز المناعه ضد بروتين M تفاعل مناعي ضد بروتين الليف العضلي القلبي مايوسن،[11] و غلايكوجين عضلات القلب, وخلايا العضلات الملساء للشرايين، مما يحفز اطلاق السايتوكاينات وتدمير الانسجه. لكن التفاعل المناعي المتصالب الوحيد المثبت هو مع الانسجه الضامه المحيطه بالاوعيه. هذا الالتهاب يحدث من خلال اتصال مباشر بين الخلايا المتممه و مستقبل Fc مما يحفز استجلاب للنيوتروفيل (العدلات) والخلايا الاكوله. اجسام آشوف المميزه، مكونه من كولاجين ايوزينوفيلي منتفخ محاط بخلايا ليمفيه وخلايا اكوله ويمكن رؤيته باستخدام المجهر الضوئي. من الممكن ان تتحول الخلايا الاكوله الاكبر الى خلايا انتيشو او خلايا آشوف ضخمه. الضرر الصمامي المتسبب من الروماتزم الحاد ممكن ان يتضمن ايضا مناعه خلويه, تتضمن افات الصمام بشكل رئيسي خلايا T المساعده وخلايا اكوله. [12]
في الحمى الروماتيزميه، هذه الافات يمكن ان تتواجد في اي طبقه من طبقات القلب, ولذلك سميت التهاب القلب الشامل. يمكن ان يسبب الالتهاب ارتشاح مصل فبيريني تاموري توصف بانها تأمور الخبز والزبدة والتي عاده تنتهي دون اي اثار. اشراك بطانه القلب ينتج اجمالا نخر شبه فبريني و تكوين ثآليل على طول خط اغلاق الصمام القلب اليساري. ينتج من الترسيب ثآليل, ولكن ينتج تسميك غير متساوي من الافات التحت الشغاف تسمى لويحات ماكاليوم.
داء القلب الروماتيزمي
داء القلب الروماتيزمي المزمن يتميز بنوبات متكرره من الالتهاب و الترميم الليفي. التغيرات الأساسية التي تحدث للصمامات تتضمن تسميك لشرفات الصمام، التحام في الصواري، وتسميك وتقصير في الاربطه الوتريه.[12] تَحدُث نتيجه تفاعل مناعي ذاتي ضد بكتريا عقديه محلله نوع A بيتا تسبب تدمير للصمامات[13] . ينتج من التليف والتندب لشرفات الصمام، الصواري، والشرفات اعاقات تسبب تضيق او قَلَس للصمامات.[14] يطلق على الالتهاب الناتج من الحمى الروماتيزميه – عادة يحدث خلال فتره الطفوله - التهاب الصمام الروماتيزمي. ويكون نصف مرضى الحمى الروماتيزميه مصابين بالتهاب بطانه الصمام. ومعظم نسبة المراضة والوفيات المتعلقة بالحمى الروماتيزمية سببها التدمير الذي تحدثه الحمى الروماتيزميه لانسجة صمامات القلب.[14] إنّ آلية تطور المرض لداء القلب الروماتيزمي معقده وغير مفهومه بشكل كامل، لكن من المعلوم انها تتضمن التمويه الجزيئي والقابيليه الجينيه التي تؤدي الى تفاعل مناعي ذاتي.
التمويه الجزيئي يحدث عندما تتشارك الحواتم بين مولد الضد للمُضيف ومولد الضد للبكتيريا.[15] يسبب هذا تفاعل مناعي ذاتي ضد الانسجه الاصليه في القلب التي يتم التعرف عليها بالخطا كاجسام غريبه نتيجه التفاعليه المتصالبه للاجسام المضاده التي تتكون نتيجه الحواتم المشتركه. تكون بطانه الصمامات هي المكان الرئيسي للدمار الناتج من الخلايا الليمفيه. وتعتبر خلاياCD4 T هي الخلايا الرئيسيه المؤثره في داء القلب الروماتيزمي. [16] تبدأ عمليه تحفيز خلايا T عاده باظهار مولدات الضد للبكتيريا العقديه A. في داء القلب الروماتيزمي، يسبب التمويه الجزيئي تحفيز غير صحيح لخلايا T والتي بدورها تُحفّز خلايا B التي تبدا بانتاج اجسام مضاده خاصة لمولدات ضد ذاتيه. وهذا ينتج استجابة مناعية ضد انسجة القلب التي تم التعرف عليها على اساس انها اجسام غريبه. تزيد الصمامات الروماتيزميه من استعراض VCAM-1 على سطح الخلية وهو بروتين يساعد على التصاق الخلايا الليمفيه.[17] وتتم اعاده تنظيم VCAM-1 بعد ارتباطها ببطانه الصمام عن طريق اجسام مضاده خاصة لمولدات ضد ذاتيه ناتجه بسبب التمويه الجزيئي بين بروتينات الشخص ومولدات الضد للبكتيريا العقديه A، وهذا يؤدي الى التهابات وندوبات في الصمام تُلاحظ في التهاب الصمام الروماتيزمي، والتي تحدث عاده بسبب ارتشاح لخلايا T CD4.[17] بينما تبقى القابليه الجينيه غير واضحه، وجدت بعض العوامل الجينيه التي تزيد من القابليه للتفاعل المناعي المتصالب في الحمى الروماتيزميه. اما العامل الرئيسي المساهم هو النوع الثاني من الجزيء MHC ، الموجود على الخلايا الليمفيه والخلايا المقدمه لمولد الضد، خاصه أليل DR, DQ على الكروموسوم البشري ٦.[18] ويزيد اتحاد أليلات معينه من التفاعل المناعي المتصالب في داء القلب الروماتيزمي. مستضد الكريات البيضاء البشري النوع الثاني (HLA class II) أليل DR7 (HLA-DR7) غالبا لها ارتباط بداء القلب الروماتيزمي، واتحادها مع أليلات معينه من DQ لها ارتباط ظاهري لنشوء الضرر الصمامي.[18] العمليه التي من خلالها تزيد جزيئات MHC- II قابليه المُضيف للتفاعل المناعي التصالبي في الحمى الروماتيزميه غير معروفه، لكن من المحتمل ان لها علاقه بدور جزيء HLA في تقدمة مولد الضد لمستقبلات خلايا T، وهذا يحفز العمليه المناعيه. ووجد ايضا على كروموسوم رقم ٦ سايتوكاين TNF-a الذي له علاقه بداء القلب الروماتيزمي.[18] ويفاقم الظهورعالي المستوى ل TNF-a من التهاب الانسجه الصماميه وهذا يساهم في تطور داء القلب الروماتيزمي. مانوز بايندينغ ليكتين MBL هو بروتين التهابي يستخدم في التعرف على مسبب المرض. وتوجد مغايرات مختلفه من مواقع جين MBL2 على الحمض النووي لها علاقه بداء القلب الروماتيزمي. فالتضيق في الصمام التاجي الناتج من داء القلب الروماتيزمي له ارتباط ب MBL2 أليل التي تنسخ كميات كبيره من MBL.[19] اما القَلَس في الصمام الابهري في مرضى داء القلب الروماتيزمي له ارتباط ب MBL2 أليل التي تنسخ كميات قليله من MBL.[20] وتم فحص جينات اخرى لفهم اكثر لتعقيدات التفاعليات المناعيه المتصالبه في داء القلب الروماتيزمي.
التشخيص

نُشِرَ مقياس جونز المعدل لاول مره في عام ١٩٤٤ بواسطه ت. دوكيت جونز،(دكتور في الطب MD ) .[21] وكان يراجع دوريا من خلال جمعيه القلب الامريكيه بالتعاون مع مجموعات اخرى.[22] واعتمادا على مقياس جونز المعدل، يتم تشخيص الحمى الروماتيزمية من خلال وجود اثنتين من المعايير الرئيسية، او معيار رئيسي واحد ومعيارين ثانويين، مع وجود دليل على التهاب ببكتيريا عقدية: من خلال ارتفاع معيار ضد الحالّة العِقْدِيّة O او انزيم DNAase.[6] يستثنى من ذلك رقص سيدنهام والتهاب القلب الخامل، حيث تعتبر كل واحده منهن بنفسها اشاره الى الحمى الروماتيزميه.[23][24][25] نشرت مقاله في ابريل ٢٠١٣ في الجريدة الهنديه للابحاث الطبية صرحت ان ابحاث مخطط صدى القلب و دوبلر E,D، رغم وجود تحفظات على منافعهم, ساهمت بشكل كبير في تشخيص مرض داء القلب الروماتيزمي، مما يرجح عدم كفايه مقياس جونز ١٩٩٢. وشخصت ابحاث E,D التهابا للقلب مصابين بحمى الروماتيزم الحادة ، وبالمثل عند متابعه مرضى حمى الروماتيزم ممن اتوا في البدايه برقص سيدنهام وحدها.[26] ومن العلامات السابقه لعدوى العقديات: حمى قرمزية مؤخرا، ارتفاع عيار مستضد الحاله العقديه O او عيار اجسام مضاده ضد عقديه اخرى، او موجبية زراعه الحلق.[27]
المعايير الرئيسية
- التهاب المفاصل: التهاب مؤقت متنقل في المفاصل الكبرى، عاده يبدا في الساق وينتقل الى الاعلى.
- التهاب القلب: التهاب في عضلة القلب ( myocarditis) تظهر كفشل القلب الاحتقاني مع ضيق في التنفس، او التهاب غلاف القلب مع احتكاك، او نفخه قلبيه جديده.
- عقيدات تحت جلديه: تجاميع صلبةغير مؤلمة من الالياف فوق العظام او الاربطه. عاده تظهر خلف الرسغ، خارج الكوع، و على مقدمة الركبه.
- حمامى هامشيه: طفح جلدي محمر طويل المدى يبدا في الجذع او الذراع على شكل بقع، تنتشر الى الخارج وتُمسح من الداخل لتشكل حلقه، تستمر بالانتشار لتتحد مع حلقات اخرى، لتكون شكل حيه، تنتشر إلى الوجه وتسوء مع الحراره.
- رقص سيدنهام: سلسله من الحركات السريعه المميزه لا يتأثر بها الوجه والذراعين. تحدث في اخر اوقات المرض على الاقل ثلاث اشهر من بدايه العدوى.
المعايير الثانوية
- حراره ٣٨.٢-٣٨.٩ س ( 100,8 – 102,0 ف )
- الم مفاصل: الم في المفاصل بدون انتفاخ ( لا يتم احتسابها اذا كان التهاب المفاصل المتعدد موجود من ضمن المعايير الرئيسية)
- ارتفاع سرعه تثفل كريات الدم الحمر او البروتين المتفاعل C
- ارتفاع الكريات البيض
- خصائص مميزه في تخطيط القلب تشير لتوقف القلب، مثل استطوال فتره PR[27][28] ( لا تحتسب اذا كان التهاب القلب من ضمن المعايير الرئيسية)
- نوبات قديمه من الحمى الروماتيزميه او مرض قلبي خامل
حمى الروماتيزم في جثه مشرحة مع خصائص مميزه (تسميك للصمام التاجي و تسميك الحبال الوتريه القلبيه و تضخيم بطانه البطين الايسر).
الوقاية
الوقايه من تكرار المرض يتم من خلال استئصال العدوى الحاده واعطاء مضادات حيويه وقائيه. تقترح جمعيه القلب الامريكيه المحافظه على صحة الاسنان، واعطاء مضادات حيويه وقائيه على المدى البعيد للاشخاص المعروفين بالتهاب الشغاف الجرثومي، او زراعه قلب، او لديهم صمام قلب صناعي، او انواع من عيوب قلبيه خلقيه.[29]
العلاج
ان معالجه الحمى الرروماتيزميه تتجه نحو تقليل الالتهاب بعلاجات ضد الالتهاب مثل اسبيرين او كورتيكوستيرويد. والاشخاص الذين أثبتت الزراعة إصابتهم بعقديات الحلق يجب معالجتهم بالمضادات الحيويه. يعتبر الاسبيرين هو الدواء الافضل ويجب ان يعطى في جرعات عاليه ١٠٠مغ/كغ/يوم. يجب متابعه الاعراض الجانبيه مثل التهاب المعده، وتسمم بالساليسايلات. في الاطفال والمراهقين استخدام الاسبيرين والمنتجات المحتويه على الاسبيرين لها علاقة بمتلازمة ريز، وهي حاله خطرة ومميته .يجب ان يوضع بالحسبان الاخطار، والفوائد، والعلاجات البديله عند استخدام الاسبيرين والمنتجات المحتويه على الاسبيرين في الاطفال والمراهقين. يستخدم الايبوبروفين للالم وعدم الارتياح والكورتيكوستيرويد للالتهابات المتوسطه والشديده في الحمى الروماتيزميه للاطفال والمراهقين. اما استخدام الستيرويد فيبقى للحالات التي يوجد فيها دليل على اصابه القلب. استخدام الستيرويد يمكن ان يمنع الندوبات المستقبليه للانسجه ويمكن ان يمنع حدوث مضاعفات مثل التضيق التاجي. وتعطى حقنه شهريا من بينسلسن طويل المدى لمده خمس سنوات لمرضى تعرضو لنوبه واحده من الحمى الروماتيزميه. اما اذا كان هناك دليل على التهاب القلب، فان مدة العلاج قد تطول ل٤٠ سنه ومن الاساسيات للعلاج في الحمى الروماتيزميه استمراريه استخدام مضادات حيويه بجرعات قليله ( مثل البنسلين، سلفاديازين، ايريثرومايسين) لمنع حدوث التكرار.
التطعيم
حاليا لا يوجد مطعوم للبكتيريا العقديه المقيحه، ولكن يوجد ابحاث لتطوير هذا المطعوم. تتضمن الصعوبات في ايجاد مطعوم الانواع المختلفه من البكتيريا العقديه المقيحه في الطبيعه وضروره وجود عدد كبير من الناس ووقت كثير لمحاولات صناعته بامان وكفاءه عاليه.[30]
العدوى
الاشخاص موجبيي الزراعه للعقديات المقيحه يجب علاجهم بالبنسلين مادامت الحساسيه للدواء غير موجوده. هذا العلاج لن يغير مسار المرض الحاد. ان افضل العلاجات الموجوده في كتب اوكسفورد (Oxford Handbook of Clinical Medicine) للحمى الروماتيزميه هو بينزاثين بينزيل بينيسلين.
الالتهاب
يستخدم عاده الكورتيكوستيرويد، ولكن لا يوجد دليل قوي لاثبات ذلك. [1] ويستخدم الساليساليت لتخفيف الالم.
فشل القلب
بعض الاشخاص يصابون بالتهاب قلبي قوي تظهر اعراضه على شكل فشل قلب احتقاني. وهذا يحتاج الى الادويه المستخدمه عاده في فشل القلب: مثبطات ACE، مدرات بول، مُحْصِر بيتا، ديجوكسين. على العكس من فشل القلب العادي، فان فشل القلب الروماتيزمي يستجيب جيدا للكورتيكوستيرويد.
الاوبئه

حمى الروماتيزم منتشره عالميا ومسؤوله عن حالات كثيره لدمار صمامات القلب.كان عدد الوفيات عالميا في ٢٠١٠ بسببها ٣٤٥.٠٠٠ مقارنه ب ٤٦٣.٠٠٠ في عام١٩٩٠.[32] في الدول الغربيه، اصبحت نادره منذ ستينيات القرن العشرين، ربما نتيجه انتشار استخدام المضادات الحيويه لمعالجه عدوى العقديات. بينما اصبحت اقل بكثير في الولايات المتحده منذ بداية القرن العشرين و لكان هناك عدة حالات تفشي للمرض منذ ١٩٨٠.على الرغم من ان المرض يحدث نادرا، الا انه مرض خطير وله نسبه وفيات من ٢-٥٪.[33] الحمى الروماتيزميه اساسا تصيب الاطفال بين الاعمار ٥-١٧ سنه، وتحدث تقريبا بعد ٢٠ يوم من التهاب الحلق. ولا تكون هناك اي اعراض بسبب عدوى البكتيريا العقيدية في ثلث الحالات. نسبه تطور الحمى الروماتيزميه في الاشخاص المصابين بعدوى عقديه غير معالجه يتوقع ان تكون٣٪. ونسبه اعاده حدوثها مع عدوى متكرره غير معالجه تزداد ل(تقريبا٥٠٪).[34] وتكون نسبه الحدوث اقل بكثير في الاشخاص المستخدمين للمضادات الحيويه للعلاج. اما الاشخاص الذين اصيبوا بحمى روماتيزميه لديهم القابليه لحدوث نوبات احتدام مع تكرار العدوى بالعقديات. تكرار الحمى الروماتيزميه نوعا ما شائع في غياب استمرار اخد جرعات صغيره من المضادات الحيوية، خصوصا في اول ثلاث الى خمس سنين بعد اول حادثه. المضاعفات التي تصيب القلب قد تكون على المدى الطويل خطيره، خصوصا اذا كان الصمام قد اصيب. الباقين على قيد الحياه من الحمى الروماتيزميه عاده يجب ان ياخدوا بينسلين لمنع عدوى العقديات التي من المحتمل ان تؤدي الى حالات اخرى من الحمى الروماتيزميه القاتله.
المراجع
- ^ أ ب ت ث ج ح خ د ذ ر Marijon، E؛ Mirabel، M؛ Celermajer، DS؛ Jouven، X (10 مارس 2012). "Rheumatic heart disease". Lancet. ج. 379 ع. 9819: 953–64. DOI:10.1016/S0140-6736(11)61171-9. PMID:22405798.
- ^ أ ب Lee، KY؛ Rhim، JW؛ Kang، JH (مارس 2012). "Kawasaki disease: laboratory findings and an immunopathogenesis on the premise of a "protein homeostasis system"". Yonsei medical journal. ج. 53 ع. 2: 262–75. DOI:10.3349/ymj.2012.53.2.262. PMID:22318812.
- ^ Ashby، Carol Turkington, Bonnie Lee (2007). The encyclopedia of infectious diseases (ط. 3rd). New York: Facts On File. ص. 292. ISBN:9780816075072.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Rheumatic Fever 1997 Case Definition". cdc.gov. 3 فبراير 2015. اطلع عليه بتاريخ 2015-02-19.
- ^ Spinks، A؛ Glasziou، PP؛ Del Mar، CB (5 نوفمبر 2013). "Antibiotics for sore throat". The Cochrane database of systematic reviews. ج. 11: CD000023. DOI:10.1002/14651858.CD000023.pub4. PMID:24190439.
- ^ أ ب Kumar، Vinay؛ Abbas، Abul K؛ Fausto، Nelson؛ Mitchell، Richard N (2007). Robbins Basic Pathology (ط. 8th). Saunders Elsevier. ص. 403–6. ISBN:978-1-4160-2973-1.
- ^ GBD 2013 Mortality and Causes of Death، Collaborators (17 ديسمبر 2014). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013". Lancet. ج. 385 ع. 9963: 117–171. DOI:10.1016/S0140-6736(14)61682-2. PMC:4340604. PMID:25530442.
{{استشهاد بدورية محكمة}}:|first1=باسم عام (مساعدة)صيانة الاستشهاد: أسماء عددية: قائمة المؤلفين (link) - ^ Quinn، RW (1991). "Did scarlet fever and rheumatic fever exist in Hippocrates' time?". Reviews of infectious diseases. ج. 13 ع. 6: 1243–4. DOI:10.1093/clinids/13.6.1243. PMID:1775859.
- ^ "rheumatic fever" في معجم دورلاند الطبي
- ^ Abbas، Abul K.؛ Lichtman، Andrew H.؛ Baker، David L.؛ وآخرون (2004). Basic immunology: functions and disorders of the immune system (ط. 2). Philadelphia, Pennsylvania: Elsevier Saunders. ISBN:978-1-4160-2403-3.
- ^ Faé KC، da Silva DD، Oshiro SE، وآخرون (مايو 2006). "Mimicry in recognition of cardiac myosin peptides by heart-intralesional T cell clones from rheumatic heart disease". J. Immunol. ج. 176 ع. 9: 5662–70. DOI:10.4049/jimmunol.176.9.5662. PMID:16622036.
- ^ أ ب Cotran, Ramzi S.; Kumar, Vinay; Fausto, Nelson; Nelso Fausto; Robbins, Stanley L.; Abbas, Abul K. (2005). Robbins and Cotran pathologic basis of disease. St. Louis, Mo: Elsevier Saunders. ISBN:0-7216-0187-1.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Kaplan، MH؛ Bolande، R؛ Rakita، L؛ Blair، J (1964). "Presence of Bound Immunoglobulins and Complement in the Myocardium in Acute Rheumatic Fever. Association with Cardiac Failure". The New England Journal of Medicine. ج. 271 ع. 13: 637–45. DOI:10.1056/NEJM196409242711301. PMID:14170842.
- ^ أ ب Brice، Edmund A. W؛ Commerford، Patrick J. (2005). "Rheumatic Fever and Valvular Heart Disease". في Rosendorff، Clive (المحرر). Essential Cardiology: Principles and Practice. Totowa, New Jersey: Humana Press. ص. 545–563. DOI:10.1007/978-1-59259-918-9_30. ISBN:978-1-59259-918-9.
- ^ Guilherme، L؛ Kalil، J؛ Cunningham، M (2006). "Molecular mimicry in the autoimmune pathogenesis of rheumatic heart disease". Autoimmunity. ج. 39 ع. 1: 31–9. DOI:10.1080/08916930500484674. PMID:16455580.
- ^ Kemeny، E؛ Grieve، T؛ Marcus، R؛ Sareli، P؛ Zabriskie، JB (1989). "Identification of mononuclear cells and T cell subsets in rheumatic valvulitis". Clinical immunology and immunopathology. ج. 52 ع. 2: 225–37. DOI:10.1016/0090-1229(89)90174-8. PMID:2786783.
- ^ أ ب Roberts، S؛ Kosanke، S؛ Terrence Dunn، S؛ Jankelow، D؛ Duran، CM؛ Cunningham، MW (2001). "Pathogenic mechanisms in rheumatic carditis: Focus on valvular endothelium". The Journal of infectious diseases. ج. 183 ع. 3: 507–11. DOI:10.1086/318076. PMID:11133385.
- ^ أ ب ت Stanevicha، V؛ Eglite، J؛ Sochnevs، A؛ Gardovska، D؛ Zavadska، D؛ Shantere، R (2003). "HLA class II associations with rheumatic heart disease among clinically homogeneous patients in children in Latvia". Arthritis Research & Therapy. ج. 5 ع. 6: R340–R346. DOI:10.1186/ar1000. PMC:333411. PMID:14680508.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Schafranski، MD؛ Pereira Ferrari، L؛ Scherner، D؛ Torres، R؛ Jensenius، JC؛ De Messias-Reason، IJ (2008). "High-producing MBL2 genotypes increase the risk of acute and chronic carditis in patients with history of rheumatic fever". Molecular immunology. ج. 45 ع. 14: 3827–31. DOI:10.1016/j.molimm.2008.05.013. PMID:18602696.
- ^ Ramasawmy، R؛ Spina، GS؛ Fae، KC؛ Pereira، AC؛ Nisihara، R؛ Messias Reason، IJ؛ Grinberg، M؛ Tarasoutchi، F؛ Kalil، J؛ Guilherme، L. (2008). "Association of Mannose-Binding Lectin Gene Polymorphism but Not of Mannose-Binding Serine Protease 2 with Chronic Severe Aortic Regurgitation of Rheumatic Etiology". Clinical and Vaccine Immunology : CVI. ج. 15 ع. 6: 932–936. DOI:10.1128/CVI.00324-07. PMC:2446618. PMID:18400978.
- ^ Jones، T Duckett (1944). "The diagnosis of rheumatic fever". JAMA. ج. 126 ع. 8: 481–4. DOI:10.1001/jama.1944.02850430015005.
- ^ Ferrieri، P؛ Jones Criteria Working، Group (2002). "Proceedings of the Jones Criteria workshop". Circulation. Jones Criteria Working Group. ج. 106 ع. 19: 2521–3. DOI:10.1161/01.CIR.0000037745.65929.FA. PMID:12417554.
- ^ Parrillo، Steven J. "Rheumatic Fever". eMedicine. DO, FACOEP, FACEP. اطلع عليه بتاريخ 2007-07-14.
- ^ "Guidelines for the diagnosis of rheumatic fever. Jones Criteria, 1992 update". JAMA. Special Writing Group of the Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease of the Council on Cardiovascular Disease in the Young of the American Heart Association. ج. 268 ع. 15: 2069–73. 1992. DOI:10.1001/jama.268.15.2069. PMID:1404745.
- ^ Saxena، Anita (2000). "Diagnosis of rheumatic fever: Current status of Jones criteria and role of echocardiography". Indian Journal of Pediatrics. ج. 67 ع. 4: 283–6. DOI:10.1007/BF02758174. PMID:11129913.
- ^ Kumar، RK؛ Tandon، R (2013). "Rheumatic fever & rheumatic heart disease: The last 50 years". The Indian Journal of Medical Research. ج. 137 ع. 4: 643–658. PMC:3724245. PMID:23703332.
- ^ أ ب Ed Boon, Davidson's General Practice of Medicine, 20th edition. P. 617.
- ^ Aly، Ashraf (2008). "Rheumatic Fever". Core Concepts of Pediatrics. University of Texas. اطلع عليه بتاريخ 2011-08-06.
- ^ "What About My Child and Rheumatic Fever?" (PDF). American Heart Association. اطلع عليه بتاريخ 2014-02-23.
- ^ "Initiative for Vaccine Research (IVR) - Group A Streptococcus". World Health Organization. اطلع عليه بتاريخ 2012-06-15.
- ^ "WHO Disease and injury country estimates". World Health Organization. 2009. اطلع عليه بتاريخ 2009-11-11.
- ^ Lozano، R؛ Naghavi، M؛ Foreman، K؛ Lim، S؛ Shibuya، K؛ Aboyans، V؛ Abraham، J؛ Adair، T؛ Aggarwal، R (15 ديسمبر 2012). "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. ج. 380 ع. 9859: 2095–128. DOI:10.1016/S0140-6736(12)61728-0. PMID:23245604.
{{استشهاد بدورية محكمة}}: الوسيط|first10=يفتقد|first10=(مساعدة)، الوسيط|first11=يفتقد|first11=(مساعدة)، الوسيط|first12=يفتقد|first12=(مساعدة)، الوسيط|first13=يفتقد|first13=(مساعدة)، الوسيط|first14=يفتقد|first14=(مساعدة)، الوسيط|first15=يفتقد|first15=(مساعدة)، الوسيط|first16=يفتقد|first16=(مساعدة)، الوسيط|first17=يفتقد|first17=(مساعدة)، الوسيط|first18=يفتقد|first18=(مساعدة)، الوسيط|first19=يفتقد|first19=(مساعدة)، الوسيط|first20=يفتقد|first20=(مساعدة)، الوسيط|first21=يفتقد|first21=(مساعدة)، الوسيط|first22=يفتقد|first22=(مساعدة)، الوسيط|first23=يفتقد|first23=(مساعدة)، الوسيط|first24=يفتقد|first24=(مساعدة)، الوسيط|first25=يفتقد|first25=(مساعدة)، الوسيط|first26=يفتقد|first26=(مساعدة)، الوسيط|first27=يفتقد|first27=(مساعدة)، الوسيط|first28=يفتقد|first28=(مساعدة)، الوسيط|first29=يفتقد|first29=(مساعدة)، والوسيط|first30=يفتقد|first30=(مساعدة) - ^ "Medline Plus Medical Encyclopedia". NLM/NIH
{{استشهاد بدورية محكمة}}: الاستشهاد بدورية محكمة يطلب|دورية محكمة=(مساعدة) والوسيط|contribution=تم تجاهله (مساعدة)صيانة الاستشهاد: postscript (link). - ^ Porth، Carol (2007). Essentials of pathophysiology: concepts of altered health states. Hagerstown, MD: Lippincott Williams & Wilkins. ISBN:0-7817-7087-4.
وصلات خارجية
- Rheumatic fever information from Seattle Children's Hospital Heart Center
- Jones major criteria, Mnemonic
- Rheumatic Heart Disease Network
