متلازمة هيدروهالوس: الفرق بين النسختين
بليغ الفقيه (نقاش | مساهمات) اضافة مقال جديدة وسمان: تمت إضافة وسم nowiki المحرر المرئي: تبديل |
(لا فرق)
|
نسخة 14:51، 27 أكتوبر 2021
| متلازمة هيدروهالوس | |
|---|---|
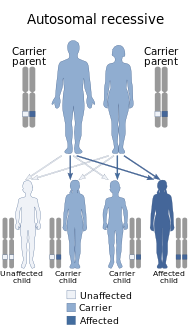
متلازمة هيدروهالوس موروثة بطريقة وراثية متنحية
| |
| تسميات أخرى | متلازمة سالونين هيرفا نوريو |
| معلومات عامة | |
| الاختصاص | علم الوراثة الطبية |
| من أنواع | اضطراب صبغي جسدي متنحي ، ومتلازمة |
| تعديل مصدري - تعديل | |
متلازمة هيدروهالوس بالإنجليزية: (Hydrolethalus syndrome) يرتبط HLS بطفرات HYLS1. الجين المشفر HYLS1 مسؤول عن التطور الصحيح لأهداب داخل جسم الإنسان. الأهداب هي إسقاطات مجهرية تسمح بالإدخال الحسي وإخراج الإشارات داخل الخلايا ، بالإضافة إلى حركة الخلية. [1] ينتج عن الخلل مجموعة من التشوهات التي غالبًا ما تكون نتيجة لإشارات الخلية غير الصحيحة. [2] الشكل البديل ، HLS2 ، مع طفرات إضافية لجين KIF7 ، أقل شيوعًا. [3] يضمن KIF7 أيضًا تكوين الأهداب الصحيح ووظيفتها ، وتحديداً ثبات الأهداب وطولها. [4]
تم التعرف على متلازمة هيدروهالوس (HLS) عن طريق الخطأ لأول مرة في فنلندا ، خلال دراسة عن متلازمة ميكل . [5] مثل HLS ، تظهر متلازمة ميكل مع تشوهات فسيولوجية شديدة ، وهي اضطرابات في الجهاز العصبي المركزي ووجود أصابع أو أصابع إضافية ( تعدد الأصابع). [5] يمكن تمييز HLS عن متلازمة ميكل من خلال تحليل وظائف الكلى ، والتي تكون غير فعالة في متلازمة ميكل نتيجة لتكوين الكيس. [6]
العلامات والأعراض
يقدم HLS نفسه على أنه تشوهات تطورية مختلفة مميتة ، والتي غالبًا ما تؤدي إما إلى ولادة جنين ميت مبكر أو الوفاة بعد الولادة بوقت قصير. [7] لوحظت حالات نادرة لأطفال ولدوا مصابين بداء HLS على قيد الحياة لعدة أشهر. [8] الشذوذ المميز لـ HLS هو عدم وجود أنسجة المخ وهياكل خط الوسط ، مع وجود سوائل دماغية زائدة ( استسقاء الرأس ) نتيجة للتطور غير الطبيعي للجهاز العصبي المركزي. [7] تشمل العيوب الشائعة الأخرى نمو الرئة غير المكتمل وعيوب القلب والشفة المشقوقة أو الحنك المشقوق وتعدد الأصابع والفك الصغير بشكل غير طبيعي. [7] يُعد موت الجنين ميتًا وزيادة السائل الأمنيوسي ( polyhydramnios ) أمرًا شائعًا أثناء الحمل مع جنين مصاب بمرض HLS ، حيث يتم الاستشهاد بحالات تصل إلى 8 لترات مقارنة بـ 1 لتر الطبيعي. [8] الأعراض الأقل شيوعًا مثل العيون الصغيرة بشكل غير طبيعي والأنف العريض ممكنة أيضًا.
الأسباب
الوراثة
يحدث HLS بسبب طفرة خطأ وراثي في الجين HYLS1 ، الذي يشفر بروتين متلازمة هيدروهالوس 1 ، على الكروموسوم 11 ؛ [9] تغيير قاعدة واحدة في الأحماض الأمينية تسلسل HYLS1 في اكسون 6 ينطوي على استبدال حمض الأسبارتيك 211 مع الجلايسين (D211G) في سلسلة ببتيد. [10] إكسون 6 هو إكسون البروتين الوحيد في HYLS1 ؛ يضمن الأداء السليم للإكسونات 1-5 تنظيم البروتين بأكمله والتعبير عنه. [9] HLS هو متلازمة وراثية متنحية. [11] يكون التطور ممكنًا فقط إذا كان كلا الوالدين يحملان الجين المعيب ، وفي هذه الحالة ، يكون خطر إصابة الجنين بالمتلازمة بنسبة 25٪. HLS هو عضو في تراث المرض الفنلندي ، [9] مع حدوث حالات أكثر شيوعًا في فنلندا من بقية العالم ؛ يتأثر ما يقرب من 1 من كل 20000 من الأجنة النامية في فنلندا. [12] كما تم توثيق حالات نادرة في مناطق أخرى ، غالبًا مع أنماط ظاهرية أقل حدة نتيجة لتباين الأليل عبر البلدان ، مما يسمح ببقاء النسل المصاب لمدة تصل إلى عدة أشهر. [9] يُنصح الأفراد من أصل فنلندي بالخضوع لاختبارات جينية قبل محاولة الإنجاب.
قبل اكتشاف HLS ، كان جين HYLS1 غير معروف ، ولم يتم تحديد الجينات المماثلة داخل البشر. [13] تم فحص المتعاملين ، الجينات في الأنواع الأخرى ذات تراث الأسلاف المشترك ، لشرح الفيزيولوجيا المرضية لـ HLS ؛ جين مشابه داخل الدودة المستديرة ، Caenorhabditis elegans ، مسؤول عن تكوين الأهداب. [14] تضع الفرضيات الحالية خللاً وظيفيًا في الأهداب باعتباره السبب الرئيسي لعيوب HLS الناشئة عن طفرة HYLS1 في البشر. [13] [15] الاختلافات بين النوع البري و HYLS1 المتحولة قد لوحظت بوضوح. يتم ترجمة شكل النوع البري إلى السيتوبلازم ، في حين يتم ترجمة الشكل المتحور إلى النواة ويشكل مجموعات صغيرة ، مما يشير إلى أن الجين الطافر يعطل التوطين الخلوي. [15] البروتين المشفر بواسطة شكل متحور HYLS1 غير قادر على تنفيذ الاستهداف الأساسي للمريكزات لغشاء البلازما ، مما يعطل الوظيفة الهدبية ، مما يؤدي إلى اعتلال الهدبية . [14] نظرًا لوجود الأهداب في جميع الخلايا تقريبًا في جميع أنحاء الجسم ، فإن الخلل الوظيفي الهدبي يسبب عيوبًا في النمو في مجموعة من الأعضاء ، وبالتالي يمكن أن يختلف النمط الظاهري لـ HLS بشكل كبير ، على الرغم من ملاحظة تشوه الدماغ وتعدد الأصابع بشكل شائع.
البيئة
في الوقت الحالي ، لا توجد عوامل بيئية معروفة بأنها تزيد من احتمالية تطور HLS أو تقدمه ؛ يحدث HLS فقط بسبب التشوهات الجينية . [16]
الفيزيولوجيا المرضية
الفيزيولوجيا المرضية لـ HLS هي تطور غير طبيعي لأهداب ناشئة عن عدم قدرة جين HYLS1 المتحول على استهداف المريكزات بشكل صحيح لغشاء البلازما. [17] على وجه التحديد ، تفتقر الألياف الانتقالية داخل المنطقة الانتقالية ، عند قاعدة المحور العصبي والمجاورة لغشاء البلازما ، إلى التطور المناسب. [18] نظرًا لأن هذه الهياكل تشكل البوابة الهدبية ، فإن التطور غير السليم يؤدي إلى فقدان الانتقائية لدخول البروتين إلى المقصورة الهدبية. [19]
الاختلافات والأمراض ذات الصلة
كما لوحظت الطفرات في KIF7 في المرضى الذين يقدمون نمطًا ظاهريًا مشابهًا لـ HLS وتحول HYLS1 A إلى G المميز ؛ متماثل الحذف من الجينات KIF7 يؤدي إلى شكل متغير من HLS، HLS2. [20] يشفر KIF7 عاملًا بنيويًا حيويًا للنقل الهدبي ، كما أنه متورط في اضطرابات النمو الأخرى ، مثل متلازمة جوبيرت (JS). [21] بالإضافة إلى ذلك ، لم تعد الطفرات في HYLS1 مرتبطة صراحةً بـ HLS في البشر. [21] تؤدي الطفرات المتماثلة اللواقح التي تزيل كودون الإيقاف في exon 4 من HYLS1 إلى اضطراب تسلسل جينومي مختلف للطفرة الخاطئة لـ HLS ، وتوجد نمطًا ظاهريًا مثل JS. [22] "علامة السن المولية" للدماغ ، وهي حالة شاذة يتم فيها تقليل حجم المخيخ مع الاحتفاظ بشكل المخيخ ، تشبه الضرس وتستخدم لتحديد JS. [21] يظهر JS مع طفرات في أكثر من 30 جينًا ، في حين أن طفرة HYLS1 هي السبب الوحيد لـ HLS ، ولكنها موجودة أيضًا في شكل متغير HLS2 مع جين KIF7 المتحور. [20]
التشخيص
يمكن تشخيص HLS بسهولة أثناء الحمل من خلال استخدام الموجات فوق الصوتية ، والتي غالبًا ما تكشف عن استسقاء الرأس والبنية غير الطبيعية للدماغ. [23] يعد الفحص الدقيق عن طريق الموجات فوق الصوتية أو عند الولادة ضروريًا لاستبعاد متلازمة ميكل أو التثلث الصبغي 13 أو متلازمة سميث ليملي أوبيتز التي تظهر مع عيوب فسيولوجية مماثلة. [24] يمكن اكتشاف HLS في نهاية الثلث الأول من الحمل ، حوالي 13 أسبوعًا من الحمل
العلاج
لا يوجد علاج أو خيار علاجي للأفراد الذين يعانون من HLS حاليًا. [25] بسبب شدة عيوب الجنين وسوء التشخيص بالنسبة لأولئك الذين يعانون من HLS ، غالبًا ما يتم إنهاء الحمل. [26] لا يمكن تحقيق بعض الوقاية إلا من خلال تجنب الحمل إذا أشارت الاختبارات الجينية إلى أن كلا الوالدين المحتملين هما حاملان للجين المعيب HYLS1. [27]
انظر ايضا
• HYLS1
المراجع
- ^ "A novel HYLS1 homozygous mutation in living siblings with Joubert syndrome". Clinical Genetics. ج. 89 ع. 6: 739–43. يونيو 2016. DOI:10.1111/cge.12752. PMID:26830932.
- ^ "Ciliopathies: an expanding disease spectrum". Pediatric Nephrology. ج. 26 ع. 7: 1039–56. يوليو 2011. DOI:10.1007/s00467-010-1731-7. PMID:21210154.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "KIF7 mutations cause fetal hydrolethalus and acrocallosal syndromes". Nature Genetics. ج. 43 ع. 6: 601–6. يونيو 2011. DOI:10.1038/ng.826. PMID:21552264.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Gated entry into the ciliary compartment". Cellular and Molecular Life Sciences. ج. 73 ع. 1: 119–27. يناير 2016. DOI:10.1007/s00018-015-2058-0. PMID:26472341.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ أ ب "Hydrolethalus syndrome". Journal of Medical Genetics. ج. 27 ع. 12: 756–59. ديسمبر 1990. DOI:10.1136/jmg.27.12.756. PMID:2074561.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "The molecular basis of hydrolethalus syndrome". ResearchGate: 756–59. مارس 2009.
- ^ أ ب ت "Hydrolethalus syndrome". Journal of Medical Genetics. ج. 27 ع. 12: 756–59. ديسمبر 1990. DOI:10.1136/jmg.27.12.756. PMID:2074561.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ أ ب "The molecular basis of hydrolethalus syndrome". ResearchGate: 756–59. مارس 2009.
- ^ أ ب ت ث "The molecular basis of hydrolethalus syndrome". ResearchGate: 756–59. مارس 2009.
- ^ "Unraveling the disease pathogenesis behind lethal Hydrolethalus syndrome revealed multiple changes in molecular and cellular level". PathoGenetics. ج. 2 ع. 2: 2. أبريل 2009. DOI:10.1186/1755-8417-2-2. PMID:19400947.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Hydrolethalus syndrome is caused by a missense mutation in a novel gene HYLS1". Human Molecular Genetics. ج. 14 ع. 11: 1475–88. أبريل 2005. DOI:10.1093/hmg/ddi157. PMID:15843405.
- ^ "Hydrolethalus syndrome". Journal of Medical Genetics. ج. 27 ع. 12: 756–59. ديسمبر 1990. DOI:10.1136/jmg.27.12.756. PMID:2074561.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ أ ب "The molecular basis of hydrolethalus syndrome". ResearchGate: 756–59. مارس 2009.
- ^ أ ب "The Hydrolethalus syndrome protein HYLS-1 links core centriole structure to cilia formation". Genes & Development. ج. 23 ع. 17: 2046–59. سبتمبر 2009. DOI:10.1101/gad.1810409. PMID:19656802.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ أ ب "Hydrolethalus syndrome is caused by a missense mutation in a novel gene HYLS1". Human Molecular Genetics. ج. 14 ع. 11: 1475–88. أبريل 2005. DOI:10.1093/hmg/ddi157. PMID:15843405.
- ^ "Gated entry into the ciliary compartment". Cellular and Molecular Life Sciences. ج. 73 ع. 1: 119–27. يناير 2016. DOI:10.1007/s00018-015-2058-0. PMID:26472341.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "The Hydrolethalus syndrome protein HYLS-1 links core centriole structure to cilia formation". Genes & Development. ج. 23 ع. 17: 2046–59. سبتمبر 2009. DOI:10.1101/gad.1810409. PMID:19656802.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "The hydrolethalus syndrome protein HYLS-1 regulates formation of the ciliary gate". Nature Communications. ج. 7 ع. 12437: 12437. أغسطس 2016. Bibcode:2016NatCo...712437W. DOI:10.1038/ncomms12437. PMID:27534274.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Gated entry into the ciliary compartment". Cellular and Molecular Life Sciences. ج. 73 ع. 1: 119–27. يناير 2016. DOI:10.1007/s00018-015-2058-0. PMID:26472341.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ أ ب "KIF7 mutations cause fetal hydrolethalus and acrocallosal syndromes". Nature Genetics. ج. 43 ع. 6: 601–6. يونيو 2011. DOI:10.1038/ng.826. PMID:21552264.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ أ ب ت "A novel HYLS1 homozygous mutation in living siblings with Joubert syndrome". Clinical Genetics. ج. 89 ع. 6: 739–43. يونيو 2016. DOI:10.1111/cge.12752. PMID:26830932.
- ^ "Ciliopathies: an expanding disease spectrum". Pediatric Nephrology. ج. 26 ع. 7: 1039–56. يوليو 2011. DOI:10.1007/s00467-010-1731-7. PMID:21210154.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Orphanet: Hydrolethalus" (بالإنجليزية). 10 Sep 2017. Retrieved 2017-09-10.
- ^ "The molecular basis of hydrolethalus syndrome". ResearchGate: 756–59. مارس 2009.
- ^ "Orphanet: Hydrolethalus" (بالإنجليزية). 10 Sep 2017. Retrieved 2017-09-10.
- ^ "The molecular basis of hydrolethalus syndrome". ResearchGate: 756–59. مارس 2009.
- ^ "Hydrolethalus syndrome is caused by a missense mutation in a novel gene HYLS1". Human Molecular Genetics. ج. 14 ع. 11: 1475–88. أبريل 2005. DOI:10.1093/hmg/ddi157. PMID:15843405.
روابط خارجية
| في كومنز صور وملفات عن: متلازمة هيدروهالوس |