1-بروبانول
| 1-بروبانول | |
|---|---|
 |
 |
| الاسم النظامي (IUPAC) | |
بروبان-1-ول[1] |
|
| أسماء أخرى | |
|
|
| المعرفات | |
| رقم CAS | 71-23-8 |
| بوب كيم (PubChem) | 1031 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C3H8O |
| كتلة مولية | 60.1 غ.مول−1 |
| المظهر | Colorless liquid |
| الكثافة | .803 g/mL |
| نقطة الانصهار | -126 °س، 147 °ك، -195 °ف |
| نقطة الغليان | 97-98 °س، 370-371 °ك، 206-208 °ف |
| الذوبانية في الماء | قابل للامتزاج |
| log P | 0.329 |
| ضغط البخار | 1.99 kPa (at 20 °C) |
| حموضة (pKa) | 16 |
| القاعدية (pKb) | −2 |
| معامل الانكسار (nD) | 1.387 |
| اللزوجة | 1.938 mPa s |
| عزم جزيئي ثنائي القطب | 1.68 D |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
−302.79–−302.29 kJ mol-1 |
| تغير الإنتالبي القياسي للاحتراق ΔcH |
−2.02156–−2.02106 MJ mol-1 |
| إنتروبيا مولية قياسية S |
192.8 J K−1 mol−1 |
| الحرارة النوعية، C | 143.96 J K−1 mol−1 |
| المخاطر | |
| رمز الخطر وفق GHS |    |
| وصف الخطر وفق GHS | DANGER |
| بيانات الخطر وفق GHS | H225, H318, H336 |
| بيانات وقائية وفق GHS | P210, P261, P280, P305+351+338 |
| فهرس المفوضية الأوروبية | 603-003-00-0 |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| NFPA 704 |
|
| نقطة الوميض | 22 °C |
| درجة حرارة الاشتعال الذاتي |
371 °C |
| حدود الاشتعال | 13.7% |
| مركبات متعلقة | |
| مركبات ذات علاقة | Butane Propanamine |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
1- بروبانول أحد الكحولات ويكون الكحول أولياً إذا كانت مجموعة OH على أول ذرة كربون في الكحول. ويسمى الكحول حينئذ (1 ـ الكانول) .
CH3CH2CH2OH.
البروبانول: يعرف أيضًا باسم الكحول البروبيلي ، ويحتوي على مجموعة واحدة من الهيدروكسيل
- الصيغة الكيميائية: C3H8O.
وهنالك صورتان للبروبانول يعرفان بالمتماكبات.
- والمتماكبات مركبات كيميائية تحتوي على أنواع وأعداد متماثلة من الذرات ولكنها مختلفة من حيث التركيب الجزيئي ، وبالتالي من حيث الخصائص الكيميائية والفيزيائية.
- فمثلا يغلي أحد مماكبات البروبانول المعروف باسم البروبانول العادي أو 1ـ بروبانول أو الكحول البروبيلي العادي عند 98°م ويتجمد عند - 126°م.
- أما المماكب الآخر المعروف باسم الآيسوبروبانول أو 2ـ البروبانول أو الكحول الآيسوبروبيلي فيغلي عند 83°م ويتجمد عند -88°م،
الخواص الكيميائية[عدل]
- تتميز الرابطة بين الأوكسجين والهيدروجين في مجموعة الهيدروكسيل بالقطبية وبذلك تنعكس هذه الخاصية على خواص الكولات :
- تغلي الكحولات عند درجات غليان عالية مقارنة بالهيدروكربونات المطابقة ويعزى الارتفاع في درجة الغليان لتكوين روابط هيدروجينية بين الجزيئات مع بعضها البعض
- تذوب الكحولات البسيطة في الماء وتقل الذوبانية بازدياد الوزن الجزيئي
التحضير[عدل]
يصنع البروبانول العادي تجاريا من الإثيلين والغاز الاصطناعي وهو خليط من الهيدروجين وأول أكسيد الكربون في وجود حفاز هو الروديوم أو الكوبالت ، يستخدم الكحول البروبيلي في تحضير مواد كيميائية أخرى ، كما يستخدم مذيبًا للمواد اللاصقة المعروفة باسم الراتينج ، ينتج الآيزوبروبانول بتفاعل غاز البروبيلين وهو أحد مكونات خام البترول مع الماء في وجود فلز أو حامض بمثابة حفاز ، ويستخدم أساسًا في إنتاج الأسيتون (وهو مذيب صناعي معروف) كما يُستخدم للتنظيف وفي صناعة مستحضرات التجميل ومحاليل الغسيل. .[2]
- H2C=CH2 + CO + H2 → CH3CH2CH=O
- CH3CH2CH=O + H2 → CH3CH2CH2OH
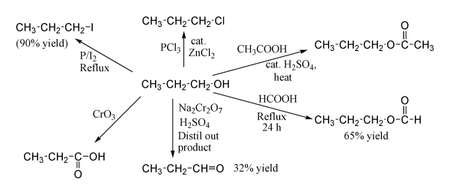
تفاعلات الكحولات[عدل]
- 1/ حمضية الكحولات (تكوين الأملاح)
نجد إن الكحول يشبه الماء في تركيبه ، لذلك يتفاعل مع فلزات المجموعة الأولى والثانية في الجدول الدوري ولكن بسرعة ابطا مقارنة بتفاعل الماء.
- 2/ تفاعل الكحولات مع هاليدات الهيدروجين
عند تفاعل الكحولات مع هاليدات الهيدروجين تتكون هاليدات الالكيل، ويتم التفاعل في وجود الحمض ونجد أن فاعلية الكحولات تجاه هاليدات الهيدروجين تكون كالأتي :الاولية ˃ الثانوية ˃الثالثية. فالكحول الثالثي يتفاعل مع حمض الهيدروكلوريك المخفف عند درجة حرارة الغرفة ، أما الكحول الأولي لا يتفاعل إلا مع حمض الهيدروكلوريك المركز مع التسخين.
- 3/ انتزاع الماء من الكحولات
يتم انتزاع الماء من الكحول لتكوين الالكين المقابل وذلك عند درجات حرارة عالية وبوجود تركيز عالي من حمض مثل الكبريتيك 0 ونجد أن الكحول الثالثي يتفاعل بسرعة أكثر مقارنة بالثانوي والأولي.
4/تكوين الاسترات
المراجع[عدل]
- ^ "1-Propanol - Compound Summary". PubChem Compound. USA: National Center for Biotechnology Inتنسيقion. 26 مارس 2005. Identification and Related Records. مؤرشف من الأصل في 2014-02-09. اطلع عليه بتاريخ 2011-10-10.
- ^ Anthony J. Papa "Propanols" in Ullmann’s Encyclopedia of Industrial Chemistry 2011, Wiley-VCH, Weinheim. دُوِي:10.1002/14356007.a22_173.pub2
قراءات اضافية[عدل]
- Furniss, B. S.; Hannaford, A. J.; Smith, P. W. G.; Tatchell, A. R. (1989)، Vogel's Textbook of Practical Organic Chemistry (ط. 5th)، Harlow: Longman، ISBN:0-582-46236-3
{{استشهاد}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - CRC Handbook of Chemistry and Physics, 87th الطبعة (ط. 87). TF-CRC. 26 يونيو 2006. ISBN:0-8493-0487-3.
{{استشهاد بكتاب}}: الوسيط غير المعروف|المحرر-الأخير=تم تجاهله (مساعدة) والوسيط غير المعروف|المحرر-الأول=تم تجاهله (مساعدة) - Maryadele J. O'Neil، المحرر (3 نوفمبر 2006). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (ط. 14). Merck. ISBN:0-911910-00-X.
- Perkin، W. H.؛ Kipping، F. S (1922). Organic Chemistry. London: W. & R. Chambers. ISBN:0-08-022354-0. مؤرشف من الأصل في 2008-12-13.
وصلات خارجية[عدل]
| 1-بروبانول في المشاريع الشقيقة: | |
| |




