مرض شلل الرعاش: الفرق بين النسختين
أُنشئَت بترجمة الصفحة "Parkinson's disease" |
(لا فرق)
|
نسخة 19:21، 2 مايو 2021
| Parkinson's disease | |
|---|---|
 Illustration of Parkinson's disease by William Richard Gowers, first published in A Manual of Diseases of the Nervous System (1886)
| |
| تسميات أخرى | Parkinson disease, idiopathic or primary parkinsonism, hypokinetic rigid syndrome, paralysis agitans, shaking palsy |
| معلومات عامة | |
| الاختصاص | Neurology |
| الأسباب | |
| الأسباب | Unknown[1] |
| عوامل الخطر | Pesticide exposure, head injuries[1] |
| المظهر السريري | |
| البداية المعتادة | Age over 60[2][3] |
| الأعراض | tremor, rigidity, slowness of movement, difficulty walking[2] |
| المضاعفات | Dementia, depression, anxiety[4] |
| الإدارة | |
| التشخيص | Based on symptoms[2] |
| العلاج | Medications, surgery[2] |
| أدوية | |
| المآل | Life expectancy about 7–15 years [5] |
| حالات مشابهة | Dementia with Lewy bodies, progressive supranuclear palsy, essential tremor, antipsychotic use[6] |
| الوبائيات | |
| انتشار المرض | 6.2 million (2015)[7] |
| الوفيات | 117,400 (2015)[8] |
| تعديل مصدري - تعديل | |
مرض باركنسون (PD) ، أو ببساطة مرض باركنسون ، هو اضطراب تنكسي طويل الأمد للجهاز العصبي المركزي يؤثر بشكل أساسي على الجهاز الحركي. عادة ما تظهر الأعراض ببطء ، ومع تفاقم المرض ، تصبح الأعراض غير الحركية أكثر شيوعًا. أكثر الأعراض المبكرة وضوحًا هي الرعاش ، والتصلب ، وبطء الحركة ، وصعوبة المشي. قد تحدث مشاكل معرفية وسلوكية أيضًا مع الاكتئاب والقلق واللامبالاة التي تحدث في كثير من الأشخاص المصابين بالباركنج. يصبح خرف مرض باركنسون شائعًا في المراحل المتقدمة من المرض. يمكن أن يعاني الأشخاص المصابون بمرض باركنسون أيضًا من مشاكل في النوم والأنظمة الحسية. تنجم الأعراض الحركية للمرض عن موت الخلايا في المادة السوداء ، وهي منطقة من الدماغ المتوسط ، مما يؤدي إلى عجز الدوبامين. سبب موت هذه الخلية غير مفهوم جيدًا ، ولكنه ينطوي على تراكم البروتينات المشوهة في أجسام ليوي في الخلايا العصبية. بشكل جماعي ، تُعرف الأعراض الحركية الرئيسية أيضًا باسم "باركنسون" أو "متلازمة باركنسون".
سبب PD غير معروف ، حيث يُعتقد أن العوامل الموروثة والبيئية تلعب دورًا. يتعرض الأشخاص المصابون بأحد أفراد الأسرة بمرض باركنسون لخطر متزايد للإصابة بالمرض ، مع وجود جينات معينة معروفة بأنها عوامل خطر وراثية. عوامل الخطر الأخرى هي أولئك الذين تعرضوا لبعض مبيدات الآفات والذين لديهم إصابات سابقة في الرأس. إن مدخني التبغ وشرب القهوة والشاي معرضون لخطر أقل.
يعتمد تشخيص الحالات النموذجية بشكل أساسي على الأعراض ، حيث الأعراض الحركية هي الشكوى الرئيسية. يمكن استخدام الاختبارات الخاصة بالتصوير العصبي (التصوير المغناطيسي أو التصوير الفوتوغرافي). يظهر المرض الذي سبق أن شعرت شهرته في واحد من هؤلاء الأشخاص الذين يعبرون عن شهر واحد منهم. نسبة ما تتأثر بأكثر من حوالي 3: 2. عندما يُشاهد عند الأشخاص قبل سن الخمسين ، يُطلق عليه اسم شلل الرعاش المبكر. البحث عام 2015 ، أثر مرض PD على 6.2 مليون شخص وأسفر عن حوالي 117400 حالة وفاة على مستوى العالم. متوسط العمر المتوقع بعد التشخيص ما بين 7 و 15 سنة.
لا يوجد علاج لمرض باركنسون ؛ يهدف العلاج إلى تحسين الأعراض. يكون العلاج الأولي عادةً باستخدام أدوية ليفودوبا (L-DOPA) أو مثبطات MAO-B أو ناهضات الدوبامين. مع تقدم المرض ، تصبح هذه الأدوية أقل فعالية ، بينما تنتج في نفس الوقت آثارًا جانبية تتميز بحركات العضلات اللاإرادية. في ذلك الوقت ، يمكن استخدام الأدوية معًا ويمكن زيادة الجرعات. أظهر النظام الغذائي وأشكال معينة من إعادة التأهيل بعض الفعالية في تحسين الأعراض. تم استخدام الجراحة لوضع أقطاب كهربائية دقيقة لتحفيز الدماغ العميق لتقليل الأعراض الحركية في الحالات الشديدة حيث تكون الأدوية غير فعالة. الأدلة على علاجات أعراض شلل الرعاش غير المرتبطة بالحركة ، مثل اضطرابات النوم والمشاكل العاطفية ، أقل قوة.
تمت تسمية المرض على اسم الطبيب الإنجليزي جيمس باركنسون ، الذي نشر أول وصف تفصيلي في An Essay on the Shaking Palsy ، في عام 1817. وتشمل حملات التوعية العامة اليوم العالمي لمرض باركنسون (في عيد ميلاد جيمس باركنسون ، 11 أبريل) واستخدام الخزامى الأحمر كرمز للمرض. الأشخاص المصابون بمرض باركنسون الذين زادوا من وعي الجمهور بهذه الحالة هم الملاكم محمد علي ، والممثل مايكل جيه فوكس ، والدراج الأولمبي ديفيس فيني ، والممثل آلان ألدا.
تصنيف
تمت تسمية المرض على اسم الطبيب الإنجليزي جيمس باركنسون ، الذي نشر أول وصف تفصيلي في An Essay on the Shaking Palsy ، في عام 1817. وتشمل حملات التوعية العامة اليوم العالمي لمرض باركنسون (في عيد ميلاد جيمس باركنسون ، 11 أبريل) واستخدام الخزامى الأحمر كرمز للمرض. الأشخاص المصابون بمرض باركنسون الذين زادوا من وعي الجمهور بهذه الحالة هم الملاكم محمد علي ، والممثل مايكل جيه فيوجد تداخل سريري ومرضي كبير بين اعتلالات تاوباثيات واعتلالات النسيج الخلوي ، ولكن هناك أيضًا اختلافات. على عكس مرض باركنسون ، يعاني الأشخاص المصابون بمرض الزهايمر غالبًا من فقدان الذاكرة. العلامات الأساسية لمرض باركنسون (البطء ، والرعشة ، والتصلب ، وعدم استقرار الوضع) ليست سمات طبيعية لمرض الزهايمر.وكس ، والدراج الأولمبي ديفيس فيني ، والممثل آلان ألدا.
بذلت محاولات لتصنيف مرض باركنسون إلى أنواع فرعية مختلفة ، مع التركيز على سن البداية ، وتطور الأعراض ، وهيمنة الرعاش. لم يتم اعتماد أي منها حاليًا على نطاق واسع كنموذج كامل

ب
بذلت محاولات لتصنيف مرض باركنسون إلى أنواع فرعية مختلفة ، مع التركيز على سن البداية ، وتطور الأعراض ، وهيمنة الرعاش. لم يتم اعتماد أي منها حاليًا على نطاق واسع كنموذج كامل
محرك
تعتبر أربعة أعراض حركية من العلامات الأساسية في شلل الرعاش: الرعاش ، وبطء الحركة (بطء الحركة) ، والصلابة ، وعدم استقرار الوضع.
أكثر علامات التقديم شيوعًا هي رعاش اليد البطيء الخشن أثناء الراحة والذي يختفي أثناء الحركة الإرادية للذراع المصابة وفي المراحل الأعمق من النوم. يظهر عادةً في يد واحدة فقط ، ويؤثر في النهاية على كلتا اليدين مع تقدم المرض. يتراوح تواتر الرعاش PD بين 4 و 6 هرتز (دورات في الثانية). تتمثل إحدى سمات الرعاش في دحرجة حبوب منع الحمل ، وميل السبابة والإبهام للمس والقيام بحركة دائرية معًا. المصطلح مشتق من التشابه بين حركة الأشخاص المصابين بالشلل الدماغي والتقنية الصيدلانية المبكرة لصنع الحبوب يدويًا.
بطء الحركة وجدت (بطء الحركة) في كل حالة من PD، وهذا يرجع إلى اضطرابات في التخطيط السيارات من بدء الحركة، وما يرتبط بها من يعانون من صعوبات على طول مجرى الإجراءات كله حركة، بدءا من التخطيط لبدء لتنفيذ حركة. ضعف أداء الحركة المتتابعة والمتزامنة. يعد بطء الحركة أكثر أعراض مرض باركنسون إعاقة مما يؤدي إلى صعوبات في المهام اليومية مثل ارتداء الملابس والتغذية والاستحمام. يؤدي إلى صعوبة خاصة في القيام بنشاطين حركيين مستقلين في نفس الوقت ويمكن أن يتفاقم بسبب الإجهاد العاطفي أو الأمراض المتزامنة. من المفارقات أن الأشخاص المصابين بمرض باركنسون يمكنهم في كثير من الأحيان ركوب الدراجة أو صعود السلالم بسهولة أكبر من المشي على مستوى. في حين أن معظم الأطباء قد يلاحظون بطء الحركة بسهولة ، فإن التقييم الرسمي يتطلب من الشخص القيام بحركات متكررة بأصابعه وقدميه.
الصلابة هي تصلب ومقاومة لحركة الأطراف ناتجة عن زيادة توتر العضلات ، والتقلص المفرط والمستمر للعضلات. في مرض باركنسون ، يمكن أن تكون الصلابة موحدة ، والمعروفة باسم "صلابة أنبوب الرصاص" ، أو السقاطة ، والمعروفة باسم "صلابة العجلة المسننة". يعتبر الجمع بين الرعاش والنغمة المتزايدة سببًا في صلابة العجلة المسننة. قد يترافق الصلابة مع آلام المفاصل. هذا الألم هو مظهر أولي متكرر للمرض. في المراحل المبكرة من مرض باركنسون ، غالبًا ما تكون الصلابة غير متكافئة وتميل إلى التأثير على عضلات العنق والكتف قبل عضلات الوجه والأطراف. مع تطور المرض ، يؤثر الصلابة عادة على الجسم كله ويقلل من القدرة على ذلك
يعتبر عدم استقرار الوضعية نموذجيًا في المراحل اللاحقة من المرض ، مما يؤدي إلى ضعف التوازن والسقوط المتكرر ، وثانيًا إلى كسور العظام وفقدان الثقة وتقليل الحركة. غالبًا ما يكون عدم الاستقرار غائبًا في المراحل الأولية ، خاصة عند الشباب ، خاصة قبل ظهور الأعراض الثنائية. ما يصل إلى 40٪ من الأشخاص الذين تم تشخيصهم بمرض باركنسون قد يعانون من السقوط وحوالي 10٪ قد يتعرضون للسقوط أسبوعياً ، ويرتبط عدد حالات السقوط بشدة شدة شلل الرعاش
تشمل العلامات والأعراض الحركية الأخرى المعترف بها اضطرابات المشي والوضعية مثل الاحتفالات (خطوات خلط سريعة ووضعية مائلة للأمام عند المشي بدون أرجوحة ذراع منحنية). تجميد المشي (اعتقالات قصيرة عندما يبدو أن القدمين عالقة على الأرض ، خاصة عند الدوران أو تغيير الاتجاه) ، والصوت الرتيب الهادئ ، وتعبيرات الوجه التي تشبه القناع ، والكتابة اليدوية التي تصبح أصغر وأصغر من العلامات الشائعة الأخرى.
يمكن أن يسبب مرض باركنسون اضطرابات نفسية عصبية ، والتي يمكن أن تتراوح من خفيفة إلى شديدة. وهذا يشمل اضطرابات الإدراك والمزاج والسلوك والفكر.
يمكن أن تحدث الاضطرابات المعرفية في المراحل المبكرة من المرض وأحيانًا قبل التشخيص ، وتزيد من انتشار المرض مع مدة المرض. يعد الخلل الوظيفي التنفيذي هو أكثر أنواع العجز المعرفي شيوعًا ، والذي يمكن أن يشمل مشاكل التخطيط والمرونة المعرفية والتفكير المجرد واكتساب القواعد وتثبيط الإجراءات غير الملائمة وبدء الإجراءات المناسبة والذاكرة العاملة والتحكم في الانتباه. تشمل الصعوبات المعرفية الأخرى سرعة المعالجة المعرفية البطيئة ، والتذكر الضعيف ، وضعف الإدراك وتقدير الوقت. ومع ذلك ، يظهر التحسن عندما يكون الاسترجاع مدعومًا بالإشارات. تعد الصعوبات الإبصارية المكانية أيضًا جزءًا من المرض ، حيث يُرى على سبيل المثال عندما يُطلب من الفرد إجراء اختبارات للتعرف على الوجه وإدراك اتجاه الخطوط المرسومة.
يعاني الشخص المصاب بالشلل الدماغي من خطر الإصابة بالخرف بمرتين إلى ستة أضعاف مقارنة بعامة السكان. يعاني ما يصل إلى 78٪ من المصابين بداء باركنسون من الخرف. يزداد انتشار الخرف مع تقدم العمر ، وبدرجة أقل ، مدة المرض. يرتبط الخرف بتدني نوعية الحياة لدى الأشخاص المصابين بالشلل الدماغي والقائمين على رعايتهم ، وزيادة معدل الوفيات ، واحتمال أكبر للحاجة إلى رعاية المسنين في المنزل.
يمكن أن تحدث اضطرابات السيطرة على الانفعالات ، بما في ذلك المقامرة المرضية ، والسلوك الجنسي القهري ، ونهم الأكل ، والتسوق القهري والكرم المتهور بسبب الأدوية ، وخاصة منبهات الدوبامين النشطة عن طريق الفم. تعد متلازمة خلل تنظيم الدوبامين - مع الحاجة إلى تناول الأدوية التي تؤدي إلى زيادة الجرعة - من المضاعفات النادرة لاستخدام ليفودوبا.
التقلص ، حيث تحدث سلوكيات نمطية معقدة ومتكررة وبلا هدف لعدة ساعات ، هو اضطراب آخر تسببه الأدوية المضادة لمرض باركنسون.
ذهان
يمكن اعتبار الذهان عرضًا ينتشر على أوسع نطاق له من 26 إلى 83٪. تحدث الهلوسة أو الأوهام لدى حوالي 50٪ من المصابين بالشلل الدماغي خلال فترة المرض ، وقد تنذر بظهور الخرف. تتراوح هذه من الهلوسة البسيطة - "الإحساس بالمرور" (شيء يمر بسرعة بجانب الشخص) أو "الإحساس بالوجود" (تصور شيء ما / شخص يقف على جانب الشخص أو خلفه) - إلى بصري مفعم بالحيوية ومُشَكَّل الهلوسة والتفكير بجنون العظمة. الهلوسة السمعية غير شائعة في شلل الرعاش ونادراً ما توصف بأنها أصوات. يُعتقد الآن أن الذهان جزء لا يتجزأ من المرض. الذهان المصحوب بالأوهام والهذيان المرتبط به هو أحد المضاعفات المعروفة للعلاج بالعقاقير المضادة لمرض باركنسون وقد ينتج أيضًا عن التهابات المسالك البولية (كما يحدث في كثير من الأحيان عند كبار السن الهشّين) ، لكن العقاقير والعدوى ليست العوامل الوحيدة ، وأمراض الدماغ الكامنة أو التغيرات في النواقل العصبية أو مستقبلاتها (مثل الأسيتيل كولين والسيروتونين) يُعتقد أيضًا أنها تلعب دورًا في الذهان في شلل الرعاش.
تعد التغيرات السلوكية والمزاجية أكثر شيوعًا في شلل الرعاش دون ضعف إدراكي مقارنةً بعموم السكان ، وعادةً ما تكون موجودة في شلل الرعاش مع الرف. الصعوبات المزاجية الأكثر شيوعًا هي الاكتئاب واللامبالاة والقلق .
تشير التقديرات إلى أن الاكتئاب يظهر في أي مكان من 20 إلى 35٪ من الأشخاص المصابين بشلل الرعاش ، ويمكن أن يظهر في أي مرحلة من مراحل المرض. في مرض باركنسون ، يمكن أن يظهر الاكتئاب مع أعراض شائعة في عملية المرض (التعب والأرق وصعوبة التركيز) مما يجعل التشخيص صعبًا. من المعروف أن اختلال التوازن والتغير في هرمونات الدوامين والسير وتونين والنورأدرينرجيك سبب رئيسي للاكتئاب لدى الأشخاص المصابين بمرض باركنسون. سبب آخر هو الضعف الوظيفي الذي يسببه المرض. يمكن أن تشمل أعراض الاكتئاب فقدان الاهتمام والحزن والشعور بالذنب ومشاعر العجز / اليأس / الذنب والتفكير الانتحاري. التفكير في الانتحار لدى الأشخاص المصابين بداء باركنسون أعلى منه لدى عامة السكان ، ولكن محاولات الانتحار نفسها أقل من الأشخاص المصابين بالاكتئاب غير المصابين باضطراب الشخصية الحادة. يمكن أن تشمل عوامل الخطر للاكتئاب في PD ظهور المرض تحت سن 50 ، كونك امرأة ، والتاريخ السابق للاكتئاب ، والأعراض الحركية الشديدة ، وغيرها.
تشير التقديرات إلى أن القلق ينتشر في الأشخاص المصابين بداء باركنسون بحوالي 30٪ -40٪ (ومع ذلك تم العثور على ما يصل إلى 60٪). غالبًا ما يمكن العثور على القلق خلال فترات "التوقف" (الفترات الزمنية التي لا يعمل فيها الدواء كما كان من قبل) مع الأشخاص المصابين بمرض شلل الرعاش الذين يعانون من نوبات الهلع بشكل متكرر مقارنةً بعامة السكان. تم العثور على كل من القلق والاكتئاب مرتبطين بانخفاض نوعية الحياة. يمكن أن تتراوح الأعراض من خفيفة وعرضية إلى مزمنة مع أسباب محتملة تتمثل في مستويات غير طبيعية من حمض جاما أمينوبوتيريك بالإضافة إلى الإحراج أو الخوف من الأعراض / المرض. عوامل الخطر للقلق في شلل الرعاش هي ظهور المرض تحت سن 50 ، والنساء ، وفترات "التوقف".
يمكن تعريف اللامبالاة وانعدام التلذذ على أنهما فقدان الدافع وضعف القدرة على تجربة المتعة ، على التوالي. إنها أعراض مرتبطة كلاسيكيًا بالاكتئاب ، ومع ذلك ، فهي تختلف في الأشخاص المتأثرين بشلل الرعاش في العلاج والآلية ولا تحدث دائمًا مع الاكتئاب. تظهر اللامبالاة في حوالي 16.5-40٪. تشمل أعراض اللامبالاة انخفاض المبادرة / الاهتمامات في الأنشطة الجديدة أو العالم من حولهم ، واللامبالاة العاطفية ، وفقدان المودة أو الاهتمام بالآخرين. ترتبط اللامبالاة بالعجز في الوظائف المعرفية بما في ذلك الذاكرة التنفيذية واللفظية.
آخر
تعتبر اضطرابات النوم سمة من سمات المرض ويمكن أن تتفاقم بسبب الأدوية. يمكن أن تظهر الأعراض على شكل نعاس أثناء النهار (بما في ذلك نوبات النوم المفاجئة التي تشبه التغفيق) ، أو اضطرابات نوم حركة العين السريعة ، أو الأرق. قد يبدأ اضطراب سلوك حركة العين السريعة (RBD) ، حيث يتصرف الناس بأحلام ، وأحيانًا يتسببون في إصابة أنفسهم أو شريكهم في الفراش ، قبل سنوات عديدة من تطور السمات الحركية أو ايمكن أن تؤدي التغييرات في الجهاز العصبي اللاإرادي إلى انخفاض ضغط الدم الانتصابي (انخفاض ضغط الدم عند الوقوف) ، والجلد الدهني والتعرق المفرط ، وسلس البول ، وتغير الوظيفة الجنسية. يمكن أن يكون الإمساك وضعف إفراغ المعدة (خلل الحركة في المعدة) شديدين بما يكفي للتسبب في عدم الراحة وحتى تعريض الصحة للخطر. قد تشمل التغييرات في الإدراك ضعف حاسة الشم ، واضطراب في الرؤية ، وألم ، وتنمل (وخز وتنميل). يمكن أن تحدث كل هذه الأعراض قبل سنوات من تشخيص المرض.لمعرفية للـ PD أو DLB.
يمكن أن تؤدي التغييرات في الجهاز العصبي اللاإرادي إلى انخفاض ضغط الدم الانتصابي (انخفاض ضغط الدم عند الوقوف) ، والجلد الدهني والتعرق المفرط ، وسلس البول ، وتغير الوظيفة الجنسية. يمكن أن يكون الإمساك وضعف إفراغ المعدة (خلل الحركة في المعدة) شديدين بما يكفي للتسبب في عدم الراحة وحتى تعريض الصحة للخطر. قد تشمل التغييرات في الإدراك ضعف حاسة الشم ، واضطراب في الرؤية ، وألم ، وتنمل (وخز وتنميل). يمكن أن تحدث كل هذه الأعراض قبل سنوات من تشخيص المرض.
الأسباب
تم اقتراح العديد من عوامل الخطر ، في بعض الأحيان فيما يتعلق بالنظريات المتعلقة بالآليات المحتملة للمرض ؛ ومع ذلك ، لم يتم إثبات أي منها بشكل قاطع. العلاقات الأكثر تكرارًا هي زيادة المخاطر لدى أولئك المعرضين لمبيدات الآفات ، وانخفاض المخاطر لدى المدخنين. هناك صلة محتملة بين عدوى PD و H. pylori التي يمكن أن تمنع امتصاص بعض الأدوية بما في ذلك ليفودوبا.
تم ربط كل من التعرض لمبيدات الآفات وتاريخ إصابة في الرأس بمرض باركنسون (PD) ، لكن المخاطر متواضعة. كما أن عدم تدخين السجائر مطلقًا وعدم شرب المشروبات التي تحتوي على الكافيين مطلقًا يرتبط أيضًا بزيادات طفيفة في خطر الإصابة بالشلل الرعاش
يرتبط انخفاض تركيزات اليورات في مصل الدم بزيادة خطر الإصابة بمرض شلل الرعاش. [11]
الشلل الرعاش الناجم عن المخدرات
تم استخدام عقاقير طبية مختلفة في حالات مرض باركنسون. الشلل الرعاش الناجم عن المخدرات يمكن عكسه عادة عن طريق إيقاف العامل المسيء. [12] تشمل الأدوية على سبيل المثال لا الحصر:
- الفينوثيازينات (كلوربرومازين ، برومازين ، إلخ.) بيوتيروفينونات (هالوبيريدول ، بينبيريدول ، إلخ.) ميتوكلوبراميد تترابينازين
1-methyl-4-phenyl-1،2،3،6-tetrahydropyridine (MPTP) هو دواء معروف بالتسبب في مرض باركنسون لا رجعة فيه ويستخدم بشكل شائع في أبحاث النماذج الحيوانية. [12] [13] [14]
مرض باركنسون الناجم عن السموم
علم الوراثة
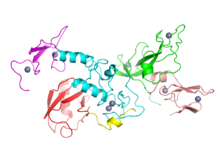
تشير الأبحاث إلى أن PD هو نتاج تفاعل معقد بين العوامل الوراثية والبيئية. حوالي 15٪ من الأفراد المصابين بمرض باركنسون لديهم قريب من الدرجة الأولى مصاب بالمرض ، ومن المعروف أن 5-10٪ من الأشخاص المصابين بهذا المرض لديهم أشكال من المرض تحدث بسبب طفرة في واحد من عدة جينات محددة. إن إيواء إحدى هذه الطفرات الجينية قد لا يؤدي إلى المرض ؛ تعرض عوامل الحساسية الفرد لخطر متزايد ، وغالبًا ما يكون مصحوبًا بعوامل خطر أخرى ، والتي تؤثر أيضًا على عمر البداية والشدة والتقدم. ما لا يقل عن 11 طفرة جسمية سائدة و 9 طفرات وراثية متنحية وراثية متورطة في تطوير PD. تشمل الجينات الصبغية السائدة SNCA و PARK3 و UCHL1 و LRRK2 و GIGYF2 و HTRA2 و EIF4G1 و TMEM230 و CHCHD2 و RIC3 و VPS35. تتضمن الجينات المتنحية الجسدية PRKN و PINK1 و PARK7 و ATP13A2 و PLA2G6 و FBXO7 و DNAJC6 و SYNJ1 و VPS13C. بعض الجينات مرتبطة بـ X أو لديها نمط وراثي غير معروف: وتشمل تلك الجينات PARK10 و PARK12 و PARK16. من المعروف أيضًا أن حذف 22q11 يرتبط بـ PD. ارتبط الشكل الصبغي الجسدي السائد بطفرات في جين LRP10.
يعاني حوالي 5٪ من المصابين بالشلل الدماغي من طفرات في جين GBA1. توجد هذه الطفرات في أقل من 1٪ من السكان غير المصابين. يزداد خطر الإصابة بـ PD 20-30 مرة إذا كانت هذه الطفرات موجودة. PD المرتبط بهذه الطفرات له نفس السمات السريرية ، ولكن في سن مبكرة وتراجع سريع في الإدراك والحركة. هذا الجين يشفر الجلوكوسيريبروسيداز . تسبب المستويات المنخفضة من هذا الإنزيم مرض جوشر .
تعتبر الطفرات الجينية SNCA مهمة في PD لأن البروتين الذي يشفره هذا الجين ، alpha-synuclein ، هو المكون الرئيسي لأجسام ليوي التي تتراكم في أدمغة الأشخاص المصابين بهذا المرض. ينشط Alpha-synuclein أجهزة الصراف الآلي (ترنح توسع الشعيرات المتحور) ، وهو ضرر رئيسي لإصلاح تلف الحمض النووي يشير إلى كيناز. بالإضافة إلى ذلك ، ينشط alpha-synuclein الطرف غير المتماثل الذي ينضم إلى مسار إصلاح الحمض النووي. يبدو أن تراكم ألفا سينوكلين في أجسام ليوي هو رابط بين انخفاض إصلاح الحمض النووي وموت خلايا الدماغ في شلل الرعاش.
تم العثور على الطفرات في بعض الجينات ، بما في ذلك SNCA ، LRRK2 و GBA ، ليكون من عوامل الخطر "متفرقة" (غير العائلي) PD. الطفرات في الجين LRRK2 هي السبب المعروف الأكثر شيوعًا للـ PD العائلي والمتقطع ، وهو ما يمثل حوالي 5٪ من الأفراد الذين لديهم تاريخ عائلي للمرض و 3٪ من الحالات المتفرقة. تمثل الطفرة في GBA أكبر خطر وراثي للإصابة بمرض باركنسون.
تشارك العديد من الجينات المرتبطة بمرض باركنسون في وظيفة الجسيمات الحالة ، وهي العضيات التي تهضم منتجات النفايات الخلوية. تم اقتراح أن بعض حالات شلل الرعاش قد تكون ناجمة عن الاضطرابات الليزوزومية التي تقلل من قدرة الخلايا على تكسير ألفا سينوكلين .
باركنسون الأوعية الدموية
تشمل الأسباب الأخرى المحددة لمرض باركنسون الالتهابات واضطراب التمثيل الغذائي. قد تظهر أيضًا العديد من الاضطرابات العصبية التنكسية مع مرض باركنسون ويشار إليها أحيانًا باسم "مرض باركنسون غير النموذجي" أو متلازمات "باركنسون بلس" (أمراض مصحوبة بمرض باركنسون بالإضافة إلى بعض السمات الأخرى التي تميزها عن شلل الرعاش). وهي تشمل الضمور الجهازي المتعدد ، والشلل فوق النووي التدريجي ، والتنكس القشري القاعدي ، والخرف بأجسام ليوي (DLB). [15] [16] يعد الخرف المصاحب لأجسام ليوي اعتلالًا غويًا آخر وله أوجه تشابه مرضية وثيقة مع شلل الرعاش ، خاصة مع مجموعة فرعية من حالات شلل الرعاش المصابة بالخرف المعروفة باسم مرض باركنسون. العلاقة بين PD و DLB معقدة وغير مفهومة تمامًا. [17] قد تمثل أجزاء من سلسلة متصلة ذات سمات سريرية ومرضية مميزة متغيرة أو قد تكون أمراضًا منفصلة.
الرئيسي المرضية خصائص PD هي موت الخلايا في الدماغ العقد القاعدية (يؤثر على ما يصل إلى 70٪ من الدوبامين إفراز الخلايا العصبية في المادة السوداء بارس المكتنزة بحلول نهاية الحياة). [18] في مرض باركنسون، ويصبح ألفا synuclein تتجمع و تتجمع معا مع الآخرين ألفا synuclein. الخلايا غير قادرة على إزالة هذه الكتل وتصبح ألفا سينوكلين سامة للخلايا ، مما يؤدي إلى إتلاف الخلايا. [19] [20] يمكن رؤية هذه الكتل في الخلايا العصبية تحت المجهر وتسمى أجسام ليوي . يترافق فقدان الخلايا العصبية مع موت الخلايا النجمية (الخلايا الدبقية على شكل نجمة) وزيادة كبيرة في عدد الخلايا الدبقية الصغيرة (نوع آخر من الخلايا الدبقية) في المادة السوداء. [21] يعد تصنيف براك طريقة لشرح تطور أجزاء الدماغ المصابة بمرض باركنسون. وفقًا لهذا التدريج ، يبدأ PD في النخاع والبصلة الشمية قبل الانتقال إلى المادة السوداء وبقية الدماغ المتوسط / الدماغ الأمامي. يرتبط ظهور أعراض الحركة عندما يبدأ المرض في التأثير على المادة السوداء بارس كومباكتا. [22]
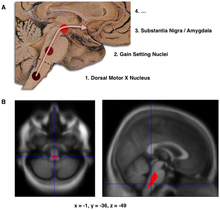
- Schematic initial progression of Lewy body deposits in the first stages of Parkinson's disease, as proposed by Braak and colleagues
- Localization of the area of significant brain volume reduction in initial PD compared with a group of participants without the disease in a neuroimaging study, which concluded that brainstem damage may be the first identifiable stage of PD neuropathology[23]
هناك خمسة مسارات رئيسية في الدماغ تربط مناطق الدماغ الأخرى بالعقد القاعدية. تُعرف هذه الدوائر بالمحرك ، ومحرك العين ، والدوائر الترابطية ، والحوفية ، والدوائر الأمامية المدارية ، مع أسماء تشير إلى منطقة الإسقاط الرئيسية لكل دائرة. [24] جميعهم مصابون بمرض شلل الرعاش ، واضطرابهم يفسر العديد من أعراض المرض ، حيث تشارك هذه الدوائر في مجموعة متنوعة من الوظائف ، بما في ذلك الحركة والانتباه والتعلم. علميًا ، تم فحص الدائرة الحركية بشكل مكثف.

كان للنموذج المفاهيمي الخاص للدائرة الحركية وتغييرها مع PD تأثير كبير منذ عام 1980 ، على الرغم من الإشارة إلى بعض القيود التي أدت إلى تعديلات. [24] في هذا النموذج ، تمارس العقد القاعدية عادةً تأثيرًا مثبطًا ثابتًا على مجموعة واسعة من الأنظمة الحركية ، مما يمنعها من أن تصبح نشطة في أوقات غير مناسبة. عندما يتم اتخاذ قرار بأداء إجراء معين ، يتم تقليل التثبيط لنظام المحرك المطلوب ، وبالتالي إطلاقه للتفعيل. يعمل الدوبامين على تسهيل إطلاق هذا التثبيط ، لذلك تميل المستويات العالية من وظيفة الدوبامين إلى تعزيز النشاط الحركي ، بينما تتطلب المستويات المنخفضة من وظيفة الدوبامين ، مثل التي تحدث في PD ، بذل جهد أكبر لأي حركة معينة. وبالتالي ، فإن التأثير الصافي لاستنفاد الدوبامين هو إحداث نقص في الحركة ، وهو انخفاض إجمالي في إنتاج المحرك. وعلى العكس من ذلك ، فإن الأدوية المستخدمة في علاج شلل الرعاش قد تنتج نشاطًا مفرطًا من الدوبامين ، مما يسمح بتنشيط الأنظمة الحركية في أوقات غير مناسبة وبالتالي إنتاج خلل الحركة .
هناك تكهنات حول العديد من الآليات التي يمكن من خلالها فقدان خلايا الدماغ. [25] تتكون إحدى الآليات من تراكم غير طبيعي لبروتين ألفا سينوكلين المرتبط بـ يوبيكويتين في الخلايا التالفة. يتراكم هذا البروتين غير القابل للذوبان داخل الخلايا العصبية مكونًا شوائب تسمى أجسام ليوي. [18] [26] وفقًا لتصنيف براك ، وهو تصنيف للمرض بناءً على النتائج المرضية التي اقترحها هيكو براك ، تظهر أجسام ليوي أولاً في البصلة الشمية ، والنخاع المستطيل ، والجسم الجسري ؛ قد يكون الأفراد في هذه المرحلة بدون أعراض أو قد يعانون من أعراض غير حركية مبكرة (مثل فقدان حاسة الشم ، أو بعض النوم أو اختلال وظيفي تلقائي). مع تقدم المرض ، تتطور أجسام ليوي في المادة السوداء ، ومناطق الدماغ المتوسط والدماغ الأمامي ، وأخيراً القشرة المخية الحديثة . هذه المواقع الدماغية هي الأماكن الرئيسية للتنكس العصبي في شلل الرعاش. ومع ذلك ، قد لا تسبب أجسام ليوي موت الخلايا وقد تكون وقائية (مع عزل البروتين غير الطبيعي أو عزله). قد تكون الأشكال الأخرى من ألفا سينوكلين (على سبيل المثال ، أوليغومرات ) غير المجمعة في أجسام ليوي وعصابات ليوي هي الأشكال السامة للبروتين. في الأشخاص المصابين بالخرف ، يعد الوجود العام لأجسام ليوي أمرًا شائعًا في المناطق القشرية. التشابك الليفي العصبي ولويحات الشيخوخة ، المميزة لمرض الزهايمر ، ليست شائعة ما لم يكن الشخص مصابًا بالخرف. [21]
وتشمل آليات الخلية الموت أخرى proteasomal و الليزوزومية ضعف النظام وخفض الميتوكوندريا النشاط. [25] عادة ما يتم ملاحظة تراكم الحديد في المادة السوداء بالتزامن مع شوائب البروتين. قد يكون مرتبطًا بالإجهاد التأكسدي وتجمع البروتين وموت الخلايا العصبية ، لكن الآليات ليست مفهومة تمامًا. [27]
سيقوم الطبيب في البداية بتقييم مرض باركنسون من خلال تاريخ طبي دقيق وفحص عصبي . [28] يتم التركيز على تأكيد الأعراض الحركية (بطء الحركة ، ورعاش الراحة ، وما إلى ذلك) ودعم الاختبارات بمعايير التشخيص السريري التي تتم مناقشتها أدناه. عادةً ما يُعتبر العثور على جثث ليوي في الدماغ المتوسط عند تشريح الجثة دليلًا نهائيًا على إصابة الشخص بمرض شلل الرعاش. قد يكشف المسار السريري للمرض بمرور الوقت أنه ليس مرض باركنسون ، مما يتطلب مراجعة العرض السريري بشكل دوري للتأكد من دقة التشخيص. [29]
يمكن أن تكون هناك أسباب متعددة لمرض باركنسون أو أمراض تبدو متشابهة. يمكن أن تسبب السكتة الدماغية وبعض الأدوية والسموم "باركنسون ثانوي" ويجب تقييمها أثناء الزيارة. [22] [29] يجب أيضًا مراعاة متلازمات باركنسون بلس ، مثل الشلل فوق النووي التدريجي وضمور الأجهزة المتعددة ، واستبعادها بشكل مناسب بسبب اختلاف العلاج وتطور المرض (الأدوية المضادة لمرض باركنسون عادةً ما تكون أقل فعالية في السيطرة على الأعراض في متلازمات باركنسون زائد). [28] قد تشير معدلات التقدم الأسرع ، أو الخلل المعرفي المبكر أو عدم الاستقرار الوضعي ، أو الحد الأدنى من الرعاش ، أو التماثل في البداية إلى مرض باركنسون بلس بدلاً من مرض باركنسون نفسه. [30]
وضعت المنظمات الطبية معايير تشخيصية لتسهيل عملية التشخيص وتوحيدها ، خاصة في المراحل المبكرة من المرض. تأتي المعايير الأكثر شهرة على نطاق واسع من بنك كوين سكوير للمخ في المملكة المتحدة للاضطرابات العصبية والمعهد الوطني الأمريكي للاضطرابات العصبية والسكتة الدماغية . تتطلب معايير Queen Square Brain Bank بطئًا في الحركة (بطء الحركة) بالإضافة إلى الصلابة أو الهزة أثناء الراحة أو عدم الاستقرار الوضعي. يجب استبعاد الأسباب المحتملة الأخرى لهذه الأعراض. أخيرًا ، هناك حاجة إلى ثلاثة أو أكثر من السمات الداعمة التالية أثناء البداية أو التطور: ظهور أحادي الجانب ، ورعاش أثناء الراحة ، والتقدم في الوقت المناسب ، وعدم تناسق الأعراض الحركية ، والاستجابة لليفودوبا لمدة خمس سنوات على الأقل ، ودورة سريرية لمدة عشر سنوات على الأقل و ظهور خلل الحركة الناجم عن تناول ليفودوبا المفرط. [31]
عندما يتم فحص تشخيصات شلل الرعاش عن طريق تشريح الجثة ، وجد خبراء اضطرابات الحركة في المتوسط أنهم دقيقون بنسبة 79.6٪ في التقييم الأولي و 83.9٪ بعد أن قاموا بتنقيح تشخيصهم في فحص المتابعة. عندما يتم فحص التشخيصات السريرية التي يتم إجراؤها بشكل رئيسي من قبل غير الخبراء عن طريق التشريح ، يكون متوسط الدقة 73.8٪. بشكل عام ، 80.6٪ من تشخيصات شلل الرعاش دقيقة ، و 82.7٪ من التشخيصات باستخدام معايير بنك الدماغ دقيقة. [32]
عادةً ما تبدو فحوصات التصوير المقطعي المحوسب (CT) للمصابين بالشلل الدماغي طبيعية. [33] أصبح التصوير بالرنين المغناطيسي أكثر دقة في تشخيص المرض بمرور الوقت ، وتحديداً من خلال تسلسل T2 * و SWI الحساس للحديد عند شدة مجال مغناطيسي لا تقل عن 3 تيرابايت ، وكلاهما يمكن أن يبرهن على عدم وجود نمط تصوير "ذيل السنونو" المميز في المادة الظهرية الوحشية السوداء. [34] في التحليل التلوي، كان غياب هذا النمط غاية الحساسية و محدد لهذا المرض. [35] وجد التحليل التلوي لعام 2020 أن neuromelanin-MRI كان له أداء تشخيصي إيجابي في التمييز بين الأفراد المصابين بمرض باركنسون والأشخاص الأصحاء. [36] أظهر التصوير بالرنين المغناطيسي للانتشار إمكانية التمييز بين متلازمات شلل الرعاش ومتلازمات باركنسون بلس ، على الرغم من أن قيمته التشخيصية لا تزال قيد التحقيق. يستخدم التصوير المقطعي والتصوير بالرنين المغناطيسي أيضًا لاستبعاد الأمراض الأخرى التي يمكن أن تكون أسبابًا ثانوية لمرض باركنسون ، والأكثر شيوعًا التهاب الدماغ والإهانات الإقفارية المزمنة ، بالإضافة إلى الكيانات الأقل شيوعًا مثل أورام العقد القاعدية واستسقاء الرأس .
يمكن قياس النشاط الأيضي لناقلات الدوبامين في العقد القاعدية مباشرةً باستخدام التصوير المقطعي بالإصدار البوزيتروني والتصوير المقطعي المحوسب بإصدار فوتون واحد ، مع كون DaTSCAN نسخة ملكية شائعة لهذه الدراسة. لقد أظهر توافقًا كبيرًا مع التشخيصات السريرية لمرض باركنسون. [37] يمكن أن يساعد انخفاض النشاط المرتبط بالدوبامين في العقد القاعدية في استبعاد مرض باركنسون الناجم عن المخدرات. ومع ذلك ، فإن هذه النتيجة ليست محددة تمامًا ، ويمكن رؤيتها في كل من اضطرابات باركنسون وباركنسون. [33] في الولايات المتحدة ، تمت الموافقة على DaTSCANs فقط من قِبل إدارة الأغذية والعقاقير (FDA) لتمييز مرض باركنسون أو متلازمات باركنسون عن الرعاش الأساسي . [38]
يمكن أن يساعد التصوير الومضاني لعضلة القلب باليود -123-يودوبنزيل جوانيدين في العثور على إزالة العصب من الأعصاب حول القلب ، والتي يمكن أن تدعم تشخيص مرض باركنسون. [22]
الشلل الرعاش الثانوي - يمكن أن يكون هناك أسباب متعددة لمرض باركنسون بما في ذلك الأدوية والسموم وحوادث الأوعية الدموية (مثل السكتات الدماغية). يمكن التمييز بينها وبين التاريخ الدقيق والتصوير الجسدي والتصوير المناسب. [12] [22] [39] تمت مناقشة هذا الموضوع بمزيد من التفصيل في قسم الأسباب هنا .
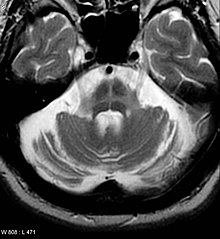
متلازمة باركنسون بلس - يمكن اعتبار الأمراض المتعددة جزءًا من مجموعة باركنسون بلس ، بما في ذلك متلازمة القشرة القاعدية ، وضمور الجهاز المتعدد ، والشلل فوق النووي التدريجي ، والخرف مع الأجسام الليفية . يمكن تضييق نطاق التشخيص التفريقي من خلال التاريخ الدقيق والجسدي (يركز بشكل خاص على ظهور أعراض محددة) ، وتطور المرض ، والاستجابة للعلاج. [40] [39] بعض الميزات الرئيسية بينهما: [12]
- متلازمة كورتيكوباسال - مقاومة ليفودوبا ، رمع عضلي ، خلل التوتر ، فقدان حسي قشري ، تعذر الأداء ، وحبسة غير طلاقة .
- الضمور الجهازي المتعدد - مقاومة ليفودوبا ، التقدم السريع ، الفشل اللاإرادي ، الصرير ، علامة بابينسكي الحالية ، ترنح المخيخ ، ونتائج التصوير بالرنين المغناطيسي المحددة.
- الشلل فوق النووي التقدمي - مقاومة ليفودوبا ، والنظرة العمودية التقييدية ، ونتائج التصوير بالرنين المغناطيسي المحددة ، والصعوبات المبكرة والمختلفة في الوضع.
- الخرف المصحوب بأجسام ليوي - مقاومة ليفودوبا ، والهيمنة المعرفية قبل الأعراض الحركية ، وأعراض الحمل المتقلبة. تعتبر الهلوسة البصرية شائعة جدًا في هذا المرض ولكن يمكن أن يعاني منها مرضى شلل الرعاش أيضًا.
الرعاش مجهول السبب - يمكن أن يبدو الرعاش مجهول السبب للوهلة الأولى مثل مرض باركنسون ، ومع ذلك ، هناك عوامل تفاضل رئيسية. في الرعاش مجهول السبب ، سيزداد الرعاش سوءًا مع العمل (حيث يتحسن في PD) ، سيكون هناك نقص في الأعراض الأخرى الشائعة في PD ، و DatSCAN الطبيعي. [39] [12]
الوقاية
قد تقلل ممارسة الرياضة في منتصف العمر من خطر الإصابة بمرض باركنسون في وقت لاحق من الحياة. [41] يبدو الكافيين أيضًا وقائيًا مع انخفاض أكبر في المخاطر التي تحدث مع تناول كميات أكبر من المشروبات التي تحتوي على الكافيين مثل القهوة. [42] الأشخاص الذين يدخنون السجائر أو يستخدمون التبغ غير المُدخَّن أقل عرضة من غير المدخنين للإصابة بمرض شلل الرعاش ، وكلما زاد استخدامهم للتبغ ، قلت احتمالية إصابتهم بمرض شلل الرعاش. من غير المعروف ما الذي يقوم عليه هذا التأثير. قد يؤدي استخدام التبغ في الواقع إلى الحماية من شلل الرعاش ، أو قد يكون هناك عامل غير معروف يزيد من خطر الإصابة بشلل الرعاش ويسبب النفور من التبغ أو يجعل من السهل التوقف عن استخدام التبغ. [43] [44]

لا يوجد علاج معروف لمرض باركنسون. قد توفر الأدوية والجراحة والعلاج الطبيعي الراحة وتحسن نوعية حياة الشخص وتكون أكثر فعالية بكثير من العلاجات المتاحة للاضطرابات العصبية الأخرى مثل مرض الزهايمر ومرض الخلايا العصبية الحركية ومتلازمات باركنسون بلس . العائلات الرئيسية للأدوية المفيدة لعلاج الأعراض الحركية هي الليفودوبا دائمًا مع مثبط dopa decarboxylase وأحيانًا أيضًا مع مثبط COMT ومنبهات الدوبامين ومثبطات MAO-B . تحدد مرحلة المرض والعمر عند ظهور المرض المجموعة الأكثر فائدة. [45]
يعطي تصنيف براك لمرض باركنسون ست مراحل يمكن استخدامها لتحديد المراحل المبكرة والمراحل المتأخرة والمراحل المتأخرة. المرحلة الأولية التي تم فيها تطوير بعض الإعاقة بالفعل وتتطلب علاجًا دوائيًا تتبعها مراحل لاحقة مرتبطة بتطور المضاعفات المتعلقة باستخدام ليفودوبا ، ومرحلة ثالثة قد تسود فيها أعراض لا علاقة لها بنقص الدوبامين أو علاج ليفودوبا. [46]
يهدف العلاج في المرحلة الأولى إلى المقايضة المثلى بين التحكم في الأعراض والآثار الجانبية للعلاج. قد يتم تأجيل بدء علاج ليفودوبا عن طريق استخدام أدوية أخرى في البداية مثل مثبطات MAO-B ومنبهات الدوبامين ، على أمل تأخير ظهور المضاعفات بسبب استخدام ليفودوبا. [47] ومع ذلك ، لا يزال ليفودوبا هو العلاج الأكثر فاعلية للأعراض الحركية لمرض شلل الرعاش ويجب ألا يتأخر عند الأشخاص عندما تتأثر جودة حياتهم. يرتبط خلل الحركة المرتبط بليفودوبا ارتباطًا وثيقًا بمدة المرض وشدته أكثر من مدة علاج ليفودوبا ، لذا فإن تأخير هذا العلاج قد لا يوفر وقتًا أطول بكثير من الاستخدام المبكر لخلل الحركة. [48]
في المراحل اللاحقة ، يكون الهدف هو تقليل أعراض شلل الرعاش مع التحكم في التقلبات في تأثير الدواء. يجب إدارة الانسحابات المفاجئة من الأدوية أو الإفراط في استخدامها. [47] عندما لا تكون الأدوية الفموية كافية للسيطرة على الأعراض ، قد تكون الجراحة ، والتحفيز العميق للدماغ ، وحقن الأبومورفين تحت الجلد في يوم الاستيقاظ ومضخات الدوبا المعوية مفيدة. تقدم المرحلة المتأخرة من شلل الرعاش العديد من التحديات التي تتطلب مجموعة متنوعة من العلاجات بما في ذلك الأعراض النفسية وخاصة الاكتئاب وانخفاض ضغط الدم الانتصابي وضعف المثانة وضعف الانتصاب . [49] في المراحل الأخيرة من المرض ، يتم توفير الرعاية التلطيفية لتحسين نوعية حياة الشخص. [50]
- ^ ا ب اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعLancet2015 - ^ ا ب ج د اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعNIH2016 - ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعCar2016 - ^ ا ب اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعSv2016 - ^ Macleod AD، Taylor KS، Counsell CE (نوفمبر 2014). "Mortality in Parkinson's disease: a systematic review and meta-analysis". Movement Disorders. ج. 29 ع. 13: 1615–22. DOI:10.1002/mds.25898. PMID:24821648.
- ^ Ferri FF (2010). "Chapter P". Ferri's differential diagnosis : a practical guide to the differential diagnosis of symptoms, signs, and clinical disorders (ط. 2nd). Philadelphia, PA: Elsevier/Mosby. ISBN:978-0323076999.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعGBD2015Pre - ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعGBD2015De - ^ Photo by Arthur Londe from Nouvelle Iconographie de la Salpètrière, vol. 5, p. 226
- ^ Charcot، Jean-Martin؛ Sigerson، George (1879). Lectures on the diseases of the nervous system (ط. Second). Philadelphia: Henry C. Lea. ص. 113.
The strokes forming the letters are very irregular and sinuous, whilst the irregularities and sinuosities are of a very limited width. (...) the down-strokes are all, with the exception of the first letter, made with comparative firmness and are, in fact, nearly normal – the finer up-strokes, on the contrary, are all tremulous in appearance (...).
- ^ "Blood-based biomarkers for Parkinson's disease". Parkinsonism & Related Disorders. 20 Suppl 1: S99–103. يناير 2014. DOI:10.1016/S1353-8020(13)70025-7. PMID:24262199.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ ا ب ج د ه Simon، Roger؛ Aminoff؛ Greenberg (2017). Clinical Neurology (ط. 10). The United States of America: McGraw-Hill. ISBN:978-1-259-86172-7.Simon, Roger; Aminoff; Greenberg (2017). Clinical Neurology (10 ed.). The United States of America: McGraw-Hill. ISBN 978-1-259-86172-7. وسم
<ref>غير صالح؛ الاسم ":0" معرف أكثر من مرة بمحتويات مختلفة. - ^ Langston، J. William (6 مارس 2017). "The MPTP Story". Journal of Parkinson's Disease. ج. 7 ع. s1: S11–S19. DOI:10.3233/JPD-179006. PMID:28282815.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Song, Liang; Xu, Meng-Bei; Zhou, Xiao-Li; Zhang, Dao-pei; Zhang, Shu-ling; Zheng, Guo-qing (2017). "A Preclinical Systematic Review of Ginsenoside-Rg1 in Experimental Parkinson's Disease". Oxidative Medicine and Cellular Longevity (بالإنجليزية). 2017: 1–14. DOI:10.1155/2017/2163053. ISSN:1942-0900. PMID:28386306.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(help)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Parkinson's disease". Lancet. ج. 363 ع. 9423: 1783–93. مايو 2004. DOI:10.1016/S0140-6736(04)16305-8. PMID:15172778.
- ^ "Genetic etiology of Parkinson disease associated with mutations in the SNCA, PARK2, PINK1, PARK7, and LRRK2 genes: a mutation update". Human Mutation. ج. 31 ع. 7: 763–80. يوليو 2010 [18 May 2010]. DOI:10.1002/humu.21277. PMID:20506312.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Parkinson's disease dementia and dementia with Lewy bodies: different aspects of one entity". International Psychogeriatrics. ج. 21 ع. 2: 216–19. أبريل 2009 [28 January 2009]. DOI:10.1017/S1041610208008612. PMID:19173762.
- ^ ا ب "A review of Parkinson's disease". British Medical Bulletin. ج. 86 ع. 1: 109–27. 2008. DOI:10.1093/bmb/ldn013. PMID:18398010.Davie CA (2008). "A review of Parkinson's disease". British Medical Bulletin. 86 (1): 109–27. doi:10.1093/bmb/ldn013. PMID 18398010. وسم
<ref>غير صالح؛ الاسم "pmid18398010" معرف أكثر من مرة بمحتويات مختلفة. - ^ Villar-Piqué, Anna; Lopes da Fonseca, Tomás; Outeiro, Tiago Fleming (Oct 2016). "Structure, function and toxicity of alpha-synuclein: the Bermuda triangle in synucleinopathies". Journal of Neurochemistry (بالإنجليزية). 139: 240–255. DOI:10.1111/jnc.13249. PMID:26190401.
- ^ Burré، Jacqueline؛ Sharma، Manu؛ Südhof، Thomas C. (1 مارس 2018). "Cell Biology and Pathophysiology of α-Synuclein". Cold Spring Harbor Perspectives in Medicine. ج. 8 ع. 3: a024091. DOI:10.1101/cshperspect.a024091. ISSN:2157-1422. PMID:28108534.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ ا ب "Neuropathology of movement disorders". Parkinson's disease and movement disorders. Hagerstown, MD: Lippincott Williams & Wilkins. 2007. ص. 271–83. ISBN:978-0-7817-7881-7.Dickson DV (2007). "Neuropathology of movement disorders". In Tolosa E, Jankovic JJ (eds.). Parkinson's disease and movement disorders. Hagerstown, MD: Lippincott Williams & Wilkins. pp. 271–83. ISBN 978-0-7817-7881-7. وسم
<ref>غير صالح؛ الاسم "Jankovic_book-Neuropathology" معرف أكثر من مرة بمحتويات مختلفة. - ^ ا ب ج د Armstrong, Melissa J.; Okun, Michael S. (11 Feb 2020). "Diagnosis and Treatment of Parkinson Disease: A Review". JAMA (بالإنجليزية). 323 (6): 548–560. DOI:10.1001/jama.2019.22360. ISSN:0098-7484. PMID:32044947.Armstrong, Melissa J.; Okun, Michael S. (11 February 2020). "Diagnosis and Treatment of Parkinson Disease: A Review". JAMA. 323 (6): 548–560. doi:10.1001/jama.2019.22360. ISSN 0098-7484. PMID 32044947. وسم
<ref>غير صالح؛ الاسم ":1" معرف أكثر من مرة بمحتويات مختلفة. - ^ Jubault T، Brambati SM، Degroot C، Kullmann B، Strafella AP، Lafontaine AL، Chouinard S، Monchi O (ديسمبر 2009). Gendelman HE (المحرر). "Regional brain stem atrophy in idiopathic Parkinson's disease detected by anatomical MRI". PLOS ONE. ج. 4 ع. 12: e8247. Bibcode:2009PLoSO...4.8247J. DOI:10.1371/journal.pone.0008247. PMC:2784293. PMID:20011063.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ ا ب "Functional organization of the basal ganglia: therapeutic implications for Parkinson's disease". Movement Disorders. 23 Suppl 3 ع. Suppl 3: S548–59. 2008. DOI:10.1002/mds.22062. PMID:18781672.Obeso JA, Rodríguez-Oroz MC, Benitez-Temino B, Blesa FJ, Guridi J, Marin C, Rodriguez M (2008). "Functional organization of the basal ganglia: therapeutic implications for Parkinson's disease". Movement Disorders. 23 Suppl 3 (Suppl 3): S548–59. doi:10.1002/mds.22062. PMID 18781672. S2CID 13186083. وسم
<ref>غير صالح؛ الاسم "pmid18781672" معرف أكثر من مرة بمحتويات مختلفة. - ^ ا ب "Missing pieces in the Parkinson's disease puzzle". Nature Medicine. ج. 16 ع. 6: 653–61. يونيو 2010. DOI:10.1038/nm.2165. PMID:20495568.Obeso JA, Rodriguez-Oroz MC, Goetz CG, et al. (June 2010). "Missing pieces in the Parkinson's disease puzzle". Nature Medicine. 16 (6): 653–61. doi:10.1038/nm.2165. PMID 20495568. S2CID 3146438. وسم
<ref>غير صالح؛ الاسم "pmid20495568" معرف أكثر من مرة بمحتويات مختلفة. - ^ "The synaptic pathology of alpha-synuclein aggregation in dementia with Lewy bodies, Parkinson's disease and Parkinson's disease dementia". Acta Neuropathologica. ج. 120 ع. 2: 131–43. أغسطس 2010. DOI:10.1007/s00401-010-0711-0. PMID:20563819.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Iron transport in Parkinson's disease". Parkinsonism & Related Disorders. 15 Suppl 3 ع. Suppl 3: S209–11. ديسمبر 2009. DOI:10.1016/S1353-8020(09)70816-8. PMID:20082992.
- ^ ا ب "Parkinson's disease: clinical features and diagnosis". Journal of Neurology, Neurosurgery, and Psychiatry. ج. 79 ع. 4: 368–76. أبريل 2008. DOI:10.1136/jnnp.2007.131045. PMID:18344392. مؤرشف من الأصل في 2015-08-19.Jankovic J (April 2008). "Parkinson's disease: clinical features and diagnosis". Journal of Neurology, Neurosurgery, and Psychiatry. 79 (4): 368–76. doi:10.1136/jnnp.2007.131045. PMID 18344392. Archived from the original on 19 August 2015. وسم
<ref>غير صالح؛ الاسم "Jankovic2008" معرف أكثر من مرة بمحتويات مختلفة. - ^ ا ب The National Collaborating Centre for Chronic Conditions، المحرر (2006). "Diagnosing Parkinson's Disease". Parkinson's Disease. London: Royal College of Physicians. ص. 29–47. ISBN:978-1-86016-283-1.
{{استشهاد بكتاب}}: الوسيط|archiveurl=بحاجة لـ|مسار=(مساعدة)، الوسيط غير المعروف|chapterurl=تم تجاهله يقترح استخدام|مسار الفصل=(مساعدة)، وروابط خارجية في|chapterurl=<ref>غير صالح؛ الاسم "Nice-Diagnosis" معرف أكثر من مرة بمحتويات مختلفة. - ^ "The differential diagnosis of Parkinson's disease". European Journal of Neurology. 9 Suppl 3 ع. Suppl 3: 23–30. نوفمبر 2002. DOI:10.1046/j.1468-1331.9.s3.3.x. PMID:12464118.
- ^ "The relevance of the Lewy body to the pathogenesis of idiopathic Parkinson's disease". Journal of Neurology, Neurosurgery, and Psychiatry. ج. 51 ع. 6: 745–52. يونيو 1988. DOI:10.1136/jnnp.51.6.745. PMID:2841426.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Accuracy of clinical diagnosis of Parkinson disease: A systematic review and meta-analysis". Neurology. ج. 86 ع. 6: 566–76. فبراير 2016. DOI:10.1212/WNL.0000000000002350. PMID:26764028.
- ^ ا ب "Imaging approaches to Parkinson disease". Journal of Nuclear Medicine. ج. 51 ع. 4: 596–609. أبريل 2010. DOI:10.2967/jnumed.108.059998. PMID:20351351.Brooks DJ (April 2010). "Imaging approaches to Parkinson disease". Journal of Nuclear Medicine. 51 (4): 596–609. doi:10.2967/jnumed.108.059998. PMID 20351351. وسم
<ref>غير صالح؛ الاسم "pmid20351351" معرف أكثر من مرة بمحتويات مختلفة. - ^ "The 'swallow tail' appearance of the healthy nigrosome – a new accurate test of Parkinson's disease: a case-control and retrospective cross-sectional MRI study at 3T". PLOS ONE. ج. 9 ع. 4: e93814. 2014. Bibcode:2014PLoSO...993814S. DOI:10.1371/journal.pone.0093814. PMID:24710392.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Meta-analysis of dorsolateral nigral hyperintensity on magnetic resonance imaging as a marker for Parkinson's disease". Movement Disorders. ج. 32 ع. 4: 619–23. أبريل 2017. DOI:10.1002/mds.26932. PMID:28151553.
- ^ "Diagnostic performance of neuromelanin-sensitive magnetic resonance imaging for patients with Parkinson's disease and factor analysis for its heterogeneity: a systematic review and meta-analysis". European Radiology. ج. 30 ع. 10: 1–13. سبتمبر 2020. DOI:10.1007/s00330-020-07240-7. PMID:32886201.
- ^ "The diagnostic accuracy of dopamine transporter SPECT imaging to detect nigrostriatal cell loss in patients with Parkinson's disease or clinically uncertain parkinsonism: a systematic review". EJNMMI Research. ج. 5: 12. 2015. DOI:10.1186/s13550-015-0087-1. PMID:25853018.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "DaTSCAN Approval Letter" (PDF). FDA.gov. Food and Drug Administration. اطلع عليه بتاريخ 2019-03-22.
- ^ ا ب ج John Van Geest Centre for Brain Repair, Department of Clinical Neurosciences, University of Cambridge, UK؛ Greenland، Julia C.؛ Barker، Roger A.؛ John Van Geest Centre for Brain Repair, Department of Clinical Neurosciences, University of Cambridge, UK (22 ديسمبر 2018)، John Van Geest Centre for Brain Repair, Department of Clinical Neurosciences, University of Cambridge, UK؛ Stoker، Thomas B.؛ Greenland، Julia C.؛ John Van Geest Centre for Brain Repair, Department of Clinical Neurosciences, University of Cambridge, UK (المحررون)، "The Differential Diagnosis of Parkinson's Disease"، Parkinson’s Disease: Pathogenesis and Clinical Aspects، Codon Publications: 109–128، DOI:10.15586/codonpublications.parkinsonsdisease.2018.ch6، ISBN:978-0-9944381-6-4، اطلع عليه بتاريخ 2021-01-27
{{استشهاد}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)John Van Geest Centre for Brain Repair, Department of Clinical Neurosciences, University of Cambridge, UK; Greenland, Julia C.; Barker, Roger A.; John Van Geest Centre for Brain Repair, Department of Clinical Neurosciences, University of Cambridge, UK (22 December 2018), John Van Geest Centre for Brain Repair, Department of Clinical Neurosciences, University of Cambridge, UK; Stoker, Thomas B.; Greenland, Julia C.; John Van Geest Centre for Brain Repair, Department of Clinical Neurosciences, University of Cambridge, UK (eds.), "The Differential Diagnosis of Parkinson's Disease", Parkinson’s Disease: Pathogenesis and Clinical Aspects, Codon Publications, pp. 109–128, doi:10.15586/codonpublications.parkinsonsdisease.2018.ch6, ISBN 978-0-9944381-6-4, retrieved 27 January 2021CS1 maint: multiple names: authors list (link) وسم<ref>غير صالح؛ الاسم ":11" معرف أكثر من مرة بمحتويات مختلفة. - ^ Levin، Johannes؛ Kurz، Alexander؛ Arzberger، Thomas؛ Giese، Armin؛ Höglinger، Günter U. (5 فبراير 2016). "The Differential Diagnosis and Treatment of Atypical Parkinsonism". Deutsches Ärzteblatt International. ج. 113 ع. 5: 61–69. DOI:10.3238/arztebl.2016.0061. ISSN:1866-0452. PMID:26900156.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Does vigorous exercise have a neuroprotective effect in Parkinson disease?". Neurology. ج. 77 ع. 3: 288–94. يوليو 2011. DOI:10.1212/wnl.0b013e318225ab66. PMID:21768599.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Caffeine exposure and the risk of Parkinson's disease: a systematic review and meta-analysis of observational studies". Journal of Alzheimer's Disease. 20 Suppl 1 ع. Suppl 1: S221–38. 2010. DOI:10.3233/JAD-2010-091525. PMID:20182023.
- ^ "Nicotine from cigarette smoking and diet and Parkinson disease: a review". Translational Neurodegeneration. ج. 6: 18. 2017. DOI:10.1186/s40035-017-0090-8. PMID:28680589.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "The Emerging Evidence of the Parkinson Pandemic". J Parkinsons Dis (Review). ج. 8 ع. s1: S3–8. 2018. DOI:10.3233/JPD-181474. PMID:30584159.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Pharmacological treatment of Parkinson disease: a review". JAMA. ج. 311 ع. 16: 1670–83. 30 أبريل 2014. DOI:10.1001/jama.2014.3654. PMID:24756517.
- ^ "The non-motor and non-dopaminergic fratures of PD". Parkinson's Disease : Non-Motor and Non-Dopaminergic Features. Olanow, C. Warren., Stocchi, Fabrizio., Lang, Anthony E. Wiley-Blackwell. 2011. ISBN:978-1405191852. OCLC:743205140.
{{استشهاد بكتاب}}: صيانة الاستشهاد: آخرون (link) - ^ ا ب The National Collaborating Centre for Chronic Conditions، المحرر (2006). "Symptomatic pharmacological therapy in Parkinson's disease". Parkinson's Disease. London: Royal College of Physicians. ص. 59–100. ISBN:978-1-86016-283-1.
{{استشهاد بكتاب}}: الوسيط|archiveurl=بحاجة لـ|مسار=(مساعدة)، الوسيط غير المعروف|chapterurl=تم تجاهله يقترح استخدام|مسار الفصل=(مساعدة)، وروابط خارجية في|chapterurl=<ref>غير صالح؛ الاسم "Nice-pharma" معرف أكثر من مرة بمحتويات مختلفة. - ^ "Revisiting the Medical Management of Parkinson's Disease: Levodopa versus Dopamine Agonist". Current Neuropharmacology. ج. 14 ع. 4: 356–63. 2016. DOI:10.2174/1570159X14666151208114634. PMID:26644151.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Review: management of Parkinson's disease". Neuropsychiatric Disease and Treatment (Review). ج. 9: 321–40. 2013. DOI:10.2147/NDT.S32302. PMID:23487540.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ The National Collaborating Centre for Chronic Conditions، المحرر (2006). "Palliative care in Parkinson's disease". Parkinson's Disease. London: Royal College of Physicians. ص. 147–51. ISBN:978-1-86016-283-1.
{{استشهاد بكتاب}}: الوسيط|archiveurl=بحاجة لـ|مسار=(مساعدة)، الوسيط غير المعروف|chapterurl=تم تجاهله يقترح استخدام|مسار الفصل=(مساعدة)، وروابط خارجية في|chapterurl=
