حالة المادة

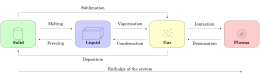
حالة المادة هي الصفة الفيزيائية والكيمائية للمادة والتي تشير إلى شكل الروابط بين جزيئاتها، أو الذرات أو الأيونات.
- الحالة الصلبة (الجامدة): المواد الصّلبة لها شكل ثابت حيث أن الجزيئات لا تنتقل من مكانها؛ تكون الجزيئات متقاربة بقدر كبير في الحالة الجامدة، الكثافة في المواد الصلبة عالية، لأن الفراغات صغيرة جدًّا بين الجزيئات
- الحالة السائلة: تأخذ السّوائل شكل الوعاء الذي توضع فيه، والجزيئات في السوائل ليست ثابّتة. السّوائل عالية الكثافة إلى حدّ ما، وليس هناك مساحات كبيرة بين الجزيئات.
- الحالة الغازية: ليس للغازات شكل محدد لكن الغازات تملأ أيّ فراغ متاح لأن الجزيئات تتحرّك بسرعة في كلّ الاتّجاهات، يمكن ضغط الغازات بسهولة، ولجزيئات الغازات مساحات كبيرة فيما بينها، لذلك فإنه من السهل أن تتقارب جزيئات الغاز. كثافة الغازات منخفضة جدًّا، وهناك مساحات فارغة كبيرة بين الجزيئات.
- حالة البلازما (هِيولي): هي حالة متميزة من حالات المادة يمكن وصفها بأنها غاز متأين تكون فيه الإلكترونات حرة وغير مرتبطة بالذرة أو بالجزيء. فإذا كانت المادة توجد في الطبيعة في ثلاث حالات: صلبة وسائلة وغازية، فإنه بالإمكان تصنيف البلازما على أنها الحالة الرابعة التي يمكن أن توجد عليها المادة.
الحالات الممكنة للمادة[عدل]
الحالات الممكنة للمادة في الطبيعة هي الغازية والسائلة والصلبة، وحديثاً تم تصنيف البلازما على أنها صنف من إحدى حالات المادة، كما توجد حالة بين الصلب والسائل تسمى الكريستال السائل.
طبيعة حالات المادة[عدل]
الحالة الصلبة[عدل]
تتجمع الجُزيئات المكوِّنة لهذه الحالة من المادة بالقرب من بعضها، وتترابط بشكلٍ قويّ للغاية، حتّى أنّك لا تستطيع تحريك إحدى هذه الجزيئات بمعزلٍ عن الجُزيئات الأخرى، بالأضافة إلى امتلاكها طاقةً حركيّةً قليلةً جدًا، ولكن من الجدير بالذكر أنّ ذرات هذه الجزيئات تهتز باستمرارٍ في موضعها الذي تتواجد فيه. والحالة الصلبة للمادة لها شكل ثابت وحجم محدد، ولا تأخذ شكل الإناء الموضوعة فيه. ونتيجةً لقوّة ترابط جُزيئاتها، لن تستطيع التأثير على حجمها بالضغط.[2]
الحالة السائلة[عدل]
تتميز جُزيئات هذه الحالة من المادة بارتفاع الطاقة الحركية عن مثيلتها في الحالة الصلبة، ولا تُشكِّل هذه الجزيئات شكلًا محددًا للمادة، ولكنّها تترابط مع بعضها بشكلٍ ضعيف، ما يسمح لها بأن تأخذ شكل الإناء المحويّة فيه. ولكنّها تمتلك حجمًا ثابتًا ومحددًا، بالإضافة إلى عدم إمكانيّة ضغطها، أيّ مثل الحالة الصلبة. عند التأثير بقوّةٍ على سطح المادة السائلة، فإنّ هذه القوى تتوزع بالتساوي على السطح ما يسمح لأيّ جسم بأزاحة أيّ قدر من السائل والحلول محلّه.
وفي أبريل 2016 أعلن العلماء عن حالةٍ غريبةٍ من المادة في حالتها السائلة، ففي هذه الحالة يُمكن حمل السائل باليد وكأنه مادةٌ صلبة . عند فحص هذه المادة بالميكروسكوبات ظهرت الإلكترونات في حالة ارتباطٍ عشوائيّ، وكأنّها مادة في حالتها السائلة. سُمِّيَت هذه المادة الجديدة بسائل كيتيف الكموميّ المغزليّ، يعود هذا لدخول إلكترونات هذه المادة في حالةٍ من الرقص العشوائيّ، مُخالفةً بذلك الوضع المٌتعارف عليه حينها، حيث أنّ تبريد السوائل ينظّم الإلكترونات، لتبدأ الحالة الصلبة للمادة بالتشكّل، ولكنّ إلكترونات هذه المادة تتجه للعشوائيّة بغض النظر عن درجة حرارة الوسط المحيط المنخفضة.[3]
الحالة الغازية[عدل]
هناك مسافات بينيّة شاسعة بين جُزيئات الغاز، ما يسمح بازدياد طاقتها الحركيّة، وإن لم تُحصَر هذه الجُزيئات في إناء أو أيّ وسط مُحدد، سوف تنتشر بشكلٍ عشوائيّ في الفضاء. عند حصر جُزيئات الغاز في حاوية، تنتشر هذه الجُزيئات لتشغل كلّ أجزاء الحاوية أو الإناء المحوية فيه. وعند ازدياد الضغط عليها ترتفع درجة حرارتها وطاقتها الحركيّة. بالإضافة إلى ذلك، في حال ظلّ حجم الإناء ثابتًا وازادت درجة حرارة الجُزيئات، ستزداد حينها طاقتها الحركيّة، ويزداد ضغطها على جُدارن الإناء.[3][4]
البلازما[عدل]
قد لا تكون هذه الحالة شائعةً على الأرض، ولكنّها أكثر حالات المادة شيوعًا في الكون بأكمله. فالبلازما تتكوّن بالأساس من جُسيماتٍ عالية الشُحنة الكهربائيّة، كما أنّها تمتلك طاقةً حركيّةً كبيرةً جدًا، وغالبًا ما تُستخدم الغازات النبيلة الخاملة لصُنع البلازما على الأرض. تُعتبَر النجوم أساسًا كراتٍ ملتهبةً وكبيرةً من البلازما.[3][5]
حالات المادة عند درجات الحرارة المنخفضة[عدل]
الميوعة الفائقة[عدل]
عند الاقتراب من درجة حرارة الصفر المُطلق، تفقد السوائل لزوجتها ومقومتها على الانسياب تمامًا، وقد اكتُشِفَت هذه الحالة لأوّل مرة في الحالة السائلة لغاز الهيليوم عام 1937، وتتميّز هذه الحالة بتوصيلها الفائق الّلانهائيّ للحرارة دون أدنى مقاومة تُذكَر.[6]
تكاثف بوز أينشتاين[عدل]
تنبأ ألبرت أينشتاين وناث بوس بوجود حالةٍ من المادة، والتي تتوقّف فيها عن التصرّف بمثابة جزيئاتٍ مُستقلة، وتنهار جميعها كموميًا، لدرجة أنّه يمكن وصفها بواسطة دالةٍ موجيّةٍ واحدة، ويكون ذلك عند وصول بعض الغازات لدرجة الصفر المُطلق.[6]
التكاثف الفيرموني[عدل]
هي حالة شبيهة بتكاثف “بوز أينشتاين”، ولكنّها تشمل الفيرميونات فقط.
جُزيئات ريدبيرج[عدل]
هي إحدى الحالات المُستقرة من البلازما، وتكون عند تكثيف الذرات المُثارة عند درجة حرارة معيّنة.
المواد الضوئيّة[عدل]
حالة من حالات المادة تحدث نتيجة تفاعل فوتونات الضوء مع غازاتٍ ذات كُتلٍ كبيرة، ما يُنتج جُزيئاتٍ فوتونيّةً أو ضوئيّة.
حالات المادة عند الطاقة العالية[عدل]
المادة المُتحللة[عدل]
تتواجد هذه المادة غالبًا في النجوم تحت ضغطٍ عالٍ جدًا، كما أنّها تمتلك كثافةً عاليةً جدًا. وهي تلعب في تولدها صفات كموميّة لتلك الأجرام .
مادة الكوارك[عدل]
الكوارك هو المكوِّن الرئيسيّ لبُنية البروتونات والنيترونات المتواجدة في نواة الذرة. عند تحرير هذه الكواركات من القوى التي تربطها ببعضها البعض عند كثافة ودرجات حرارة مرتفعة، فإنّ هذه الكواركات تمرّ بأطوارٍ مختلفة من المادة يُطلق عليها اسم مادة الكوارك.
كما أنّ هناك حالات أخرى للمادة سنتعرف عليها في مقالاتٍ لاحقة مثل الصلابة الفائقة، أو المادة المظلمة.
انظر أيضا[عدل]
المراجع[عدل]
- ^ وصلة مرجع: http://pediaa.com/difference-between-phase-of-matter-and-state-of-matter/. الوصول: 20 أبريل 2018.
- ^ "حالات المادة الأربعة" نسخة محفوظة 14 فبراير 2019 على موقع واي باك مشين.
- ^ أ ب ت "هل هناك أربع حالات للمادة حقا؟" نسخة محفوظة 14 فبراير 2019 على موقع واي باك مشين.
- ^ F. White (2003). Fluid Mechanics. McGraw-Hill. ص. 4. ISBN:978-0-07-240217-9.
- ^ G. Turrell (1997). Gas Dynamics: Theory and Applications. John Wiley & Sons. ص. 3–5. ISBN:978-0-471-97573-1. مؤرشف من الأصل في 2020-04-03.
- ^ أ ب "حالات المادة" نسخة محفوظة 08 فبراير 2019 على موقع واي باك مشين.
- ألفريد مارتن، كتاب الصيدلة الفيزيائية
| حالة المادة في المشاريع الشقيقة: | |
| |