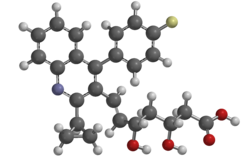
بيتافاستاتين
| بيتافاستاتين | |
|---|---|
| الاسم النظامي | |
| (3R,5S,6E)-7-[2-cyclopropyl-4-(4-fluorophenyl)quinolin-3-yl]-3,5-dihydroxyhept-6-enoic acid | |
| يعالج | وذمة شحمية، واعتلال ليبيدات الدم النادر [1] |
| اعتبارات علاجية | |
| ASHPDrugs.com | أفرودة |
| مدلاين بلس | a610018 |
| الوضع القانوني | إدارة الغذاء والدواء:وصلة |
| فئة السلامة أثناء الحمل | X |
| طرق إعطاء الدواء | oral tablets 1, 2, & 4 mg |
| بيانات دوائية | |
| توافر حيوي | 60% |
| ربط بروتيني | 96% |
| استقلاب (أيض) الدواء | minimally CYP4502C9 |
| عمر النصف الحيوي | 11 hours |
| إخراج (فسلجة) | Faeces |
| معرّفات | |
| CAS | 147511-69-1 |
| ك ع ت | C10C10AA08 AA08 |
| بوب كيم | CID 5282452 |
| ECHA InfoCard ID | 100.171.153 |
| درغ بنك | 08860 |
| كيم سبايدر | 4445604 |
| المكون الفريد | M5681Q5F9P |
| كيوتو | C13334 |
| ChEMBL | CHEMBL1201753 |
| بيانات كيميائية | |
| الصيغة الكيميائية | C25H24FNO4 |
| الكتلة الجزيئية | 421.461 |
| تعديل مصدري - تعديل | |
بيتافاستاتين أحد الأدوية الحديثة التي تنتمي إلى مجموعة الستاتين (أو مثبطات إنزيم HMG-CoA) وهي ادوية مخفضة للكوليسترول .[2][3][4]
ويتوفر بيتافاستاتين بجرعات مختلفة (1 ملغ، 2ملغ، 4ملغ) .
الأيض والتفاعلات الدوائية[عدل]
أكثر الأدوية في مجموعة ستاتين يتم أيضها في الكبد بواسطة إنزيمات سايتوكروم ب450 (Cytochrome P450) وخصوصا الإنزيم CYP3A4 مما يجعلها عرضه للتفاعلات الدوائية مع الكثير من الأدوية والأغذية مثل عصير كريب فروت .
لكن وكما يبدو فإن أيض بيتافاستاتين يتم غالبا بواسطة الإنزيم CYP2C9 لذلك فإن هذا الدواء له تفاعلات دوائية أقل من بقية الستاتينات .
تاريخه[عدل]
تعتبر شركة كووا (Kowa Pharmaceuticals) اليابانية أول شركة منتجة له تحت اسم ليفالو (Livalo) وذلك منذ عام 2003 .
بعد ذلك تم إنتاجه وتسويقه في كوريا الجنوبية والهند بامتياز من الشركة ذاتها .
ثم انتشر استخدامه في دول جنوب آسيا ودول جنوب شرق آسيا .
تم إقرار استخدامه في الولايات المتحدة الأمريكية من قبل إدارة الأغذية والأدوية (FDA) بتاريخ 8 آذار من عام 2009 وبدأت شركة ليلي (Eli Lilly and Company) الأمريكية بالتعاون مع كووا (Kowa Pharmaceuticals) اليابانية بإنتاجه وتسويقه في الولايات المتحدة الأمريكية .
وقد تم إقرار استخدامه في المملكة المتحدة بتاريخ 17 آب 2010 .
انظر أيضا[عدل]
- تصلب عصيدي
- بروتين دهني منخفض الكثافة
- بروتين دهني مرتفع الكثافة
- جليسريد ثلاثي
- ذبحة صدرية
- سكتة دماغية
- فشل كلوي
- تكلس
مراجع[عدل]
- ^ Drug Indications Extracted from FAERS، DOI:10.5281/ZENODO.1435999، QID:Q56863002
- ^ Kajinami، K؛ Takekoshi، N؛ Saito، Y (2003). "Pitavastatin: efficacy and safety profiles of a novel synthetic HMG-CoA reductase inhibitor". Cardiovascular drug reviews. ج. 21 ع. 3: 199–215. PMID:12931254.
- ^ Zydus Cadila launches pitavastatin in India نسخة محفوظة 26 سبتمبر 2017 على موقع واي باك مشين.
- ^ Ogata، N.؛ Fujimori، S.؛ Oka، Y.؛ Kaneko، K. (2010). "Effects of Three Strong Statins (Atorvastatin, Pitavastatin, and Rosuvastatin) on Serum Uric Acid Levels in Dyslipidemic Patients". Nucleosides, Nucleotides and Nucleic Acids. ج. 29 ع. 4–6: 321–324. DOI:10.1080/15257771003741323.
وصلات خارجية[عدل]
| بيتافاستاتين في المشاريع الشقيقة: | |
| |