كيمياء الحالة الصلبة
تحوي هذه المقالة أو هذا القسم ترجمة آلية. (أكتوبر 2019) |


كيمياء الحالة الصلبة هي فرع من فروع الكيمياء يتم فيه دراسة الخصائص الفيزيائية للمواد الصلبة، إضافةً إلى بنيتها وطرق اصطناعها.
وهي تتداخل بشكل كبير مع كل من فيزياء الجسم الصلب، التعدين، علم البلورات، المواد السيراميكية، علم السبائك، التحريك الحراري، علم المواد، والإلكترونيات، صناعة الرقائق الإلكترونية والأقراص المضغوطة، إلا أنها تركز بشكل خاص على اصطناع مواد مبتكرة وطرق تحديدها، واستغلالها في المنافسة الصناعية.
التاريخ
[عدل]تطورت كيمياء الحالة الصلبة وتقنيتها تطورًا كبيرًا بدافع أهميتها لإنتاج منتجات تباع في الأسواق. ودفعت رغبة لصناعة والتجارة إلى التقدم في هذا المجال، دفعات قوية أقوى من الاهتمام بها من الوجهة العلمية الأكاديمية البحتة. ومن تلك المكتشفات التي اكتشفت في القرن العشرين نجد محفزات الزيوليت ومحفزات البلاتين التي تستخدم في صناعات البترول في الخمسينيات من القرن الماضي، والسيليكون عالي النقاوة والذي هو هام للصناعات الإلكترونية والإلكترونيات في الستينات، واستغلال التوصيلية الفائقة في درجات الحرارة العالية والتي ابتكرت في الثمانينيات.
كذلك مما دفع التقدم في هذا المجال أكتشاف حيود الأشعة السينية الذي اكتشفه وليام لورنس براغ في أوائل 1900 وبه استطعنا دراسة البلورات وتعيين البنيات البلورية للمواد الصلبة، فكانت هذه تجديدًا ثمينًا.
كما تطور فهمنا عن كيفية سير التفاعلات على المستوى الذرية للمواد الصلبة، ويرجع الفضل في هذا القدم إلى أعمال وأبحاث العالم كارل فاجنر المتعلقة بنظرية الأكسدة ومعدل سريان تفاعل الأكسدة، وكذلك أبحاثه عن نفاذية الأيونات، وكيمياء التشويب. وقد سمي لذلك «أبو كيمياء المواد الصلبة» .[1]
أساسيات اصطناعية
[عدل]ونظرًا لتنوع مركبات الحالة الصلبة، تستخدم مجموعة متنوعة من الطرق لتحضيرها.[2] ومن ضمنها طريقة أملاح انتقال الشحنة لتحضير المواد العضوية، وتحضر تلك المواد عند درجة حرارة الغرفة وهي مماثلة إلى حد كبير لطرق تحضير المركبات العضوية. وأحيانًا تُجرى تفاعلات الأكسدة عن طريق التبلور الكهربي electrocrystallisation، مثلما يتضح في مثال تحضير أملاح بيتشجارد Bechgaard salts من ال «تيتراثيافولفالين tetrathiafulvalene».
تقنيات الفرن
[عدل]تقنيات الفرن كثيرًا ما يعملون لمواد قوية حرارياً، أساليب ارتفاع في درجة الحرارة. على سبيل المثال، المواد الصلبة السائبة مستعدون استخدام أفران الأنبوبة، تتيح لردود الفعل على إجراء يصل إلى المرجع المصدق ca-1100 درجة مئوية المعدات الخاصة مثل الأفران يتكون من أنبوب التنتالوم من خلالها يتم تمريره تيار كهربائي يمكن أن تستخدم لدرجة حرارة أعلى حتى تصل إلى 2000 درجة مئوية. مثل ارتفاع درجات الحرارة في بعض الأحيان مطلوبة للحث على نشر المتفاعلة، ولكن هذا يعتمد بشدة على النظام درس. بعض ردود الفعل الحالة الصلبة الشروع فعلًا في درجات حرارة منخفضة تصل إلى 100 درجة مئوية.
تذويب
[عدل]كثيرًا ما يستخدم أسلوب واحد هو تذوب في الإشابة معًا وثم بعد ذلك أنيل المصهور الصلب. إذا الاشابة متقلبة ويشارك المتفاعلة كثيرًا ما توضع في الأنابيب التي يتم إخلاؤها -غالباً مع إبقاء المخلوط المعدية الباردة مثل طريق الحفاظ على الجزء السفلي من الأنابيب في النتروجين السائل- وثم أغلقت. ثم وضع في فرن الأنابيب مختومة ونظرًا لمعاملة معينة في الحرارة.
اسلوب الحل
[عدل]من الممكن استخدام المذيبات لتحضير المواد الصلبة بهطول الأمطار أو بواسطة التبخر. في بعض الأحيان المذيب يستخدم مصطلح، أي تحت ضغط عند درجات حرارة أعلى من نقطة الغليان العادي. تباين حول هذا الموضوع هو استخدام أساليب التمويه، المكان الذي تمت إضافته إلى الخليط لتعمل كمادة مذيبة ارتفاع في درجة حرارة يمكن أن تجري فيها رد الفعل المطلوب ملح نقطة انصهار منخفضة نسبيا.
التفاعلات الغازية
[عدل]يتفاعل العديد من المواد الصلبة بسهولة مع أنواع الغازات التفاعلية مثل الكلور، اليود المتسامي، والأكسجين وغيرها. وتشكل آخرين نواتج مع غازات أخرى، مثل أول أكسيد الكربون أو الإيثيلين. تجرى تلك التفاعلات عادة في أنبوب مفتوح من نهايتيه على الجانبين ويتم تمرير الغاز خلالها. وفي تجارب أخرى يتم التفاعل في جهاز قياس مثلما في التحليل الحراري الوزني thermogravimetric analysis TGA. وفي هذه الحالة يمكن الحصول على بيانات التفاعل أثناء سير التفاعل، مما يساعد على معرفة نوع المنتجات.
حالة خاصة من تفاعلات الغازات نجدها في تفاعل النقل الكيميائي. وهذه غالباً ما تنفذ في الأنابيب مغلقة ويضاف إليها كمية صغيرة من عامل النقل، مثل إضافة اليود. ثم يوضع الأنوب في فرن. ويكون هذا الفرن عادة عبارة عن فرن ذو أنبوبين (جهتين) بهما تدرج حراري (أي من جهة عالية السخونة إلى جهة أقل حرارة وتنقل العينة المتفاعلة خلالها). هذه الطريقة تستخدم بغرض إنتاج بلورات أحادية يمكن استخدامها في أجهزة تعيين البنية البلورية للمواد الصلبة بواسطة حيود الأشعة السينية.
كما تستخدم طريقة الترسيب البخاري الكيميائي وهي طريقة تتم في درجة حرارة مرتفعة بغرض تحضير تغطية رقيقة على الأسطح وصناعة أشباه الموصلات من مكونات جزيئية أولية.
مواد حساسة للهواء والرطوبة
[عدل]كثير من المواد الصلبة يعتبر حساسا لأكسجين أو يتميع سريعا في وجود بخار الماء. وكثير من مركبات هاليدات (الكلور والفلور) تكون «شرهة» للرطوبة ولا بد عند دراستها من استخدام الصناديق الجافة واستعمال قفازات، حيث تملأ تلك الصناديق الجافة بغاز جاف (أو غاز جاف خاليا من الأكسجين)، ويكون عادة غاز النيتروجين.
تعيين خواص المادة
[عدل]أطوار جديدة، مخطط الطور، والتركيب البلوري
[عدل]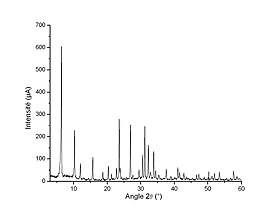
يسير تحضير مادة ملازما إلى تعيين حصائصها حيث تتم عدة تفاعلات متتالية وتعرض المخلوطات الناتجة إلي معاملة حرارية معينة. ونقوم يتغيير نسب المواد المختلطة بالتدريج بحيث نعرف عند أي نسبة للمواد الداخلة في التفاعل تنتج مركبا صلبا (بلوري) أو سائلا صلبا (عشوائي البنية). وتستخدم طريقة قياس حيود الأشعة السينية على عينة من المسحوق لتعيين المواد الناتجة من التفاعل، حيث تنتج معظم تفاعلات المواد الصلبة مساحيقا تتميز بكونها كثيرة البلورات. ويساعد قياس حيود أشعة إكس على المسحوق على معرفة الأطوار الموجودة في مخلوط (يتسم كل طور لمادة معينة ببنية بلورية خاصة بها فمنها ما يكون في هيئة نظام بلوري مكعب أو ذو بنية سداسية أو نظام بلوري رباعي أو غير ذلك). فإذا وجدنا توزيعا غير معروفا لنا من أشعة إكس المتشتتة على مسحوق المخلوط، فيمكننا تعيين البنية البلورية المجهولة بقياس أشعة إكس المرتدة من العينة. (عن طريق قياس أشعة إكس المشتتة من العينة يمكننا تعيين البنية البلورية، أي تعيين توزيع الذرات المختلفة في الهيكل البلوري لمادة نقية، وكذلك تعيين حجم الوحدة البلورية.)
وبعد التعرف على وحدة الخلية لطور المركب، يمكننا في الخطوة التالية تعيين نسب العناصر في هذا الطور. وأسهل طريقة لتعيين الوحدة البلورية وتوزيع ذرات العناصر فيه هي إجراء حيود أشعة إكس على بلورة أحادية من المركب.
وإذا أمكن فصل الناتج عن المخلوط فيمكن دراسته باستخدام المجهر الإلكتروني الماسح SEM. وأسهل الطرق هي تعيين البنية البلورية من قياس حيود أشعة إكس على بلورة أحادية لهذا الناتج المراد معرفته.
كذلك يهمنا معرفة مخطط الطور للمادة.[3] ويمكن تتبع التغيرات في مخطط الطور بطرق التحليل الحراري بواسطة مسعر مسح تبايني أو جهاز تحليل حراري تفاضلي DTA.
تعيين خواص أخرى
[عدل]تستخدم طرق لتعيين الخواص الأخرى للمركب الصلب، من ضمن تلك الطرق طرق تجمع بين كيمياء الحالة الصلبة وفيزياء الحالة الصلبة: [4]
خواص ضوئية
[عدل]يمكن بالنسبة لعينات مواد غير فلزية تعيين طيفها في نطاق الأشعة فوق البنفسجية. وفي حالة أشباه الموصلات فتعطينا تلك الطريقة بيانات عن اتساع الثغرة الإلكترونية.
خواص كهربائية
[عدل]تعين الخواص الكهربائية لعينة المادة بواسطة طريقة الأربعة نقاط (أو طريقة الخمسة نقاط) في الكهرباء، وهي تـُجرى على قطعة من المركب أو بلورة منه أو كبسولة مضغوطة منه وتقاس المقاومة والحجم وتأثير هول. تعطي نتائج تلك الاختبارات معلومات عما إذا كانت العينة عازل كهربائي أو شبه موصل، أو موصل كهربائي، وكذلك معلومات عن المادة المشوبة في العينة. بذلك نحصل على معلومات عن الرابطة الكيميائية في المادة.
خواص مغناطيسية
[عدل]يمكن قياس القابلية المغناطيسية لمادة واعتمادها على درجة الحرارة بغرض معرفة هل المادة ذات مغناطيسية حديدية أم مغناطيسية مسايرة أم فريمغناطيسية. كما يمكن تعيين البنية المغناطيسية للعينة بواسطة حيود النيوترونات، حيث أن النيوترونات لها عزم مغناطيسي يتأثر بمغناطيسية العينة.
المراجع
[عدل]- ^ For a historical perspective, cf. Pierre Teissier, L’émergence de la chimie du solide en France (1950-2000). De la formation d’une communauté à sa dispersion (Paris X: Ph.D. dissertation, 2007, 651 p.). Electronic version available: http://bdr.u-paris10.fr/sid/ نسخة محفوظة 7 أغسطس 2020 على موقع واي باك مشين.
- ^ Chapter 2 of Solid state chemistry and its applications. Anthony R. West. John Wiley & Sons 2003 ISBN 981-253-003-7
- ^ cf. Chapter 12 of Elements of X-ray diffraction, B.D. Cullity, Addison-Wesley, 2nd ed. 1977 ISBN 0-201-01174-3
- ^ cf. Chapter 2 of New directions in Solid State Chemistry. C.N.R. Rao and J. Gopalakrishnan. Cambridge U. Press 1997 ISBN 0-521-49559-8
