حمى الضنك: الفرق بين النسختين
| [نسخة منشورة] | [نسخة منشورة] |
Mahmoudalrawi (نقاش | مساهمات) |
Mahmoudalrawi (نقاش | مساهمات) |
||
| سطر 160: | سطر 160: | ||
لا يوجد [[مضاد فيروسات (دواء)|مضاد فيروسي]] محدد للضنك، لكن من المهم الحفاظ على توازن سوائل مناسب.<ref name=NEJM2012/> العلاج يعتمد على الأعراض.<ref name=WHOp32/> الأشخاص لقادرون على الشرب وإدرار البول وليس لديهم علامات خطر فهم في هذه الحالة صحيون ويمكن معالجتهم في البيت ومتابعتهم يوميا واستخدام [[العلاج بالإرواء الفموي]].<ref name=WHOp32>[[#refWHO2009|WHO (2009)]], pp. 32–37.</ref> أما الأشخاص الذين يعانون من مشاكل صحية أخرى ولديهم علامات خطر ولا يمكن متابعة حالاتهم بانتظام فيجب أن يعتنى بهم في المستشفى.<ref name=Peads10/><ref name=WHOp32/> أما الذين يعانون من حمى الضنك الشديد فيجب تقديم العناية لهم في أماكن يسهل فيها الحصول على [[وحدة عناية فائقة|عناية مركزة]].<ref name=WHOp32/> |
لا يوجد [[مضاد فيروسات (دواء)|مضاد فيروسي]] محدد للضنك، لكن من المهم الحفاظ على توازن سوائل مناسب.<ref name=NEJM2012/> العلاج يعتمد على الأعراض.<ref name=WHOp32/> الأشخاص لقادرون على الشرب وإدرار البول وليس لديهم علامات خطر فهم في هذه الحالة صحيون ويمكن معالجتهم في البيت ومتابعتهم يوميا واستخدام [[العلاج بالإرواء الفموي]].<ref name=WHOp32>[[#refWHO2009|WHO (2009)]], pp. 32–37.</ref> أما الأشخاص الذين يعانون من مشاكل صحية أخرى ولديهم علامات خطر ولا يمكن متابعة حالاتهم بانتظام فيجب أن يعتنى بهم في المستشفى.<ref name=Peads10/><ref name=WHOp32/> أما الذين يعانون من حمى الضنك الشديد فيجب تقديم العناية لهم في أماكن يسهل فيها الحصول على [[وحدة عناية فائقة|عناية مركزة]].<ref name=WHOp32/> |
||
في الحالة الحاجة ل[[تعويض السوائل]] [[علاج عن طريق الوريد|وريديا]] فعادة ما تكون الحاجة ليوم أو يومين فقط.<ref name=WHOp32/> تتم معايرة معدل إعطاء السوائل مع [[تبول|النتاج البولي]] بنسبة .5–1 مل/كغم/ساعة، ليوازن [[العلامات الحيوية]] وتسويه مكداس الدم.<ref name=Peads10/> ينصح باستخدام أقل كمية من السوائل للحصول على هذه النتيجة.<ref name=WHOp32/> يجب تجنب العمليات الطبية التداخلية مثل [[التنبيب الأنفي المعدي]] و[[الحقن العضلي]] ووخز الشرايين بسبب مخاطر النزف.<ref name=Peads10/> يستخدم ال[[باراسيتامول]] (أو الأسيتامينوفين) لل[[حمى]] والضيق بينما يجب تجنب [[مضادات الالتهاب اللاستيرويدية]] مثل ال[[إيبوبروفين]] وال[[أسبرين]] بسبب لأنها قد تفاقم من خطر النزف.<ref name=WHOp32/> يبدأ ب[[نقل الدم]] مبكرا للأشخاص الذين يعانون من علامات حيوية غير مستقرة ويعانون من نقصان في مكداس الدم عوضا عن انتظار نقصان تركيز ال[[هيموغلوبين]] إلى مستويات محتومة تستدعي نقل الدم.<ref name=WHOp40>[[#refWHO2009|WHO (2009)]], pp. 40–43.</ref> يتطلب استخدام [[كريات حمر مكدوسة]] أو [[دم كامل]]، أما [[الصفيحات الدموية]] و[[البلازما المجمدة الطازجة]] فغالبا لا يتطلب استخدامها.<ref name=WHOp40/> لا توجد ادلة كافية توضح فيم إذا كان استخدام [[الكورتيكوستيرويدات]] له تأثير إيجابي أو سلبي على حمى الضنك.<ref>{{cite journal|last1=Zhang|first1=F|last2=Kramer|first2=CV|title=Corticosteroids for dengue infection.|journal=The Cochrane database of systematic reviews|date=1 July 2014|volume=7|pages=CD003488|pmid=24984082|doi=10.1002/14651858.CD003488.pub3}}</ref> |
|||
{{...}} |
|||
يجب إيقاف إعطاء السوائل وريديا خلال فترة المعافاة لمنع حدوث حالة [[فرط حجم الدم]].<ref name=Peads10/> إذا حدثت حالة فرط حجم الدم وكانت العلامات الحيوية مستقرة فقد يكون كل ما يحتاجه هو إيقاف أي سوائل أخرى.<ref name=WHOp40/> إذا كان المريض خارجا من المرحلة الحرجة فيمكن استخدام [[مدر بول عروي]] مثل [[فوروسيميد]] للتخلص من السوائل الزائدة في جهاز الدوران.<ref name=WHOp40/> |
|||
== انتشار المرض == |
== انتشار المرض == |
||
نسخة 16:11، 25 سبتمبر 2015
هذه مقالة أو قسم، تخضع لتحريرٍ مُكثَّفٍ في الفترة الحالية لفترةٍ قصيرةٍ. لتفادي تضارب التحرير؛ يُرجى عدم تعديل الصفحة في أثناء وجود هذه الرسالة. أُجري آخر تعديل على الصفحة في 16:11، 25 سبتمبر 2015 (UTC) ( منذ 8 سنين) – . فضلًا أزل هذا القالب لو لم تكن هنالك تعديلات على المقالة في آخر 24 ساعة. إذا كنت المحرر الذي أضاف هذا القالب، فضلًا تأكد من إزالته واستبداله بقالب {{تطوير مقالة}} بين جلسات التحرير. |
| حمى الضنك Dengue fever | |
|---|---|
طفح جلدي يظهر على الشخص المصاب بحمى الضنك
| |
| معلومات عامة | |
| الاختصاص | أمراض معدية |
| من أنواع | مرض فيروسي، ومرض فيروسي معدي ، والأمراض المدارية المهملة، ومرض، ومرض منقول بالبعوض |
| الأسباب | |
| الأسباب | فيروس الضنك |
| طريقة انتقال العامل المسبب للمرض | عبر البعوض |
| المظهر السريري | |
| الأعراض | إعياء، وصداع[1]، وألم مفصلي[2]، وألم عضلي[1]، وغثيان، وتضخم العقد اللمفية، وتقيؤ، ووهن، وفقدان الشهية، وطفح بقعي حطاطي، وبطء القلب، ونزف[2] |
| التاريخ | |
| وصفها المصدر | موسوعة ناتال ، وقاموس بروكهاوس وإفرون الموسوعي، وقاموس بروكهاوس وإفرون الموسوعي الصغير ، ومعجم التخاطب لماير ، والموسوعة البريطانية نسخة سنة 1911، والموسوعة السوفيتية الأرمينية، المجلد السابع |
| تعديل مصدري - تعديل | |
حمى الضنك[3] أو الدِّنْجِيّة[3] أو أبو الرُّكَب[3] أو الدنج أو الدنك (بالإنكليزية: Dengue Fever) أو حمى تكسير العظام[4] (بالإنكليزية: breakbone fever) أو حمى عدن (بالإنكليزية: Aden fever)[4] هو مرض مداري منقول بالبعوض يحدث بسبب فيروس الضنك.
تشمل الأعراض الحمى والصداع وآلام العضلات والمفاصل وطفح جلدي متميز شبيه بطفح الحصبة. يتطور المرض في نسبة قليلة من الحالات إلى حمى الضنك النزفية[4] (بالإنكليزية: dengue hemorrhagic fever) المهددة للحياة، مما ينتج عنه نزف وقلة الصفيحات وفقدان بلازما الدم أو متلازمة صدمة الضنك (بالإنجليزية: dengue shock syndrome) حيث يحدث انخفاض خطير في ضغط الدم.
تنتقل حمى الضنك بواسطة عدد من أنواع البعوضيات من جنس الزاعجة (Aedes) وخصوصا الزاعجة المصرية (Aedes aegypti). هذا الفيروس يضم خمسة أنواع.[5] الإصابة بعدوى أحد هذه الأنواع يعطي مناعة مدى الحياة لذلك النوع، لكنه يعطي مناعة قصيرة المدى لبقية الأنواع. العدوى التالية بنوع مختلف يزيد من خطر المضاعفات. لا يوجد لقاح متوفر تجاريا. يمكن الحصول على الوقاية عن طريق تقليل مواطن وأعداد البعوض وتقليل التعرض للدغات.
علاج الضنك الحاد هو علاج داعم مثل معالجة الجفاف عن طريق الفم أو الوريد في الحالات المعتدلة إلى المتوسطة أو علاج بالسوائل الوريدية أو نقل الدم في الحالات الأشد حدة.
إزدادت حالات الإصابة حمى الضنك منذ عقد ستينات القرن العشرين بشكل مثير، حيث يصاب من بين 50 و 528 مليون شخص سنويا.[6][7]
أقدم وصف لأعراض المرض يعود لعام 1779، لكن لم يتم اكتشاف أسبابه الفيروسية وانتقاله حتى أوائل القرن العشرين. وقد أصبح الضنك مشكلة عالمية منذ الحرب العالمية الثانية حيث إنه متوطن في أكثر من 110 بلدا. فضلا عن التخلص من البعوض، فإن العمل مستمر للحصول على لقاح لحمى الضنك بالإضافة لأدوية موجهة للفيروس.
الإشارات والأعراض

بصورة عامة، فإن أكثر المرضى المصابين بعدوى فيروس حمى الضنك بدون أعراض (يشكلون نسبة 80٪) أو أنهم يشكون من أعراض معتدلة مثل الحمى بدون مضاعفات.[6][8][9] هنالك 5٪ من المرضى يشكون من أعراض أشد بالإضافة لنسبة قليلة حياتهم مهددة.[6][9]
فترة الحضانة (الفترة بين التعرض للإصابة وحتى ظهور الأعراض) تتراوح من 3 إلى 14 يوما، لكنها غالبا ما تكون من 4 إلى 7 أيام.[10] لذلك فإنه من المستبعد إصابة المسافرين الذين يعودون من أماكن استيطان المرض ولا تظهر أعراض الضنك مثل الحمى أو الأعراض الأخرى خلال 14 يوما من عودتهم لديارهم.[11] عادة ما يعاني الأطفال من أعراض شبيهة بالبرد والالتهاب المعدي المعوي (قيء وإسهال)[12] كما إنهم معرضون لخطر أكبر من المضاعفات الشديدة،[11][13] حيث تبدأ الأعراض خفيفة عموما لكن الحمى أشد.[13]
المسار السريري
الأعراض المميزة لحمى الضنك هي الحمى التي تبدأ فجأة والصداع (عادة ما يكون الألم خلف العينين) وألم العضلات والمفاصل وطفحية. من الأسماء المرادفة لحمى الضنك هو "حمى تكسير العظام"، حيث ترتبط هذه التسمية بآلام العضلات والمفاصل.[6][14] ينقسم مسار العدوى إلى 3 مراحل هي: مرحلة الحمى ثم المرحلة الحرجة ثم المعافاة.[15]

تشمل مرحلة الحمى حمى شديدة قد تتجاوز 40° سيليزية (104° فهرنهايت) ويظهر أيضا ألم عام وصداع. هذه الأعراض قد تستمر من يومين إلى 7 أيام.[15][14] قد يحدث غثيان وتقيؤ.[13] يظهر الطفح في 50–80٪ من الذين يشكون من أعراض[14][16] في اليوم الأول أو الثاني من ظهور الأعراض وعلى شكل احمرار جلدي، أو يظهر لاحقا في فترة المرض (من اليوم الرابع إلى السابع)على شكل طفح حصبي.[16][17] كما يمكن ملاحظة طفح يوصف بأنه على شكل "جزر بيضاء وسط بحر أحمر".[18] في تلك المرحلة يمكن أن تظهر حبرات (وهي بقع جلدية حمراء لا تختفي عن الضغط عليها تظهر بسبب تضرر الشعيرات الدموية)،[15] قد ينزف بعضها نزفا بسيطا من الغشاء المخاطي في الفم والأنف.[11][14]

يمر المرض عن بغض الناس بمرحلة حرجة بعد زوال الحمى.[13] خلال هذه الفترة يحصل فقدان للبلازما من الأوعية الدموية يستمر عادة يوما أو يومي،[15] مما يؤدي لتراكم السوائل في منطقة الصدر والبطن وكذلك نقص حجم الدم ونقص في الدم الواصل إلى الأعضاء الحيوية.[15] كما قد يحدث عجز في بعض أعضاء الجسم بسبب النزف الشديد وخاصة من القناة الهضمية.[11][15] الصدمة (متلازمة صدمة الضنك) والنزف (حمى الضنك النزفية) تحدث في 5٪ من مجموع حالات حمى الضنك. إن الذين أصيبوا سابقا بعدوى نمط مصلي آخر من فيروس الضنك معروضون لخطر أكبر.[11][19] رغم أن هذه المرحلة الحرجة نادرة، لكنها تحدث نسبيا أكثر شيوعا عند الأطفال والشباب.[13]

يحدث بعدها مرحلة المعافاة، حيث تتم استعادة المفقودة إلى مرجى الدم.[15] تستمر هذا المرحلة يومين أو ثلاثة.[11] عادة ما يكون التحسن محدد، حيث يمكن أن ترافقه حكة شديدة وبطء القلب.[11][15] قد يحدث الطفح مرة أخرى ويكون ذو مظهر إما بقعي حطاطي أو وعائي والذي يتبعه تقشر في الجلد.[13] خلال هذه المرحلة قد تحدث حالة فرط حجم الدم. هذه الحالة إذا أثرت في الدماغ (تسمى وذمة دماغية) فقد تتسبب بانخفاض في مستوى الوعي أو نوبات.[11] الشعور بالإعياء قد يستمر أسبوعين عند البالغين.[13]
المشاكل المرتبطة
قد تؤثر حمى الضنك أحيانا على أنظمة الجسم[15] إما بشكل معزول أو مترافق مع أعراض الضنك النمطية.[12] يحدث انخفاض مستوى الوعي في 0.5–6٪ من الحالات، والتي تعزى إلى التهاب الدماغ بالفيروس أو بشكل غير مباشر نتيجة لخلل في أعضاء حيوية مثلما يحصل في اعتلال الكبد.[12][18][20]
هنالك اعتلالات عصبية أخرى تحدث بسبب الضنك مثل التهاب النخاع المستعرض ومتلازمة غيلان باريه.[12][20] أما عدوى القلب والفشل الكبدي الحاد فهي من المضاعفات النادرة.[11][15]
الأسباب
الفيروسات
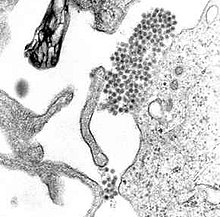
قالب:تفصيلي فيروس الضنك هو فيروس حمض نووي ريبوزي ينتمي لعائلة الفيروسات المصفرة ولجنس الفيروسة المصفرة. من الفيروسات الأخرى التي تمنتمي لهذا الجنس فيروس غرب النيل وفيروس التهاب الدماغ الياباني وفيروس التهاب دماغ القديس لويس وفيروس التهاب الدماغ المحمول بالقراد وفيروس داء غابة كياسانور وفيروس حمى أومسك النزفية.[18] أغلب هذه الفيروسات تنتقل بواسطة مفصليات الأرجل (بعوض أو قراد)، لذلك فهي تسمى أربوفيروس (بمعنى فيروسات منقولة بالمفصليات، حيث أن التسمية مشتقة من الاسم الإنكليزي ARthropod-BOrne virus).[18]
جينوم فيروس الضنك يحتوي على 11000 قاعدة نكليوتيد والتي تشفر لثلاثة أنواع من جزيئات البروتين وهي (C و prM و E) والتي تكوّن الفيروس وسبعة أنواع من جزيئات البروتين (NS1 و NS2a و NS2b و NS3 و NS4a و NS4b و NS5) والتي توجد في الخلايا المصابة بالعدوى والمطلوبة لتكاثر الفيروس فقط.[19][21] توجد خمسة[5] سلالات من الفيروس تدعى بالأنماط المصلية. الأنواع الأربعة الأولى تحمل تسميات فيروس الضنك-1 وفيروس الضنك-2 وفيروس الضنك-3 وفيروس الضنك-4،[8] أما الخامس فقد أعلن عن اكتشافه عام 2013.[5] التمييز بين الأنماط يعتمد على الاستضداد.[22]
الانتقال

ينتقل فيروس الضنك إلى الإنسان بواسطة بعوضيات من جنس الزاعجة وخصوصا الزاعجة المصرية.[8] تعيش هذه البعوضيات عادة بين خطي العرض 35° شمالا و35° جنوبا في ارتفاعات لا تتجاوز 1000 متر (3300 قدم) فوق مستوى سطح البحر.[8] تحدث اللدغات عادة أثناء النهار خصوصا بداية الصباح وفترة المساء،[23][24] لكنها قادرة على اللدغ في أي وقت من اليوم وطوال السنة.[25] من أنواع الزاعجة الأخرى التي تنقل المرض الزاعجة المنقطة بالأبيض والزاعجة البولينيزية والزاعجة الترسية.[8]
يعد الإنسان المضيف الرئيسي للفيروس،[8][18] لكن الفيروس يمكن أن ينتقل أيضا إلى رئيسيات أخرى غير البشر.[26] كما يمكن أن تحدث العدوى من لدغة واحدة فقط.[27] تتناول البعوضة الأنثى دم الشخص المصاب لتتغذى عليه، فإن لدغت شخصا مصابا بحمى الضنك خلال فترة يومين إلى 10 أيام من مرحلة الحمى تصبح البعوضة نفسها مصابة بالفيروس ويوجد في الخلايا المبطنة لقناتها الهضمية.[28] ينتشر الفيروس إلى أنسجة أخرى بعد فترة من 8 إلى 10 أيام ليشمل الغدد اللعابية للبعوضة ثم تقوم بإفراز الفيروس في لعابها. يبدو أن الفيروس ليس له تأثير على حياة البعوضة، كما أنها تبقى مصابة به مدى حياتها.[10]
تفضل الزاعجة المصرية طرح بيوضها في حاويات المياه الصناعية لتتغذى على البشر دون الفقريات الأخرى.[10]
يمكن أن تنتقل عدوى حمى الضنك بواسطة مكونات الدم الحاملة للعدوى والتبرع بالأعضاء.[29][30] خطر انتقال العدوى عن طريق نقل الدم في البلدان التي يستوطن فيها المرض مثل سنغافورة يقدر بين 1.6 إلى 6 من كل 10000 مواطن.[31] كما سجلت حالات الانتقال العمودي للعدوى من الأم إلى طفلها أثناء الحمل وخلال الولادة.[32] كما سجلت حالات انتقال العدوى من شخص إلى شخص آخر، لكن هذه الحالة غير معتادة جدا.[14] التباين الوراثي في فيروسات حمى الضنك يختلف حسب المنطقة، مما يفترض أن انتقال المرض إلى مناطق جديدة هي نادر نسبيا على الرغم من ظهور حالات حمى الضنك في مناطق جديدة في العقود الأخيرة.[13]
قابلية حصول المرض
يشيع المرض في الأطفال والرضع، بخلاف أنواع كثير أخرى من العدوى، كما إنه أكثر حدوثا في الأطفال ذوي التغذية الجيدة نسبيا.[11]
من عوامل الخطورة الأخرى هي الإناث أكثر عرضه لحدوث العدوى من الذكور ومؤشر كتلة الجسم المرتفع[13] والحمل الفيروسي.[33] رغم أن كل الأنماط المصلية يمكنها أن تسبب الطيف الكامل للمرض[19] إلا أن سلالاة الفيروس تعد عامل خطر.[13]
يعتقد أن الإصابة بنمط مصلي واحد يمكن أن توفر مناعة مدى الحياة لذلك النوع، لكنه أيضا يوفر مناعة قصيرة الأمد للأنواع الثلاثة الأخرى.[8][14] تزداد خطورة الإصابة بمرض شديد من عدوى ثانوية إذا تعرض المريض لفيروس الضنك-1 بخلاف فيروس الضنك-2 أو فيروس الضنك-3 أو تعرض لفيروس الضنك-3 ثم أصيب بفيروس الضنك-2.[21]
تعد حمى الضنك مهددة لحياة المرضى المصابين بأمراض مزمنة مثل السكري والربو.[21]
رُبِطَ تعدد أشكال مورثة معينة مع خطر الإصابة بمضاعفات شديدة للضنك. من الأمثلة على الجينات المشفرة لبروتينات مثل عامل نخر الورم ألفا ولاكتين رابط للمانان[6] وCTLA4 وعامل النمو المحول بيتا وDC-SIGN وPLCE1 وأشكال معينة من مستضد الكريات البيضاء البشرية وهي من اختلافات جين معقد التوافق النسيجي الكبير-ب.[13][21] يعد فقر الدمِ الناجم عن عوزِ سداسي فوسفات الجلوكوز النازع للهيدروجين من أبرز المشاكل الجينية التي تزيد من خطر الضنك، خصوصا عند الأفارقة.[33] يبدو أن تعدد أشكال مورثات مستقبل فيتامين د ومستقبل Fc توفر الوقاية من المرض الشديد في عدوى الضنك الثانوية.[21]
آلية حدوث المرض
عندما يحمل البعوض فيروس الضنك وتلدغ الإنسان، يدخل الفيروس الجلد مع لعاب البعوضة. يرتبط الفيروس بكريات الدم البيض ويدخلها ثم يتكاثر داخل الخلية وهي تنتقل خلال الجسم. تستجب الكريات البيض لهذه العدوى وتنتج بروتينات مثل السيتوكينات والإنترفيرونات المسؤولة عن كثير من الأعراض مثل الحمى والأعراض الشبيهة بالنزلة الوافدة والآلام الشديدة.
يزداد إنتاج الفيروس داخل الجسم بشدة في حالات العدوى الشديدة، ويمكن أن يصاب أعضاء أخرى من الجسم مثل الكبد ونخاع العظم. تتسرب السوائل من مجرى الدم خلال الأوعية الدموية الدقيقة نحو تجاويف الجسم بسبب النفاذية الوعائية. نتيجة لذلك، سيجري دم أقل في الأوعية الدموية وينخفض ضغط الدم ولا يمكن إيصال كمية من الدم إلى الأعضاء الحيوية. بالإضافة لذلك، فإن عجز نخاع العظم بسبب عدوى الخلايا السدوية يؤدي إلى نقص في عدد الصفيحات الضرورية في تخثر الدم، مما يؤدي إلى زيادة خطر الإصابة بنزف، وهو أهم مضاعفات حمى الضنك.[33]
تكاثر الفيروس
عندما يدخل الفيروس عبر الجلد يرتبط بخلايا لانغرهانس (وهي مجموعة من الخلايا المتغصنة في الجلد تتعرف على العوامل الممرضة).[33] يدخل الفيروس إلى الخلية عن طريق الارتباط بين بروتين الفيروس والبروتينات الغشائية على خلايا لانغرهانس، وخصوصا لاكتينات نوع ج التي تدعى DC-SIGN وCLEC5A ومستقبل مانوز.[19]
DC-SIGN، وهو مستقبل غير محدد للأجسام الغريبة في الخلايا المتغصنة، فيبدو أنه النقطة الرئيسية للدخول.[21] تنتقل الخلايا المتغصنة إلى أقرب عقدة لمفاوية. في هذه الأثناء، يستنسخ جينوم الفيروس في الحويصلات المرتبطة بالغشاء على الشبكة الهيولية الباطنة للخلية، حيث يقوم الجهاز المختص بإنتاج البروتين في الخلية بإنتاج بروتينات الفيروس التي تقوم بتكاثر الحمض النووي الريبوزي للفيروس للبدء بتكوين جزيئات الفيروس. تُنقل جزيئات الفيروس غير الناضجة إلى جهاز غولجي، وهو جزء الخلية التي تستقبل فيه بعض البروتينات سلاسل السكريات الضرورية (البروتين السكري). تتبرعم الفيروسات الناضجة على سطح الخلية المصابة بالعدوى وتطلق بعملية الإخراج الخلوي. وبذلك تكون قادرة على دخول كريات الدم البيض الأخرى مثل الخلايا الوحيدة والخلايا الأكولة الكبيرة.[19]
يعد إنتاج الإنترفيرون هو التفاعل الأولي في الخلايا المصابة بالعدوى، والإنترفيرون هو سيتوكين يرفع عدد الدفاعات ضد العدوى الفيروسية من خلال المناعة الطبيعية بواسطة زيادة إنتاج مجموعة كبيرة من البروتينات بوساطة سبيل إشارات جاك-ستات. يبدو أن بعض الأنماط الوراثية لفيروس جمى الضنك لديها آليات لتبطئ هذه العملية. كذلك يفعّل الإنترفيرون الجهاز المناعي التكيفي الذي يؤدي إلى توليد أجسام مضادة للفيروس بالإضافة للخلايا التائية التي تهاجم الخلايا المصابة بعدوى الفيروس مباشرة.[19] تتولد أجسام مضادة متنوعة، بعضها يرتبط بالقرب من بروتين الفيروس ويستهدفه بواسطة البلعمة (وهي عملية التهام بواسطة خلايا متخصصة وتحطيمها)، لكن يبدو أن بعضها يرتبط بأقل جودة وعوضا عن ذلك يقوم يتسليمه إلى خلايا بلعمية حيث لا يتدمر الفيروس ولكنه يتكاثر أكثر.[19]
المرض الشديد
لا تتوفر معلومات كافية حول سبب أن الإصابة بعدوى ثانوية بسلالة مختلفة من فيروس حمى الضنك تجعل الشخص معرضا لخطر أكبر بالإصابة بحمى الضنك النزفية ومتلازمة صدمة الضنك. النظرية الأكثر قبولا هي وجود استعزاز معتمد على المستضد (ADE). آلية عمل الاستعزاز المعتمد على المستضد غير واضحة. قد يكون السبب هو الارتباط الضعيف بين المستضد غير المستعدل وتسليم الفيروس إلى حيز خطأ في كرية الدم البيضاء التي التهمت الفيروس لغرض تحطيمه.[19][21] هنالك شك بأن الاستعزاز المعتمد على المستضد ليست الآلية الوحيدة المتسببة بمضاعفات حمى الضنك الشديدة،[6][20] كما أن هنالك خطوط بحثية تتضمن دور الخلية التائية والعوامل الذائية مثل السيتوكينات والجملة المتممة.[33]
يتميز المرض الشديد بمشكلة نفاذية الشعيرات الدموية (السماح بمرور السوائل والبروتين الموجودات بصورة طبيعية في الدم) ومشكلة تجلط الدم.[12][13] يبدو أن هذه التغيرات مرتبطة بحالة مرضية هي الكأس السكري البطاني الذي يقوم بدور منخل جزيئي لمكونات الدم.[13] يعتقد أن الشعيرات الدموية الناضحة سببها استجابة للجهاز المناعي.[13]
أما الطرق الأخرى المثيرة للاهتمام فتشمل الخلايا المصابة بالعدوى التي تتنخر، وهذا يؤثر على كل من تجلط الدم وانحلال الفبرين (أنظمة متضادة لتجلط الدم وتحلل التجلط) وانخفاض عدد الصفيحات الدموية، وهو كذلك عامل طبيعي في التجلط الطبيعي.[33]
التشخيص
| تدهور ألم البطن | ||||
| القيء المتواصل | ||||
| تضخم الكبد | ||||
| نزف من الطبقات المخاطية | ||||
| زيادة في مكداس الدم مع انخفاض في الصفيحات الدموية | ||||
| خمول أو فقدان الراحة | ||||
| انصبابات مصلية | ||||
من المعتاد تشخيص حمى الضنك سريريا على أساس الأعراض المسجلة والفحص السريري، وهذا مطبق في الأماكن التي يستوطن فيها المرض.[6] رغم ذلك، فإنه من الصعب تمييز المرض في مراحله الأولى عن الأمراض الفيروسية الأخرى.[11] التشخيص المحتمل قائم على نتائج تشخيص تضم الحمى بالإضافة اثنين مما يلي: الغثيان والقيء والطفح الجلدي وآلام عامة وقلة الكريات البيض واختبار العاصبة أو أي علامة أخرى (طالع الجدول) تصيب الشخص الذي يعيش في منقطة استيطان المرض.[34] عادة ما تحدث العلامات المحذرة قبل بداية المرض الشديد.[15] اختبار العاصبة النافع من الناحية العملية ويستخدم في ظروف عدم توفر الفحوص المختبرية يتضمن استخدام كفة مقياس ضغط الدم ما بين الضغطين الانبساطي والانقباضي لمدة 5 دقائق، يتلو ذلك عد أي نزف حبري. العدد الأكبر يجعل تشخيص الضنك راجحا أكثر مع قطع من 10 إلى 20 في كل بوصة مربعة (6.25 سم2).[15][35]
يجب أن يؤخذ التشخيص بنظر الاعتبار لكل فرد تحدث لديه الحمى خلال أسبوعين ويكون في منطقة استوائية أو شبه إستوائية.[13] قد يكون من الصعب التمييز بين حمى الضنك والشيكونغونيا، وهي عدوى فيروسية تشترك بكثير من الأعراض وتحدث في أجزاء من العالم تحدث فيها حمى الضنك.[14] عادة ما تجرى الفحوص لاستبعاد الأمراض الأخرى التي تسبب أعراض مشابهة مثل الملاريا وداء البريميات والحمى النزفية الفيروسية وحمى التيفوئيد ومرض المكورات السحائية والحصبة والنزلة الوافدة.[11][36]
التغيرات في نتائج الفحوص المختبرية والقابلة للكشف هي قلة الكريات البيض والتي يمكن أن يتبعها قلة الصفيحات وحماض أيضي.[11] عادة من تكون الزيادة المعتدلة في مستويات ناقلة الأمين (ناقلة الأسبارتات وناقلة الألانين) من الكبد مرتبطة بقلة الصفيحات وقلة الكريات البيض.[13] في المرض الشديد، يتسبب تسرب البلازما بتركز الدم (كما يؤشر بزيادة الهيماتوكريت) ونقص ألبومين الدم.[11] يمكن الكشف عن وجود الانصباب الجنبي أو الاستسقاء البطني بواسطة الفحص السريري عندما يكون كبيرا،[11] لكن ظهور السوائل في تخطيط الصدى قد يساعد في الكشف المبكر عن متلازمة صدمة الضنك.[6][11] إن استخدام تخطيط الصدى محدود بسبب عدم توفره في ظروف كثيرة.[6] وتوجد متلازمة صدمة الضنك إذا انخفض الضغط النبضي إلى أقل من 20 ملم زئبق مع انهيار وعائي محيطي.[13] يوصف الانهيار الوعائي المحيطي في الأطفال من خلال تأخر عود امتلاء الشعيرات أو زيادة سرعة القلب أو برودة الأطراف.[15] رغم أن العلامات المحذرة جوانب مهمة في الكشف المبكر عن مرض خطير محتمل، إلا أن الأدلة لأي علامات سريرية أو مختبرية خاصة تعد ضعيفة.[37]
التصنيف
تصنيف منظمة الصحة العالمية لعام 2009 قسم حمى الضنك إلى مجموعتين: البسيط والشديد.[6][34] هذا التصنيف استبدل عن تصنيف منظمة الصحة العالمية لعام 1997 والذي كان بحاجة لأن يبسط وقد وجد بأنه كان مقيدا جدا، لذلك فإن التصنيف القديم ما يزال يستخدم بشكل واسع[34] وبضمنها المكتب الإقليمي لمنظمة الصحة العالمية في جنوب شرق آسيا بحسب سنة 2011.[38]
يعرف مرض حمى الضنك الشديد بأنه يرتبط بنزف شديد أو اختلال وظيفي شديد في الأعضاء أو ارتشاح بلازما شديد بينما كل الحالات الأخرى فهي بسيطة.[34] قسم تصنيف عام 1997 حمى الضنك إلى حمى غير متمايزة وحمى الضنك وحمى الضنك النزفية.[11][39] قسمت حمى الضنك النزفية إلى 4 درجات، الدرجة الأولى هي وجود تكدم سهل أو اختبار عاصبة إيجابي عند شخص مصاب بالحمى، والدرجة الثانية هي وجود نزف متواصل في الجلد وأي مكان آخر، والدرجة الثالثة هي وجود دليل سريري على صدمة، والدرجة الرابعة هي صدمة شديدة جدا بحيث لا يمكن الكشف عن ضغط الدم ولا عن النبض.[39] توصف الدرجتان الثالثة والرابعة بأنهما "متلازمة صدمة الضنك".[34][39]
الفحوص المختبرية

يمكن التؤكد من تشخيص حمى الضنك من خلال اختبار مختبر الأحياء المجهرية.[34][40] يمكن إجراء الفحوص من خلال عزل الفيروس في زرع الخلايا أو اختبار الحمض النووي بواسطة تفاعل البوليميراز المتسلسل أو الكشف عن مولد ضد الفيروس (مثل اختبار مولد الضد ن س 1) أو أجسام مضادة معينة (اختبارات المصل).[21][36] عزل الفيروس والكشف عن الحمض النووي أكثر دقة من الكشف عن مولد الضد، لكن هذه الاختبارات غير متوفرة بشكل واسع بسبب ارتفاع تكلفتها.[36] تصل نتيجة الكشف عن ن س 1 خلال مرحلة الحمى في العدوى الأولية إلى أكثر من 90٪ بينما هي من 60 إلى 80٪ فقط في أنواع العدوى التالية.[13] وقد تكون كل الفحوص سالبة النتائج خلال المراحل الأولى من الإصابة بالمرض.[11][21] إن تفاعل البوليميراز المتسلسل والكشف عن مولد ضد الفيروس أكثر دقة خلال الأيام السبعة الأولى.[13] في عام 2012، قدم اختبار تفاعل بوليميراز متسلسل يمكن تشغيله على معدات الكشف عن الإنفلاونزا، ويبدو أنه يحسن الوصول إلى تشخيص قائم على تفاعل البوليميراز المتسلسل.[41]
لهذه الفحوص قيمة تشخيصية خلال المرحلة الحرجة من المرض فقط باستثناء اختبارات المصل. يمكن أن يكون لاختبارات الأجسام المضادة الخاصة بفيروس حمى الضنك من نوع الغلوبولين المناعي ج ونوع الغلوبولين المناعي م فائدة في تأكيد التشخيص في المراحل التالية من العدوى. ينتج كل من الغلوبولين المناعي ج والغلوبولين المناعي م بعد 5 إلى 7 أيام. يمكن الكشف عن أعلى تراكيز (عيار حجمي) للغلوبولين المناعي م بعد عدوى أولية، لكن الغلوبولين المناعي م ينتج أيضا في عودة العدوى. لا يمكن الكشف عن الغلوبولين المناعي م بعد 30 إلى 90 يوما من العدوى الأولية. بالضد منه، فإن الغلوبولين المناعي ج يمكن إيجاده بعد 60 سنة، وهو دليل مفيد في غياب الأعراض على وجود عدوى قديمة. يصل الغلوبولين المناعي ج إلى قمة تركيزه بعد 14–21 يوما من العدوى الأولية. أما في حالات العدوى التالية، فإن الوصول إلى التركيز الأقصى يحدث أبكر وعادة ما تكون التراكيز أعلى. يوفر كل من كل من الغلوبولين المناعي ج والغلوبولين المناعي م المناعة الواقية من العدوى بالنمط المصلي للفيروس.[10][14][21] قد تكون هنالك تفاعلية متقاطعة مع الأنواع الأخرى من الفيروسة المصفرة في اختبارات الغلوبولين المناعي ج والغلوبولين المناعي م مما قد يعطي نتائج إيجابية خاطئة بعد عدوى مستجدة أو لقاح لفيروس الحمى الصفراء أو التهاب الدماغ الياباني.[13] لا يعد الكشف عن الغلوبولين المناعي ج تشخيصيا ما لم تجمع عينات الدم تفصلها فترة 14 يوما والكشف عن زيادة أربع أضعاف في مستويات الغلوبولين المناعي ج. يعد الكشف عن الغلوبولين المناعي م في شخص تظهر عليه الأعراض كشفا تشخيصيا.[10]
الوقاية


لا توجد لقاحات مضادة لفيروس الضنك مرخصة الاستخدام.[6] لذا فإن الوقاية تعتمد على مكافحة البعوض الناقل له ومنع لدغاتها.[23][42] تنصح منظمة الصحة العالمية ببرنامج تحكم متكامل بالنواقل يتكون من خمسة عناصر:[23]
- المساندة وتعبئة الاجتماعية والتشريعات التي تضمن تقوية المجتمعات والهيئات الصحية العامة.
- التعاون بين الصحة والقطاعات الأخرى (العامة والخاصة).
- منهاج متكامل لمكافحة المرض من خلال الاستخدام الأقصى للموارد.
- صناعة قرار مستند على الأدلة لضمان توجيه أي تدخل بشكل ملائم.
- بناء الاستيعاب لضمان استجابة كافية للوضع المحلي.
تقوم الطريقة الأولية لمكافحة الزاعجة المصرية على التخلص من الموائل.[23] تجرى هذه الطريقة عن طريق التخلص من المياه مفتوحة المصدر أو إضافة مبيدات الحشرات أو مواد المكافحة الحيوية لهذه المناطق إن أمكن.[23] ولا يعتقد أن الرش العام للمبيدات من نوع الفوسفات العضوي أو بيريثرويد والتي تجرى أحيانا على أنها فعالة.[9] إن تقليل كميات المياه المفتوحة من خلال التحوير البيئي طريقة مفضلة للمكافحة بسبب مسائل تتعلق بالتأثيرات الصحية السلبية للمبيدات الحشرية ومصاعب لوجستية أكبر متعلقة بمواد المكافحة.[23] يمكن للأفراد الوقاية من لدغات البعوض عن طريق ارتداء ملابس تغطي الجلد بالكامل أو استخدام الناموسية خلال الراحة أو استخدام طارد للحشرات (يعد ديت أكثرها فعالية).[27] مع ذلك، يبدو أن هذه الطرق ليست فعالة كفاية، كما يظهر في تكرار الجائحات التي تزداد في بعض الأماكن، ويحتمل أن التدمن يزيد من توطن الزاعجة المصرية. كما يحتمل اتساع مدى المرض بسبب التغيرات المناخية.[5]
يوم مكافحة حمى الضنك
يحتفل باليوم العالمي لمكافحة حمى الضنك (بالإنجليزية: International Anti-Dengue Day) في 15 يونيو من كل عام.[43] تم الاتفاق على هذه الفكرة في عام 2010 وعقد أول مرة في جاكرتا في إندونيسيا عام 2011.[43] عقدت المناسبات التالية في يانغون في ميانمار عام 2012 وفي فيتنام في 2013.[43] الهدف منه هو زيادة وعي المجتمع بحمى الضنك واستنفار الجهود للوقاية من المرض ومكافحته وإظهار الالتزام الآسيوي بمعالجة المرض.[44]
العلاج
لا يوجد مضاد فيروسي محدد للضنك، لكن من المهم الحفاظ على توازن سوائل مناسب.[13] العلاج يعتمد على الأعراض.[45] الأشخاص لقادرون على الشرب وإدرار البول وليس لديهم علامات خطر فهم في هذه الحالة صحيون ويمكن معالجتهم في البيت ومتابعتهم يوميا واستخدام العلاج بالإرواء الفموي.[45] أما الأشخاص الذين يعانون من مشاكل صحية أخرى ولديهم علامات خطر ولا يمكن متابعة حالاتهم بانتظام فيجب أن يعتنى بهم في المستشفى.[11][45] أما الذين يعانون من حمى الضنك الشديد فيجب تقديم العناية لهم في أماكن يسهل فيها الحصول على عناية مركزة.[45]
في الحالة الحاجة لتعويض السوائل وريديا فعادة ما تكون الحاجة ليوم أو يومين فقط.[45] تتم معايرة معدل إعطاء السوائل مع النتاج البولي بنسبة .5–1 مل/كغم/ساعة، ليوازن العلامات الحيوية وتسويه مكداس الدم.[11] ينصح باستخدام أقل كمية من السوائل للحصول على هذه النتيجة.[45] يجب تجنب العمليات الطبية التداخلية مثل التنبيب الأنفي المعدي والحقن العضلي ووخز الشرايين بسبب مخاطر النزف.[11] يستخدم الباراسيتامول (أو الأسيتامينوفين) للحمى والضيق بينما يجب تجنب مضادات الالتهاب اللاستيرويدية مثل الإيبوبروفين والأسبرين بسبب لأنها قد تفاقم من خطر النزف.[45] يبدأ بنقل الدم مبكرا للأشخاص الذين يعانون من علامات حيوية غير مستقرة ويعانون من نقصان في مكداس الدم عوضا عن انتظار نقصان تركيز الهيموغلوبين إلى مستويات محتومة تستدعي نقل الدم.[46] يتطلب استخدام كريات حمر مكدوسة أو دم كامل، أما الصفيحات الدموية والبلازما المجمدة الطازجة فغالبا لا يتطلب استخدامها.[46] لا توجد ادلة كافية توضح فيم إذا كان استخدام الكورتيكوستيرويدات له تأثير إيجابي أو سلبي على حمى الضنك.[47]
يجب إيقاف إعطاء السوائل وريديا خلال فترة المعافاة لمنع حدوث حالة فرط حجم الدم.[11] إذا حدثت حالة فرط حجم الدم وكانت العلامات الحيوية مستقرة فقد يكون كل ما يحتاجه هو إيقاف أي سوائل أخرى.[46] إذا كان المريض خارجا من المرحلة الحرجة فيمكن استخدام مدر بول عروي مثل فوروسيميد للتخلص من السوائل الزائدة في جهاز الدوران.[46]
انتشار المرض
هذا القسم فارغ أو غير مكتمل. ساهم في توسيعه. |

تنتقل عدوى الضنك بواسطة بعوض الآييدس، تحديدا بعوض A. aegypti وA. albopictus.. وقد تنتقل عدوى الضنك أيضا بواسطة منتجات الدم الفاسدة (المعدية) (نقل الدم، البلازما والصفائح الدموية) ولكن يظل مستوى هذه المشكلة مجهولا.[48]

ظهرت أول أوبئة الضنك في الثمانينات من القرن الثامن عشر ميلادية بعد اكتشاف وتسمية المرض بفترة قصيرة وفي نفس التوقيت في كل من آسيا، أفريقا وأمريكا الشمالية. في الخمسينات من القرن العشرين حصلت جائحة لحمى الضنك في الجنوب الشرقي لقارة آسيا، وبحلول العام 1975 باتت حمى الضنك النزفية سببا رئيسيا لموت الأطفال في تلك المنطقة. أصبح وباء حمى الضنك أكثر شيوعا منذ الثمانينات من القرن العشرين وبأواخر التسعينات من القرن ذاته أصبحت حمى الضنك أهم الأمراض المنتقلة للإنسان بواسطة البعوض بعد مرض الملاريا وذلك بحوالي 40 مليون حالة لحمى الضنك وعدة مئات من الألوف لحالات حمى الضنك النزفية سنويا. تميل حمى الضنك إلى التفشي بشكل كبير كل 5 إلى 6 أشهر. يعتقد بأن الارتفاع والانخفاض الدوري في أعداد حالات حمى الضنك يحدث نتيجة لدورات موسمية من التفاعل مع المناعة المشتركة قصيرة الأمد بين جميع الأنماط المصلية الأربعة (تداخل مناعي) داخل الأشخاص الذين أصيبوا بحمى الضنك. وبانتهاء هذه المناعة المشتركة، يصبح السكان أكثر عرضة لانتقال العدوى وقت حلول موعد التفشي الموسمي المقبل. وبذلك فإنه مع مرور الوقت يتبقى أعداد كبيرة من الأشخاص المعرضين للإصابة بالمرض في التجمعات السكانية المصابة على الرغم من التفشيات السابقة للمرض بسبب وجود أربعة أنماط مصلية مختلفة لفيروس الضنك ولوجود أفراد غير معرضين من حديثي الولادة أو المهاجرين.
هنالك أدلة ملموسة_ اقتُرحت في الأصل بواسطة (S.B. Halstead) في السبعينات من القرن العشرين _ تشير إلى أن حمى الضنك النزفية تحدث على الأرجح في المرضى المصابين بعدوى ثانوية بواسطة أحد الأنماط المصلية الأربعة لحمى الضنك يختلف عن مسبب الإصابة السابقة. هنالك نموذج يستخدم لشرح هذه العملية يعرف بـ (التعزيز المعتمد على الأجسام المضادة) (ADE) والذي يسمح بزيادة استيعاب الفيروس واستنساخه أثناء عدوى ثانوية بسلالة أخرى، من خلال ظاهرة مناعية تعرف بـالإنجليزية بـ (original antigenic sin) وتعني أن الجهاز المناعي يفضل استخدام ذاكرته المناعية التي سجلت استجابته للعدوى الأولية ويستخدمها بلا تحوير مع هذه العدوى الجديدة المختلفة قليلا، حينها يصبح جهاز المناعة غير قادر على الاستجابة الكافية للعدوى الجديدة، فتصبح العدوى الثانوية حينها أكثر خطورة.[49] تعرف هذه العملية أيضا باسم (العدوى الإضافية).[50][51]
في عام 2002 وجد أن المرض يستوطن جنوب المحيط الهادي وآسيا والكاريبي والمناطق الاستوائية الأمريكية والأفريقية. هذا وتعتبر حمى الضنك من الأمراض المدارية المهملة، كما أنها تقتل قرابة 22 ألف شخص سنويا حول العالم لذلك ينصح بالقضاء على البعوض في ظل عدم توفر العلاجات بشكل تجاري.[52] الحالات التي يبلغ عنها من حمى الضنك لا تمثل العدد الفعلي لحالات الإصابة التي تشمل الحالات غير الظاهرة سريريا والحالات التي لم يطلب أصحابها الخدمة الطبية.في سنغافورة، يبلغ عن 4 إلى 5 آلاف حالة من حمى الضنك أو حمى الضنك النزفية سنويا.وفي العام 2004 حصلت 7 وفيات نتيجة متلازمة صدمة الضنك.[53]. عانت بوليفيا من وباء حمى الضنك بداية العام 2009 حيث أصيب 31 ألف شخصٍ ومات منهم 18 شخصا. حصل وباء أيضا في كيرنز (Cairns) التي تقع في كوينزلاند بأستراليا في الأول من ديسمبر من عام 2008م. وفي مارس عام 2009 كان هناك 503 حالة مؤكدة في المجتمع المكون من 152 ألفا و137 شخصا. بدأت بعدها الأوبئة تنتشر في المدن المجاورة. وكانت الحالات تشمل الأنماط الأربعة من الضنك. وفي الرابع من مارس 2009 أكدت صحة كوينزلاند أن امرأة مسنة ماتت في كرينز بسبب حمى الضنك كأول حالة وفاة منذ انتشار المرض. وبالرغم من أن المرأة كانت تعاني من مشاكل صحية أخرى إلا أن نتيجة فحصها كانت موجبة للإصابة بحمى الضنك مما يجعله سببا لوفاتها.انتشرت حمى الضنك أيضا كوباء في عدة مناطق من الأرجنيتين حيث بلغ عن أكثر من 9673 حالة في الحاديعشر من أبريل عام 2009 عن طريق وزارة الصحة. [1] يتسبب بعض المسافرين من المناطق الموبوءة بنقل المرض إلى مناطق أخرى. [2] بذلت جهود كبيرة لمحاربة الوباء في الأرجنتين مركزة على منع البعوض الناقل للمرض من التكاثر عن طريق تجفيف جميع المواطن المائية التي قد يتكاثر حولها البعوض. أقيمت أيضا حملة معلوماتية تهتم بمنع حمى الضنك وساهمت الحكومة برش المبيدات الحشرية لقتل البعوض..[54]
الانتعاش
خلال مرحلة الانتعاش يتمّ توقيف السوائل الوريدية لمنع حالة زيادة السوائل[55]. إذا حصلت زيادة السوائل والعلامات الحيوية مستقرّة قد يكون توقيف السوائل الأخرى كل ما هو مطلوب. إن لم يكن الشخص في مرحلة حرجة قد يتم استعمال الحلقة المدرّة للبول فوروسيميد لإزالة السوائل الزائدة من التداول.[56]
أصل الكلمة
أصل كلمة الضنك غير واضح تماما، لكن هناك فرضية تقول أنها مشتقة من عبارة من اللغة السواحلية (لغة سواحل أفريقيا الشرقية) وهي "Ka-dinga pepo" والتي تصف المرض كمرض تسببه روح شريرة.[57] وقد تكون الكلمة السواحلية "dinga " مشتقة من الكلمة الإسبانية "dengue" وتعني حساس أومتحفظ ويصعب إرضاؤه واصفة الشخص المصاب بحمى الضنك.[58] وقد يكون العكس صحيحا أيضا فتكون الكلمة الإسبانية مأخوذة من شبيهتها باللغة السواحلية.[59] عرفت أيضا بحمى المتأنق الغندور " Dandy Fever" حيث كانت مشية العبيد المصابين بالمرض غرب الهند توصف بأنها مشية متأنق.[60]
لمحة تاريخية
أول حالة يحتمل أنها حمى الضنك موجودة في موسوعة طبية صينية وقد أطلق عليها الصينيون "تسمم مائي" له علاقة بحشرة طائرة.[59] أول حالة حمى ضنك مؤكدة كانت عام 1789 وقد وصفها "بنيامين رش" بحمى تكسر العظم بسبب آلام العضلات والمفاصل المصاحبة لها.[61] ولم يعرف سببها الفيروسي وانتقالها بواسطة البعوض إلا في القرن العشرين. تسببت تحركات جموع الناس خلال الحرب العالمية الثانية بانتشار المرض في الكرة الأرضية كاملة. وبدأ اجتياح المرض كوباء عالمي من الجنوب الشرقي لآسيا بعد هذه الحرب ومنها انطلقت في العالم كله حتى الآن.
استخدام الفيروس كسلاح حيوي
تعد حمى الضنك واحدة من العوامل التي درست الولايات المتحدة الأمريكية إمكانية استخدامها كسلاح بيولوجي قبل أن تعطل الدولة برنامج الأسلحة البيولوجية.[62]
علم الأوبئة
معظم الناس الذين يعانون من حمى الضنك يتعافون دون أي مشاكل[63]. نسبة الوفيات تترواح بين 1-5% من دون علاج وأقل من 1% مع العلاج ولكن في حالة المرض الشديد ترتفع نسبة الوفيات إلى 26%[55]
مراجع
- ^ https://www.cdc.gov.tw/Category/Page/e6K1xXr0VJQ7FuxsMtMVhw. اطلع عليه بتاريخ 2020-04-28.
{{استشهاد ويب}}:|url=بحاجة لعنوان (مساعدة) والوسيط|title=غير موجود أو فارغ (من ويكي بيانات) (مساعدة) - ^ Disease Ontology (بالإنجليزية), 27 May 2016, QID:Q5282129
- ^ ا ب ج قاموس المورد، البعلبكي، بيروت، لبنان.
- ^ ا ب ج المعجم الطبي الموحد
- ^ ا ب ج د Normile D (2013). "Surprising new dengue virus throws a spanner in disease control efforts". Science. ج. 342 ع. 6157: 415. DOI:10.1126/science.342.6157.415. PMID:24159024.
- ^ ا ب ج د ه و ز ح ط ي يا Whitehorn J, Farrar J (2010). "Dengue". Br. Med. Bull. ج. 95: 161–73. DOI:10.1093/bmb/ldq019. PMID:20616106.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعBhatt2013 - ^ ا ب ج د ه و ز WHO (2009), pp. 14–16.
- ^ ا ب ج Reiter P (11 مارس 2010). "Yellow fever and dengue: a threat to Europe?". Euro Surveill. ج. 15 ع. 10: 19509. PMID:20403310.
- ^ ا ب ج د ه Gubler DJ (2010). "Dengue viruses". في Mahy BWJ, Van Regenmortel MHV (المحرر). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. ص. 372–82. ISBN:0-12-375147-0.
- ^ ا ب ج د ه و ز ح ط ي يا يب يج يد يه يو يز يح يط ك كا كب Ranjit S, Kissoon N (يناير 2011). "Dengue hemorrhagic fever and shock syndromes". Pediatr. Crit. Care Med. ج. 12 ع. 1: 90–100. DOI:10.1097/PCC.0b013e3181e911a7. PMID:20639791.
- ^ ا ب ج د ه Varatharaj A (2010). "Encephalitis in the clinical spectrum of dengue infection". Neurol. India. ج. 58 ع. 4: 585–91. DOI:10.4103/0028-3886.68655. PMID:20739797.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ ا ب ج د ه و ز ح ط ي يا يب يج يد يه يو يز يح يط ك كا كب كج Simmons CP, Farrar JJ, Nguyen vV, Wills B (أبريل 2012). "Dengue". N Engl J Med. ج. 366 ع. 15: 1423–32. DOI:10.1056/NEJMra1110265. PMID:22494122.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) وسم<ref>غير صالح؛ الاسم "NEJM2012" معرف أكثر من مرة بمحتويات مختلفة. - ^ ا ب ج د ه و ز ح Chen LH, Wilson ME (أكتوبر 2010). "Dengue and chikungunya infections in travelers". Current Opinion in Infectious Diseases. ج. 23 ع. 5: 438–44. DOI:10.1097/QCO.0b013e32833c1d16. PMID:20581669.
- ^ ا ب ج د ه و ز ح ط ي يا يب يج يد WHO (2009), pp. 25–27. وسم
<ref>غير صالح؛ الاسم "WHOp25" معرف أكثر من مرة بمحتويات مختلفة. - ^ ا ب Wolff K, Johnson RA (eds.) (2009). "Viral infections of skin and mucosa". Fitzpatrick's color atlas and synopsis of clinical dermatology (ط. 6th). New York: McGraw-Hill Medical. ص. 810–2. ISBN:978-0-07-159975-7.
{{استشهاد بكتاب}}:|author=باسم عام (مساعدة) - ^ Knoop KJ, Stack LB, Storrow A, Thurman RJ (eds.) (2010). "Tropical medicine". Atlas of emergency medicine (ط. 3rd). New York: McGraw-Hill Professional. ص. 658–9. ISBN:0-07-149618-1.
{{استشهاد بكتاب}}:|author=باسم عام (مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب ج د ه Gould EA, Solomon T (فبراير 2008). "Pathogenic flaviviruses". The Lancet. ج. 371 ع. 9611: 500–9. DOI:10.1016/S0140-6736(08)60238-X. PMID:18262042.
- ^ ا ب ج د ه و ز ح Rodenhuis-Zybert IA, Wilschut J, Smit JM (أغسطس 2010). "Dengue virus life cycle: viral and host factors modulating infectivity". Cell. Mol. Life Sci. ج. 67 ع. 16: 2773–86. DOI:10.1007/s00018-010-0357-z. PMID:20372965.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب ج Carod-Artal FJ, Wichmann O, Farrar J, Gascón J (سبتمبر 2013). "Neurological complications of dengue virus infection". Lancet Neurol. ج. 12 ع. 9: 906–19. DOI:10.1016/S1474-4422(13)70150-9. PMID:23948177.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب ج د ه و ز ح ط ي Guzman MG, Halstead SB, Artsob H؛ وآخرون (ديسمبر 2010). "Dengue: a continuing global threat". Nature Reviews Microbiology. ج. 8 ع. 12 Suppl: S7–S16. DOI:10.1038/nrmicro2460. PMID:21079655.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|author=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Solomonides، Tony (2010). Healthgrid applications and core technologies : proceedings of HealthGrid 2010 (ط. [Online-Ausg.].). Amsterdam: IOS Press. ص. 235. ISBN:978-1-60750-582-2.
- ^ ا ب ج د ه و WHO (2009), pp. 59–64.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعWHO2012 - ^ "Travelers' Health Outbreak Notice". Centers for Disease Control and Prevention. 2 يونيو 2010. مؤرشف من الأصل في 2010-08-26. اطلع عليه بتاريخ 2010-08-27.
{{استشهاد ويب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ "Vector-borne viral infections". World Health Organization. اطلع عليه بتاريخ 2011-01-17.
- ^ ا ب Center for Disease Control and Prevention. "Chapter 5 – dengue fever (DF) and dengue hemorrhagic fever (DHF)". 2010 Yellow Book. اطلع عليه بتاريخ 2010-12-23.
- ^ St. Georgiev, Vassil (2009). National Institute of Allergy and Infectious Diseases, NIH (ط. 1). Totowa, N.J.: Humana. ص. 268. ISBN:978-1-60327-297-1.
- ^ Wilder-Smith A, Chen LH, Massad E, Wilson ME (يناير 2009). "Threat of dengue to blood safety in dengue-endemic countries". Emerg. Infect. Dis. ج. 15 ع. 1: 8–11. DOI:10.3201/eid1501.071097. PMC:2660677. PMID:19116042.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Stramer SL, Hollinger FB, Katz LM؛ وآخرون (أغسطس 2009). "Emerging infectious disease agents and their potential threat to transfusion safety". Transfusion. 49 Suppl 2: 1S–29S. DOI:10.1111/j.1537-2995.2009.02279.x. PMID:19686562.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|author=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Teo D, Ng LC, Lam S (أبريل 2009). "Is dengue a threat to the blood supply?". Transfus Med. ج. 19 ع. 2: 66–77. DOI:10.1111/j.1365-3148.2009.00916.x. PMC:2713854. PMID:19392949.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Wiwanitkit V (يناير 2010). "Unusual mode of transmission of dengue". Journal of Infection in Developing Countries. ج. 4 ع. 1: 51–4. DOI:10.3855/jidc.145. PMID:20130380.
- ^ ا ب ج د ه و Martina BE, Koraka P, Osterhaus AD (أكتوبر 2009). "Dengue virus pathogenesis: an integrated view". Clin. Microbiol. Rev. ج. 22 ع. 4: 564–81. DOI:10.1128/CMR.00035-09. PMC:2772360. PMID:19822889.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب ج د ه و ز WHO (2009), pp. 10–11.
- ^ Halstead، Scott B. (2008). Dengue. London: Imperial College Press. ص. 180 & 429. ISBN:978-1-84816-228-0.
- ^ ا ب ج WHO (2009), pp. 90–95.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعYacoub2014 - ^ Comprehensive guidelines for prevention and control of dengue and dengue haemorrhagic fever (PDF) (ط. Rev. and expanded.). New Delhi, India: World Health Organization Regional Office for South-East Asia. 2011. ص. 17. ISBN:978-92-9022-387-0.
- ^ ا ب ج WHO (1997). "Chapter 2: clinical diagnosis". Dengue haemorrhagic fever: diagnosis, treatment, prevention and control (PDF) (ط. 2nd). Geneva: World Health Organization. ص. 12–23. ISBN:92-4-154500-3.
- ^ Wiwanitkit، V (يوليو 2010). "Dengue fever: diagnosis and treatment". Expert review of anti-infective therapy. ج. 8 ع. 7: 841–5. DOI:10.1586/eri.10.53. PMID:20586568.
- ^ "New CDC test for dengue approved". Centers for Disease Control and Prevention. 20 يونيو 2012.
- ^ WHO (2009), p. 137.
- ^ ا ب ج "Marking ASEAN Dengue Day". اطلع عليه بتاريخ 2015-06-16.
- ^ ACTION AGAINST DENGUE Dengue Day Campaigns Across Asia. World Health Organization. 2011. ISBN:9789290615392.
- ^ ا ب ج د ه و ز WHO (2009), pp. 32–37.
- ^ ا ب ج د WHO (2009), pp. 40–43.
- ^ Zhang، F؛ Kramer، CV (1 يوليو 2014). "Corticosteroids for dengue infection". The Cochrane database of systematic reviews. ج. 7: CD003488. DOI:10.1002/14651858.CD003488.pub3. PMID:24984082.
- ^ Wilder-Smith A, Chen LH, Massad E, Wilson ME (2009). "Threat of dengue to blood safety in dengue-endemic countries". Emerg Infect Dis. ج. 15 ع. 1: 8–11. DOI:10.3201/eid1501.071097. PMID:19116042.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Rothman AL (2004). "Dengue: defining protective versus pathologic immunity". J. Clin. Invest. ج. 113 ع. 7: 946–51. DOI:10.1172/JCI200421512. PMC:379334. PMID:15057297.
- ^ Nowak MA, May RM (1994). "Superinfection and the evolution of parasite virulence". Proceedings. Biological sciences / the Royal Society. ج. 255 ع. 1342: 81–9. DOI:10.1098/rspb.1994.0012. PMID:8153140.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|month=تم تجاهله (مساعدة) - ^ Levin SA، Pimentel D (1981). "Selection of intermediate rates of increase in parasite-host systems". American Naturalist. ج. 117: 308–15. DOI:10.1086/283708.
- ^ حمى الدنج تقتل 65 شخصا فقط في كمبوديا العام الحالي - رويترز - تاريخ النشر 29 ديسمبر-2008- تاريخ الوصول 29 ديسمبر-2008
- ^ http://www.sciencedirect.com/science?_ob=ArticleURL&_udi=B7CPT-4KKNNH5-2&_user=130561&_rdoc=1&_fmt=&_orig=search&_sort=d&view=c&_acct=C000010878&_version=1&_urlVersion=0&_userid=130561&md5=4cc1b9743b4fddf5a0567b16b99bc130
- ^ Marcos Wozniak (12 مارس 2009)،
{{استشهاد}}: الوسيط|title=غير موجود أو فارغ (مساعدة)صيانة الاستشهاد: التاريخ والسنة (link). - ^ ا ب http://www.ncbi.nlm.nih.gov/pubmed/20639791
- ^ WHO (2009). Dengue Guidelines for Diagnosis, Treatment, Prevention and Control. Geneva: World Health Organization. ISBN 9241547871. http://whqlibdoc.who.int/publications/2009/9789241547871_eng.pdf.
- ^ "Dengue fever: essential data". 1999. اطلع عليه بتاريخ 2008-10-05.
- ^ Harper D (2001). "Etymology: dengue". Online Etymology Dictionary. اطلع عليه بتاريخ 2008-10-05.
- ^ ا ب "etymologia: dengue" (PDF). Emerging Infectious Diseases. ج. 12 ع. 6: 893. 2006.
- ^ url=http://www.medterms.com/script/main/art.asp?articlekey=6620
- ^ Gubler DJ (1998). "Dengue and dengue hemorrhagic fever". Clinical microbiology reviews. ج. 11 ع. 3: 480–96. PMC:88892. PMID:9665979.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|month=تم تجاهله (مساعدة) - ^ "Chemical and Biological Weapons: Possession and Programs Past and Present", James Martin Center for Nonproliferation Studies, Middlebury College, April 9, 2002, accessed November 14, 2008.
- ^ http://whqlibdoc.who.int/publications/2009/9789241547871_eng.pdf
| في كومنز صور وملفات عن: حمى الضنك |
