حمض نووي ريبوزي منقوص الأكسجين: الفرق بين النسختين
| [نسخة منشورة] | [نسخة منشورة] |
إضافة عنوان: التقنية النانوية للدنا |
إضافة عنوان: التاريخ والأنثروبولوجيا |
||
| سطر 284: | سطر 284: | ||
=== التاريخ والأنثروبولوجيا === |
=== التاريخ والأنثروبولوجيا === |
||
{{مفصلة|علم الوراثة العرقي|علم الأنساب الجيني}} |
{{مفصلة|علم الوراثة العرقي|علم الأنساب الجيني}} |
||
لأن [[طفرة (أحياء)|الطفرات]] تتراكم في الدنا مع مرور الوقت وبعدها يتم [[توريث (أحياء)|توريثها]] للأجيال التالية، فإن الدنا يحتوي على معلومات تاريخية وبمقارنة تسلسلات الدنا المختلفة يمكن لعلماء الوراثة استنتاج [[علم الأحياء التطوري|التاريخ التطوري]] للكائنات وهذا ما يعرف ب[[علم الوراثة العرقي]] <ref>{{cite journal | vauthors = Wray GA | title = Dating branches on the tree of life using DNA | journal = Genome Biology | volume = 3 | issue = 1 | pages = REVIEWS0001 | year = 2002 | pmid = 11806830 | pmc = 150454 | doi = 10.1046/j.1525-142X.1999.99010.x | nopp = true }}</ref>. يشكل هذا المجال -بوضع [[علم الوراثة]] في خدمة [[علم أحياء الحفريات]]- أداة قوية في [[علم الأحياء التطوري]]، إذا تمت مقارنة سلاسل الدنا داخل نفس [[نوع (تصنيف)|النوع]] يمكن لعلماء [[وراثيات سكانية|الوراثيات السكانية]] معرفة تاريخ شعوب معينة، ويمكن استخدام ذلك في دراسات تترواح بين [[علم الوراثة البيئي]] إلى [[علم الإنسان|الأنثروبولوجيا]]. |
|||
دراسة [[دنا المتقدرة]] داخل التجمعت البشرية يستخدم لتحديد [[هجرة بشرية|هجرات]] [[إنسان عاقل|الإنسان العاقل]]، على سبيل المثال تمت دراسة [[نمط جماعي |النمط الجماعي]] [[نمط جماعي|X]] في [[علم الديموغرافيا القديم]] لتقييم القرابة المحتملة ل[[أسلاف الهنود]] بالشعوب الأوربية التي تعود أصولها إلى [[عصر حجري قديم علوي|العصر الحجري القديم العلوي]]. <ref name="10.1002/humu.20921">{{Article| nom1 = Mannis van Oven et Manfred Kayser| titre = Updated comprehensive phylogenetic tree of global human mitochondrial DNA variation| périodique = Human Mutation| volume = 30| numéro = 2| jour = | mois = février| année = 2009| pages = E386-E394| url texte = http://onlinelibrary.wiley.com/doi/10.1002/humu.20921/abstract| consulté le = 27 mars 2015| doi = 10.1002/humu.20921| pmid = 18853457| pmc = }}</ref> |
|||
<gallery mode="packed" heights="220"> |
|||
شجرة الحياة مبسطة.svg| [[شجرة تطور السلالات]] توضح [[نطاق (تصنيف)|نطاقات]] الأحياء الثلاثة: [[حقيقيات النوى]] بالأحمر، [[بكتيريا قديمة|العتائق]] بالأخضر وال[[بكتيريا]] بالأزرق.<ref name="10.1126/science.1123061">{{article | langue = en | nom1 = Francesca D. Ciccarelli, Tobias Doerks, Christian von Mering, Christopher J. Creevey, Berend Snel et Peer Bork | titre = Toward automatic reconstruction of a highly resolved tree of life | journal = Science | volume = 311 | numéro = 5765 | pages = 1283–1287 | année = 2006 | url texte = http://isites.harvard.edu/fs/docs/icb.topic136804.files/Apr_30_Sanderson/Ciccarella_et_al_2006.pdf | pmid = 16513982 | doi = 10.1126/science.1123061 | bibcode = 2006sci...311.1283c}}</ref> |
|||
Map-of-human-migrations.jpg | خريطة [[هجرة بشرية|الهجرة البشرية]] المستنتجة من دراسات [[علم الوراثة العرقي]] ل[[دنا المتقدرة]] [[إنسان عاقل|البشري]]، المقياس 1000 سنة [[قبل الحاضر]].<ref name="http://www.mitomap.org/MITOMAP">{{Lien web | langue = en | format = pdf | url = http://www.mitomap.org/pub/MITOMAP/MitomapFigures/WorldMigrations.pdf | titre = Human mtDNA Migrations | année = 2002 | site = [http://www.mitomap.org/MITOMAP MITOMAP, A human mitochondrial genome database] | consulté le = 27 mars 2015}}</ref> |
|||
</gallery> |
|||
=== تخزين المعلومات === |
|||
{{رئيسية| تخزين الدنا للبيانات الرقمية}} |
|||
== انظر أيضا == |
== انظر أيضا == |
||
نسخة 14:24، 17 أبريل 2018

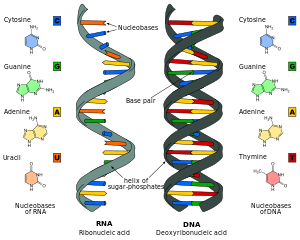
الحمض الريبوزي النووي المنزوع الأكسجين أو حمض الديوكسي ريبونيوكليك[1] أو الحمض النووي الريبوزي منقوص الأكسجين أو الحمض النووي الصبغي أو كما يسمى في هذه المقالة دي إن إيه (DNA) بالإنجليزية، والدِنا هو مجموعات كبيرة متكررة من الأحماض النووية تتشكل في هيئة سلسلتين طويلتين حلزونتين من الجزيئات وتربط بين السلسلتين أحماضا نووية مثل درجات السلم. الدي أن إيه هو العماد الأساسي للكائنات الحية ووجود الحياة على الأرض. إذ أنه يمكن أن يكرر نفسه، أي يصنع مثيلا له. وهو الذي يحتوي على التعليمات الجينية التي تصف التطور البيولوجي للكائنات الحية ومعظم الفيروسات؛ كما أنه يحوي التعليمات الوراثية اللازمة لتكوين أعضاء الجنين سواء في الرحم أو البيضة أو النبات، أي لكل الكائنات الحية.
يعتبر وسيلة التخزين الطويل الأجل للمعلومات الوراثية وهي الوظيفة الأساسية لجزيئات الدي أن إيه بالإضافة إلى أنه يمكن من خلال هذه الجزيئات الحصول على المعلومات اللازمة لبناء البروتينات والحمض الريبي النووي (بالإنجليزية: RNA). تسمى قطع الدي أن إيه (DNA) التي تحمل معلومات وراثية يمكن ترجمتها لبروتينات بالمورثات أو الجينات. تتواجد بعض قطع الدي أن إيه لأغراض تركيبية وتنظيمية.
كيميائياً؛ يتكون الدي أن إيه من سلسلتين من الجزيئات مرتبطتين ببعضهما البعض وتشكل اللولب المزدوج. وهذه السلسلتان تمثلان ضلعي "سلم"، وحداته البنائية تسمى النيوكليوتيدات. وتتكون السلسلتان من سكر خماسي الكربون ريبوزي منقوص الأكسجين ومجموعة فوسفات. وتربط القواعد النتروجينية - وهي تمثل درجات السلم - بين السلسلتين؛ وهذه القواعد النتروجينة هي: غوانين (G) وأدينين (A) وثيمين (T) وسيتوزين (C). وكل قاعدتين تشكل درجة من درجات "السلم" تربط الضلعين ببعضهما البعض. وكل اثنين من تلك النيوكليوتيدات (القواعد النتروجينية) ترتبط مع بعضها البعض برابطة تساهمية، ويتم الإرتباط بين جزيئات السكر والفوسفات بشكل متتابع لتكوين ما يعرف بهيكل سكر الفوسفات (الضلعين). وبناء على قواعد الإرتباط، فإن كل سلسلة دي أن إيه تحتوي على قواعد نيتروجينية ترتبط ببعضها (الأدنين مع الثيامين والجوانين مع السايتوسين) برابطة هيدروجينية مكونة بذلك الروابط العرضية للحلزون المزدوج (السلم).
لكل من غوانين (G) وأدينين (A) وثيمين (T) وسيتوزين (C) شكله الخاص. فشكل الأدينين (A) يرتبط ب ثيمين (T)؛ والسيتوزين (C) يمكن أن يرتبط مباشرة بالغوانين (G). وتسمى هذه "أزواج قواعد" Base pairs. ويمكن بناءا على ذلك تخيل أن جزيء الدي أن إيه عبارة عن سلم حلزوني تتكون فيه كل درجة من زوج قواعد واحد. وعلى هذا الأساس تكون هناك أربعة احتمالات للترابط وتكوين درجة للسلم T-A , A-T : C-G , G-C : فإذا حدث وأن أصاب أحد القواعد تلفا أو ضاع، فإن تعويضه يمكن أن يتم بسهولة عن طريق نصف الدرجة الباقي فلا يتم تعويض ثيمين T مثلا إلا بثيمين T. أي أن الحلزون المزدوج في استطاعته تكوين نسخة منه، حيث أن كلا الضلعين يمكن أن يكون قالبا لصناعة نسخة منه. فإذا قمت بقسم السلم إلى ضلعيه عبر الروابط بين أزواج القواعد بطول الدي أن إيه ، فإن كل من الضلعين يحوي المعلومات الكاملة لإعادة بناء نسخة من الأصل.
بالتالي يمكن تصور أن الدي أن إيه عبارة عن مخطوطة، أو برمجة سوفتوير، موجودة في نواة خلية. واللغة المكتوبة بها تتكون من أربعة حروف. والجملة المكونة من عدة كلمات منها تعرف بأنها جين. وكل جين يتكون من مئات أو آلاف الحروف. وجميع الوظائف التي تؤديها الخلية - حتى لو كانت خلية بشرية معقدة مثلنا - فهي تنظم عملها وفقا لترتيب الشفرة المكتوبة بالحروف الأربعة في هذا المخطوط.
يعطي تتابع القواعد النيتروجينية على طول هيكل سكر الفوسفات في جزيء الدي أن إيه شفرات codes يمكن من خلالها تحديد تتابع الأحماض الأمينية التي تكون البروتين. ويتم ذلك كما يلي: يتم نسخ جزيء آر أن إيه مقابلا لجزيء الدي أن إيه المحتوي على كود البروتين في عملية تسمي بعملية النسخ. ويتم ترجمة الرموز إلى أحماض أمينية مقابلة خلال عملية الترجمة لتعطي البروتين المقابل. وليس بالضرورة أن تترجم كامل الشفرة إلى بروتين إذ أن بعض جزيئات الآر أن إيه تقوم بوظائف تركيبية أخرى مثل الريبوسومات وجسيمات التضفير.
حجم الدي أن إيه داخل كل خلية ضخم فلذلك يرتبط ببروتين يسمى الهستون وهو مشحون بشحنة موجبة فيستطيع الإرتباط بالدي أن إيه ذو الشحنة السالبة فيكون تركيبات تسمى الكروموسومات، والكروموسومات في مجموعها تكون ما يعرف بالجينوم (المحتوى الجيني أو الصبغي للخلية). وقبل أنقسام الخلية تتضاعف الصبغيات فيما يعرف بتضاعف الدي أن إيه ويتم ذلك في كل من بدائيات النوى وفي حقيقيات النواة.
لمحة تاريخية
تعود أول ملاحظة للدي أن إيه في العلم الحديث للطبيب السويسري فريدريك ميسشر في سنة 1869 عندما استطاع استخلاص مادة مجهرية من القيح واسمها نووين (نيوكلين) بسبب وجودها داخل النواة. وفي سنة 1929 استطاع فيبي ليفني من اكتشاف مكونات الوحدة الأساسية للدي أن إيه وهي النوويدات وبين أن الدي أن إيه ما هو إلا تكرار لهذه الوحدة.
في سنة 1943 أجرى أوزوالد آفري تجربة بمزج بكتيريا نيموكوكس (الاسم العلمي: Pneumococcus) ميتة وتحمل خاصية السطح الناعم مع بكتيريا حية من نفس النوع ولكنها ذات سطح خشن. نتائج التجربة كانت انتقال خاصية السطح الخشن إلى البكتيريا ذات السطح الناعم. وسمي الدي أن إيه بالعامل الناقل.
و في سنة 1953 وبالاعتماد على الصور السينية المأخوذة بواسطة روزاليند فرانكلين والمعلومات المتوفرة عن القواعد وطريقة ارتباطها ببعضها، طرح كل من جيمس واتسون وفرانسيس كريك نموذجهما (اللولبي المزدوج)و نشروا تجاربهم في مجلة الطبيعة. وفي سنة 1957 وضح كريك العقيدة الأساسية لعلم الأحياء الجزيئي ووضح العلاقة ما بين الدي أن إيه والآر أن إيه(RNA) والبروتينات. وبين كريك لاحقا أن الكودونات تتكون من 3 قواعد مما ساعد علماء آخرين على فك الشيفرة الوراثية وتحديد الكودونات المشفرة للأحماض الأمينية. وفي سنة 1958 أوضح العالمان ميليسون وستال طريقة تناسخ الدي أن إيه ووصفاها بالشبه محافظة. حصل واتسون وكريك وموريس على جائزة نوبل في الطب لاكتشافاتهم في هذا الحقل في سنة 1962.
الخصائص
الدنا عبارة عن بوليمر طويل مكون من وحدات متكررة تسمى نوكليوتيدات [2][3]، بُنية الدنا ديناميكية على طول امتدادها، كونها قادرة على الالتفاف إلى حلقات ضيقة وأشكال أخرى [4]. في كل الأصناف يتكون الدنا من سلسلتين لولبيتين مربوطتين إلى بعضهما البعض بواسطة روابط هيدروجينية، كلا السلسلتين ملتفتان حول نفس المحور ولهما نفس طول السن الولبي 34 أنغستروم (3.4 نانومتر) والقطر 10 أنغستروم (1 نانومتر). [5] تبعا لدراسة أخرى تم فيها القياس في محلول مختلف، كان عرض سلسلة الدنا من 22 إلى 26 أنغستروم (2.2-2.6 نانومتر) وطول نوكليوتيدة واحدة 3.3 أنغستروم (0.33 نانومتر) [6]، رغم أن وحدة النوكليوتيد المتكررة صغيرة جدا إلا أن بوليمرات الدنـا يمكن أن تكون كبيرة جدا وتحوي ملايين أو مئات الملايين من النوكليوتيدات، مثلا: الدنا في أكبر كروموسوم بشري الصبغي 1 يتكون مما يقارب 220 مليون زوج قاعدي [7] وسيبلغ طوله 85 ملم لو تمت إطالته.
لا يتواجد الدنا عـادة في الكائنات الحية على شكل جزيء واحد، وإنما زوج من الجزيئات مشدود لبعضه بشدة [5][8]، يلتف هذان الجزيئان (الشريطان) حول بعضهما البعض على شكل لولب مزدوج، تحوي النوكليوتيد على كل من الوحدة الأساسية للجزيء (التي تضمن تماسك السلسلة) وقاعدة نووية (التي تتفاعل مع الشريط الآخر في اللولب). القاعدة النووية المرتبطة بسكر تسمى نيوكليوسيد والقاعدة المرتبطة بسكر ومجموعة من الفوسفات أو أكثر تسمى نوكليوتيد. البوليمر المتكون من عدة نوكليوتيدات مترابطة يسمى عَدِيْدُ النوكليوتيد. [9]
الوحدة الأساسية لسلسة الدنـا تتكون من سكر وفوسفات [10]، السكر في الدنا هو ريبوز منقوص الأكسجين وهو بنتوز (سكر يحتوي على خمس ذرات كربون)، ترتبط جزيئات السكر ببعضها بواسطة مجموعات فوسفات والتي تشكل روابط فوسفات ثنائية الأستر بين الذرة الثالثة والخامسة لحلقتي سكر متجاورتين. هذه الروابط اللامتناظرة تعني أن لسلسلة الدنا اتجاه، وفي اللولب المزدوج اتجاه النوكليوتيدات في أحد السلسلتين مضاد للاتجاه في السلسلة الأخرى وهذا يعني أن السلسلتين عكسيتا التوازي، نهايتا سلسلتا الدنا اللامتناظرتين يقال بأن لها اتجاهية خمسة فتحة (5') و ثلاثة فتحة (3') حيث تحتوي نهاية 5' على مجموعة فوسفات طرفية والنهاية 3' على مجموعة هيدروكسيل طرفية، أحد الفروق الكبيرة بين الدنا والرنا هو السكر ففي الرنا يحل مكان الريبوز منقوص الأكسجين بنتوز وهو الريبوز. [8]
يستقر اللولب المزدوج للدنا أساسا بواسطة قوتين: الروابط الهيدروجينية بين النوكليوتيدات وتفاعلات التراص بين القواعد النووية العطرية. [11]، في الوسط المائي للخلية روابط باي (π) المترافقة لقواعد النوكليوتيدات تتراص عموديا مع محور جزيء الدنا مقللة تفاعلاتها مع الصدفة المائية. القواعد الأربعة المكونة للدنا هي أدينين (A)، سايتوسين (C)، غوانين (G) والثايمين (T)، وترتبط هذه القواعد بـ سكر-فوسفات لتشكل نوكليوتيدات كاملة (الصور بالأسفل)، يرتبط الأدينين مع الثايمين والغوانين مع سايتوسين ويمثلان بالزوج القاعدي A-T والزوج القاعدي G-C. [12][13]
تصنيف وترابط القواعد النووية
تنقسم قواعد الدنا النووية الأساسية إلى قسمين: البيورينات ويندرج ضمنها الأدنين والغوانين وهما جزيئان ثنائيي الحلقة يحويان حلقتان متغايرتان مندمجتان إحدهما سداسية والأخرى خماسية، والبريميدينات ويندرج ضمنها السايتوسين والثايمين وهما جزيئان أحاديي الحلقة عبارة عن حلقة سداسية متغايرة[8]. تتشكل الأزواج القاعدية للولب المزدوج للدنا بترابط بيورين في إحدى السلسلتين مع بيريميدين في السلسلة الأخرى بواسطة اثنتين أو ثلاثة من الروابط الهيدروجينية:
- يرتبط الأدينين مع الثايمين بواسطة رابطتي هيدروجين ليشكل الرابطة A=T.
- يرتبط الغوانين مع السايتوسين بواسطة ثلاث روابط هيدروجينية ليشكل الرابطة G≡C.
يسمى هذا الترابط لقاعدتين نوويتين من سلسلتي اللولب المزدوج برابطة واتسون-كريك، يوجد نوع آخر من الترابط يسمى ترابط هوغستين يتم فيه ترابط قاعدتي الغوانين والسايتوسين بواسطة رابطتي هيدروجين. [14]، كون الروابط الهيدروجينية غير تساهمية يسمح بكسرها وإعادة ربطها بسهولة معتبرة ومنه يمكن فصل سلسلتي اللولب المزدوج للدنا كالسحاب سواء بقوة ميكانيكية أو بدرجة حرارة مرتفعة. [15] ونتيجة لهذا التكامل في ترابط القواعد فإن جميع المعلومات التي تحويها إحدى سلسلتي اللولب المزدوج منسوخة في السلسلة الأخرى وهو أمر أساسي في عملية تضاعف الدنا ومختلف وظائفه الأخرى لدى الكائنات الحية.[3]
توجد قاعدة نووية خامسة وهي بيريميدين يسمى اليوراسيل (U) يأخذ مكان الثايمين في الرنا (RNA) ويختلف عنه بأنه لا يملك مجموعة ميثيل في حلقته، بالإضافة إلى الدنا والرنا تم إنتاج العديد من نظائر الأحماض النووية الاصطناعية لدراسة خصائصها أو لاستعمالها في التقنية الحيوية.[16]
الاتجاه وضد الاتجاه

لإنتاج رنـا وظيفي لا يتم سوى نسخ جزء معين من إحدى سلسلتي الدنا التي تحوي على الجين وذلك لأن السلسلتين ليستا متماثلتين، ويقال لتسلسل الدنا بأنه "اتجاه" إذا كان مماثلا للتسلسل على نسخة الرنا الرسول التي تُرجمت إلى بروتين [17] ويكون ذلك في السلسلة التي لم يتم نسخها (انظر الشكل)، أما تسلسل السلسلة القالب (التي تم نسخها) فيسمى "ضد الاتجاه" وذلك لأنه مكمل لتسلسل الرنا الرسول. تسمى أحيانا السلسلة التي يتم نسخها "سلسلة التشفير" والمقابلة لها "سلسلة اللاتشفير" إلا أن هذه الدلالة صالحة فقط بالنسبة لجين معين وذلك لأن سلسلتي نفس اللولب المزدوج من الدنا يمكن أن تشفرا بروتينات مختلفة. يمكن أن يتواجد كلا التسلسُلَين "الاتجاه" و"ضد الاتجاه" على أجزاء مختلفة من نفس سلسلة الدنا (أي يمكن لكلا السلسلتين أن تحويا كلا من الاتجاه وضد الاتجاه).
يتم إنتاج تسلسلات رنـا ضد الاتجاه في كل من حقيقيات وبدائيات النوى، إلا أن وظائفها غير واضحة بالكامل [18]، ويشير أحد الإقتراحات إلى أن سلاسل الرنا ضد الاتجاه تساهم في ضبط التعبير الجيني عبر ترابط قواعد رنا-رنا. [19]
بعض تسلسلات الدنا في بدائيات وحقيقيات النوى وبنسبة أكثر في البلازميدات والفيروسات يتعسر فيها التمييز بين سلسلتي الاتجاه وضد الاتجاه لوجود جينات متداخلة [20]. في هذه الحالات تقوم تسلسلات الدنا بوظيفة مضاعفة، تشفير بروتين معين حين تتم قراءتها على طول إحدى السلسلتين، وبروتين آخر حين تقرأ في الاتجاه المعاكس على طول السلسلة الأخرى. في البكتيريا قد يساهم هذا التداخل في ضبط نسخ الجينات [21]، أما لدى الفيروسات فيزيد في مقدار المعلومة التي يمكن تشفيرها داخل جينوم فيروسي صغير. [22]
دنا فائق الالتفاف
يكون الدنا خلال معظم عمر الخلية ملفوفا بخفة حول الهستونات ولا يكون مركزا على هيئة كروموسوم، ولا يظهر اللف الفائق للدنا على شكل كروموسومات إلا خلال مرحلة انقسام الخلية [23]. يمكن لف الدنا مثل الحبل خلال عملية تسمى لف الدنا الفائق، وفي حالة الراحة تلتف سلسلة الدنا حول محور اللولب المزدوج مرة كل 10.4 زوج قاعدي، أما إن كان الدنا ملفوفا فإن سلسلتيه تصبحان أشد أو أخف التفافا [24]. حيث إن كان ملفوفا في اتجاه اللولب المزدوج فإن القواعد تصبح متراصة أكثر ويسمى ذلك الالتفاف الفائق الموجب إما إن كان ملفوفا عكس اتجاه اللولب المزدوج فإن القواعد تصبح أقل تراصا ويسمى ذلك بالالتفاف الفائق السالب. لِمعظمِ الدنا في الطبيعة التفافٌ فائق سلبي تُحدِثـه إنزيمات التوبوايزوميراز [25] ، هذه الانزيمات مطلوبة لتزيل التفاف سلسلتي الدنا أثناء عمليتي نسخ وتضاعف الدنا. [26]
أشكال الدنا

يتواجد الدنا على عدة أشكال منها الدنا أ، الدنا ب والدنا ز، رغم أنه لم يتم سوى ملاحظة الشكلين دنا أ ودنا ب في كائناتٍ وظيفيةٍ [10]. البنية التي يتخذها الدنا تعتمد على مستوى التميؤ، تسلسل الدنا، كمية واتجاه اللف الفائق، التغيرات الكيميائية للقواعد، نوع وتركيز الآيونات المعدنية ووجود متعددات الأمين في المحلول. [27]
لمعرفة بنية الدنا قام العلماء باستخدام تقنية دراسة البلورات بالأشعة السينية وكانت التقارير المنشورة الأولى حول أنماط حيود الأشعة السينية للدنا أ وب قد استخدمت دراسات مبنية على تحول باتيرسون التي أعطت معلومات محدودة عن هيئة سلال الدنا الموجهة [28][29]. وسنة 1953 تم اقتراح دراسات أخرى بواسطة ويلكنز وآل لأنماط حيود وانتشار الأشعة السينية للدنا ب العالي التميؤ في الكائنات الحية وكانت عبارة عن مربعات دوال بيسل [30]. وفي نفس الصحيفة قدم جيمس واتسون وفرنسيس كريك دراساتهما حول النموذج الجزيئي لأنماط حيود الأشعة السينية للدنا مقترحين أن الهيئة كانت لولبا مزدوجا. [5]
رغم أن الهيئة ب هي الأكثر شيوعا في الظروف الموجودة داخل الخلايا [31] إلا أنها ليست هيئة محددة بدقة وإنما عائلة متقاربة من هيئات الدنا [32] التي تظهر في حالات التميؤ العالية الموجودة داخل الخلايا الحية، وأنماط حيود وانتشار الأشعة السينية الخاصة بها هي سمة تميز البلورات الناقِصَة (paracrystals) مع درجة معتبرة من عدم الانتظام. [33][34]
مقارنة بالدنا ب فإن الدنا أ له قطر أكبر ويميني الإتجاه كذلك وله ثلم صغير سطحي وعريض وثلم كبير أضيق وأعمق، تظهر هذه الهيئة في الظروف غير الفيسيولوجية في عينات الدنا المجففة جزئيا، أما في الخلايا الحية فيمكن أن يتم إنتاجه في تزواج هجين لسلاسل الدنا والرنا وفي معقدات إنزيم-دنا. [35][36]، قِطعُ الدنا التي عُدِلت فيها القواعد كيميائيا بواسطة المثيلة يمكن أن تخضع لتحول كبير في الهيئة وتتخذ البنية ز التي تلتف فيها القواعد على يسار محور اللولب عكس البنية ب الأكثر شيوعا [37] هذا الشكل غير الاعتيادي يمكن التعرف عليه بواسطة بروتينات ترتبط بشكل خاص مع الدنا ز ويمكن أن يكون له دور في ضبط النسخ. [38]

| خصائص | دنا أ | دنا ب | دنا ز |
|---|---|---|---|
| اتجاه اللولب المزدوج | يمين | يمين | يسار |
| تكرار الوحدة | 1 bp | 1 bp | 2 bp |
| زاوية دوران اللولب المزدوج لكل زوج قاعدي | 32,7° | 34,3° | 60°/2 |
| عدد الأزواج القاعدية لكل دورة للولب المزدوج | 11 | 10,5 | 12 |
| السن اللولبي للولب المزدوج لكل دورة | 2.82 نانومتر | 3.32 نانومتر | 4.56 نانومتر |
| البعد بين القواعد داخل اللولب المزدوج | 0.26 نانومتر | 0.34 نانومتر | 0.37 نانومتر |
| القطر | 2.3 نانومتر | 2.0 نانومتر | 1.8 نانومتر |
| انحناء الأزواج القاعدية بالنسبة لمحور اللولب المزدوج | +19° | −1,2° | −9° |
| متوسط الالتواء (propeller twist) | +18° | +16° | 0° |
| اتجاه القواعد بالنسبة للسكر | عكس | عكس | بيريميدين : عكس بيورين : مع |
| انحناء روابط ذرات السكر (Sugar pucker) |
'C3-إندو | 'C2 - إندو | سايتوسين : 'C2 - إندو غوانين : 'C2 - إكسو |
أشكال خاصة
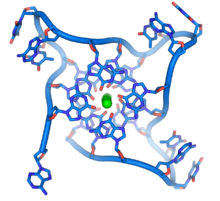
- موصل هوليداي: يتم تكوين موصل هوليداي خلال التأشيب المتماثل بين جزيئي دنا يحملان نفس المعلومة الوراثية (صبغيات متماثلة، كروماتيد شقيق)، لدى هذا الموصل هيئة على شكل صليب مع تسلسلات متماثلة تسمح له بالتحرك نحو اتجاه واحد أو الآخر. يتم إنشاؤه بواسطة مركب إنزيمي يسمى ريزولفاز (رتإ 3.1.22.4) ويمكن أن يقود إلى تعابر بين الجزيئين ينتج عنه تبادلٌ للمعلومات الوراثية. [43].
- دنا دبوس الشعر: يمكن لتسلسلات الدنا المتناظرة الالتفاف وتشكيل بنية تسمى الحلقة الجذعية [44]. بعض التسلسلات وخاصة التسلسلات ثلاثية النوكليوتيد (CAG)n أو (CTG)n يمكن أن تشكل دبابيس شعر غير تامة تكون فيها بقايا الغوانين والسايتوسين مترابطة وبقايا الأدينين والثايمين غير مترابطة. [45].
- الدنا الثلاثي: هي هيئة دنا تقوم فيها ثلاث جزيئات قليل النوكليوتيد بالالتفاف حول بعضها لتشكيل لولب ثلاثي، في هذه البنية تقوم تقوم سلسة دنا منفردة بالارتباط بلولب دنا مزدوج من البنية ب بواسطة الروابط الهيدروجينية العادية أو المعكوسة لهوغستين، ويمكن أن تلعب هذه الهيئة دورا في الضبط الوظيفي للتعبير الجيني عن طريق تعديل نسخها لجزيئات رنا.
- الدنا الرباعي: تحتوي نهاية الصبغي الخطي على مناطق خاصة تدعى قسيمات طرفية وظيفتها السماح للخلية بمضاعفة نهايات الصبغي باستخدام إنزيم تيلوميراز وذلك لأن الإنزيمات التي تُضاعِف الدنا عادة لا يمكنها نسخ النهايات 3' للصبغيات [46]. كما تساعد هذه المناطق في حماية نهايات الدنا وإيقاف أنظمة الترميم في الخلية من اعتبارها تلفا يجب إصلاحه [47]. في الخلايا البشرية القسيمات الطرفية عبارة سلسلة منفردة من الدنا تحوي الآلاف من الوحدات النوكليوتدية البسيطة TTAGGG المتكررة. [48]

الثالثة بالأصفر.
هذه التسلسلات الغنية بالغوانين يمكن أن تجعل نهايات الصبغي مستقرة بتشكيل هياكل مرصوصة بوحدات رباعية القواعد بدل ثنائية القواعد المعتادة الموجودة في هياكل الدنا الأخرى، حيث تقوم أربع قواعد غوانين بتشكيل وحدة رباعية مسطحة وبعدها تتراص هذه الوحدات الرباعية فوق بعضها لتشكيل بنية رباعي-غ مستقرة [49]. تستقر هذه الهياكل الرباعية بواسطة روابط هيروجينية بين نهايات هذه القواعد وتمخلب أيون معدني في مركز كل وحدة رباعية [50].
بالإضافة إلى هذه الهياكل المرصوصة، تشكل القسيمات الطرفية كذلك هياكل تسمى حلقات القسيم الطرفي أو حلقات ت تقوم فيها سلسلة دنا منفردة بالالتواء في حلقة طويلة تستقر بواسطة إنزيمات ترتبط بالقسيمات الطرفية [51]. في نهاية الحلقة ت يتم ضم السلسلة المنفردة للقسيم الطرفي إلى منطقة لدنًا مضاعفِ السلسلة وهذا يتسبب في إخلال التزاوج القاعدي لإحدى سلسلتي هذا اللولب المزدوج وتشكيل بنية ثلاثية السلاسل تسمى حلقة الإزاحة أو الحلقة د. [49]
- الدنا المتفرع: يحدث انسلال الدنا في إحدى نهايتي اللولب المزدوج حين تتوقف تسلسلات سلسلتَيْهِ عن كونها متكاملة حيث تفترق السلسلتان عن بعضهما وتتخذان هيئة Y، ويمكن للدنا أن يتشعب إن وُجدت سلسلة دنا ثالثة تحوي تسلسلا مكملا لكلا تسلسلي السلسلتين المفترقتين، فتتشكل هيئة مزدوجة متكاملة على شكل Y. مع أن أبسط أمثلة الدنا المتفرع تحوي ثلاث سلاسل دنا فقط فإن تواجد مركبات متفرعة تحوي سلاسل إضافية وعدة تفرعات أخرى ممكن كذلك [52]. ويتم استخدام الدنا المتفرع في تقنية النانو للدنا لإنشاء أشكال هندسية.
التغيرات الكيميائية وتحزيم الدنا المعدل
تغير القواعد وتحزيم الدنا
|

|

|
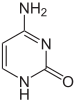
| سايتوسين | 5-ميثيل سايتوسين | ثايمين |
يتأثر التعبير الجيني بطريقة تحزيم الدنا في الصبغيات على هيئة تسمى كروماتين، يمكن لبعض القواعد أن تتغير حين يتم تكوين الكروماتينات في المناطق ضعيفة أو عديمة التعبير الجيني والغنية بقواعد السايتوسين عن طريق المثيلة خاصة في المناطق CpG، يمكن للهستونات التي يلتف حولها الدنا في الكروماتين أن تتغير بطريقة تساهمية ويمكن للكروماتين بحد ذاته أن يتغير بواسطة مركبات إعادة تشكيل الكروماتين، علاوة على ذلك فإن مثيلة الدنا والتعديل التساهمي للهستونات يساهمان معا في التأثير على الكروماتين والتعبير الجيني. [53]
على سبيل المثال تُنتج مثيلة السايتوسين 5-ميثيل سايتوسين وهو ضروري في تعطيل الصبغي X [54]، يختلف متوسط معدلات المثيلة بين الكائنات فالدودة ربداء رشيقة تعوز مثيلة السايتوسين في حين أن الفقاريات لديها معدل مرتفع يصل حتى 1% من الدنا الخاص بها يحوي 5-ميثيل سايتوسين [55]، رغم أهمية الـ5-ميثيل سايتوسين إلا أنه قد يتعرض إلى نزع أمين ويصبح ثايمين وكذلك السايتوسين الذي يصبح يوراسيل، قواعد السايتوسين المُمَثْيَلة عرضة للطفرات [56]. من التغييرات الأخرى للقواعد مثيلة الأدنين عند البكتيريا ووجود 5-هيدروكسي ميثيل سايتوسين في الدماغ. [57] وغلكزة اليوراسيل لإنتاج القاعدة ج لدى ذوات منشأ الحركة. [58][59] التي تعمل كإشارة إنهاء النسخ للأنزيم بوليميرايز الرنا 2. [60] [61]
تضرر
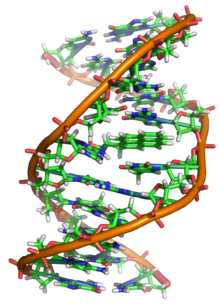
يمكن للدنا التضرر بأنواع مختلفة من المطفِّرات التي تغير تسلسله، تتضمن هذه المطفرات: المؤكسدات، عوامل الألكلة والإشعاعات الكهرومغناطيسية عالية الطاقة مثل الأشعة فوق البنفسجية والأشعة السينية. يتعلق نوع الضرر الحاصل بنوع المطفّر فعلى سبيل المثال يمكن للأشعة فوق البنفسجية الإضرار بالدنا بإنتاج مثنويات الثايمين وهي روابط جانبية بين قواعد البيريميدين .[63]. من جهة أخرى تسبب المؤكسدات مثل الجذور الكيميائية الحرة أو بيروكسيد الهيدروجين أنواع مختلفة من الأضرار منها تغيير القواعد -خاصة الغوانوزين- وتقطعات في السلسلة المزدوجة للدنا [64]، حيث يبلغ متوسط عدد القواعد التي عانت أضرارا من المؤكسدات في خلية نموذجية حوالي 150 ألف قاعدة [65]. أخطر هذه الآفات التأكسدية هي تقطعات السلاسل المزدوجة وذلك لأنها صعبة الإصلاح وقد تُنتج طفرات نقطية، غرز، أو حذف في تسلسللات الدنا وكذلك انتقالات صبغية [66]. يمكن لهذه الطفرات أن تسبب السرطان بسبب آليات إصلاح الدنا المحدودة طبيعيا، لذا إن عاش البشر لوقت طويل بما فيه الكفاية فإن جميعهم في النهاية سيصاب بالسرطان. [67][68]
تضررات الدنا التي تحدث طبيعيا بسبب النشاطات الطبيعية للخلية التي تنتج كائنات متفاعلة مع الأكسجين، نشاطات الحلمأة لماء الخلية تظهر بشكل متواتر كذلك رغم أن معظم هذه الأضرار يتم إصلاحها. في أي خلية تبقى بعض تضررات الدنا رغم عمليات الإصلاح وتتراكم هذه التضرارت مع مرور الزمن في الخلايا تالية التفتل لأنسجة الثديات، هذا التراكم يبدو عاملا أساسيا مهما في الشيخوخة. [69][70][71].
تدخل العديد من المطفِّرات في الفراغ الموجود بين زوجين قاعديين متجاورين فيما يعرف بـ الإقحام ومعظم المقتحمات جزيئات عطرية و مستوية ومن الأمثلة: بروميد الإيثيديوم، الأكريدينات و داونوروبيسين، لكي يدخل المقتحم بين القواعد يجب عليه فصلها وهذا يشوه سلسلتي الدنا بسبب فك التواء اللولب المزدوج، هذا التشوه يمنع كلا من نسخ وتضاعف الدنا ويسبب تسمما وطفرات [72]. وكنتيجة لذلك يمكن لمقتحمات الدنا أن تكون مسرطنات وفي حالة الثاليدوميد، ماسخات [73]، مقتحمات أخرى مثل بنزو(a)بيرين ديول إيبوكسيد وأفلاتوكسين يشكلان نواتج إضافة تُحدث أخطاءً في التضاعف [74]. مع ذلك وبسبب قدرتها على تعطيل ومنع نسخ وتضاعف الدنا؛ تستخدم مقتحمات سامة أخرى مشابهة في العلاج الكيميائي لمنع النمو السريع للخلايا السرطانية. [75]
وظائف بيولوجية

عادة ما يكون الدنا على شكل صبغيات خطية عند حقيقيات النوى وصبغيات دائرية عند بدائيات النوى ومجموع الصبغيات في خلية واحدة يشكل الجينوم، يحتوي جينوم الإنسان على ما يقارب 3 ملايير زوج قاعدي منتظمة في 46 صبغيا [76]. المعلومات المحمولة في الدنا موجودة في تسلسلات قطع منه تسمى الجينات، يتم نقل المعلومة الوراثية بواسطة تكامل الأزواج القاعدية مثلا: حين تستخدم الخلية المعلومة الموجودة في الجين يتم نسخ تسلسل الدنا إلى تسلسل رنا مكمل عبر التجاذب بين الدنا والنوكليوتيدات الصحيحة للرنا. وتستخدم هذه النسخة -عادة- لتخليق بروتين مماثل في التسلسل عبر عملية تسمى الترجمة والذي يعتمد على نفس التجاذب بين نوكليوتيدات الرنا، ومن جهة أخرى يمكن للخلية نسخ معلوماتها الوراثية خلال عملية تسمى تضاعف الدنا، تفاصيل هذه العمليات ستذكر في العناوين التالية وسيكون التركيز في العوان التالي على التفاعلات بين الدنا والجزيئات الأخرى التي تتدخل في وظائف الجينوم.
الجينات والجينومات

يُحزم جينوم الدنا بشدة وانتظام خلال عملية تسمى تكثيف الدنا ليسع الأحجام الصغيرة المتوفرة في الخلية، يتواجد الدنا عند حقيقيات النوى في النواة مع كميات صغيرة في الميتوكندريون والبلاستيدات الخضراء أما عند بدائيات النوى فإن الدنا مخزن في جسيم غير منتظم الشكل يسمى نوواني [77]. المعلومات الجينية في الجينوم موجودة داخل الجينات ومجموع هذه المعلومات في كان حي يسمى نمط جيني، والجين هو وحدة وراثة وهو عبارة عن منطقة من الدنا تؤثر في صفة معينة لكائن ما، تحوي الجينات قالب قراءة مفتوح يمكن نسخه بالإضافة إلى تسلسلات معدلة مثل المحفزات والمعززات والتي تتحكم في عملية نسخ قالب القراءة المفتوح.
في العديد من الأجناس لا يٌشفِّرالبروتين سوى كيمة صغيرة من المجموع الكلي للجينوم، على سبيل المثال عند البشر 1.5% من الجينوم البشري عبارة إكسونات تشفر بروتينات، مع وجود 50% من الدنا البشري عبارة عن تسلاسلات متكررة غير مُشفِّرة [78]. يمثل سبب وجود كم كبير من الدنا غير المشفر في جينوم حقيقيات النوى والفروق الكبيرة في حجم الجينوم -القيمة س- بين الأجناس لغزا طويل الأمد يعرف بـ معضلة القيمة س [79]. رغم ذلك بعض تسلسلات الدنا غير المشفرة يمكن أن تشفر رنا غير مشفر وظيفيا مهمته ضبط التعبير الجيني. [80]
بعض تسلسلات الدنا غير المشفرة تلعب أدوارا بنيوية في الصبغيات، تحتوي القسيمات الطرفية والقطع المركزية على بعض الجينات لكنها مهمة لوظيفة واستقرار الصبغيات [47][81]. الجينات الكاذبة نوع وافر في الجينوم البشري من الدنا غير المشفر وهي نسخ من جينات تم تعطيلها بواسطة الطفرات [82]، هذه الجينات الكاذبة عبارة عن مستحاثات جزيئية رغم أنها تلعب أحيانا دور المادة الجينية الخام لإنشاء جينات جديدة عبر عملية التضاعف الجيني وعملية التطور التباعدي. [83]
تضاعف الدنا
انقسام الخلايا عملية أساسية لنمو الكائن، وحين تتم هذه العملية فعلى الخلية مضاعفة الدنا في جينومها لكي تحصل الخليتين البنت على نفس المعلومات المتواجدة في الخلية الأم، توفر هيئة الدنا اللولبية المزدوجة طريقة بسيطة لتضاعف الدنا. أثناء عملية التضاعف تقوم إنزيمات التوبوإيزوميراز بفك التواء السلسلة المضاعفة ثم تقوم إنزيمات الهيليكاز بحل الروابط الهيدروجينية بين النوكليوتيدات وفصل السلسلتين عن بعضهما وبعدها يتم إنتاج سلسلتين متكاملتين بواسطة إنزيم بوليميراز الدنا، تقوم هذه الإنزيمات بإنتاج سلسلة مكملة بإيجاد القاعدة الصحيحة عبر ترابط القواعد المكمل ثم ربطها بالسلسلة الأصلية، ولأن إنزيمات بوليمراز الدنا لا تُنتج السلاسل سوى في الاتجاه 5' إلى 3' يتم استخدام طريقة أخرى لنسخ سلاسل التوازي العكسي في لولب الدنا المضاعف [84]. بهذه الطريقة القاعدة في السلسلة القديمة تحدد القاعدة التي ستظهر في السلسلة الجديدة ويغدو لدى الخلية نسخة جديدة من دناها.

التعبير الجيني

التعبير الجيني هو عبارة عن تحول النمط الجيني لكائن ما إلى نمط ظاهري أي إلى مجموعة الخصائص المميزة للكائن، تتأثر هذه العملية بالعديد من المحفزات الخارجية المختلفة وتحتوي ثلاث مراحل كبيرة أساسية هي:
- نسخ الدنا إلى رنا وهو حمض نووي مختلف يملك وظيفة بيولوجية معينة على حسب نوعه (ناقل، ريبوسومي..إلخ) أو الرنا الرسول الذي يعمل كوسيط وحامل المعلومة لاصطناع البروتين.
- ترجمة الرنا الرسول إلـى بروتين.
- نشاط جزيئات الرنا غير المشفرة والبروتينات داخل الكائنات.
مع ملاحظة أنه يمكن لنفس الدنا الخاص بكائن ذو مرحلتي تطور أن يُعبر عن نفسه بشكل غير متشابه تماما (بسبب مثبطات ومحفزات مختلفة)، أفضل مثال معروف عن ذلك هو اليسروع والفراشة حيث أنهما شكليا مختلفان كثيرا.

النسخ والترجمة
النسخ عملية بيولوجية يتم فيها نسخ المعلومة الوراثية المشفَّرة في جين معين من تسلسلات نوكليوتيدات الدنا الموافقة له وإنتاج جزيئات رنا مختلفة مشفِّرة وغير مشفِّرة بواسطة إنزيمات بوليميراز الرنا، سلسلة هذه الجزيئات مماثلة في تركيبها لسلسلة الدنا باستثناء احتواء وحدتها الأساسية على ريبوز بدل الريبوز منقوص الأكسجين وقاعدة اليوراسيل مكان الثايمين، تخضع جزيئات الرنا الأولية الناتجة والتي تسمى الرنا قبل الرسول إلى تعديلات ما بعد الترجمة من تقبيع وتذييل بعديد الأدينيلات لإنتاج رنا رسول مستقر وناضج قادرٍ على تحمل عملية الترجمة أثناء تخليق البروتين. العلاقة بين تسلسل نوكليوتيدات الجين والحمض الأميني محددة بقواعد الترجمة المعروفة بالشيفرة الجينية، تتكون الشيفرة الجينية من كلمات ذات ثلاث أحرف تسمى رامزات أو كودونات مكونة من تسلسل حروف ثلاث نوكليوتيدات (مثال ACT، CAG ،TTT).
الترجمة هي عملية تحويل المعلومة الوراثية المحمولة في جزيء الرنا الرسول الناضج المغادر للنواة إلى بروتين (أوفي بعض الأحيان عدة بروتينات)، حيث يتم فك شيفرته بواسطة الريبوسوم الذي يقرأ تسلسلات الرنا وذلك بربط تسلسلات قواعد الرنا الرسول مع قواعد ضد الكودون للرنا الناقل الذي يحمل معه الأحماض الآمينية، وبما أنه توجد أربع قواعد؛ في توليفة ثلاثة حروف تكون هنالك 64 رامزة ممكنة (43 توليفة) هذه التوليفات تشفِّر العشرين حمض أميني الأساسية، مانحة معظم الأحماض الأمينية أكثر من رامزة واحدة ممكنة، كما توجد ثلاث رامزات 'توقف' أو 'بلا معنى' تشير إلى نهاية المنطقة المشفرة وهذه الرامزات هي TAA، TGA وTAG.
الأحماض النووية خارج الخلية
يصدر معظم الحمض النووي الصبغي الخارجي المجرد (eDNA) بموت الخلية، وهو واسع الإنتشار في الطبيعة حيث يبلغ تركيزه في التربة حوالي 2 ميكروغرام/ل وتركيزه في الأوساط المائية الطبيعية قد يبلغ 88 ميكروغرام/ل [85]. تم اقتراح العديد من الوظائف للدنـا الخارجي: فقد تكون له علاقة في نقل الجينات الأفقي [86]؛ قد يوفر مغذيات [87]؛ وقد يعمل كمنظم لجذب أو معايرة الأيونات أو المضادات الحيوية [88]. يعمل الدنا الخارجي كمكون -عبارة عن مصفوفة وظيفية خارجية- في بيـوفيلم العديد من الأجناس البكتيرية، كما يمكن أن يعمل كعامل تعرّف لتنظيم ارتباط وتشتيت أنواع خلايا محددة في البيوفيلم [89]، كما يمكن أن يساهم في تكون البيوفيلم [90]، ويمكن أن يساهم في القوة الفيزيائية للبيوفيلم ومقاومته للضغظ البيولوجي. [91]
يوجد الدنا الجنيني من دون خلايا في دم الأم، ويمكن فحص تسلسله لمعرفة معلومات كثيرة حول تطور الجنين. [92]
تفاعلات مع البروتينات
جميع وظائف الدنا تعتمد على التفاعلات مع البروتينات، قد تكون هذه التفاعلات غير محددة أو يمكن للبروتين الارتباط بشكل محدد على تسلسل معين للدنا، يمكن للإنزيمات الارتباط بالدنـا كذلك ومن بين هذه الإنزيمات البوليميرايزات التي تنسخ تسلسل قواعد الدنا أثناء عمليتي النسخ والتضاعف والتي تعتبر ذات أهمية كبيرة.
بروتينات مرتبطة بالدنا

البروتينات الهيكلية التي ترتبط بالدنا هي أمثلة مفهومة جدا عن التفاعلات غير المحدَّدَة للدنا مع البروتين. يوضع الدنا داخل الصبغيات في مركبات مع بروتينات هيكلية، تنظم هذه البروتينات الدنا على شكل هيئة متراصة تدعى كروماتين، لدى حقيقيات النوى يتطلب حدوث هذه الهياكل ترابط الدنا مع بروتينات صغيرة تسمى الهستونات، أما عند بدائيات النوى فيتطلب ذلك أنواعا عديدة من البروتينات [93][94]. تشكل الهستونات مركب على شكل قرص يسمى جسيم نووي يحوي دورتين كاملين لدنا مزدوج السلاسل ملفوف على سطحه، تشكلت هذه التفاعلات غير المحددة بسبب قيام الوحدات الأساسية في الهستونات (أحماض أمينية) بتشكيل روابط أيونية مع مجموعات الفوسفات الحمضية في الوحدة الأساسية للدنا ومنه لا تعتمد هذه التفاعلات بشكل كبير على تسلسل القواعد [95]. التغيرات الكيميائية لهذه الأحماض الآمينية تشمل المثيلة، الفسفرة والأستلة [96]. تُغيِّر هذه التغيرات الكيميائية قوة التفاعل بين الدنا والهستونات، جاعلة الدنا أكثر أو أقل قابلية لوصول عوامل النسخ إليه وتغير معدل سرعة النسخ [97]. بروتينات الترابط غير المحدد بالدنا الأخرى في الكروماتين تشمل مجموعة البروتين عالية الحركة التي ترتبط بالدنا لتحنِيَه أو تلويه [98]. وهذه البروتينات ضرورية لطي مصفوفات من الجسيمات النووية وترتيبها في هيئة أكبر تشكـل الكروموسومات. [99]
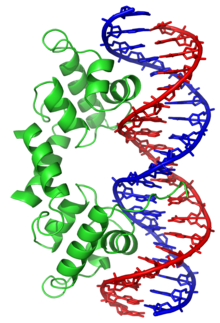
توجد مجموعة مميزة من البروتينات المرتبطة بالدنا ترتبط بشكل محدد في سلسلة واحدة من الدنا، لدى البشر بروتين التضاعف أ هو أفضل عنصر مفهوم من هذه العائلة ويستخدم في عمليات يكون فيها اللولب المزدوج مفصولا، بما في ذلك تضاعف الدنا، إعادة التركيب وإصلاح الدنا [101]، يبدو أن هذه البروتينات تعمل على استقرار سلسلة الدنا المفردة ومنعها من تشكيل حلقة جذعية أو تحللها بواسطة النوكليازات.
في المقابل تطورت بروتينات أخرى لترتبط بتسلسل دنا محدد، أكثر أنواع هذه البروتينات دراسة هي عوامل النسخ المختلفة، وهي بروتينات تنظم عملية النسخ حيث يرتبط كل عامل نسخ بتسلسل دنا واحد مخصص لتفعيل أو تثبيط نسخ الجينات التي يتواجد تسلسلها بالقرب من محفزاتها. تقوم عوامل النسخ بذلك بطريقتين، أولا يمكنها الارتباط ببوليميراز الرنا المسؤول عن عملية النسخ سواء مباشرة أو عبر بروتينات وسيطة أخرى، هذا يجعل البوليميراز يتواجد على المحفز ويسمح ببدء النسخ [102]. ثانيا يمكن لعوامل النسخ الارتباط بالإنزيمات المعدلة للهستونات في المحفز، وهذا يغير قابلية الوصول لسلسة الدنا القالب بالنسبة للبوليميراز. [103]
لأن مواقع الارتباط بالدنا هذه يمكن أن تظهر في مختلف جينوم الكائن؛ فإن تغيرات في نشاط أحد أنواع عوامل النسخ يمكن أن يؤثر على الآلاف من الجينات [104]. ونتيجة لذلك فإن هذه البروتينات عادة أهدافٌ لتوصيل الإشارة التي تتحكم بالردود اتجاه التغيرات المحيطية أو التمايز الخلوي والنمو. اختصاص تفاعلات عوامل النسخ هذه مع الدنا يأتي من قيام هذه البروتينات باتصالات عديدة مع حواف قواعد الدنا، وهذا يسمح لها بقراءة تسلسل الدنا. تتم معظم تفاعلات القواعد هذه في الثلم الكبير أين يكون الوصول لمعظم القواعد ممكنا. [105]
إنزيمات معدلة للدنا
النوكلياز والليغاز

النوكليازات هي إنزيمات تقوم بقص سلاسل الدنا بتحفيز حلمـأة روابط الفوسفات ثنائية الأستر. تسمى النولكيازات التي تقوم بحلمأة النوكليوتيدات عند نهايات سلسلتي الدنا نوكليازات خارجية وتسمى التي تقوم بالقص داخل السلاسل نوكليازات داخلية، أكثر إنزيمات النوكلياز استخدما في علم الأحياء الجزيئي هي إنزيمات التقييد الداخلية التي تقطع الدنا في تسلسلات محددة، على سبيل المثال: إنزيم EcoRV الموضح في الصورة يمينا يتعرف على على التسلسل السداسي 5′-GATATC-3′ ويقوم بالقطع على الخط الأفقي. في الطبيعة تحمي هذه البروتينات البكتيريا من عدوى العاثيات وذلك بهضم دنا العاثية لدى دخوله خلية البكتيريا، متصرفة كجزء من نظام منع التغييرات [107]، وفي التكنولوجيا تستخدم هذه الإنزيمات المختصة بتسلسلات معية في التنسيل الجزيئي والبصمة الوراثية
يمكن لإنزيمات تسمى ليغازات الدنا إعادة وصل سلاسل الدنا المقطوعة أو المبتورة [108]، وهي مهمة بشكل خاص للسلسة المتأخرة في عملية تضاعف الدنا حيث تقوم بتجميع قطع أوكازاكي القصيرة في شوكة التضاعف إلى نسخة كاملة من السلسلة الدنا القالب، كما تستخدم في ترميم الدنا وإعادة التركيب الجيني. [108]
توبوإيزوميراز والهيليكاز
التوبوإيزوميرازات هي إنزيمات تجمع نشاط كل من النوكلياز والليغاز، حيث تغير هذه البروتينات في كمية لف الدنا الفائف، تعمل بعض هذه الإنزيمات على قطع لولب الدنا والسماح لأحد مقاطعه بالدوران ومنه التخفيف في مستوى اللف الفائق وبعدها يقوم الإنزيم بإعادة وصل القطع [25]، أنواع أخرى من هذه الإنزيمات يمكنها قطع إحدى سلسلتي لولب الدنا ثم تمرير السلسلة الأخرى عبر ذلك القطع قبل إعادة جمع اللولب [109]. وهذه الإنزيمات مطلوبة في العديد من العمليات المتعلقة بالدنا مثل تضاعف الدنا والنسخ. [26]
الهيليكازات هي بروتينات تعتبر كنوع من المحركات الجزيئية، حيث تستخدم الطاقة الكيميائية في النوكليسيدات ثلاثية الفوسفات وفي الغالب أدينوسين ثلاثي الفوسفات لكسر الروابط الهيدروجينية بين القواعد وفك لولب الدنا المزدوج لسلسلتين مفردتين [110]. هذه الإنزيمات ضرورية في معظم العمليات التي تتطلب وصول الإنزيمات إلى قواعد الدنـا.
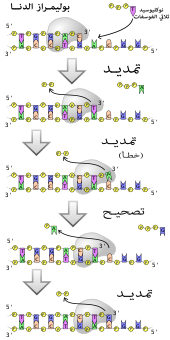
بوليميراز
البوليميرازات هي إنزيمات تقوم بتخليق سلاسل عديدة النوكليوتيد من نوكليوسيدات ثلاثية الفوسفات، تسلسل نواتجها يخلَّق اعتمادا على سلاسل عديدة النوكليتويد موجودة مسبقا تسمى السلاسل القالب، تعمل هذه الإنزيمات بإضافة مجموعة هيدروكسيل بشكل مستمر للنهاية 3' لسلسلة عديد نوكليوتيد متنامية، وكنتيجة لذلك تعمل البوليميرازات في الاتجاه 5' إلى 3' [111]. في الموقع النشط لهذه الإنزيمات تترابط قاعديا النوكليوسيدات ثلاثية الفوسفات القادمة مع السلسة القالب: وهذا يسمح للبوليميرازات بتخليق سلسلة مكملة لسلسلة القالب بشكل دقيق. تصنف البوليميرازات حسب نوع السلسلة القالب التي يستخدمونها.
في عملية تضاعف الدنا تقوم بوليمرازات الدنا -المتعلقة بالدنا- بعمل نسخ لسلاسل الدنا عديدة النوكليوتيد. للحفاظ على المعلومة البيولوجية؛ أمر جوهري أن يتم نسخ تسلسل القواعد في كل نسخة بشكل دقيق ومكمل لقواعد السلسة القالب. لدى العديد من بوليميرازات الدنا نشاط التصحيح حيث تتعرف على الأخطاء التي تقع أحيانا في تفاعلات التخليق بواسطة عدم وجود ترابط قاعدي بين النوكليوتيدات غير المتكاملة. إن تم اكتشاف عدم تكامل يُنَشّط إنزيم نوكلياز خارجي 3′ إلى 5′ وتتم إزالة القاعدة [112]. يَنشُط البوليميراز لدى معظم الكائنات في مركبات كبيرة تسمى ريبليسومات والتي تحتوي على العديد من المركبات الإنزيمية الفرعية مثل كتيلة الدنا والهيليكاز. [113]
بوليمرازات الدنا -المتعلقة بالرنا- هي قسم خاص من البوليمرازات التي تقوم بنسخ تسلسل سلسلة رنا في الدنا، حيث تشمل إنزيم النسخ العكسي وهو إنزيم شائع له علاقة بإصابة الخلايا بالفيروسات الراجعة، إنزيم التيلوميراز الضروري لتضاعف القسيمات الطرفية [46][114]. على سبيل المثال إنزيم النسخ العكسي لفيروس العوز المناعي البشري هو إنزيم لتضاعف فيروس الإيدز [114]. التيلوميراز هو بوليميراز غير اعتيادي لأنه يحوي سلسلة الرنا القالب خاصته كجزء من بنيته، ويقوم بتصنيع القسيمات الطرفية في نهايات الصبغيات حيث تمنع القسيمات الطرفية نهايات الصبغيات من الاندماج مع نهايات الصبغيات المجاورية وتحميها من التضرر كذلك. [47]
تتم عملية النسخ بواسطة بوليمرازات الرنا -المتعلقة بالدنا- حيث تقوم بنسخ تسلسل سلسلة دنا إلى رنا. للبدء في عملية نسخ جين يرتبط بوليميراز الرنا بتسلسل دنا محدد يسمى المحفز وبعدها يقوم بنسخ تسلسل الجين لإنتاج رنا رسول حتى يصل منطقة تسمى المنهي أين يتوقف وينفصل عن الدنا. كما هو الحال بالنسبة لبوليميرازات الدنا المتعلقة بالدنا؛ يعمل إنزيم بوليمراز الرنا II الذي ينسخ معظم الجينات في الجينوم البشري في مركبات إنزيمية كبيرة تحوي العديد من الوحدات الثانوية التنظيمية والملحقة. [115]
تطور المعلومة الوراثية
طفرات

الطفرة هي تغير دائم في تسلسل نوكليوتيدات جينوم كائن حي، فيروس، دنا غير صبغي أو أي عناصر جينية أخرى، وتنتج الطفرات من أخطاء أثناء عملية تضاعف الدنا أو أي أنواع أخرى من تضررات الدنا مثل التعرض للأشعة أو المسرطنات، والتي تخضع لعملية تصحيح ميّالة للخطأ خاصة (وصل النهاية الميكرو تناظري المتوسط [116]) أو أي خطأ في أنواع أخرى من التصحيح [117][118]، كما يمكن أن تنتج الطفرات من إدخال أو حذف قطع دنا بسبب عناصر وراثية متحركة [119][120][121]. قد وقد لا تُحدِث الطفرات تغيرات قابلة للتمييز في الخصائص المرئية (النمط الظاهري) للكائن وتلعب الطفرات دورا في كل العمليات البيولوجية الطبيعية والغير طبيعية: السرطان، التطور وتطور الجهاز المناعي بما في ذلك التنوع الوصلي.
يمكن للطفرات التسبب بأنواع مختلفة من التغير في التسلسل، والطفرات في الجين إما أن لا يكون لها تأثير أو أن تُغيِّر ناتج الجين أو تمنع الجين من النشاط كما ينبغي أو بشكل كامل، يمكن للطفرات الحدوث في مناطق غير جينية، تقترح إحدى الدراسات المتعلقة بالتغيرات الجينية بين مختلف أجناس الدروسوفيلا أنه إن غيرت الطفرة بروتينا يُنتَج من الجين فإن النتيجة تكون على الأرجح ضارة مع تقدير 70 بالمئة من تعددات الأشكال بسبب الحمض الأميني لها آثار ضارة والباقي يكون إما حيادي التأثير أو له فائدة هامشية [122]. بسبب التأثيرات الضارة التي يمكن أن تلحقها الطفرات بالجينات؛ يوجد لدى الكائنات آليات مثل ترميم الدنا لمنع أو تصحيح الطفرات بإعادة التسلسل المطفَّر إلى حالته الأصلية. [119]
إعادة التركيب الجيني
|

|
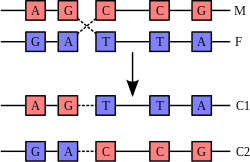
في العادة لا يتفاعل لولب الدنا مع قطع أخرى من الدنا، وفي الخلايا البشرية تشغل الصبغيات مناطق منفصلة في النواة تسمى مناطق الكروموسوم [124]. هذا الفصل الفيزيائي لمختلف الكروموسومات مهم لقدرة الدنا على العمل كمستودع للمعلومات، من المرات القليلة التي تتفاعل فيها الكروموسومات فيما بينها هي في التعابر الكروموسومي الذي يحدث أثناء التكاثرالجنسي والذي يحدث فيه التأشيب الجيني. التعابر الجيني هو انفكاك كروموسومين وتبادل قطعة دنا بينهما ثم إعادة تشكلهما.
يسمح التأشيب الجيني للكروموسومات بتبادل المعلومات الجينية وإنتاج توليفات جديدة من الجينات، والتي تزيد فعالية الإصطفاء الطبيعي ويمكن أن تكون مهمة لسرعة تطور بروتينات جديدة [125]. يمكن أن يكون للتأشيب الجيني علاقة بترميم الدنا خاصة في رد الخلايا على تقطعات السلاسل المزدوجة. [126]
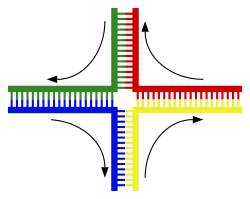
أكثر أنواع التعابر الكروموسومي شيوعا هو التأشيب المتماثل أين يتشارك فيه كروموسومين تسلسلات مماثلة جدا، أما التأشيب غير المتماثل فيمكن أن يكون مضرا بالخلايا كما يمكن أن يُنتِج انتقالات كروموسومية وتشوهات كروموسومية. تُحفَّز عملية التأشيب بواسطة إنزيمات تسمى ريكومبيناز مثل RAD51 [127]. أول خطوة في التأشيب هو تقطُّع السلسلة المزدوجة إما بواسطة نوكلياز داخلي أو ضرر في الدنا [128]، بعدها يحفز الريكومبيناز سلسلة من الخطوات تقود إلى تجميع لولبي الدنا بواسطة موصل هوليداي واحد على الأقل والتي يتم فيها تثبيت قطعة من كل سلسلة مفردة لكلا اللولبين في السلسلة المكملة للولب الآخر. موصل هوليداي بنية رباعية يمكنها التحرك على طول زوج الكروموسومات مُبدِّلّة إحدى السلسلتين بالأخرى، بعدها تُوقَفُ عملية التأشيب بفصل الموصل وإعادة تركيب الدنا المنفصل [129]. السلاسل المتماثلة في القطبية وحدها من يتبادل الدنا فيما بينها أثناء التأشيب، هناك نوعان من القص: قص شرق-غرب وقص شمال-جنوب، يشمل القص شمال-جنوب كلا السلسلتين ويقطعهما في حين أن قص شرق-غرب يبقي إحدى السلسلتين سليمة. تشكل موصل هوليداي أثناء التأشيب يسمح بالتنوع الجيني، تبادل الجينات في الكروموسومات، والتعبير عن الجينومات الفيروسية المتنوعة.
عناصر وراثية متحركة


المعلومة الجينية المشفَّرَة في الدنا ليست ثابتة عبر الزمن وبعض التسلسلات عرضة للانتقال من مكان إلى آخر في الجينوم، وهذه التسلسلات هي العناصر الوراثية المتحركة. وهي عبارة عن مطفِّرات يمكنها تغيير جينوم الخلايا ونجد من بينها خاصة الينقولات والينقولات الراجعة، تعمل هذه الأخيرة -عكس الأولى- عبر رنا وسيط مُنتِجَةً تسلسل دنا بواسطة عملية النسخ العكسي. تتحرك هذه العناصر داخل الجينوم تحت تأثير الترانسبوزازات وهي إنزيمات خاصة تفصل هذه العناصر من جهة وتربطها في جهة أخرى من الجينوم، وهي مسؤولة عن انتقال ما لا يقل عن 40% من الجينوم البشري خلال تطور الإنسان العاقل [130].
تشكل هذه العناصر القابلة للنقل نسبة مهمة من الجينوم لدى الكائنات الحية، خاصة لدى النبات أين تمثل فيه النسبة الأكبر من الحمض النووي، فمثلا لدى الذرة 49-78% من جينومه عبارة عن ينقولات راجعة [131]، جينوم القمح 90% منه عبارة عن تسلسلات متكررة و68% منه عناصر متحركة [132]، لدى الثدييات نصف الجينوم تقريبا (45-48%) عبارة عن عناصر متحركة أو بقايا عناصر متحركة، وحوالي 42% من الجينوم البشري مكون من الينقولات الراجعة في حين أن 2-3% منه عبارة عن ينقولات دنا [133]. ومنه فهي عناصر مهمة لعمل وتطور جينوم الكائنات الحية. [134].
الإنترونات التي تصنف إلى مجموعة I ومجموعة II هي نوع آخر من العناصر الوراثية المتحركة وهي عبارة عن ريبوزيمات أي تسلسللات رنا تملك قدرة التحفيز مثل الإنزيمات وقادرة على تحفيز وصلها ذاتيا. إنترونات المجموعة I تحتاج نوكليوتيدات غوانين لكي تعمل على عكس إنترونات المجموعة الثانية. توجد على سبيل المثال إنترونات المجموعة I بصورة فرادية لدى البكتيريا وبشكل أكبر قليلا لدى لدى حقيقيات النوى البسيطة وبأعداد كبيرة جدا لدى النباتات الوعائية. كما نجدها لدى عدد كبير من عاثيات البكتيريا موجبة الغرام [135]، ولدى القليل من العاثيات سالبة الغرام مثل العاثية T4. [135] [136] [137] [138]
النقل الأفقي للجينات
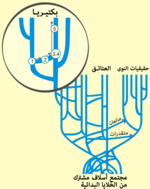
يمكن لمعلومة الخلية الوراثية التطور تحت تأثير دمج وإضافة مادة وراثية خارجية مُمتصة عبر الغشاء الخلوي ويسمى ذلك النقل الأفقي للجينات، وهو عكس النقل العمودي الناتج من تكاثر الكائنات الحية ويتم بين وحيدات الخلية و/أو متعددات الخلية [139]، وهو عامل أساسي في تطور العديد من الكائنات. [140][141]
النقل الأفقي للجينات هو الآلية الأساسية في انتشار مقاومة المضادات الحيوية لدى البكتيريا [140][142][143][144][145] ويلعب دورا مهما في تطور البكتيريا التي يمكنها تحليل المركبات الصناعية الجديدة التي يصنعها الإنسان مثل المبيدات الحشرية [146]، وتطور وصيانة وانتقال حدة الجرثوم [147] وغالبا ما يتعلق ذلك بالعاثيات والبلازميدات [148][149][150]. يمكن أن تنتقل الجينات المسؤولة عن مقاومة المضادات الحيوية لدى إحدى أنواع البكتيريا إلى أنواع أخرى عبر عدة آليات منها F-pilus أو الشعرة الإخصابية مانحة إيها مقاومة لهذه المضادات هو أمر طبي صار التعامل معه عسيرا، ويفترض كذلك أن النقل الأفقي للجينات يعزز المحافظة على حياة كيموحيوية شاملة، وكنتيجة لذلك على شمولية الشيفرة الجينية. [151]
تركز معظم الاهتمام والبحث في علم الوراثة على النقل العمودي، لكن بدأت أهمية النقل الأفقي للجينات بين وحيدات الخلية تلقى الاهتمام. [152][153]
يمكن اعتبار توصيل الجين كنقل أفقي للجينات وهو نوع من الهندسة الوراثية.
تطور

يحتوي الدنا على المعلومة الوراثية التي تسمح لكل الكائنات الحية المعاصرة بالتكاثر والنمو والقيام بمختلف الوظائف، لكن من غير الواضح منذ متى في تاريخ الحياة الممتد إلى 4 ملاير سنة كان الدنا يقوم بهذه الوظيفة، وقد اقترح أن أشكال الحياة الأولى من الممكن أن تكون استعملت الرنا كمادتها الوراثية [154][155]. يمكن أن يكون الرنا قد لعب دورا رئيسيا في أيض الخلايا الأولية حيث يمكنه القيام بكل من نقل المعلومة الوراثية وبدأ تحفيزات التفاعلات لكونه جزء من الريبوزيم [156]، يمكن لعالم الرنا القديم هذا الذي كانت تستخدم فيه الأحماض النووية لكل من التحفيز والوراثة أن يكون أثّـر على تطور الشيفرة الجينية الحالية التي أساسها أربع قواعد نووية، وهذا سيحدث لأن رقم مختلف القواعد في كائن بتلك الصفة عبارة عن توافق بين رقم صغير من القواعد يزيد في دقة النسخ ورقم كبير من القواعد يزيد في فعالية التحفيز لدى الريبوزيمات. [157]، بيد أنه لا يوجد دليل مباشر على الأنظمة الجينية القديمة لأن استخلاص الدنا من المستحثات مستحيل لكون الدنا يعيش في الطبيعة لأقل من مليون سنة، ثم يتحلل تدريجيا إلى قطع صغيرة في المحاليل [158]. هنالك ادعاءات بوجود دنا أقدم من ذلك وخاصة التقرير الذي يتحدث عن استخلاص بكتيريا حية من بلورة ملح عمرها 250 مليون سنة [159]، لكن هذه الادعاءات مثيرة للجدل وغير متفق عليها. [160][161]
يمكن أن تكون مكونات الدنا (الأدينين، الغوانين وما يتعلق بها من مركبات عضوية) قد تشكلت خارج الأرض في الفضاء الخارجي [162][163][164]. مكونات مركبات الدنا والرنا بما في ذلك اليوراسيل، السايتوسين والثايمين تم تشكيلها كذلك في المخابر تحت ظروف تماثل تلك الموجودة في الفضاء الخارجي باستخدامات متفاعلات بدء كيميائية مثل البيريميدينات المعثور عليها في الأحجار النيزكية، يمكن للبيريميدينات مثل الهيدرو كربونات الأروماتية متعددة الحلقات -أغنى مركب كيميائي بالكربون وجد في الكون- أن يكون تشكل في عملاق أحمر أو في غبار كوني و سحب غاز بين النجوم. [165]
استخدامات في التكنولوجيا
هندسة وراثية

تم تطوير طرق عديدة لاستخلاص الدنا من الكائنات الحية مثل طريقة استخلاص فينول-كلوروفورم وطرقٍ لمعالجته وتعديله في المختبر مثل طريقتي اهتضام التقييد وتفاعل البوليميراز المتسلسل. يستخدم علما الأحياء والكيمياء الحيوية الحديثين هذه الطرق بشكل كبير في تكنولوجيا الدنا المؤشب، الدنا المؤشب هو تسلسل دنا من صنع الإنسان تم تجميعه من تسلسللات دنا أخرى، حيث يمكن نقله إلى كائنات مختلفة على شكل بلازميدات أو على الشكل المناسب باستخدام ناقل فيروسي [168].
الكائنات المعدلة وراثيا المنتَجَة يمكن استخدامها لإنتاج منتجات مثل البروتينات المؤشبة المستخدمة في البحث الطبي [169] أو لزرعها وتحسين منتجات الزراعة [170][171]، تم تعديل نباتاتٍ لحمايتها من الحشرات وجعل مقاومتها أكبر ضد مبيدات الحشرات، الفيروسات والظغوط الطبيعية وتحسين قيمتها الغذائية ولإنتاج اللقاحات الصالحة للأكل [172]. معظم الكائنات المعدلة وراثيا المروج لها هي إما محاصيل نباتات مقاومة للحشرات أو للمبيدات [173]. يتم استخدام الحيوانات المعدلة جينيا في البحوث أو لتحسين نماذجها أو لإنتاج منتجات زراعية وصيدلية. وتشمل هذه التعديلات إزالة جيناتٍ لجعلها أقل عرضة للمرض، وزيادة الهرمونات لنمو أكبر وللقدرة على توفير البروتينات في الحليب. [174]
الشرطة العلمية والطب الشرعي

يمكن لعلماء الأدلة الجنائية استخدام الدنا الموجود في الدم، المني، الجلد، اللعاب والشعر المعثور عليه في مسرح الجريمة لتحديد دنا مطابق لفرد ما، كالجاني مثلا [175]، ويطلق على هذه العملية البصمة الوراثية. يُقارن في البصمة الوراثية تسلسل أطوال مختلفة متكررة من الدنا مثل التكرارات المترادفة القصيرة ودنا الساتل الصغير بين الناس. هذه الطريقة في العادة موثوق بها جدا لتحديد دنا متطابق [176]، لكن يمكن أن يكون التحديد معقدا إذا كان المسرح ملوثا بدنا من عدة أشخاص [177]. تم ابكتار تقنية البصمة الوراثية سنة 1984 بواسطة عالم الوراثة البريطاني أليك جيفريز [178]، واستخدمت أول مرة في علم الأدلة الجنائي لإدانة كولين بيتشفورك سنة 1988 في قضية قتيلتي إندربي. [179]
تستخدم البصمة الوراثية كذلك في اختبار الأبوة بالدنا لتحديد إن كان أحدهم الوالد أو الجد البيولوجي للطفل مع احتمال تطابق تصل نسبته إلى 99.99% حين يكون الوالد المزعوم قريبا بيولوجيا للطفل. وتستخدم لذلك طرق كشف التسلسل العادية بعد الولادة، في حين تستخدم طرق جديدة لاختبار الأبوة حين تكون الأم مازالت حاملا. [180]

المعلوماتية الحيوية
تتضمن المعلوماتية الحيوية تطوير تقنياتٍ لتخزين وتنقيب وبحث ومعالجة البيانات البيولوجية بما في ذلك بيانات تسلسل الأحماض النووية، وقاد ذلك إلى تطورات مستخدمة بشكل واسع في علم الحاسوب خاصة في خوارزميات البحث التسلسلية، تعلم الآلة ونظرية قواعد البيانات [181]، تم تطوير البحث التسلسلي أو خوارزميات التطابق التي تعثر على وجود تسلسل حروف معين داخل تسلسل حروف أكبر خصيصا للبحث عن تسلسلات نوكليوتيدات معينة. [182]
يمكن أن يتم صف تسلسل دنا مع تسلسل دنا آخر لتحديد التسلسللات المتماثلة وتعيين مواضع الطفرات التي تجعلهما مختلفين، تستخدم هذه التقنيات وخاصة تقنية تراصف التسلسلات المتعدد في دراسة العلاقات في علم الوراثة العرقي ووظيفة البروتين [183]. مجموعات البيانات التي تمثل تسلسلات جينومات كاملة مثل تلك الناتجة عن مشروع الجينوم البشري يصعب استخدامها من دون حاشية شرح لتحديد أماكن الجينات والعناصر المنظِّمة في كل كروموسوم، مناطق الدنا التي لديها الخصائص النمطية المتعلقة بجينات البروتين -أو الرنا- يمكن تحديدها بخوارزميات البحث عن الجين، وهو ما يسمح للباحثين بتوقع وجود نواتج جينية معينة ووظائفها المحتملة في الكائنات قبل حتى استخلاصها تجريبيا ودراستها [184]. كما يمكن مقارنة جينومات بأكملها وهو ما يسمح بتسليط الضوء على تاريخ تطور بعض الكائنات وفحص أحداث تطورية معقدة.
التقنية النانوية للدنا

تَستخدِم تقنيات الدنا النانوية خصائص التعرف الجزيئي الفريدة للدنا والأحماض النووية الأخرى لإنشاء مركبات دنا متفرعة ذاتية التجميع لها خصائص مفيدة [185]، ومنه فإن الدنا يستخدم كمادة هيكلية بدلا من أن يستخدم كحامل للمعلومة البيولوجية، وقاد هذا إلى إنشاء شبكيات دورية ثنائية الأبعاد باستخدام طريقة التجميع بالوحدات الأساسية (tile-based) وكذلك طريقة أوريغامي الدنا وإنشاء هياكل ثلاثية الأبعاد على شكل متعدد سطوح [186]. كما تم إنجاز أدوات نانومترية وخوارزمية التجميع الذاتي [187]. وتم استخدام هياكل الدنا هذه كقالب تُرتَّبُ فيه جزيئات أخرى مثل الجسيمات النانوية من الذهب وبروتينات الستربتافيدين [188] وهي بروتينات تشكل مركبات مع البيوتين.
قادت البحوث في مجال الإلكترونيات الجزيئية المبنية على الدنا شركة مايكروسوفت لتطوير لغة برمجة تسمى إزاحة سلسلة الدنا DNA Strand Displacement (DSD) [189] وتم استخدامها في تجسيد بعض المكونات النانوإلكترونية الجزيئية المبنية على الدنا. [190] [191]
التاريخ والأنثروبولوجيا
لأن الطفرات تتراكم في الدنا مع مرور الوقت وبعدها يتم توريثها للأجيال التالية، فإن الدنا يحتوي على معلومات تاريخية وبمقارنة تسلسلات الدنا المختلفة يمكن لعلماء الوراثة استنتاج التاريخ التطوري للكائنات وهذا ما يعرف بعلم الوراثة العرقي [192]. يشكل هذا المجال -بوضع علم الوراثة في خدمة علم أحياء الحفريات- أداة قوية في علم الأحياء التطوري، إذا تمت مقارنة سلاسل الدنا داخل نفس النوع يمكن لعلماء الوراثيات السكانية معرفة تاريخ شعوب معينة، ويمكن استخدام ذلك في دراسات تترواح بين علم الوراثة البيئي إلى الأنثروبولوجيا.
دراسة دنا المتقدرة داخل التجمعت البشرية يستخدم لتحديد هجرات الإنسان العاقل، على سبيل المثال تمت دراسة النمط الجماعي X في علم الديموغرافيا القديم لتقييم القرابة المحتملة لأسلاف الهنود بالشعوب الأوربية التي تعود أصولها إلى العصر الحجري القديم العلوي. [193]
-
شجرة تطور السلالات توضح نطاقات الأحياء الثلاثة: حقيقيات النوى بالأحمر، العتائق بالأخضر والبكتيريا بالأزرق.[194]
-
خريطة الهجرة البشرية المستنتجة من دراسات علم الوراثة العرقي لدنا المتقدرة البشري، المقياس 1000 سنة قبل الحاضر.[195]
تخزين المعلومات
انظر أيضا
معلومات إضافية
- DNA على مشروع الدليل المفتوح
- DNA binding site prediction on protein
- DNA coiling to form chromosomes
- DNA from the Beginning Another DNA Learning Center site on DNA, genes, and heredity from Mendel to the human genome project.
- DNA Lab, demonstrates how to extract DNA from wheat using readily available equipment and supplies.
- DNA the Double Helix Game From the official Nobel Prize web site
- DNA under electron microscope
- Dolan DNA Learning Center
- Double Helix: 50 years of DNA, نيتشر
- Double Helix 1953–2003 National Centre for Biotechnology Education
- Francis Crick and James Watson talking on the BBC in 1962, 1972, and 1974
- Genetic Education Modules for Teachers — DNA from the Beginning Study Guide
- Guide to DNA cloning
المراجع
- ^ القاموس الطبي الموحد Deoxyribonucleic acid تاريخ الولوج 14 كانون الثاني 2014 نسخة محفوظة 27 أغسطس 2017 على موقع واي باك مشين.
- ^ Saenger، Wolfram (1984). Principles of Nucleic Acid Structure. New York: Springer-Verlag. ISBN:0-387-90762-9.
{{استشهاد بكتاب}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ أ ب Alberts، Bruce؛ Johnson، Alexander؛ Lewis، Julian؛ Raff، Martin؛ Roberts، Keith؛ Peter، Walters (2002). Molecular Biology of the Cell (ط. Fourth). New York and London: Garland Science. ISBN:0-8153-3218-1. OCLC:145080076.
{{استشهاد بكتاب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) والوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Irobalieva RN، Fogg JM، Catanese DJ، Catanese DJ، Sutthibutpong T، Chen M، Barker AK، Ludtke SJ، Harris SA، Schmid MF، Chiu W، Zechiedrich L (أكتوبر 2015). "Structural diversity of supercoiled DNA". Nature Communications. ج. 6: 8440. Bibcode:2015NatCo...6E8440I. DOI:10.1038/ncomms9440. PMC:4608029. PMID:26455586.
- ^ أ ب ت Watson JD، Crick FH (أبريل 1953). "Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid" (PDF). Nature. ج. 171 ع. 4356: 737–8. Bibcode:1953Natur.171..737W. DOI:10.1038/171737a0. PMID:13054692. مؤرشف من الأصل (PDF) في 4 فبراير 2007.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Mandelkern M، Elias JG، Eden D، Crothers DM (أكتوبر 1981). "The dimensions of DNA in solution". Journal of Molecular Biology. ج. 152 ع. 1: 153–61. DOI:10.1016/0022-2836(81)90099-1. PMID:7338906.
- ^ Gregory SG, Barlow KF, McLay KE, Kaul R, Swarbreck D, Dunham A, et al. (May 2006). "The DNA sequence and biological annotation of human chromosome 1". Nature. 441 (7091): 315–21. Bibcode:2006Natur.441..315G. doi:10.1038/nature04727. PMID 16710414.
- ^ أ ب ت Berg J., Tymoczko J. and Stryer L. (2002) Biochemistry. W. H. Freeman and Company (ردمك 0-7167-4955-6)
- ^ Abbreviations and Symbols for Nucleic Acids, Polynucleotides and their Constituents نسخة محفوظة 5 February 2007 على موقع واي باك مشين. IUPAC-IUB Commission on Biochemical Nomenclature (CBN). Retrieved 3 January 2006.
- ^ أ ب Ghosh A، Bansal M (أبريل 2003). "A glossary of DNA structures from A to Z". Acta Crystallographica Section D. ج. 59 ع. Pt 4: 620–6. DOI:10.1107/S0907444903003251. PMID:12657780.
- ^ Yakovchuk P، Protozanova E، Frank-Kamenetskii MD (2006). "Base-stacking and base-pairing contributions into thermal stability of the DNA double helix". Nucleic Acids Research. ج. 34 ع. 2: 564–74. DOI:10.1093/nar/gkj454. PMC:1360284. PMID:16449200.
- ^ Burton E. Tropp – "Molecular Biology"- Jones and Barlett Learning, (ردمك 978-0-7637-8663-2)
- ^ "Watson-Crick Structure of DNA – 1953". Steven Carr. Memorial University of Newfoundland. مؤرشف من الأصل في 19 يوليو 2016. اطلع عليه بتاريخ 13 يوليو 2016.
{{استشهاد ويب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Nikolova EN، Zhou H، Gottardo FL، Alvey HS، Kimsey IJ، Al-Hashimi HM (2013). "A historical account of Hoogsteen base-pairs in duplex DNA". Biopolymers. ج. 99 ع. 12: 955–68. DOI:10.1002/bip.22334. PMC:3844552. PMID:23818176.
- ^ Clausen-Schaumann H، Rief M، Tolksdorf C، Gaub HE (أبريل 2000). "Mechanical stability of single DNA molecules". Biophysical Journal. ج. 78 ع. 4: 1997–2007. Bibcode:2000BpJ....78.1997C. DOI:10.1016/S0006-3495(00)76747-6. PMC:1300792. PMID:10733978.
- ^ Verma S، Eckstein F (1998). "Modified oligonucleotides: synthesis and strategy for users". Annual Review of Biochemistry. ج. 67: 99–134. DOI:10.1146/annurev.biochem.67.1.99. PMID:9759484.
- ^ Designation of the two strands of DNA نسخة محفوظة 24 April 2008 على موقع واي باك مشين. JCBN/NC-IUB Newsletter 1989. Retrieved 7 May 2008
- ^ Hüttenhofer A، Schattner P، Polacek N (مايو 2005). "Non-coding RNAs: hope or hype?". Trends in Genetics. ج. 21 ع. 5: 289–97. DOI:10.1016/j.tig.2005.03.007. PMID:15851066.
- ^ Munroe SH (نوفمبر 2004). "Diversity of antisense regulation in eukaryotes: multiple mechanisms, emerging patterns". Journal of Cellular Biochemistry. ج. 93 ع. 4: 664–71. DOI:10.1002/jcb.20252. PMID:15389973.
- ^ Makalowska I، Lin CF، Makalowski W (فبراير 2005). "Overlapping genes in vertebrate genomes". Computational Biology and Chemistry. ج. 29 ع. 1: 1–12. DOI:10.1016/j.compbiolchem.2004.12.006. PMID:15680581.
- ^ Johnson ZI، Chisholm SW (نوفمبر 2004). "Properties of overlapping genes are conserved across microbial genomes". Genome Research. ج. 14 ع. 11: 2268–72. DOI:10.1101/gr.2433104. PMC:525685. PMID:15520290.
- ^ Lamb RA، Horvath CM (أغسطس 1991). "Diversity of coding strategies in influenza viruses". Trends in Genetics. ج. 7 ع. 8: 261–6. DOI:10.1016/0168-9525(91)90326-L. PMID:1771674.
- ^ What Is the Advantage of Having the DNA Tightly Wrapped Into the Chromosomes?. نسخة محفوظة 13 فبراير 2018 على موقع واي باك مشين.
- ^ Benham CJ، Mielke SP (2005). "DNA mechanics". Annual Review of Biomedical Engineering. ج. 7: 21–53. DOI:10.1146/annurev.bioeng.6.062403.132016. PMID:16004565.
- ^ أ ب Champoux JJ (2001). "DNA topoisomerases: structure, function, and mechanism". Annual Review of Biochemistry. ج. 70: 369–413. DOI:10.1146/annurev.biochem.70.1.369. PMID:11395412.
- ^ أ ب Wang JC (يونيو 2002). "Cellular roles of DNA topoisomerases: a molecular perspective". Nature Reviews. Molecular Cell Biology. ج. 3 ع. 6: 430–40. DOI:10.1038/nrm831. PMID:12042765.
- ^ Basu HS، Feuerstein BG، Zarling DA، Shafer RH، Marton LJ (أكتوبر 1988). "Recognition of Z-RNA and Z-DNA determinants by polyamines in solution: experimental and theoretical studies". Journal of Biomolecular Structure & Dynamics. ج. 6 ع. 2: 299–309. DOI:10.1080/07391102.1988.10507714. PMID:2482766.
- ^ Franklin RE، Gosling RG (6 مارس 1953). "The Structure of Sodium Thymonucleate Fibres I. The Influence of Water Content" (PDF). Acta Crystallogr. ج. 6 ع. 8–9: 673–7. DOI:10.1107/S0365110X53001939. مؤرشف من الأصل (PDF) في 9 يناير 2016.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة)
Franklin RE، Gosling RG (1953). "The structure of sodium thymonucleate fibres. II. The cylindrically symmetrical Patterson function". Acta Crystallogr. ج. 6 ع. 8–9: 678–85. DOI:10.1107/S0365110X53001940. - ^ Franklin RE، Gosling RG (أبريل 1953). "Molecular configuration in sodium thymonucleate" (PDF). Nature. ج. 171 ع. 4356: 740–1. Bibcode:1953Natur.171..740F. DOI:10.1038/171740a0. PMID:13054694. مؤرشف من الأصل (PDF) في 3 يناير 2011.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Wilkins MH، Stokes AR، Wilson HR (أبريل 1953). "Molecular structure of deoxypentose nucleic acids" (PDF). Nature. ج. 171 ع. 4356: 738–40. Bibcode:1953Natur.171..738W. DOI:10.1038/171738a0. PMID:13054693. مؤرشف من الأصل (PDF) في 13 مايو 2011.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Leslie AG، Arnott S، Chandrasekaran R، Ratliff RL (أكتوبر 1980). "Polymorphism of DNA double helices". Journal of Molecular Biology. ج. 143 ع. 1: 49–72. DOI:10.1016/0022-2836(80)90124-2. PMID:7441761.
- ^ Baianu, I.C. (1980). "Structural Order and Partial Disorder in Biological systems". Bull. Math. Biol. ج. 42 ع. 4: 137–141. DOI:10.1007/BF02462372. "Archived copy". مؤرشف من الأصل في 25 يوليو 2009. اطلع عليه بتاريخ 6 مايو 2009.
{{استشهاد ويب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة)صيانة الاستشهاد: الأرشيف كعنوان (link) - ^ Hosemann R., Bagchi R.N., Direct analysis of diffraction by matter, North-Holland Publs., Amsterdam – New York, 1962.
- ^ Baianu, I.C. (1978). "X-ray scattering by partially disordered membrane systems". Acta Crystallogr A. ج. 34 ع. 5: 751–753. Bibcode:1978AcCrA..34..751B. DOI:10.1107/S0567739478001540.
- ^ Wahl MC، Sundaralingam M (1997). "Crystal structures of A-DNA duplexes". Biopolymers. ج. 44 ع. 1: 45–63. DOI:10.1002/(SICI)1097-0282(1997)44:1<45::AID-BIP4>3.0.CO;2-#. PMID:9097733.
- ^ Lu XJ، Shakked Z، Olson WK (يوليو 2000). "A-form conformational motifs in ligand-bound DNA structures". Journal of Molecular Biology. ج. 300 ع. 4: 819–40. DOI:10.1006/jmbi.2000.3690. PMID:10891271.
- ^ Rothenburg S، Koch-Nolte F، Haag F (ديسمبر 2001). "DNA methylation and Z-DNA formation as mediators of quantitative differences in the expression of alleles". Immunological Reviews. ج. 184: 286–98. DOI:10.1034/j.1600-065x.2001.1840125.x. PMID:12086319.
- ^ Oh DB، Kim YG، Rich A (ديسمبر 2002). "Z-DNA-binding proteins can act as potent effectors of gene expression in vivo". Proceedings of the National Academy of Sciences of the United States of America. ج. 99 ع. 26: 16666–71. Bibcode:2002PNAS...9916666O. DOI:10.1073/pnas.262672699. PMC:139201. PMID:12486233.
- ^
Richard R، Sinden (15 يناير 1994). DNA structure and function. Academic Press. ص. 398. ISBN:0-12-645750-6.
{{استشهاد بكتاب}}: الوسيط غير المعروف|édition=تم تجاهله (مساعدة) - ^
Rich A, Norheim A, Wang AHJ. "The chemistry and biology of left-handed Z-DNA". Annual Review of Biochemistry. ج. 53: 791–846. DOI:10.1146/annurev.bi.53.070184.004043. PMID:6383204.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|année=تم تجاهله يقترح استخدام|date=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Ho PS (27 سبتمبر 1994). "The non-B-DNA structure of d(CA/TG)n does not differ from that of Z-DNA". Proc Natl Acad Sci USA. ج. 91 ع. 20: 9549–9553. Bibcode:1994PNAS...91.9549H. DOI:10.1073/pnas.91.20.9549. PMC:44850. PMID:7937803.
- ^ Created from نسخة محفوظة 17 October 2016 على موقع واي باك مشين.
- ^ Frédéric Pâques et James E. Haber, « Multiple Pathways of Recombination Induced by Double-Strand Breaks in Saccharomyces cerevisiae », في Microbiology and Molecular Biology Reviews, vol. 63, no 2, juin 1999, ص. 349-404 [النص الكامل, lien PMID (pages consultées le 19-02-2018)]
- ^ Irina Voineagu, Vidhya Narayanan, Kirill S. Lobachev et Sergei M. Mirkin, « Replication stalling at unstable inverted repeats: Interplay between DNA hairpins and fork stabilizing proteins », في Proceedings of the National Academy of Sciences of the United States of America, vol. 105, no 29, 22 juillet 2008, ص. 9936-9941 [النص الكامل, lien PMID, lien DOI (pages consultées le 14 mars 2015)]
- ^ Guy-Franck Richard, Alix Kerrest et Bernard Dujon, « Comparative Genomics and Molecular Dynamics of DNA Repeats in Eukaryotes », في Microbiology and Molecular Biology Reviews, vol. 72, no 4, décembre 2008, ص. 686–727 [النص الكامل, lien PMID, lien DOI (pages consultées le 14 mars 2015)]
- ^ أ ب Greider CW، Blackburn EH (ديسمبر 1985). "Identification of a specific telomere terminal transferase activity in Tetrahymena extracts". Cell. ج. 43 ع. 2 Pt 1: 405–13. DOI:10.1016/0092-8674(85)90170-9. PMID:3907856.
- ^ أ ب ت Nugent CI، Lundblad V (أبريل 1998). "The telomerase reverse transcriptase: components and regulation". Genes & Development. ج. 12 ع. 8: 1073–85. DOI:10.1101/gad.12.8.1073. PMID:9553037.
- ^ Wright WE، Tesmer VM، Huffman KE، Levene SD، Shay JW (نوفمبر 1997). "Normal human chromosomes have long G-rich telomeric overhangs at one end". Genes & Development. ج. 11 ع. 21: 2801–9. DOI:10.1101/gad.11.21.2801. PMC:316649. PMID:9353250.
- ^ أ ب Burge S، Parkinson GN، Hazel P، Todd AK، Neidle S (2006). "Quadruplex DNA: sequence, topology and structure". Nucleic Acids Research. ج. 34 ع. 19: 5402–15. DOI:10.1093/nar/gkl655. PMC:1636468. PMID:17012276.
- ^ Parkinson GN، Lee MP، Neidle S (يونيو 2002). "Crystal structure of parallel quadruplexes from human telomeric DNA". Nature. ج. 417 ع. 6891: 876–80. Bibcode:2002Natur.417..876P. DOI:10.1038/nature755. PMID:12050675.
- ^ Griffith JD، Comeau L، Rosenfield S، Stansel RM، Bianchi A، Moss H، de Lange T (مايو 1999). "Mammalian telomeres end in a large duplex loop". Cell. ج. 97 ع. 4: 503–14. DOI:10.1016/S0092-8674(00)80760-6. PMID:10338214.
- ^ Seeman NC (نوفمبر 2005). "DNA enables nanoscale control of the structure of matter". Quarterly Reviews of Biophysics. ج. 38 ع. 4: 363–71. DOI:10.1017/S0033583505004087. PMC:3478329. PMID:16515737.
- ^ Hu Q، Rosenfeld MG (2012). "Epigenetic regulation of human embryonic stem cells". Frontiers in Genetics. ج. 3: 238. DOI:10.3389/fgene.2012.00238. PMC:3488762. PMID:23133442.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Klose RJ، Bird AP (فبراير 2006). "Genomic DNA methylation: the mark and its mediators". Trends in Biochemical Sciences. ج. 31 ع. 2: 89–97. DOI:10.1016/j.tibs.2005.12.008. PMID:16403636.
- ^ Bird A (يناير 2002). "DNA methylation patterns and epigenetic memory". Genes & Development. ج. 16 ع. 1: 6–21. DOI:10.1101/gad.947102. PMID:11782440.
- ^ Walsh CP، Xu GL (2006). "Cytosine methylation and DNA repair". Current Topics in Microbiology and Immunology. Current Topics in Microbiology and Immunology. ج. 301: 283–315. DOI:10.1007/3-540-31390-7_11. ISBN:3-540-29114-8. PMID:16570853.
- ^ Kriaucionis S، Heintz N (مايو 2009). "The nuclear DNA base 5-hydroxymethylcytosine is present in Purkinje neurons and the brain". Science. ج. 324 ع. 5929: 929–30. Bibcode:2009Sci...324..929K. DOI:10.1126/science.1169786. PMC:3263819. PMID:19372393.
- ^ Ratel D، Ravanat JL، Berger F، Wion D (مارس 2006). "N6-methyladenine: the other methylated base of DNA". BioEssays. ج. 28 ع. 3: 309–15. DOI:10.1002/bies.20342. PMC:2754416. PMID:16479578.
- ^ Gommers-Ampt JH، Van Leeuwen F، de Beer AL، Vliegenthart JF، Dizdaroglu M، Kowalak JA، Crain PF، Borst P (ديسمبر 1993). "beta-D-glucosyl-hydroxymethyluracil: a novel modified base present in the DNA of the parasitic protozoan T. brucei". Cell. ج. 75 ع. 6: 1129–36. DOI:10.1016/0092-8674(93)90322-H. PMID:8261512.
- ^ Henri G.A.M. van Luenen, Carol Farris, Sabrina Jan, Paul-Andre Genest, Pankaj Tripathi, Arno Velds, Ron M. Kerkhoven, Marja Nieuwland, Andrew Haydock, Gowthaman Ramasamy, Saara Vainio, Tatjana Heidebrecht, Anastassis Perrakis, Ludo Pagie, Bas van Steensel, Peter J. Myler et Piet Borst, « Glucosylated Hydroxymethyluracil, DNA Base J, Prevents Transcriptional Readthrough in Leishmania », في Cellvolume = 150, no 5, 31 août 2012, ص. 909-921 [النص الكامل, lien PMID, lien DOI (pages consultées le 12 mars 2015)]
- ^ Dane Z. Hazelbaker et Stephen Buratowski, « Transcription: Base J Blocks the Way », في Current Biology, vol. 22, no 22, 2012, ص. R960-R962 [النص الكامل, lien PMID, lien DOI (pages consultées le 12 mars 2015)]
- ^ Created from PDB 1JDG نسخة محفوظة 22 سبتمبر 2008 على موقع واي باك مشين.
- ^ Douki T، Reynaud-Angelin A، Cadet J، Sage E (أغسطس 2003). "Bipyrimidine photoproducts rather than oxidative lesions are the main type of DNA damage involved in the genotoxic effect of solar UVA radiation". Biochemistry. ج. 42 ع. 30: 9221–6. DOI:10.1021/bi034593c. PMID:12885257.
- ^ Cadet J، Delatour T، Douki T، Gasparutto D، Pouget JP، Ravanat JL، Sauvaigo S (مارس 1999). "Hydroxyl radicals and DNA base damage". Mutation Research. ج. 424 ع. 1–2: 9–21. DOI:10.1016/S0027-5107(99)00004-4. PMID:10064846.
- ^ Beckman KB، Ames BN (أغسطس 1997). "Oxidative decay of DNA". The Journal of Biological Chemistry. ج. 272 ع. 32: 19633–6. DOI:10.1074/jbc.272.32.19633. PMID:9289489.
- ^ Valerie K، Povirk LF (سبتمبر 2003). "Regulation and mechanisms of mammalian double-strand break repair". Oncogene. ج. 22 ع. 37: 5792–812. DOI:10.1038/sj.onc.1206679. PMID:12947387.
- ^ Johnson، George (28 ديسمبر 2010). "Unearthing Prehistoric Tumors, and Debate". نيويورك تايمز. مؤرشف من الأصل في 24 يونيو 2017.
If we lived long enough, sooner or later we all would get cancer.
{{استشهاد بخبر}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) والوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Alberts B، Johnson A، Lewis J، وآخرون (2002). "The Preventable Causes of Cancer". Molecular biology of the cell (ط. 4th). New York: Garland Science. ISBN:0-8153-4072-9. مؤرشف من الأصل في 2 يناير 2016.
هناك كمية معينة غير قابلة للخفض متوقعة من السرطان بغض النظر عن الظروف: الطفرات لا يمكن تجنبها نهائيا لأنها نتائج لا مفر منها لحدود طبيعية أساسية في دقة تضاعف الدنا كما هو موضح في العنوان 5: إعادة تركيب الجينات. لو عاش الإنسان مدة كافية فلا مفر من أن إحدى خلاياه على الأقل ستتراكم لديها في النهاية طفرات كافية للتسبب بالسرطان.
{{استشهاد بكتاب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Bernstein H، Payne CM، Bernstein C، Garewal H، Dvorak K (2008). "Cancer and aging as consequences of un-repaired DNA damage". في Kimura H، Suzuki A (المحررون). New Research on DNA Damage. New York: Nova Science Publishers. ص. 1–47. ISBN:978-1-60456-581-2. مؤرشف من الأصل في 25 أكتوبر 2014.
{{استشهاد بكتاب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) والوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Hoeijmakers JH (أكتوبر 2009). "DNA damage, aging, and cancer". The New England Journal of Medicine. ج. 361 ع. 15: 1475–85. DOI:10.1056/NEJMra0804615. PMID:19812404.
- ^ Freitas AA، de Magalhães JP (2011). "A review and appraisal of the DNA damage theory of ageing". Mutation Research. ج. 728 ع. 1–2: 12–22. DOI:10.1016/j.mrrev.2011.05.001. PMID:21600302.
- ^ Ferguson LR، Denny WA (سبتمبر 1991). "The genetic toxicology of acridines". Mutation Research. ج. 258 ع. 2: 123–60. DOI:10.1016/0165-1110(91)90006-H. PMID:1881402.
- ^ Stephens TD، Bunde CJ، Fillmore BJ (يونيو 2000). "Mechanism of action in thalidomide teratogenesis". Biochemical Pharmacology. ج. 59 ع. 12: 1489–99. DOI:10.1016/S0006-2952(99)00388-3. PMID:10799645.
- ^ Jeffrey AM (1985). "DNA modification by chemical carcinogens". Pharmacology & Therapeutics. ج. 28 ع. 2: 237–72. DOI:10.1016/0163-7258(85)90013-0. PMID:3936066.
- ^ Braña MF، Cacho M، Gradillas A، de Pascual-Teresa B، Ramos A (نوفمبر 2001). "Intercalators as anticancer drugs". Current Pharmaceutical Design. ج. 7 ع. 17: 1745–80. DOI:10.2174/1381612013397113. PMID:11562309.
- ^ Venter JC، Adams MD، Myers EW، Li PW، Mural RJ، Sutton GG، وآخرون (فبراير 2001). "The sequence of the human genome". Science. ج. 291 ع. 5507: 1304–51. Bibcode:2001Sci...291.1304V. DOI:10.1126/science.1058040. PMID:11181995.
- ^ Thanbichler M، Wang SC، Shapiro L (أكتوبر 2005). "The bacterial nucleoid: a highly organized and dynamic structure". Journal of Cellular Biochemistry. ج. 96 ع. 3: 506–21. DOI:10.1002/jcb.20519. PMID:15988757.
- ^ Wolfsberg TG، McEntyre J، Schuler GD (فبراير 2001). "Guide to the draft human genome". Nature. ج. 409 ع. 6822: 824–6. Bibcode:2001Natur.409..824W. DOI:10.1038/35057000. PMID:11236998.
- ^ Gregory TR (يناير 2005). "The C-value enigma in plants and animals: a review of parallels and an appeal for partnership". Annals of Botany. ج. 95 ع. 1: 133–46. DOI:10.1093/aob/mci009. PMID:15596463.
- ^ Birney E، Stamatoyannopoulos JA، Dutta A، Guigó R، Gingeras TR، Margulies EH، وآخرون (يونيو 2007). "Identification and analysis of functional elements in 1% of the human genome by the ENCODE pilot project". Nature. ج. 447 ع. 7146: 799–816. Bibcode:2007Natur.447..799B. DOI:10.1038/nature05874. PMC:2212820. PMID:17571346.
- ^ Pidoux AL، Allshire RC (مارس 2005). "The role of heterochromatin in centromere function". Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. ج. 360 ع. 1455: 569–79. DOI:10.1098/rstb.2004.1611. PMC:1569473. PMID:15905142.
- ^ Harrison PM، Hegyi H، Balasubramanian S، Luscombe NM، Bertone P، Echols N، Johnson T، Gerstein M (فبراير 2002). "Molecular fossils in the human genome: identification and analysis of the pseudogenes in chromosomes 21 and 22". Genome Research. ج. 12 ع. 2: 272–80. DOI:10.1101/gr.207102. PMC:155275. PMID:11827946.
- ^ Harrison PM، Gerstein M (مايو 2002). "Studying genomes through the aeons: protein families, pseudogenes and proteome evolution". Journal of Molecular Biology. ج. 318 ع. 5: 1155–74. DOI:10.1016/S0022-2836(02)00109-2. PMID:12083509.
- ^ Albà M (2001). "Replicative DNA polymerases". Genome Biology. ج. 2 ع. 1: REVIEWS3002. DOI:10.1186/gb-2001-2-1-reviews3002. PMC:150442. PMID:11178285.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|nopp=تم تجاهله يقترح استخدام|no-pp=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Tani، Katsuji؛ Nasu، Masao (2010). "Roles of Extracellular DNA in Bacterial Ecosystems". في Kikuchi، Yo؛ Rykova، Elena Y. (المحررون). Extracellular Nucleic Acids. Springer. ص. 25–38. ISBN:978-3-642-12616-1.
{{استشهاد بكتاب}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Vlassov VV، Laktionov PP، Rykova EY (يوليو 2007). "Extracellular nucleic acids". BioEssays. ج. 29 ع. 7: 654–67. DOI:10.1002/bies.20604. PMID:17563084.
- ^ Finkel SE، Kolter R (نوفمبر 2001). "DNA as a nutrient: novel role for bacterial competence gene homologs". Journal of Bacteriology. ج. 183 ع. 21: 6288–93. DOI:10.1128/JB.183.21.6288-6293.2001. PMC:100116. PMID:11591672.
- ^ Mulcahy H، Charron-Mazenod L، Lewenza S (نوفمبر 2008). "Extracellular DNA chelates cations and induces antibiotic resistance in Pseudomonas aeruginosa biofilms". PLoS Pathogens. ج. 4 ع. 11: e1000213. DOI:10.1371/journal.ppat.1000213. PMC:2581603. PMID:19023416.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Berne C، Kysela DT، Brun YV (أغسطس 2010). "A bacterial extracellular DNA inhibits settling of motile progeny cells within a biofilm". Molecular Microbiology. ج. 77 ع. 4: 815–29. DOI:10.1111/j.1365-2958.2010.07267.x. PMC:2962764. PMID:20598083.
- ^ Whitchurch CB، Tolker-Nielsen T، Ragas PC، Mattick JS (فبراير 2002). "Extracellular DNA required for bacterial biofilm formation". Science. ج. 295 ع. 5559: 1487. DOI:10.1126/science.295.5559.1487. PMID:11859186.
- ^ Hu W، Li L، Sharma S، Wang J، McHardy I، Lux R، Yang Z، He X، Gimzewski JK، Li Y، Shi W (2012). "DNA builds and strengthens the extracellular matrix in Myxococcus xanthus biofilms by interacting with exopolysaccharides". PLoS One. ج. 7 ع. 12: e51905. Bibcode:2012PLoSO...751905H. DOI:10.1371/journal.pone.0051905. PMC:3530553. PMID:23300576.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Hui L، Bianchi DW (فبراير 2013). "Recent advances in the prenatal interrogation of the human fetal genome". Trends in Genetics. ج. 29 ع. 2: 84–91. DOI:10.1016/j.tig.2012.10.013. PMC:4378900. PMID:23158400.
- ^ Sandman K، Pereira SL، Reeve JN (ديسمبر 1998). "Diversity of prokaryotic chromosomal proteins and the origin of the nucleosome". Cellular and Molecular Life Sciences. ج. 54 ع. 12: 1350–64. DOI:10.1007/s000180050259. PMID:9893710.
- ^ Dame RT (مايو 2005). "The role of nucleoid-associated proteins in the organization and compaction of bacterial chromatin". Molecular Microbiology. ج. 56 ع. 4: 858–70. DOI:10.1111/j.1365-2958.2005.04598.x. PMID:15853876.
- ^ Luger K، Mäder AW، Richmond RK، Sargent DF، Richmond TJ (سبتمبر 1997). "Crystal structure of the nucleosome core particle at 2.8 A resolution". Nature. ج. 389 ع. 6648: 251–60. Bibcode:1997Natur.389..251L. DOI:10.1038/38444. PMID:9305837.
- ^ Jenuwein T، Allis CD (أغسطس 2001). "Translating the histone code" (PDF). Science. ج. 293 ع. 5532: 1074–80. DOI:10.1126/science.1063127. PMID:11498575. مؤرشف من الأصل (PDF) في 8 أغسطس 2017.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Ito T (2003). "Nucleosome assembly and remodeling". Current Topics in Microbiology and Immunology. Current Topics in Microbiology and Immunology. ج. 274: 1–22. DOI:10.1007/978-3-642-55747-7_1. ISBN:978-3-540-44208-0. PMID:12596902.
- ^ Thomas JO (أغسطس 2001). "HMG1 and 2: architectural DNA-binding proteins". Biochemical Society Transactions. ج. 29 ع. Pt 4: 395–401. DOI:10.1042/BST0290395. PMID:11497996.
- ^ Grosschedl R، Giese K، Pagel J (مارس 1994). "HMG domain proteins: architectural elements in the assembly of nucleoprotein structures". Trends in Genetics. ج. 10 ع. 3: 94–100. DOI:10.1016/0168-9525(94)90232-1. PMID:8178371.
- ^ Created from PDB 1LMB نسخة محفوظة 6 January 2008 على موقع واي باك مشين.
- ^ Iftode C، Daniely Y، Borowiec JA (1999). "Replication protein A (RPA): the eukaryotic SSB". Critical Reviews in Biochemistry and Molecular Biology. ج. 34 ع. 3: 141–80. DOI:10.1080/10409239991209255. PMID:10473346.
- ^ Myers LC، Kornberg RD (2000). "Mediator of transcriptional regulation". Annual Review of Biochemistry. ج. 69: 729–49. DOI:10.1146/annurev.biochem.69.1.729. PMID:10966474.
- ^ Spiegelman BM، Heinrich R (أكتوبر 2004). "Biological control through regulated transcriptional coactivators". Cell. ج. 119 ع. 2: 157–67. DOI:10.1016/j.cell.2004.09.037. PMID:15479634.
- ^ Li Z، Van Calcar S، Qu C، Cavenee WK، Zhang MQ، Ren B (يوليو 2003). "A global transcriptional regulatory role for c-Myc in Burkitt's lymphoma cells". Proceedings of the National Academy of Sciences of the United States of America. ج. 100 ع. 14: 8164–9. Bibcode:2003PNAS..100.8164L. DOI:10.1073/pnas.1332764100. PMC:166200. PMID:12808131.
- ^ Pabo CO، Sauer RT (1984). "Protein-DNA recognition". Annual Review of Biochemistry. ج. 53: 293–321. DOI:10.1146/annurev.bi.53.070184.001453. PMID:6236744.
- ^ Created from PDB 1RVA نسخة محفوظة 6 January 2008 على موقع واي باك مشين.
- ^ Bickle TA، Krüger DH (يونيو 1993). "Biology of DNA restriction". Microbiological Reviews. ج. 57 ع. 2: 434–50. PMC:372918. PMID:8336674.
- ^ أ ب Doherty AJ، Suh SW (نوفمبر 2000). "Structural and mechanistic conservation in DNA ligases". Nucleic Acids Research. ج. 28 ع. 21: 4051–8. DOI:10.1093/nar/28.21.4051. PMC:113121. PMID:11058099.
- ^ Schoeffler AJ، Berger JM (ديسمبر 2005). "Recent advances in understanding structure-function relationships in the type II topoisomerase mechanism". Biochemical Society Transactions. ج. 33 ع. Pt 6: 1465–70. DOI:10.1042/BST20051465. PMID:16246147.
- ^ Tuteja N، Tuteja R (مايو 2004). "Unraveling DNA helicases. Motif, structure, mechanism and function". European Journal of Biochemistry. ج. 271 ع. 10: 1849–63. DOI:10.1111/j.1432-1033.2004.04094.x. PMID:15128295.
- ^ Joyce CM، Steitz TA (نوفمبر 1995). "Polymerase structures and function: variations on a theme?". Journal of Bacteriology. ج. 177 ع. 22: 6321–9. DOI:10.1128/jb.177.22.6321-6329.1995. PMC:177480. PMID:7592405.
- ^ Hubscher U، Maga G، Spadari S (2002). "Eukaryotic DNA polymerases". Annual Review of Biochemistry. ج. 71: 133–63. DOI:10.1146/annurev.biochem.71.090501.150041. PMID:12045093.
- ^ Johnson A، O'Donnell M (2005). "Cellular DNA replicases: components and dynamics at the replication fork". Annual Review of Biochemistry. ج. 74: 283–315. DOI:10.1146/annurev.biochem.73.011303.073859. PMID:15952889.
- ^ أ ب Tarrago-Litvak L، Andréola ML، Nevinsky GA، Sarih-Cottin L، Litvak S (مايو 1994). "The reverse transcriptase of HIV-1: from enzymology to therapeutic intervention". FASEB Journal. ج. 8 ع. 8: 497–503. PMID:7514143.
- ^ Martinez E (ديسمبر 2002). "Multi-protein complexes in eukaryotic gene transcription". Plant Molecular Biology. ج. 50 ع. 6: 925–47. DOI:10.1023/A:1021258713850. PMID:12516863.
- ^ Sharma S، Javadekar SM، Pandey M، Srivastava M، Kumari R، Raghavan SC (مارس 2015). "Homology and enzymatic requirements of microhomology-dependent alternative end joining". Cell Death & Disease. ج. 6 ع. 3: e1697. DOI:10.1038/cddis.2015.58. PMC:4385936. PMID:25789972.
- ^ Chen J، Miller BF، Furano AV (أبريل 2014). "Repair of naturally occurring mismatches can induce mutations in flanking DNA". eLife. ج. 3: e02001. DOI:10.7554/elife.02001. PMC:3999860. PMID:24843013.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Rodgers K، McVey M (يناير 2016). "Error-Prone Repair of DNA Double-Strand Breaks". Journal of Cellular Physiology. ج. 231 ع. 1: 15–24. DOI:10.1002/jcp.25053. PMC:4586358. PMID:26033759.
- ^ أ ب Bertram JS (ديسمبر 2000). "The molecular biology of cancer". Molecular Aspects of Medicine. إلزيفير. ج. 21 ع. 6: 167–223. DOI:10.1016/S0098-2997(00)00007-8. PMID:11173079.
- ^ Aminetzach YT، Macpherson JM، Petrov DA (يوليو 2005). "Pesticide resistance via transposition-mediated adaptive gene truncation in Drosophila". Science. الجمعية الأمريكية لتقدم العلوم. ج. 309 ع. 5735: 764–7. Bibcode:2005Sci...309..764A. DOI:10.1126/science.1112699. PMID:16051794.
- ^ Burrus V، Waldor MK (يونيو 2004). "Shaping bacterial genomes with integrative and conjugative elements". Research in Microbiology. Elsevier. ج. 155 ع. 5: 376–86. DOI:10.1016/j.resmic.2004.01.012. PMID:15207870.
- ^ Sawyer SA، Parsch J، Zhang Z، Hartl DL (أبريل 2007). "Prevalence of positive selection among nearly neutral amino acid replacements in Drosophila". Proceedings of the National Academy of Sciences of the United States of America. الأكاديمية الوطنية للعلوم. ج. 104 ع. 16: 6504–10. Bibcode:2007PNAS..104.6504S. DOI:10.1073/pnas.0701572104. PMC:1871816. PMID:17409186.
- ^ Created from PDB 1M6G نسخة محفوظة 10 January 2010 على موقع واي باك مشين.
- ^ Cremer T، Cremer C (أبريل 2001). "Chromosome territories, nuclear architecture and gene regulation in mammalian cells". Nature Reviews. Genetics. ج. 2 ع. 4: 292–301. DOI:10.1038/35066075. PMID:11283701.
- ^ Pál C، Papp B، Lercher MJ (مايو 2006). "An integrated view of protein evolution". Nature Reviews. Genetics. ج. 7 ع. 5: 337–48. DOI:10.1038/nrg1838. PMID:16619049.
- ^ O'Driscoll M، Jeggo PA (يناير 2006). "The role of double-strand break repair - insights from human genetics". Nature Reviews. Genetics. ج. 7 ع. 1: 45–54. DOI:10.1038/nrg1746. PMID:16369571.
- ^ Vispé S، Defais M (أكتوبر 1997). "Mammalian Rad51 protein: a RecA homologue with pleiotropic functions". Biochimie. ج. 79 ع. 9–10: 587–92. DOI:10.1016/S0300-9084(97)82007-X. PMID:9466696.
- ^ Neale MJ، Keeney S (يوليو 2006). "Clarifying the mechanics of DNA strand exchange in meiotic recombination". Nature. ج. 442 ع. 7099: 153–8. Bibcode:2006Natur.442..153N. DOI:10.1038/nature04885. PMC:5607947. PMID:16838012.
- ^ Dickman MJ، Ingleston SM، Sedelnikova SE، Rafferty JB، Lloyd RG، Grasby JA، Hornby DP (نوفمبر 2002). "The RuvABC resolvasome". European Journal of Biochemistry. ج. 269 ع. 22: 5492–501. DOI:10.1046/j.1432-1033.2002.03250.x. PMID:12423347.
- ^ "Transposase" (PDF). PDB-101. 2006. اطلع عليه بتاريخ 23 mars 2015.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) دُوِي:10.2210/rcsb_pdb/mom_2006_12 - ^ Phillip Sanmiguel et Jeffrey L. Bennetzen, « Evidence that a Recent Increase in Maize Genome Size was Caused by the Massive Amplification of Intergene Retrotransposons », في Annals of Botany, vol. 82, no Supplement A, décembre 1998, ص. 37-44 [النص الكامل, lien DOI (pages consultées le 23 mars 2015)]
- ^ Wanlong Li,Peng Zhang, John P. Fellers, Bernd Friebe et Bikram S. Gill, « Sequence composition, organization, and evolution of the core Triticeae genome », في The Plant Journal, vol. 40, no 4, novembre 2004, ص. 500-511 [النص الكامل, lien PMID, lien DOI (pages consultées le 23 mars 2015)]
- ^ International Human Genome Sequencing Consortium, « Initial sequencing and analysis of the human genome », في Nature, vol. 409, no 6822, 1الأول {{{1}}} février 2001, ص. 860-921 [النص الكامل, lien PMID, lien DOI (pages consultées le 23 mars 2015)]
- ^ Etienne Bucher, Jon Reinders et Marie Mirouze, « Epigenetic control of transposon transcription and mobility in Arabidopsis », في Current Opinion in Plant Biology, vol. 15, no 6, novembre 2012, ص. 503-510 [النص الكامل, lien PMID, lien DOI (pages consultées le 23 mars 2015)]
- ^ أ ب David R. Edgel Marlene Belfort et David A. Shub, « Barriers to Intron Promiscuity in Bacteria », في Journal of Bacteriology, vol. 182, no 19, octobre 2000, ص. 5281-5289 [النص الكامل, lien PMID, lien DOI (pages consultées le 24 mars 2015)]
- ^ Linus Sandegren et Britt-Marie Sjöberg, « Distribution, sequence homology, and homing of group I introns among T-even-like bacteriophages: evidence for recent transfer of old introns », في Journal of Biological Chemistry, vol. 279, no 21, 21 mai 2004, ص. 22218-22227 [النص الكامل, lien PMID, lien DOI (pages consultées le 24 mars 2015)]
- ^ Richard P. Bonocora et David A. Shub, « A Self-Splicing Group I Intron in DNA Polymerase Genes of T7-Like Bacteriophages », في Journal of Bacteriology, vol. 186, no 23, décembre 2004, ص. 8153-8155 [النص الكامل, lien PMID, lien DOI (pages consultées le 24 mars 2015)]
- ^ Chia-Ni Lee, Juey-Wen Lin, Shu-Fen Weng et Yi-Hsiung Tseng, « Genomic Characterization of the Intron-Containing T7-Like Phage phiL7 of Xanthomonas campestris », في Applied and Environmental Microbiology, vol. 75, no 24, décembre 2009, ص. 7828-7837 [النص الكامل, lien PMID, lien DOI (pages consultées le 24 mars 2015)]
- ^ Keeling, P. J., & Palmer, J.D. (أغسطس 2008). "Horizontal gene transfer in eukaryotic evolution". Nature Reviews Genetics. ج. 9 ع. 8: 605–618. DOI:10.1038/nrg2386. PMID:18591983.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ أ ب Gyles، C.؛ Boerlin, P. (مارس 2014). "Horizontally transferred genetic elements and their role in pathogenesis of bacterial disease". Veterinary Pathology. ج. 51 ع. 2: 328–340. DOI:10.1177/0300985813511131. PMID:24318976.
- ^ Vaux، Felix؛ Trewick، Steven A.؛ Morgan-Richards، Mary (2017). "Speciation through the looking-glass". Biological Journal of the Linnean Society. ج. 120 ع. 2: 480–488. DOI:10.1111/bij.12872.
- ^ OECD, Safety Assessment of Transgenic Organisms, Volume 4: OECD Consensus Documents, 2010, pp.171-174
- ^ Kay E، Vogel TM، Bertolla F، Nalin R، Simonet P (يوليو 2002). "In situ transfer of antibiotic resistance genes from transgenic (transplastomic) tobacco plants to bacteria". Appl. Environ. Microbiol. ج. 68 ع. 7: 3345–51. DOI:10.1128/aem.68.7.3345-3351.2002. PMC:126776. PMID:12089013.
- ^ Koonin EV، Makarova KS، Aravind L (2001). "Horizontal gene transfer in prokaryotes: quantification and classification". Annu. Rev. Microbiol. ج. 55 ع. 1: 709–42. DOI:10.1146/annurev.micro.55.1.709. PMID:11544372.
- ^ Nielsen KM (1998). "Barriers to horizontal gene transfer by natural transformation in soil bacteria". APMIS Suppl. ج. 84: 77–84. PMID:9850687.
- ^ McGowan C، Fulthorpe R، Wright A، Tiedje JM (أكتوبر 1998). "Evidence for interspecies gene transfer in the evolution of 2,4-dichlorophenoxyacetic acid degraders". Appl. Environ. Microbiol. ج. 64 ع. 10: 4089–92. PMC:106609. PMID:9758850.
- ^ Keen، E. C. (ديسمبر 2012). "Paradigms of pathogenesis: Targeting the mobile genetic elements of disease". Frontiers in Cellular and Infection Microbiology. ج. 2: 161. DOI:10.3389/fcimb.2012.00161. PMC:3522046. PMID:23248780.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Naik GA، Bhat LN، Chpoade BA، Lynch JM (1994). "Transfer of broad-host-range antibiotic resistance plasmids in soil microcosms". Curr. Microbiol. ج. 28 ع. 4: 209–215. DOI:10.1007/BF01575963.
- ^ Varga M, Kuntova L, Pantucek R, Maslanova I, Ruzickova V, Doskar J (2012). "Efficient transfer of antibiotic resistance plasmids by transduction within methicillin-resistant Staphylococcus aureus USA300 clone". FEMS Microbiol. Lett. ج. 332 ع. 2: 146–152. DOI:10.1111/j.1574-6968.2012.02589.x. PMID:22553940.
- ^ Varga M, Pantucek R, Ruzickova V, Doskar J (2016). "Molecular characterization of a new efficiently transducing bacteriophage identified in meticillin-resistant Staphylococcus aureus". Journal of General Virology. ج. 97 ع. 1: 258–268. DOI:10.1099/jgv.0.000329. PMID:26537974.
- ^ Kubyshkin، V.؛ Acevedo-Rocha، C. G.؛ Budisa، N. (2017). "On universal coding events in protein biogenesis". Biosystems. DOI:10.1016/j.biosystems.2017.10.004.
- ^ Lin Edwards (4 أكتوبر 2010). "Horizontal gene transfer in microbes much more frequent than previously thought". PhysOrg.com. اطلع عليه بتاريخ 2012-01-06.
- ^ Carrie Arnold (18 أبريل 2011). "To Share and Share Alike: Bacteria swap genes with their neighbors more frequently than researchers have realized". Scientific American. مؤرشف من الأصل في 2012-11-02. اطلع عليه بتاريخ 2012-01-06.
- ^ Joyce GF (يوليو 2002). "The antiquity of RNA-based evolution". Nature. ج. 418 ع. 6894: 214–21. Bibcode:2002Natur.418..214J. DOI:10.1038/418214a. PMID:12110897.
- ^ Orgel LE (2004). "Prebiotic chemistry and the origin of the RNA world". Critical Reviews in Biochemistry and Molecular Biology. ج. 39 ع. 2: 99–123. CiteSeerX:10.1.1.537.7679. DOI:10.1080/10409230490460765. PMID:15217990.
- ^ Davenport RJ (مايو 2001). "Ribozymes. Making copies in the RNA world". Science. ج. 292 ع. 5520: 1278. DOI:10.1126/science.292.5520.1278a. PMID:11360970.
- ^ Szathmáry E (أبريل 1992). "What is the optimum size for the genetic alphabet?". Proceedings of the National Academy of Sciences of the United States of America. ج. 89 ع. 7: 2614–8. Bibcode:1992PNAS...89.2614S. DOI:10.1073/pnas.89.7.2614. PMC:48712. PMID:1372984.
- ^ Lindahl T (أبريل 1993). "Instability and decay of the primary structure of DNA". Nature. ج. 362 ع. 6422: 709–15. Bibcode:1993Natur.362..709L. DOI:10.1038/362709a0. PMID:8469282.
- ^ Vreeland RH، Rosenzweig WD، Powers DW (أكتوبر 2000). "Isolation of a 250 million-year-old halotolerant bacterium from a primary salt crystal". Nature. ج. 407 ع. 6806: 897–900. Bibcode:2000Natur.407..897V. DOI:10.1038/35038060. PMID:11057666.
- ^ Hebsgaard MB، Phillips MJ، Willerslev E (مايو 2005). "Geologically ancient DNA: fact or artefact?". Trends in Microbiology. ج. 13 ع. 5: 212–20. DOI:10.1016/j.tim.2005.03.010. PMID:15866038.
- ^ Nickle DC، Learn GH، Rain MW، Mullins JI، Mittler JE (يناير 2002). "Curiously modern DNA for a "250 million-year-old" bacterium". Journal of Molecular Evolution. ج. 54 ع. 1: 134–7. Bibcode:2002JMolE..54..134N. DOI:10.1007/s00239-001-0025-x. PMID:11734907.
- ^ Callahan MP، Smith KE، Cleaves HJ، Ruzicka J، Stern JC، Glavin DP، House CH، Dworkin JP (أغسطس 2011). "Carbonaceous meteorites contain a wide range of extraterrestrial nucleobases". Proceedings of the National Academy of Sciences of the United States of America. ج. 108 ع. 34: 13995–8. Bibcode:2011PNAS..10813995C. DOI:10.1073/pnas.1106493108. PMC:3161613. PMID:21836052.
- ^ Steigerwald، John (8 أغسطس 2011). "NASA Researchers: DNA Building Blocks Can Be Made in Space". ناسا. مؤرشف من الأصل في 23 يونيو 2015. اطلع عليه بتاريخ 10 أغسطس 2011.
{{استشهاد ويب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) والوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ ScienceDaily Staff (9 أغسطس 2011). "DNA Building Blocks Can Be Made in Space, NASA Evidence Suggests". ScienceDaily. مؤرشف من الأصل في 5 سبتمبر 2011. اطلع عليه بتاريخ 9 أغسطس 2011.
{{استشهاد ويب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Marlaire، Ruth (3 مارس 2015). "NASA Ames Reproduces the Building Blocks of Life in Laboratory". ناسا. مؤرشف من الأصل في 5 مارس 2015. اطلع عليه بتاريخ 5 مارس 2015.
{{استشهاد ويب}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) والوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Yukihisa Katsumoto, Masako Fukuchi-Mizutani, Yuko Fukui, Filippa Brugliera, Timothy A. Holton, Mirko Karan, Noriko Nakamura, Keiko Yonekura-Sakakibara, Junichi Togami, Alix Pigeaire, Guo-Qing Tao, Narender S. Nehra, Chin-Yi Lu, Barry K. Dyson, Shinzo Tsuda, Toshihiko Ashikari, Takaaki Kusumi, John G. Mason et Yoshikazu Tanaka, « Engineering of the Rose Flavonoid Biosynthetic Pathway Successfully Generated Blue-Hued Flowers Accumulating Delphinidin », في Plant & Cell Physiology, vol. 48, no 11, novembre 2007, ص. 1589-1600 [النص الكامل, lien PMID, lien DOI (pages consultées le 2 avril 2015)]
- ^ "Plant gene replacement results in the world's only blue rose". www.phys.org. 2005. اطلع عليه بتاريخ 2 avril 2015.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Goff SP، Berg P (ديسمبر 1976). "Construction of hybrid viruses containing SV40 and lambda phage DNA segments and their propagation in cultured monkey cells". Cell. ج. 9 ع. 4 PT 2: 695–705. DOI:10.1016/0092-8674(76)90133-1. PMID:189942.
- ^ Houdebine LM (2007). "Transgenic animal models in biomedical research". Methods in Molecular Biology. ج. 360: 163–202. DOI:10.1385/1-59745-165-7:163. ISBN:1-59745-165-7. PMID:17172731.
- ^ Daniell H، Dhingra A (أبريل 2002). "Multigene engineering: dawn of an exciting new era in biotechnology". Current Opinion in Biotechnology. ج. 13 ع. 2: 136–41. DOI:10.1016/S0958-1669(02)00297-5. PMC:3481857. PMID:11950565.
- ^ Job D (نوفمبر 2002). "Plant biotechnology in agriculture". Biochimie. ج. 84 ع. 11: 1105–10. DOI:10.1016/S0300-9084(02)00013-5. PMID:12595138.
- ^ "GM traits list". International Service for the Acquisition of Agri-Biotech Applications.
- ^ "ISAAA Brief 43-2011: Executive Summary". International Service for the Acquisition of Agri-Biotech Applications.
- ^ Connor، Steve (2 نوفمبر 2007). "The mouse that shook the world". The Independent.
- ^ Curtis، Caitlin؛ Hereward، James (29 أغسطس 2017). "From the crime scene to the courtroom: the journey of a DNA sample". The Conversation. مؤرشف من الأصل في 22 أكتوبر 2017. اطلع عليه بتاريخ 22 أكتوبر 2017.
{{استشهاد بخبر}}: الوسيط غير المعروف|dead-url=تم تجاهله (مساعدة) والوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Collins A، Morton NE (يونيو 1994). "Likelihood ratios for DNA identification". Proceedings of the National Academy of Sciences of the United States of America. ج. 91 ع. 13: 6007–11. Bibcode:1994PNAS...91.6007C. DOI:10.1073/pnas.91.13.6007. PMC:44126. PMID:8016106.
- ^ Weir BS، Triggs CM، Starling L، Stowell LI، Walsh KA، Buckleton J (مارس 1997). "Interpreting DNA mixtures". Journal of Forensic Sciences. ج. 42 ع. 2: 213–22. PMID:9068179.
- ^ Jeffreys AJ، Wilson V، Thein SL (1985). "Individual-specific 'fingerprints' of human DNA". Nature. ج. 316 ع. 6023: 76–9. Bibcode:1985Natur.316...76J. DOI:10.1038/316076a0. PMID:2989708.
- ^ Colin Pitchfork — first murder conviction on DNA evidence also clears the prime suspect Forensic Science Service Accessed 23 December 2006 نسخة محفوظة 18 مايو 2016 على موقع واي باك مشين.
- ^ "Paternity Blood Tests That Work Early in a Pregnancy" New York Times June 20, 2012 نسخة محفوظة 24 June 2017 على موقع واي باك مشين.
- ^ Baldi، Pierre؛ Brunak، Soren (2001). Bioinformatics: The Machine Learning Approach. MIT Press. ISBN:978-0-262-02506-5. OCLC:45951728.
{{استشهاد بكتاب}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Gusfield, Dan. Algorithms on Strings, Trees, and Sequences: Computer Science and Computational Biology. مطبعة جامعة كامبريج, 15 January 1997. (ردمك 978-0-521-58519-4).
- ^ Sjölander K (يناير 2004). "Phylogenomic inference of protein molecular function: advances and challenges". Bioinformatics. ج. 20 ع. 2: 170–9. DOI:10.1093/bioinformatics/bth021. PMID:14734307.
- ^ Mount DM (2004). Bioinformatics: Sequence and Genome Analysis (ط. 2nd). Cold Spring Harbor, NY: Cold Spring Harbor Laboratory Press. ISBN:0-87969-712-1. OCLC:55106399.
- ^ Rothemund PW (مارس 2006). "Folding DNA to create nanoscale shapes and patterns". Nature. ج. 440 ع. 7082: 297–302. Bibcode:2006Natur.440..297R. DOI:10.1038/nature04586. PMID:16541064.
- ^ Andersen ES، Dong M، Nielsen MM، Jahn K، Subramani R، Mamdouh W، Golas MM، Sander B، Stark H، Oliveira CL، Pedersen JS، Birkedal V، Besenbacher F، Gothelf KV، Kjems J (مايو 2009). "Self-assembly of a nanoscale DNA box with a controllable lid". Nature. ج. 459 ع. 7243: 73–6. Bibcode:2009Natur.459...73A. DOI:10.1038/nature07971. PMID:19424153.
- ^ Ishitsuka Y، Ha T (مايو 2009). "DNA nanotechnology: a nanomachine goes live". Nature Nanotechnology. ج. 4 ع. 5: 281–2. Bibcode:2009NatNa...4..281I. DOI:10.1038/nnano.2009.101. PMID:19421208.
- ^ Aldaye FA، Palmer AL، Sleiman HF (سبتمبر 2008). "Assembling materials with DNA as the guide". Science. ج. 321 ع. 5897: 1795–9. Bibcode:2008Sci...321.1795A. DOI:10.1126/science.1154533. PMID:18818351.
- ^ "Programming DNA circuits". Microsoft Research. 2015. اطلع عليه بتاريخ 28 mars 2015.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Yaniv Amir, Eldad Ben-Ishay, Daniel Levner, Shmulik Ittah, Almogit Abu-Horowitz et Ido Bachelet, « Universal computing by DNA origami robots in a living animal », في Nature Nanotechnology, vol. 9, no 5, mai 2014, ص. 353-357 [النص الكامل, lien PMID, lien DOI (pages consultées le 28 mars 2015)]
- ^ Lulu Qian, Erik Winfree et Jehoshua Bruck, « Neural network computation with DNA strand displacement cascades », في Nature, vol. 475, no 7356, 21 juillet 2011, ص. 368-372 [النص الكامل, lien PMID, lien DOI (pages consultées le 28 mars 2015)]
- ^ Wray GA (2002). "Dating branches on the tree of life using DNA". Genome Biology. ج. 3 ع. 1: REVIEWS0001. DOI:10.1046/j.1525-142X.1999.99010.x. PMC:150454. PMID:11806830.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|nopp=تم تجاهله يقترح استخدام|no-pp=(مساعدة) - ^ Mannis van Oven et Manfred Kayser, « Updated comprehensive phylogenetic tree of global human mitochondrial DNA variation », في Human Mutation, vol. 30, no 2, février 2009, ص. E386-E394 [النص الكامل, lien PMID, lien DOI (pages consultées le 27 mars 2015)]
- ^ (بالإنجليزية) Francesca D. Ciccarelli, Tobias Doerks, Christian von Mering, Christopher J. Creevey, Berend Snel et Peer Bork, « Toward automatic reconstruction of a highly resolved tree of life », في Science, vol. 311, no 5765, 2006, ص. 1283–1287 [النص الكامل, lien PMID, lien DOI]
- ^ "Human mtDNA Migrations" (PDF). MITOMAP, A human mitochondrial genome database. 2002. اطلع عليه بتاريخ 27 mars 2015.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) وروابط خارجية في|موقع=
| في كومنز صور وملفات عن: حمض نووي ريبوزي منقوص الأكسجين |

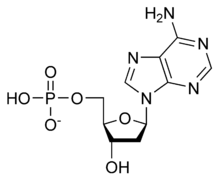

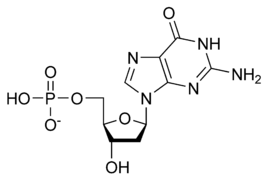



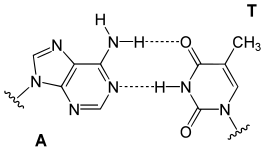


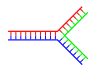

![شجرة تطور السلالات توضح نطاقات الأحياء الثلاثة: حقيقيات النوى بالأحمر، العتائق بالأخضر والبكتيريا بالأزرق.[194]](http://upload.wikimedia.org/wikipedia/commons/thumb/4/4e/%D8%B4%D8%AC%D8%B1%D8%A9_%D8%A7%D9%84%D8%AD%D9%8A%D8%A7%D8%A9_%D9%85%D8%A8%D8%B3%D8%B7%D8%A9.svg/438px-%D8%B4%D8%AC%D8%B1%D8%A9_%D8%A7%D9%84%D8%AD%D9%8A%D8%A7%D8%A9_%D9%85%D8%A8%D8%B3%D8%B7%D8%A9.svg.png)
![خريطة الهجرة البشرية المستنتجة من دراسات علم الوراثة العرقي لدنا المتقدرة البشري، المقياس 1000 سنة قبل الحاضر.[195]](http://upload.wikimedia.org/wikipedia/commons/thumb/a/ab/World_map_of_prehistoric_human_migrations.jpg/462px-World_map_of_prehistoric_human_migrations.jpg)