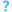أسطوانية كنتونية
أسطوانية كنتونية | |
|---|---|
| المرتبة التصنيفية | نوع |
| التصنيف العلمي | |
| المملكة: | حيوان |
| الشعبة: | ديدان اسطوانية |
| الطائفة: | سيسيرنينتيات |
| الرتبة: | الاسطونيات |
| الفصيلة: | Metastrongylidae |
| الجنس: | الأسطوانية |
| النوع: | الأسطوانية الكنتونية |
| الاسم العلمي | |
| Angiostrongylus cantonensis | |
| تعديل مصدري - تعديل | |
الأسطوانية الكنتونية (الاسم العلمي: Angiostrongylus cantonensis) دودة أسطوانية اكتشفت سنة 1964 وهي المسبب لداء الأسطوانيات والسبب الأكثر شيوعا للالتهابُ السَّحايا اليُوزِيْنِيّ في جنوب شرق آسيا وحوض المحيط الهادئ.[1] هذه الديدان الاسطوانية تتواجد عادة في الأوعية الدموية للرئة عند الفئران ما أعطاها لقب دودة رئة الفئران. القواقع هي المضيف الابتدائي والإعدادي حيث تنمو اليرقات حتى تصبح معدية. يعتبر الإنسان مستضيف عرضي يمكن أن يصاب من خلال ابتلاع اليرقات في قواقع نيئة أو غير مطبوخة جيداً أو ناقلات أخرى كالمياه الملوثة والخضروات. ثم تنتقل اليرقات عبر الدم إلى الجهاز العصبي المركزي حيث هي السبب الأكثر شيوعا لالتهاب السحايا اليوزِيني وهو حالة خطيرة يمكن أن تؤدي إلى الموت أو تلف دائم في الدماغ والأعصاب.[2]
العلاج[عدل]
تعتمد الشدة والفترة السريرية بشكل كبير على ما كمية اليرقات ذات المرحلة الثالثة[3]؛ مما يخلق اختلافا كبيراً من حالة لأخرى، جاعلاً التجارب السريرية صعبة التحديد وفعالية الدواء صعبة التبيٌن، وتوفر الإدارة الطبية النموذجية من المهدئات و المسكنات الحد الأدنى من الراحة من الصداع والإرهاق الشديد.
ويعد تقليل الضغط داخل القحف على فترات منتظمة من ثلاثة إلى سبعة أيام الطريقة الوحيدة المؤكدة لتقليل الضغط داخل الجمجمة بشكل كبير ويمكن استخدامها لعلاج أعراض مثل الصداع[4] وقد تتكرر هذه العملية حتى يظهر التحسن.[5] وهناك أدلة متزايدة ذات جودة متوسطة تشير إلى أن العلاج ب الكورتيكوستيرويد باستخدام بريدنيزولون[6] أو ديكساميثازون[4] له تأثير مفيد في علاج أعراض الجهاز العصبي المركزي المرتبطة بالتهابات الكانتونينيس.[7][8] وعلى الرغم من أن الأبحاث المبكرة لم تظهر أي علاج بالعوامل الطاردة للديدان (مثل الأدوية القاتلة للطفيليات) مثل تيابيندازول أو البيندازول الفعال في تحسين المسار السريري للمرض [9] [10]؛ أظهرت عدد من الدراسات الحديثة من تايلاند والصين أن الجمع بين الهرمون قشري سكري وطاردات الديدان آمن ويقلل من مدة الصداع وعدد المرضى الذين يعانون من صداع كبير.[4][6][11][7] وعلى الرغم من أن إضافة عوامل مضادة للالتهاب الرئوي لإدارة عدوى الكانتونينيس ينطوي على خطر نظري يتمثل في حدوث أزمة عصبية من خلال إطلاق كمية هائلة من المستضدات خلال الوفاة المتزامنة لليرقات [4]، لم تظهر أي دراسة أن هذا موجود في البيئة السريرية.[6][4][7][7] بالإضافة إلى ذلك فإن الفشل في قتل الطفيليات قبل أن تحاول الهجرة خارج الجهاز العصبي المركزي يزيد من خطر التلف الميكانيكي عن طريق ترحيل اليرقات. على الرغم من أن العلاج المركب باستخدام ألبيندازول وبريدنيزولون ليس له أي ميزة كبيرة مقارنة بالمعالجة باستخدام بريدنيزولون بمفرده في الحالات الخفيفة [12]؛ فإن العلاج بطاردات الديدان آمن بشكل واضح وقد يكون له فائدة كبيرة للمرضى الذين يعانون من حمولات طفيلية عالية ومعرضين لخطر الإصابة بالإعاقة الدائمة أو الوفاة.[13]
التشخيص[عدل]
غالبا ما يكون تشخيص المرض الناجم عن إصابة أ.كانتونينس صعبًا ويعتمد اعتمادًا كبيرًا على تاريخ الابتلاع المحتمل لعائل مصاب عادةً ووجود سمات نموذجية للمرض. التشخيص المفترض يكون قويا خاصة عندما يمكن تأكيد التهاب السحايا والدماغ. يمكن التوصل إلى تشخيص التهاب السحايا اليوزيني من خلال التحقق من ارتفاع الضغط في الجمجمة وزيادة أعداد بروتين الخلايا الأساسي الحمضي. تشخيص سبب التهاب السحايا ووجود أ. كانتونيسيس يكون أكثر صعوبة بشكل ملحوظ ويجب أخذ عينة بزل قطني وعينة من السائل الدماغي الشوكي CSF لأكثر من نصف الأفراد المصابين للبحث عن ديدان أو يرقات أ كانتونينس، ويكون أ كانتونيسيس غير قابل للكشف عنه بالسائل الدماغي الشوكي في أكثر من نصف الأفراد المصابين.
ولا يمكن الاعتماد على الوسائل الحالية للتحقق من مستضدات معينة متعلقة ب أ كانتونيسيس، وبالتالي يتم اكتشاف طرق جديدة للكشف عن تفاعلات الأجسام المضادة الخاصة بالمستضد مثل اختبار تفاعل البوليمريز المتسلسل المناعي[14] كما يكون اختبار تقنية الإليزا متوفرا على وجه السرعة.[15]
المراجع[عدل]
- ^ Baheti NN & Sreedharan M et al. (2008). "Eosinophilic meningitis and an ocular worm in a patient from Kerala, south India" J. Neurol. Neurosurg. Psychiatry 79 (271).
- ^ Hua Li, Feng Xu, Jin-Bao Gu and Xiao-Guang Chen (2008). "Case Report: A Severe Eosinophilic Meningoencephalitis Caused by Infection of Angiostrongylus cantonensis". Am. J. Trop. Med. Hyg., 79(4): 568–570.
- ^ Ma، Mingsheng؛ Zhang، Mengqi؛ Qiu، Zhengqing (2018-06). "Eosinophilic meningitis caused by Angiostrongylus cantonensis in an infant". Medicine. ج. 97 ع. 24: e10975. DOI:10.1097/md.0000000000010975. ISSN:0025-7974. مؤرشف من الأصل في 2019-12-08.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ أ ب ت ث ج Sawanyawisuth، Kittisak؛ Sawanyawisuth، Kanlayanee (1 أكتوبر 2010). "Drug Target in Eosinophilic Meningitis Caused by Angiostrongylus cantonensis". Infectious Disorders - Drug Targets. ج. 10 ع. 5: 322–328. DOI:10.2174/187152610793180867. ISSN:1871-5265. مؤرشف من الأصل في 2019-12-08.
- ^ "ESCARGOTS AND EOSINOPHILIC MENINGITIS". The Lancet. ج. 332 ع. 8606: 320. 1988-08. DOI:10.1016/s0140-6736(88)92366-5. ISSN:0140-6736. مؤرشف من الأصل في 2019-12-08.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ أ ب ت CHOTMONGKOL، VERAJIT؛ SAWADPANITCH، KOOKWAN؛ LOUHAWILAI، SITICHOKE؛ SAWANYAWISUTH، KITTISAK؛ LIMPAWATTANA، PANITA (1 يونيو 2006). "TREATMENT OF EOSINOPHILIC MENINGITIS WITH A COMBINATION OF PREDNISOLONE AND MEBENDAZOLE". The American Journal of Tropical Medicine and Hygiene. ج. 74 ع. 6: 1122–1124. DOI:10.4269/ajtmh.2006.74.1122. ISSN:0002-9637. مؤرشف من الأصل في 2019-12-08.
- ^ أ ب ت ث Chotmongkol، Verajit؛ Sawanyawisuth، Kittisak؛ Thavornpitak، Yupa (1 سبتمبر 2000). "Corticosteroid Treatment of Eosinophilic Meningitis". Clinical Infectious Diseases. ج. 31 ع. 3: 660–662. DOI:10.1086/314036. ISSN:1537-6591. مؤرشف من الأصل في 2020-05-11.
- ^ Goldman-Cecil medicine. ISBN:9781455750177. OCLC:899727756. مؤرشف من الأصل في 2019-12-08.
- ^ Kliks، Michael M.؛ Hardman، John M.؛ Kroenke، Kurt (1 نوفمبر 1982). "Eosinophilic Radiculomyeloencephalitis: An Angiostrongyliasis Outbreak in American Samoa Related to Ingestion of Achatina fulica Snails". The American Journal of Tropical Medicine and Hygiene. ج. 31 ع. 6: 1114–1122. DOI:10.4269/ajtmh.1982.31.1114. ISSN:0002-9637. مؤرشف من الأصل في 2019-12-08.
- ^ Yii، Chin-Yun (1 مارس 1976). "Clinical Observations on Eosinophilic Meningitis and Meningoencephalitis caused by Angiostrongylus Cantonensis on Taiwan". The American Journal of Tropical Medicine and Hygiene. ج. 25 ع. 2: 233–249. DOI:10.4269/ajtmh.1976.25.233. ISSN:0002-9637. مؤرشف من الأصل في 2019-12-08.
- ^ Tu، Wu-Chun؛ Lai، Shih-Chan (2006-05). "Angiostrongylus cantonensis: Efficacy of albendazole–dexamethasone co-therapy against infection-induced plasminogen activators and eosinophilic meningitis". Experimental Parasitology. ج. 113 ع. 1: 8–15. DOI:10.1016/j.exppara.2005.11.017. ISSN:0014-4894. مؤرشف من الأصل في 2019-12-08.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ Day، Jeremy (17 ديسمبر 2009). "Faculty of 1000 evaluation for Comparison of prednisolone plus albendazole with prednisolone alone for treatment of patients with eosinophilic meningitis". F1000 - Post-publication peer review of the biomedical literature. مؤرشف من الأصل في 2019-12-08. اطلع عليه بتاريخ 2019-11-09.
- ^ Eamsobhana، Praphathip؛ Prasartvit، Anchana؛ Yong، Hoi-Sen؛ Tungtrongchitr، Anchalee؛ Wanachiwanawin، Darawan (2019). "Evaluation of a user-friendly test device (AcQuickDx) for detection of specific antibodies to human angiostrongyliasis". SDRP Journal of Food Science & Technology. ج. 4 ع. 4: 748–752. DOI:10.25177/jfst.4.4.ra.520. ISSN:2472-6419. مؤرشف من الأصل في 2019-12-08.
- ^ Chye، S.-M. (1 يناير 2004). "Immuno-PCR for Detection of Antigen to Angiostrongylus cantonensis Circulating Fifth-Stage Worms". Clinical Chemistry. ج. 50 ع. 1: 51–57. DOI:10.1373/clinchem.2003.020867. ISSN:0009-9147. مؤرشف من الأصل في 2019-12-08.
- ^ Eamsobhana، Praphathip؛ Yong، Hoi Sen (2009-07). "Immunological diagnosis of human angiostrongyliasis due to Angiostrongylus cantonensis (Nematoda: Angiostrongylidae)". International Journal of Infectious Diseases. ج. 13 ع. 4: 425–431. DOI:10.1016/j.ijid.2008.09.021. ISSN:1201-9712. مؤرشف من الأصل في 2019-12-08.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة)
| Angiostrongylus cantonensis في المشاريع الشقيقة: | |
| |