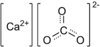كربونات الكالسيوم
| كربونات الكالسيوم | |
|---|---|
 |
|
| الاسم النظامي (IUPAC) | |
Calcium carbonate |
|
| أسماء أخرى | |
الكلس ، الطبشور ، الكالسيت ، رخام ، حجر جيري ، اراگونيت ، الكالسيت ، الطباشير |
|
| المعرفات | |
| رقم CAS | 471-34-1 |
| بوب كيم (PubChem) | 10112 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | CaCO3 |
| الكتلة المولية | 100.0869 غ/مول |
| المظهر | مسحوق أبيض ناعم |
| الكثافة | 2.711 غ/سم3 كالسيت 2.83 غ/سم3 أراغونيت |
| نقطة الانصهار | 1339 °س كالسيت 825 °س أراغونيت |
| نقطة الغليان | يتفكك |
| الذوبانية في الماء | ضعيف الانحلال في الماء |
| حموضة (pKa) | 9 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
كربونات كالسيوم مركب كيميائي له الصيغة CaCO3، ويكون على شكل مسحوق أبيض.
الخواص
[عدل]- توجد أشكال مختلفة من أشكال البنية البلورية لمركب كربونات الكالسيوم. يوجد بشكل مكعب في معدن الكالسيت وبنظام معيني قائم في كل من معدني الأراغونيت والفاتيريت.
- يعد مركب كربونات الكالسيوم عملياً غير منحل في الماء (فقط 1.4 مغ لكل 100 مل من الماء). ولكن في حال احتواء الماء على غاز ثنائي أكسيد الكربون فإن انحلالية كربونات الكالسيوم في الماء تزداد وذلك نتيجة لتشكل البيكربونات.
- يتفكك مركب كربونات الكالسيوم بشكل سريع نتيجة أثر الأحماض عليه، حيث يحرر غاز ثنائي أكسيد الكربون.
التحضير
[عدل]يحضر صناعياً بإشباع محلول رائق الكلس هيدروكسيد الكالسيوم بغاز ثنائي أكسيد الكربون حسب المعادلة:
- Ca(OH)2 + CO2 → CaCO3 + H2O
تحضر من تسخين بيكربونات الكالسيوم سواء الصلبة أو السائلة حسب المعادلة التالية:
- Ca(HCO3)2 → CaCO3 + CO2 + H2O
الاستخدامات
[عدل]
- يستعمل بشكل واسع في تحضير الاسمنت.
- يستخدم لجعل بعض أنواع المربى كاليقطين والباذنجان تكتسب قساوه وذلك بنقعها قبل الغلي.
- يستخدم للتخلص من آثار الأمطار الحمضية في البحيرات
- كان يستخدم في السابق في الكتابة على اللوح (السبورة) إلى أن ظهرت اقلام الحبر والسبورة البيضاء
'الاستخدام الصيدلاني:' ممدد في المضغوطات والمحافظ وعامل علاجي.
تُوظف كربونات الكالسيوم كسواغ صيدلاني حيث يُستخدم غالباً في الأشكال الصلبة كممدد كما أنه يستخدم كأساس في المستحضرات السنية المشبعة بالدواء و يستخدم كذلك كوقاء وكعامل مساعد على الانحلال في المضغوطات القابلة للتفتت وكعامل رافع للحجم في عمليات التلبيس (التغطية) بالسكر. علاجياً كمضاد للحموضة ومتتم لكالسيوم الجسم. يستخدم كمادة ممددة في الطلائات الدهنية والمائية.
التأثير على صحة الجسم
[عدل]تُستخدم غالباً في الأشكال الفموية وتُعد عموماً مادة غير سامة.و مع ذلك فإن وصفها فموياً قد يسبب الإمساك وتناول كميات كبيرة (4-60غ يومياً)قد يقود إلى فرط كالسيوم الدم أو إلى تلف الكلية. و علاجياً تُوصف جرعات فموية بحدود 1غ كمضاد للحموضة.
LD50 (rat,oral) = 6.45 g/kg [3]
المصادر
[عدل]- ^ ا ب ج CALCIUM CARBONATE (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Handbook of Pharmaceutical Excipients SIXTH EDITION Edited by Raymond C Rowe BPharm, PhD, DSC, FRPharmS, FRSC, CPhys, MInstP Chief Scientist Intelligensys Ltd, Stokesley, North Yorkshire, UK Paul J Sheskey BSc, RPh Application Development Leader The Dow Chemical Company, Midland, MI, USA Marian E Quinn BSc, MSc Development Editor Royal Pharmaceutical Society of Great Britain, London, UK
Taschenbuch chemische Substanzen, Willmes, Verlag Harri Deutsch, ISBN 3-8171-1662-4