ورم الخلايا البدائية العصبية
| ورم الخلايا البدائية العصبية | |
|---|---|
رؤية مجهرية لوجود ورم الخلايا البدائية العصبية النموذجية مع تشكيل الوريدة
| |
| معلومات عامة | |
| الاختصاص | علم الأورام |
| من أنواع | مرض، وسرطان الأطفال |
| الإدارة | |
| أدوية | |
| تعديل مصدري - تعديل | |
ورمٌ أروميٌّ عصبي [2] أو ورم الخلايا البدائية العصبية (بالإنجليزية: neuroblastoma) هو الورم الصلب الأكثر شيوعا خارج القحف في مرحلة الطفولة وأكثر أنواع السرطان شيوعا في مرحلة الرضاعة، مع معدل حدوث سنوي يبلغ نحو 650 حالة جديدة سنويا في الولايات المتحدة.[3] ما يقرب من 50 في المئة من حالات ورم الخلايا البدائية العصبية تصيب الأطفال الذين تقل أعمارهم عن سنتين.[4] وهو ورم الغدد الصم العصبية، والذي ينشأ من أي عنصر من العرف العصبي في الجهاز العصبي الودي أو SNS. أنه ينشأ بشكل متكرر في إحدى الغدد الكظرية، ولكن يمكن أيضا أن يتطور في الأنسجة العصبية في الرقبة والصدر والبطن، أو الحوض.
ورم الخلايا البدائية العصبية هو أحد الأورام الخبيثة البشرية القليلة المعروفة لإظهار الانحدار التلقائي من حالة غير متمايزة إلى المظهر الخليوي الحميد كليا.[5] وهو مرض يظهر التباين الشديد، ومصنف ضمن فئات خطرة ثلاثة: منخفضة، متوسطة، وشديدة الخطورة. المرض منخفض الخطورة هو الأكثر شيوعا عند الرضع ومن الشائع ان تؤدي المراقبة فقط أو الجراحة إلى نتائج جيدة في علاجه، في حين أن المرض شديد الخطورة يصعب علاجه بنجاح حتى مع العلاجات المتعددة الوسائط المتوفرة والمكثفة.[6]
أما الورم الأرومي العصبي الحسي، والمعروف أيضا باسم ورم الخلايا البدائية العصبية الشمية، فيعتقد انه ينشأ من الظهارة الشمية وتصنيفه لا يزال عرضة للجدل. ومع ذلك، لأنه ليس خباثة في الجهاز العصبي الودي، فهو عبارة عن كيان مستقل سريريا ولا ينبغي الخلط بينه وبين ورم الخلايا البدائية العصبية.[7][8]
العلامات والأعراض
[عدل]الأعراض الأولى لورم الخلايا البدائية العصبية غالبا ما تكون ملتبسة مما يجعل التشخيص صعبا. الاعراض الشائعة هي الإعياء، وفقدان الشهية، والحمى، وآلام المفاصل. تعتمد الأعراض على أماكن الورم الرئيسي والنقيلة إذا كانت موجودة:[9]
- في البطن، قد يسبب الورم انتفاخا في البطن والإمساك.
- قد يسبب الورم في الصدر ضيق في النفس.
- قد يضغط الورم على النخاع الشوكي مسببا ضعفا، وبالتالي عدم القدرة على الوقوف، أو الزحف أو المشي.
- تسبب آفات العظام في الساقين والفخذين ألما وعرجا.
- يسبب الورم في العظام حول العينين أو المحاجر كدمات متميزة وانتفاخا.
- تسرب نخاع العظم يسبب شحوب الوجه بسبب فقر الدم.
غالبا ما ينتشر ورم الخلايا البدائية العصبية إلى أجزاء أخرى من الجسم قبل ظهور أي أعراض واضحة، و 50 إلى 60 ٪ من جميع حالات ورم الخلايا البدائية العصبية تظهر مع النقائل.[10]
المكان الأكثر شيوعا لنشوء ورم الخلايا البدائية العصبية (أي الورم الرئيسي) هو على الغدد الكظرية. هذا يحدث في 40 ٪ من الأورام الموضعية وفي 60 ٪ من حالات المرض واسعة الانتشار. ويمكن أيضا ان يتطور ورم الخلايا البدائية العصبية في أي مكان على امتداد سلسلة النظام العصبي الودي من الرقبة إلى الحوض. يتكرر انتشار المرض في أماكن مختلفة تشمل: الرقبة (1 ٪) اوالصدر (19 ٪) اوالبطن (30 ٪ في غير الغدة الكظرية)، أو الحوض (1 ٪). وفي حالات نادرة، لا يمكن تمييز الورم الرئيسي.[11]
من النادر ان تشمل المظاهر المميزة اعتلال النخاع العرضي (ورم النخاع الشوكي المنضغط في 5 ٪ من الحالات)، والإسهال المقاوم للعلاج (ورم إفراز الببتيد المعوي الفعال في الأوعية في 4 ٪ من الحالات)، ومتلازمة هورنر (ورم الرحم في 2.4 ٪ من الحالات)، ومتلازمة ترجرج العيون والاختلاج العضلي[12]، والترنح (يشتبه بتسبب متلازمة الأباعد الورمية في 1.3 ٪ من الحالات)، وفرط ضغط الدم (إفراز الكاتيكولامينات أو انضغاط الشريان الكلوي في1.3 ٪ من الحالات).[13]
الأسباب
[عدل]مسببات ورم الخلايا البدائية العصبية ليست مفهومة جيدا. مع ذلك تم ترشيح الإصابة ببعض الحالات بالعائلات، وجرى ربطها بعلم المورثات. وتتسبب طفرة خط الخلايا العروسية النادرة جدا في مورثة سرطان الغدد الليمفاوية المؤنزمة المتحولة (ALK) بورم الخلايا البدائية العصبية العائلية.[14]
تم العثور على مورثة LMO1 لتكون مساهمة في زيادة مخاطر تطوير الشكل الهجومي من السرطان.[15]
وقد تم ربط ورم الخلايا البدائية العصبية بمشاكل في مورثة NBPF10 فيما يتعلق بنسخ عدد المتغيرات التي تتسبب في متلازمة الحذف 1q21.1 ومتلازمة الازدواجية 1q21.1.[16]
لقد تم اقتراح العديد من عوامل الخطر لتكون موضوع البحوث الجارية. وبسبب خصائص الظهور المبكر للمرض فقد ركزت العديد من الدراسات على العوامل الأبوية حول التخصيب وأثناء فترة الحمل. وقد شمل التحقيق بالعوامل مهن الابوين (أي التعرض للمواد الكيميائية في صناعات محددة)، والتدخين وشرب الخمور، واستخدام العقاقير الطبية أثناء الحمل وعوامل الولادة، غير أن النتائج لم تأت بنتائج حاسمة.[17]
وقد فحصت الدراسات الأخرى الصلات المحتملة مع الحالة الاستشرائية والتعرض للعدوى في وقت مبكر من الحياة،[18] واستخدام الهرمونات وأدوية الخصوبة،[19] واستخدام الأمهات لصبغة الشعر.[20][21]
التشخيص
[عدل]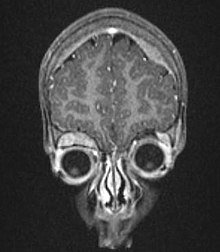
عادة ما يتم تأكيد التشخيص من قبل الطبيب الشرعي الجراحي، مع الأخذ بعين الاعتبار السمات السريرية، والنتائج المجهرية، والفحوص المخبرية الأخرى.
الكيمياء الحيوية
[عدل]في حوالي 90 ٪ من حالات ورم الخلايا البدائية العصبية، تتواجد مستويات مرتفعة من الكاتيكولامينات أو نواتج استقلابها في البول أو الدم. الكاتيكولامينات ونواتج استقلابها تشمل الدوبامين، وحمض هوموفانيلك (HVA)، و/ أو حمض الفانيليل مندليك (VMA).[22]
التصوير
[عدل]طريقة أخرى للكشف عن ورم الخلايا البدائية العصبية هو مسح mIBG (ميتا-ايدو بينزل غونديداين)، والذي يتولى نسبة 90 إلى 95 ٪ من جميع اورام الخلايا البدائية العصبية ويسمى غالبا «mIBG - الحاد».[23] آلية mIBG هي تناول الخلايا العصبية الودية ويعتبر أداء تماثلي بافراز الناقل العصبي نورإبينفرين. عندما يكون الإشعاع المتأين مع 131 - I أو I - 123 (نظائر اليود المشعة)، هو دواء مشع جيد جدا لتشخيص المرض ورصد الاستجابة للعلاج لهذا المرض. مع عمر نصف 13 ساعة، فان I – 123 هو النظير المفضل لحساسية التصوير والجودة. أما I - 131 فلديه عمر نصف 8 أيام وعلى جرعات أكبر يعتبر علاج فعال كإشعاع موجهة ضد الانتكاس وورم الخلايا البدائية العصبية المقاومة للعلاج.[24]
علم الأنسجة
[عدل]
على الفحص المجهري، توصف الخلايا السرطانية عادة بأنها صغيرة ومستديرة وزرقاء، ويمكن مشاهدة نماذج الوريدة (نموذج هومر رايت للوريدات الزائفة). الوريدات الزائفة هومر رايت، هي خلايا الورم حول القرص العصبي، ولا ينبغي الخلط بينها وبين الوريدات الحقيقية (فليكسنر – وينتر ستينر), هذه الوريدات[25] هي خلايا الورم حول الأوعية الدموية وغالبا ما تشاهد في اورام أرومة الشبكية.[26] وهي أيضا متميزة عن الوريدات الزائفة من الورم البطاني العصبي والتي تتكون من خلايا الورم مع البروتين الدبقي الليفي الحمضي (GFAP)--العمليات الايجابية تهوي باتجاه الاوعية الدموية (وبالتالي مزيج من الاثنين معا).[27] وتستخدم مجموعة متنوعة من الصبغات الكيميائية النسيجية المناعية من قبل خبراء الأمراض لتمييز ورم الخلايا البدائية العصبية من المحاكاة النسيجية، مثل الساركومة العضلية المخططة وسرطان الغدد الليمفاوية وساركومة يوينغ وورم ويلمز. في شباط 2007، أعلنت تقنيات ألثيا تطوير القدرة على التشخيص الجزيئي للتمييز بوضوح بين أنواع مختلفة من سرطانات الطفولة، ووضعت بالتعاون مع المعهد القومي الأميركي للسرطان (NCI).[28]
ورم الخلايا البدائية العصبية هو أحد أورام الأعصاب العالية الطرفية (pNTs) التي لديها جذور مماثلة، وتكشف عن نمط واسع من التمايز تتراوح بين الورم العصبي العقدي الحميد إلى الورم الأرومي العصبي العقدي السدوي الغني مع خلايا الأعصاب العالية المختلطة أو في العقيدات، إلى ورم الخلايا البدائية العصبية الخبيث جدا. هذا التمييز في علم أمراض الأورام السابق للمعالجة هو عامل تشخيصي مهم بالإضافة إلى التقدم في السن ومؤشر تمزق النواة بالانقسام الفتيلي (MKI). هذا النظام لتصنيف علم الأمراض يصف الأورام «الملائمة» و«غير الملائمة» بواسطة اللجنة الدولية لعلم أمراض اورام الخلايا البدائية العصبية (INPC، وتسمى أيضا نظام شيمادا) الذي أنشئ في عام 1999 والمنقح في عام 2003.[29]
التدريج
[عدل]«النظام الدولي لتدريج ورم الخلايا البدائية العصبية» (INSS) الذي أنشئ في عام 1986 ونقح في عام 1988 يعمل على تصنيف ورم الخلايا البدائية العصبية وفقا لوجوده التشريحي عند التشخيص:[30][31][32]
- المرحلة 1: الأورام الموضعية تنحصر في منطقة المنشأ.
- المرحلة 2A: ورم في جانب واحد مع استئصال إجمالي غير مكتمل؛ التعريف المماثل والعقدة الليمفاوية المقابلة غير مصابة بالورم.
- المرحلة 2B: ورم في جانب واحد مع استئصال إجمالي مكتمل أو غير مكتمل، مع العقدة الليمفاوية المماثلة مصابة بالورم؛ وتعريف العقدة الليمفاوية المقابلة بأنها غير مصابة بالورم.
- المرحلة 3: الأورام تتسلل عبر خط الوسط مع أو بدون اصابة العقدة الليمفاوية المحلية، أو الأورام في جانب واحد مع اصابة العقدة الليمفاوية المقابلة، أو الورم في خط الوسط اصابة تورط العقد الليمفاوية في الجانبين.
- المرحلة 4: انتشار الأورام إلى العقد الليمفاوية البعيدة، ونخاع العظام، والعظام والكبد، أو ال أجهزة الأخرى باستثناء ما حدد في المرحلة 4S.
- المرحلة 4S: العمر أقل من عام واحد مع الإصابة بالورم الرئيسي الموضعي على النحو المحدد في المرحلة 1 أو 2، ومع انتشاريتقتصر على نخاع الكبد والجلد والعظام أو (أقل من 10 في المئة من أنوية خلايا نخاع العظم هي أورام).
على الرغم من استخدام اتفاقية دولية للتدريج (INSS)، الا انه تم الاعتراف بالحاجة إلى إجماع دولي في الآراء بشأن تقييم الخطر من أجل مقارنة أفواج مماثلة في نتائج الدراسات. ابتداء من عام 2005، التقى ممثلو المجموعات الرئيسية التعاونية لعلم الأورام عند الأطفال لمراجعة بيانات المرضى ل 8800 حالة من ورم الخلايا البدائية العصبية التي تمت معالجتها في أوروبا واليابان والولايات المتحدة وكندا وأستراليا بين عامي 1990 و 2002. وقد اقترحت فرقة العمل نظام تصنيف المجموعة الدولية لمخاطر ورم الخلايا البدائية العصبية (INRG). وكشفت الدراسات بأثر رجعي بأن معدل البقاء على قيد الحياة عالية في المجموعة التي اعمارهم تتراوح من 12-18 شهرا، والمصنفة سابقا كحالة عالية الخطورة، مما دفع بقرار إعادة تصنيف الأطفال الذين اعمارهم تتراوح من 12-18 شهرا من دون تضخيم N - myc (كما يشار إليها عادة بوصفها MYCN) إلى فئة الخطر المتوسط.[33]
إن التقييم الجديد للخطر INRG سيصنف ورم الخلايا البدائية العصبية عند التشخيص استنادا إلى نظام التدريج الجديد للمجموعة الدولية لمخاطر ورم الخلايا البدائية العصبية (INRGSS):
- المرحلة L1: المرض الموضعي من دون صورة محددة لعوامل الخطر.
- المرحلة L2: المرض الموضعي مع صورة محددة لعوامل الخطر.
- المرحلة M: المرض النقيلي.
- المرحلة MS: المرض النقيلي «خاصة» MS حيث المرحلة تعادل المرحلة 4S.
وسوف يستند تقسيم الخطر الجديد على نظام التدريج INRGSS الجديد، والعمر (ينقسم إلى قسمين في 18 شهرا)، ودرجة الورم، وتضخيم N-myc، وانحراف 11Q غير المتوازن، والصيغة الصبغية حيث ينقسم الخطر إلى أربع مجموعات خطر قبل العلاج: منخفضة جدا، منخفضة، متوسطة، وشديدة الخطورة.[34][35]
الفحص
[عدل]مستوى الكاتيكولامينات بالبول يمكن أن يكون مرتفعا في مرحلة ورم الخلايا البدائية العصبية ما قبل السريرية. وقد اجري الفحص للأطفال الرضع من دون أعراض في عمر ثلاثة أسابيع، وستة أشهر، وعام واحد في اليابان وكندا والنمسا وألمانيا منذ ثمانينات القرن الماضي.[36][37] بدأت اليابان بفحص الأطفال بعمر ستة أشهر من أجل ورم الخلايا البدائية العصبية عبر تحليل مستويات حمض هوموفانيلك وحمض فانيلمانديلك في عام 1984. أوقف الفحص في عام 2004 بعد الدراسات التي أجريت في كندا وألمانيا والتي لم تظهر أي انخفاض في عدد الوفيات الناجمة عن ورم الخلايا البدائية العصبية، وإنما تسببت بدلا عن ذلك بزيادة التشخيصات التي اختفت من دون علاج، وإخضاع هؤلاء الأطفال إلى جراحة وعلاج كيميائي لا لزوم لهما.[38][39][40]
العلاج
[عدل]عندما تكون الافة موضعية، فانها تشفى بشكل عام. ومع ذلك، فإن احتمال البقاء لفترة أطول ضعيف بالنسبة للأطفال المصابين بمرحلة متقدمة من المرض والأكبر سنا من 18 شهرا على الرغم من العلاج الهجومي متعدد الوسائط (العلاج الكيميائي المكثف والجراحة والعلاج الإشعاعي وزرع الخلايا الجذعية، وتمايز العامل يسوتريتينوين والمسمى أيضا حمض 13 - رتينويك، وتكرار العلاج المناعي[41] مع العلاج المضاد ل GD2 الأجسام المضادة وحيدة النسيلة).
وقد تم تحديد الخصائص البيولوجية والوراثية التي عندما تضاف إلى التدريج السريري التقليدي تسمح بتقيم المريض إلى مجموعات الخطر لتخطيط كثافة العلاج.[42] تلك المعايير تشمل عمر المريض ومدى انتشار المرض، والظهور المجهري، والسمات الوراثية بما فيها الصيغة الصبغية للDNA وتضخيم الجين الورمي N - myc (N - myc ينظم الرنا الميكروية[43])، هذه الخصائص تصنف الأمراض إلى امراض منخفضة الخطر ومتوسطة وشديدة. دراسة بيولوجية اجريت مؤخرا (COG ANBL00B1) قامت بتحليل 2687 مريضا مصابا بورم الخلايا البدائية العصبية وتم تحديد نطاق تقييم الخطر كالاتي: 37 ٪ من الحالات هي منخفضة الخطر، 18 ٪ من الحالات متوسطة الخطر، و 45 ٪ من الحالات شديدة الخطر[44](وهناك بعض الأدلة التي تشير إلى ان الأنواع شديدة الخطر ومنخفضة الخطر يمكن ان تحدث عن طريق آليات مختلفة، وليست مجرد درجتين مختلفتين للتعبير عن نفس الآلية).[45]
العلاجات لفئات الخطر المختلفة هذه مختلفة جدا.
- يلاحظ بشكل متكرر الشفاء من دون علاج على الإطلاق للمرضى في المرحلة منخفضة الخطر أو يشفون مع الجراحة وحدها.[46]
- يتم علاج المرضى في المرحلة متوسطة الخطر بالجراحة والعلاج الكيميائي.[47]
- يتم علاج المرحلة شديدة الخطر من ورم الخلايا البدائية العصبية بالعلاج الكيميائي المكثف والجراحة والعلاج الإشعاعي، وزراعة نخاع العظم / زراعة الخلايا الجذعية المكونة للدم،[48] والعلاج البيولوجي المستند مع حمض 13 - رتينويك (يسوتريتينوين أو اكوتاني)[49]، وعادة يعطى علاج الأجسام المضادة مع السيتوكين GM - CSF (الخلايا البالعة المحببة عامل تنشيط المستعمرة) وIL - 2 (انترلوكين 2).[50]
مع طرق العلاج الحالية، فإن المرضى المصابين بالمرض المنخفض والمتوسط الخطر لديهم تشخيص ممتاز مع معدلات شفاء فوق 90 ٪ للمرض منخفض الخطر و 70 ٪ إلى 90 ٪ للمرض متوسط الخطر. في المقابل، فإن علاج ورم الخلايا البدائية العصبية شديد الخطر خلال العقدين الماضيين أدى فقط إلى شفاء حوالي 30 ٪ في ذلك الوقت.[30] وبالإضافة إلى علاج الأجسام المضادة الذي رفع معدلات البقاء على قيد الحياة للأمراض شديدة الخطر بشكل ملحوظ. في مارس 2009, أظهر التحليل المبكر لدراسة مجموعة علم الأورام للأطفال (COG) مع 226 مريضا مصابين بالمرض بالمرحلة شديدة الخطر بعد سنتين من زرع الخلايا الجذعية أن 66٪ من المجموعة اختيروا عشوائيا لتلقي الأجسام المضادة ch14.18 مع عامل تحفيز مستعمرات الخلايا المحببة الأكولة وIL - 2 بقوا على قيد الحياة وخاليين من المرض مقارنة مع 46٪ فقط من المجموعة والذين لم يتلقوا الأجسام المضادة. تم إيقاف التوزيع العشوائي حتى يتسنى لجميع المرضى المسجلين في التجربة تلقي علاج الأجسام المضادة.[51]
تم ايجاد عوامل العلاج الكيميائي المستخدمة في تركيبة لتكون فعالة ضد ورم الخلايا البدائية العصبية. إن العوامل الشائع استخداها في الحث وفي تكييف زرع الخلايا الجذعية هي مركبات البلاتين (سيسبلاتينوكاربوبلاتين)و عوامل الألكلة (سيكلوفوسفاميد وانفوسفاميد وملفلان) والمثبط توبويسومراز الثاني (إيتوبوسيد)، والمضادات الحيوية أنثراسيكلين (دوكسوروبيسين) وأشباه القلويات العناقية (فينكريستين). بعض أحدث الأنظمة تشمل المثبط توبويسومراز الأول (توبوتيكان وإرينوتيكان) في الاستحثاث والتي اوجدت لتكون فعالة ضد الأمراض المتكررة.
إنذار
[عدل]بين 20 ٪ و 50 ٪ من الحالات شديدة الخطر لا تستجيب بشكل كاف لإعطاء جرعة عالية من العلاج الكيميائي وهي هجومية أو مقاومة للعلاج.[52][53] الانتكاس بعد الانتهاء من علاج خط المواجهة أمر شائع أيضا. تلقي المزيد من العلاج متوفر في المرحلة الأولى والمرحلة الثانية من التجارب السريرية التي تجرب عوامل وتركيبات جديدة من العوامل ضد ورم الخلايا البدائية العصبية، ولكن النتيجة لا تزال ضعيفة للغاية بالنسبة لانتكاسة المرض شديد الخطر.[54]
معظم الناجين على المدى الطويل والذين هم على قيد الحياة الآن كانت إصابتهم منخفضة أو متوسطة الخطر وعلاجهم أكثر اعتدالا مقارنة بعلاج المرض شديد الخطر. غالبية الناجين لديهم آثار طويلة الأجل من العلاج. وكثيرا ما يعاني الناجون من علاج الحالات المتوسطة الخطر والشديدة الخطر من فقدان السمع. أو الحد من النمو، واضطرابات وظيفة الغدة الدرقية، وصعوبات التعلم، والمزيد من خطر الإصابة بسرطانات ثانوية تؤثر على الناجين من المرض شديد الخطر.[55][56] ويقدر أن اثنين من ثلاثة من الناجين من سرطان الأطفال سيكتسبون نهاية المطاف مرض مزمن واحد على الأقل وأحيانا مشاكل في الصحة التي تهدد الحياة في غضون 20 إلى 30 سنة بعد تشخيص مرض السرطان.[57][58][59]
التشكيلات الوراثية الخلوية
[عدل]استنادا إلى سلسلة من 493 عينة من ورم الخلايا البدائية العصبية، قد أفيد بأن النمط الجيني الإجمالي، كما تم اختباره من قبل المصفوفة المستندة للنمط النووي، يشكل مؤشرا للنتائج في ورم الخلايا البدائية العصبية:[60]
- ارتبط ظهور الأورام بشكل حصري مع مجموع تغييرات عدد نسخ الكروموسوم مع البقاء الممتاز على قيد الحياة.
- ارتبط ظهور الأورام مع أي نوع من تغييرات عدد نسخ الكروموسوم المجزأ مع ارتفاع خطر الانتكاس.
- داخل الأورام تظهر التعديلات المجزأة، وعوامل التنبؤ المستقلة الإضافية بخصوص انخفاض البقاء على قيد الحياة عموما كانت تضخيم N - myc، وحذف 1p و 11Q، واكتساب 1Q.
التصنيف المكبر لمنشورات ورم الخلايا البدائية العصبية إلى ثلاث أنواع فرعية رئيسية استنادا إلى التشكيلات الوراثية الخلوية:[61][62]
- النوع الفرعي 1 : ورم الخلايا البدائية العصبية المواتي مع تثلث الصيغة الصبغية القريبة وهيمنة المكاسب العددية والخسائر، والتي تمثل في الغالب مراحل غير النقيلية NB 1 و 2 و 4S.
- الأنواع الفرعية 2A و 2B : الموجودة في ورم الخلايا البدائية العصبية المنتشرة غير المواتية والمراحل 3 و 4، مع فقدان 11Q واكتساب 17q دون تضخيم N - myc (النوع الفرعي 2A) أو مع تضخيم N-myc غالبا معا مع حذف 1P واكتساب 17q(النوع الفرعي 2B).
يمكن إجراء علم النواة الخلوية الافتراضي على الأورام جديدة أو اورام البرافين المدمجة، لتحديد عدد النسخ في هذه المراضع. ويفضل مصفوفة SNP (تعدد أشكال النوكليوتيدات الأحادية) لعلم النواة الخلوية الافتراضي لعينات الورم، بما فيها ورم الخلايا البدائية العصبية، لأنه يمكن الكشف عن خسارة النسخ المحايدة لتغاير الزيجوت (اختلال الصيغة الصبغية المكتسبة من أحد الأبوين). نسخة محايدة LOH (فقدان تغاير الزيجوت) يمكن معادلتها من الناحية البيولوجية للحذف وقد تم تحديده في مواضع رئيسية في ورم الخلايا البدائية العصبية.[63] ArrayCGH (مصفوفة التهجين الجينومي المقارن)، أو FISH(الفلورية في موضع التهجين)، أو علم الوراثة الخلوية التقليدية لا يمكنها الكشف عن نسخة محايدة LOH (فقدان تغاير الزيجوت).
علم الأوبئة
[عدل]ورم الخلايا البدائية العصبية تضم 6-10 ٪ من جميع سرطانات الطفولة، و 15 ٪ من وفيات السرطان في الأطفال. معدل الوفيات السنوي هو 10 لكل مليون طفل في الفئة العمرية 0 -- 4 سنوات، و 4 لكل مليون طفل في الفئة العمرية 4 -- 9 سنوات.[64]
أعلى معدل للوفاة يكون في العام الأول من الحياة، وبعض الحالات تكون عيبا خلقيا. الفئات العمرية واسعة، وتشمل الأطفال الأكبر سنا والبالغين،[65] ولكن فقط 10 ٪ من الحالات تحدث في الأشخاص الذين تزيد أعمارهم عن 5 سنوات.[23] وقد أفادت دراسة أوروبية كبيرة انه أقل من 2 ٪ من أكثر من 4000 حالة ورم الخلايا البدائية العصبية كانت لأشخاص أكبر من 18 سنة.[66]
التاريخ
[عدل]في عام 1864، كان الطبيب الألماني رودولف فيرشو أول من وصف ورم في بطن طفل بأنه «ورم دبقي». وأشير بعد ذلك في عام 1891 إلى خصائص الأورام من الجهاز العصبي الودي ولب الكظر من قبل الطبيب الشرعي الألماني فيليكس مارشان.[67][68] وفي عام 1901 تم وصف الظهور المميز للمرحلة 4S من المرض لدى الرضع (في الكبد ولكن ليس في نقائل العظم) من قبل ويليام بيبر. في عام 1910 فهم جيمس رايت هوميروس الورم بأنه يتكون من الخلايا العصبية البدائية، وأطلق عليه اسم ورم الخلايا البدائية العصبية. وأشار أيضا إلى كتل دائرية من الخلايا في عينات من نخاع العظم التي تسمى الآن «الوريدات الزائفة هومر رايت».[69]
الأبحاث
[عدل]علاجات خط المواجهة الجديدة
[عدل]تم التركيز مؤخرا لتخفيض علاج ورم الخلايا البدائية العصبية المنخفضة الخطر والمتوسطة الخطر مع الحفاظ على معدلات البقاء بنسبة 90 ٪.[70] وأكدت دراسة من 467 مريض في المرحلة متوسطة الخطر والمسجلين في A3961 من عام 1997 إلى 2005 الافتراض أن العلاج يمكن ان يخفض الخطر بهذه المجموعة بنجاح. هذه المجموعة مع الخصائص المواتية (درجة الورم والاستجابة) تلقت أربع مجموعات من العلاج الكيميائي، وتلك المجموعة ذات الخصائص غير المواتية تلقت ثماني مجموعات من العلاج الكيميائي، مع البقاء على قيد الحياة لمدة ثلاث سنوات خالية من المرض وبقاء الحالة مستقرة عموما بنسبة 90 ٪ بالنسبة للفئة العمرية بأكملها. الخطط المستقبلية هي تكثيف العلاج لهؤلاء المرضى المصابين بانحراف في الكروموسومات 1p36 أو 11q23 بالإضافة إلى أولئك ممن يفتقرون الاستجابة المبكرة للعلاج.[71][72]
على النقيض من ذلك، فان التركيز في 20 عاما الماضية أو أكثر كان على تكثيف العلاج لورم الخلايا البدائية العصبية شديد الخطر. يتعين بحث اختلافات العلاج الكيميائي المستحث، وتوقيت الجراحة، وأنظمة زراعة الخلايا الجذعية، وبرامج ايصال مختلفة للإشعاع، واستخدام الأجسام المضادة الوحيدة النسيلة والرتينوئيدات لعلاج الحد الأدنى من المرض المتبقي. وقد أجريت مؤخرا المرحلة الثالثة من التجارب السريرية العشوائية للإجابة عن هذه الأسئلة من أجل تحسين النجاة من المرض شديد الخطر:
- 1982-1985: قامت مجموعة دراسة ورم الخلايا البدائية العصبية الأوروبية (ENSG1) بتسجيل 167 طفلا عشوائيا لزرع نخاع العظم ذاتي الملفلان أو لا مزيد من العلاج (لا يعطى العلاج الإشعاعي لأي أحد). كل من مجموعة الزرع وعدم الزرع تحتوي على 65 مريضا، ومؤخرا فان تقرير المتابعة على المدى الطويل كشف عن أفضل 5 سنوات للبقاء بحالة خالية من المرض للمرحلة 4 لمدة أكثر من عام واحد في مجموعة زرع ملفلان - مقابل عدم تلقي مزيد من العلاج: 33 ٪ مقابل 17 ٪ على التوالي.[73]
- 1990-1999: قامت دراسة أوروبية (EU-20592 or CCLGNB-1990-11) باختيار عشوائي ل262 طفلا في حالة المرض شديد الخطر أعمارهم أكثر من عام واحد واظهرت ارتفاع معدل البقاء لاستحثاث التسلسل السريع (دورة 10 أيام) مقابل الاستحثاث القياسي (دورة 21 يوما) مع نفس إجمالي الجرعة. كانت نسبة البقاء الخالية من المرض لمدة عشر سنوات 27 ٪ و 18 ٪ على التوالي مع النهج غير العدواني الجراحي ولا العلاج الإشعاعي، ونخاع العظم ذاتي الملفلان فقط أو زرع الخلايا الجذعية لكلتا المجموعتين.[74]
- 1991-1996: تجربة المرحلة الثالثة مع اثنتين من العشوائيات المتسلسلة ل379 مريض بورم الخلايا البدائية العصبية شديد الخطر قامت بها مجموعة سرطان الأطفال (CCG - 3891) والتي أظهرت تحسن البقاء مع علاج مايلوبيتيف (مع تعرض الجسم كاملا للإشعاع) وحمض الريتينويك - 13 (اكوتاني) مع 50 مريضا في كل من المجموعات الأربعة من الدراسة.[75][76]
- 1996-2003: إن (GPOH) الدراسة الألمانية NB97 بالمقارنة مع نتائج 295 مريض عشوائي بورم الخلايا البدائية العصبية شديد الخطر لزرع الخلايا الجذعية أو دمج العلاج الكيميائي. وأظهرت النتائج زيادة البقاء على قيد الحياة مع الزرع.[77]
- 2000-2006: دراسة اجريت مؤخرا (COG - A3973)[78] شككت في الحاجة لإزالة الخلايا الجذعية لأجل زرع CEM - LI (كاربوبلاتين، وإيتوبوسيد، وملفلان، مع التعرض للإشعاع الموضعي)[79]، واجريت على 486 مريض. لم يتم العثور على خلايا جذعية منقية من أجل تحسين البقاء على قيد الحياة[53]
- 2000-2012: دراسة متزامنة (COG - ANBL0032)[80] حددت بمراجعة مبكرة أن الأجسام المضادة ch14.18 مع انترلوكين 2 وعامل تحفيز مستعمرات الخلايا المحببة الأكولة(عامل المستعمرة المحفزة للبلاعم المحببة), (درست بأثر رجعي في NB90 GPOH الألمانية وNB 97 بجرعة أقل وبدون السيتوكينات [81]) تحسن فرص النجاة، وسوف تشفي ما مجموعه 423 مريضا.[82] واتباع الدراسة في المرحلة الثالثة COG - ANBL0931 افتتحت في يناير 2010 لشفاء 105 مريضا لجمع المزيد من بيانات السلامة والكفاءة للموافقة عليها من هيئة الاغذية والعقاقير الأمريكية.[83]
- 2002-2008 : SIOP(الجمعية الدولية لعلم الأورام عند الأطفال) شكلت المجموعة الأوروبية SIOP لورم الخلايا البدائية العصبية (ESIOP NB) في عام 1994 [84]، وفعَلت بروتوكول المرحلة الثالثة لورم الخلايا البدائية العصبية شديد الخطر في عام 2002 (SIOP-EUROPE-HR-NBL-1) [85] استخدام COJEC السريع (8 دورات من العلاج الكيميائي تعطى في فترات لمدة 10 أيام)، يليه الزرع العشوائي CEM (كاربوبلاتين، إيتوبوسيد، ملفلان) أو BuMel (بوسلفان، ملفلان) ودراسة عدلت مؤخرا في أطفال تم اختيارهم عشوائيا لعلاج الأجسام المضادة ch14.18 مع أو بدون تحت الجلد IL2 (GM - CSF بدون على النحو الوارد في COG). هذه الدراسة نشرت مؤخرا الاستفادة من عوامل النمو (GCSF)، [86]، وجميع المرضى يتلقون حمض الريتينويك. وسوف تشفي هذه التجربة 1000 مريض (175 سنويا).
- 2005-2010: الألمانية الحالية NB2004 [87] ستشمل عشوائيا علاج MIBG واستخدام توبوتيكان بطريقة عشوائية مقدما في العلاج، وسوف يشفى ما مجموعه 642 مريضا لجميع فئات الخطر (النصف تقريبا سيكونون في المرحلة شديدة الخطر). بعد الزرع، فان بروتوكول المرحلة شديدة الخطر يتضمن ستة أشهر من حمض الريتينويك، وثم توقف العلاج لمدة ثلاثة أشهر وثلاثة أشهر أخرى لاحقة من حمض الريتينويك.
- 2007: COG في المرحلة الثالثة ANBL0532 [88] بدأت التجربة في ديسمبر 2007 على أساس الشفاء ل 495 مريض وسيتم مقارنة عملية زراعة واحدة مقابل عمليات زرع ترادفية، ويبدأ الاستحثاث مع دورتين من توبوتيكان.[89]
بالإضافة إلى دراسات المرحلة الثالثة، تقدم بعض المؤسسات البحثية بروتوكولات العلاج التجريبي. على سبيل المثال، انتهت مؤخرا مؤسسة القديس جود في عام (2007) من اختبار جديد لنظام العلاج الكيميائي كخط مواجهة في 23 طفلا وشمل العلاج إرينوتيكان وجيفيتينيب لمدة 16 شهرا مع المحافظة على العلاج الكيميائي بعد زرع الخلايا الجذعية بالتناوب مع حمض الريتينويك 13 وتوبوتيكان.[90] النصب التذكاري في مركز سلون كيترينج للسرطان في نيويورك يقدم العلاج الذي يشمل الأجسام المضادة أحادية المنشأ المستمدة من الفئران، 3ف8، وتستخدم في بروتوكولات العلاج منذ منتصف الثمانينات من القرن الماضي. وتستخدم هذه الأجسام المضادة لعلاج الحد الأدنى المتبقي من المرض أو الدمج بدلا من زرع الخلايا الجذعية.[91] أما COG - ANBL09P1 فهو بروتوكول نموذجي جديد ومتاح للأطفال المشخصين حديثا بمرض (شديد الخطر (في عدة مجموعات مراكز أورام أطفال (COG) التي تقدم العلاج الإشعاعي MIBG والعلاج الكيميائي لنظام الزرع.[92]
ورم الخلايا البدائية العصبية المقاومة للعلاج والانتكاس
[عدل]
بعض الأطفال (وبخاصة في الحالات شديدة الخطر) لا يستجيبون بالكامل مع علاج خط المواجهة (مع استجابة كاملة أو استجابة جزئية جيدة جدا) وتسمى هذه الحالة المقاومة للعلاج. يتم نقل أولئك الأطفال من علاج المواجهة (تجربة سريرية)، ويصبحون مؤهلين للتجارب السريرية باستخدام علاجات جديدة. العديد من الأطفال المعرضين للمرض شديد الخطر لديهم استجابة جيدة لعلاج خط المواجهة وتحقيق تخفيف المرض، ولكن في وقت لاحق يتكرر المرض (الانتكاس). هؤلاء الأطفال مؤهلين أيضا للحصول على علاجات جديدة يجري اختبارها في التجارب السريرية.
وكثيرا ما يستخدم العلاج الكيميائي مع توبوتيكان وسيكلوفوسفاميد في الوضع المقاوم للعلاج وبعد الانتكاس. وكشفت دراسة عشوائية (2004) مع 119 مريضا (مقارنة توبوتيكان وحده مع توبوتيكان وسيكلوفوسفاميد) ان نسبة 31 ٪ من المرضى استجابوا استجابة كاملة أو جزئية مع عامين من البقاء على قيد الحياة وبدون تقدم المرض بالمقارنة مع نسبة 36 ٪ في مجموعة علاج التوبوتيكان والسيكلوفوسفاميد.[93] يتم أيضا استخدام إرينوتيكان (عن طريق الوريد أو الفم) وتيموزولوميد فمويا في الحالات المقاومة للعلاج وورم الخلايا البدائية العصبية المتكرر.[94][95]
كثير من تجارب المرحلة الأولى والمرحلة الثانية تختبر حاليا عوامل جديدة ضد ورم الخلايا البدائية العصبية لدى الأطفال الذين لديهم انتكاس أو مقاومة العلاج الأولي. الباحثون يدرسون حاليا عوامل جديدة، سواء بمفردها أو تركيبات جديدة، وذلك باستخدام علاج الجزيئات الصغيرة المستهدفة والعلاج الإشعاعي 131 - I MIBG، وعوامل تكوين الأوعية الدموية، والأجسام المضادة وحيدة النسيلة الجديدة، واللقاحات وفيروسات الأورام وكذلك أنظمة مايلوبيتيف الجديدة.
مجموعة من 16 مستشفى للاطفال في الولايات المتحدة والمعروفة بالتطورات الجديدة في علاج ورم الخلايا البدائية العصبية (NANT) كونسورتيوم ينسيق تجارب علاج الإشعاع MIBG I - 131. NANT كونسورتيوم يقدم أيضا تجارب باستخدام تركيبة بودرة فموية من فينريتينيد وفينريتينيد الوريدي، وباي فوسفونتس (زوميتا) مع عوامل أخرى، والجمع بين I - 131 MIBG مع فورينوستات المثبط.[96]
مجموعات دراسة بحثية أخرى مثل ورم الخلايا البدائية العصبية واتحاد أبحاث الحركة المنتظمة النخاعية (NMTRC) تجري أيضا التجارب السريرية لعلاج انتكاس ورم الخلايا البدائية العصبية.[97] مؤسسات في أوروبا تدرس علاجات جديدة لعلاج الانتكاس، بما فيها زراعة الخلايا الجذعية متماثل النمط الفرداني.[98] والعديد من المستشفيات تجري دراسات مؤسسية خاصة بها كذلك.
ويعتقد ان البروتين بي53 يلعب دورا في تطور مقاومة العلاج الكيميائي.[99] اجريت دراسة في نوفمبر 2009 على الفئران اظهرت أن تنشيط البروتين p53 المثبط للورم مع دواء جديد هو nutlin - 3، قد يبطئ نمو الورم.[100] في هذه الدراسة، استخدم الطبيب توم فان ميركين من مستشفى جامعة جنت في بلجيكا وزملاؤه nutlin - 3 لتحييد MDM2 وهو البروتين الذي يربط إلى البروتين p53 ويعيق قدرة البروتين p53 مؤديا إلى موت الخلايا المبرمجة. وقد أظهرت دراسات سابقة أن nutlin - 3 يمكن أن يمنع على وجه التحديد MDM2 من تعطيل البروتين p53.
الجهود التشريعية
[عدل]تشيت ادواردز من واكو بولاية تكساس وهو العضو في مجلس النواب الأمريكي، والذي قدم بنجاح تشريعات لتخصيص نحو 150 مليون دولار لعلاج ورم الخلايا البدائية العصبية وأنواع أخرى من السرطان. تم توقيع المشروع ليصبح قانونا في تموز عام 2008 من قبل الرئيس الاميركي جورج دبليو بوش. وقد الهم ادواردز في مسعاه هذا المرض والوفاة اللاحقة لايرين بنجر تشانينج (1997-2009) من برايان, تكساس، ابنة أحد الناخبين في دائرته، ووالتر ل. بنجر، رئيس قسم التاريخ في جامعة تكساس وجامعة A & M.[101]
اقرأ أيضًا
[عدل]المراجع
[عدل]- ^ Inxight: Drugs Database، QID:Q57664317
- ^ المعجم الطبي الموحد
- ^ "eMedicine - Neuroblastoma : Article by Norman J Lacayo, MD". مؤرشف من الأصل في 2008-10-28. اطلع عليه بتاريخ 2008-07-30.
- ^ Janet Sassi, "Cellular Communication: Unraveling the Secrets of Histone Proteins", Fordham University, February 16, 2007 نسخة محفوظة 27 مايو 2008 على موقع واي باك مشين.
- ^ Bénard J, Raguénez G, Kauffmann A؛ وآخرون (أكتوبر 2008). "MYCN-non-amplified metastatic neuroblastoma with good prognosis and spontaneous regression: a molecular portrait of stage 4S". Mol Oncol. ج. 2 ع. 3: 261–71. DOI:10.1016/j.molonc.2008.07.002. PMID:19383347. مؤرشف من الأصل في 2017-12-10.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "ScienceDirect - The Lancet : Neuroblastoma". مؤرشف من الأصل في 2020-05-25.
- ^ "eMedicine - Esthesioneuroblastoma : Article by Pavel Dulguerov, MD". مؤرشف من الأصل في 2008-12-06. اطلع عليه بتاريخ 2008-07-30.
- ^ Cheung، Nai-Kong (2005). Neuroblastoma. p. 73. سبرنجر.
- ^ "Neuroblastoma in children : Cancerbackup". مؤرشف من الأصل في 2009-07-09. اطلع عليه بتاريخ 2008-01-01.
- ^ "Neuroblastoma: Pediatric Cancers: Merck Manual Professional". مؤرشف من الأصل في 2010-10-18. اطلع عليه بتاريخ 2008-01-01.
- ^ Friedman GK, Castleberry RP (ديسمبر 2007). "Changing trends of research and treatment in infant neuroblastoma". Pediatr Blood Cancer. ج. 49 ع. 7 Suppl: 1060–5. DOI:10.1002/pbc.21354. PMID:17943963.
- ^ Rothenberg AB, Berdon WE, D'Angio GJ, Yamashiro DJ, Cowles RA (يوليو 2009). "The association between neuroblastoma and opsoclonus-myoclonus syndrome: a historical review". Pediatr Radiol. ج. 39 ع. 7: 723–6. DOI:10.1007/s00247-009-1282-x. ISBN:2470091282. PMID:19430769.
{{استشهاد بدورية محكمة}}: تأكد من صحة|isbn=القيمة: checksum (مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Cheung، Nai-Kong (2005). Neuroblastoma. p. 66-67. سبرنجر.
- ^ Mossé YP, Laudenslager M, Longo L؛ وآخرون (أكتوبر 2008). "Identification of ALK as a major familial neuroblastoma predisposition gene". Nature. ج. 455 ع. 7215: 930–5. DOI:10.1038/nature07261. PMC:2672043. PMID:18724359.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ New Gene For Childhood Cancer Neuroblastoma Is Discovered. NewsWise (Report). نوفمبر 2010. مؤرشف من الأصل في 2018-02-27.
- ^ Copy number variation at 1q21.1 associated with neuroblastoma; Diskin et al.; Nature 459, 987-991 (18 June 2009) | doi:10.1038/nature08035; Received 14 December 2008; Accepted 30 March 2009
- ^ Olshan, AF, Bunin, GR (2000) Epidemiology of Neuroblastoma. In: Brodeur, GM, Sawada, T, Tsuchida, Y, Voute, PA eds.، Neuroblastoma, Elsevier, Amsterdam, pp 33-39. ISBN 0-444-50222-X [1] نسخة محفوظة 26 سبتمبر 2007 على موقع واي باك مشين.
- ^ Menegaux F, Olshan AF, Neglia JP, Pollock BH, Bondy ML (مايو 2004). "Day care, childhood infections, and risk of neuroblastoma". Am. J. Epidemiol. ج. 159 ع. 9: 843–51. DOI:10.1093/aje/kwh111. PMC:2080646. PMID:15105177. مؤرشف من الأصل في 2020-05-26.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Olshan AF,et al. "Hormone and Fertility Drug Use and the Risk of Neuroblastoma: A Report from the Children's Cancer Group and the Pediatric Oncology Group", Am J Epidemiol 1999;150:930-8. نسخة محفوظة 10 يوليو 2009 على موقع واي باك مشين.
- ^ ,McCall EE,et al. "Maternal hair dye use and risk of neuroblastoma in offspring", Cancer Causes and Control 2005; 16,6:743-8 نسخة محفوظة 30 سبتمبر 2012 على موقع واي باك مشين. [وصلة مكسورة]
- ^ Heck JE, Ritz B, Hung RJ, Hashibe M, Boffetta P (مارس 2009). "The epidemiology of neuroblastoma: a review". Paediatr Perinat Epidemiol. ج. 23 ع. 2: 125–43. DOI:10.1111/j.1365-3016.2008.00983.x. PMID:19159399. مؤرشف من الأصل في 2020-05-25.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Strenger V, Kerbl R, Dornbusch HJ؛ وآخرون (2007). "Diagnostic and prognostic impact of urinary catecholamines in neuroblastoma patients". Pediatr Blood Cancer. ج. 48 ع. 5: 504–9. DOI:10.1002/pbc.20888. PMID:16732582.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب Howman-Giles R, Shaw PJ, Uren RF, Chung DK (2007). "Neuroblastoma and other neuroendocrine tumors". Semin Nucl Med. ج. 37 ع. 4: 286–302. DOI:10.1053/j.semnuclmed.2007.02.009. PMID:17544628. مؤرشف من الأصل في 2019-12-17.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Pashankar F,O’Dorisio M, Menda Y (2005). "MIBG and somatostatin receptor analogs in children: current concepts on diagnostic and therapeutic use". Journal of Nuclear Medicine. ج. 46 ع. 1 (suppl): 55S–61S. PMID:15653652. مؤرشف من الأصل في 2010-06-17.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Flexner-Wintersteiner Rosette | definition of Flexner-Wintersteiner Rosette by Medical dictionary نسخة محفوظة 20 نوفمبر 2016 على موقع واي باك مشين.
- ^ Miura K, Mineta H, Yokota N, Tsutsui Y (2001). "Olfactory neuroblastoma with epithelial and endocrine differentiation transformed into ganglioneuroma after chemoradiotherapy". Pathol. Int. ج. 51 ع. 12: 942–7. DOI:10.1046/j.1440-1827.2001.01300.x. PMID:11844067.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) [بحاجة لمراجعة المصدر] - ^ Medscape: Medscape Access نسخة محفوظة 05 يناير 2010 على موقع واي باك مشين.
- ^ "Althea Technologies Announces the Development of a Diagnostic Capable of Differentiating Multiple Forms of Childhood Cancer", press release, February 20, 2007 نسخة محفوظة 04 يناير 2009 على موقع واي باك مشين. [وصلة مكسورة]
- ^ Peuchmaur M, d'Amore ES, Joshi VV؛ وآخرون (2003). "Revision of the International Neuroblastoma Pathology Classification: confirmation of favorable and unfavorable prognostic subsets in ganglioneuroblastoma, nodular". Cancer. ج. 98 ع. 10: 2274–81. DOI:10.1002/cncr.11773. PMID:14601099.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب "Neuroblastoma Treatment - National Cancer Institute". مؤرشف من الأصل في 2015-04-25. اطلع عليه بتاريخ 2008-07-30.
- ^ Brodeur GM, Seeger RC, Barrett A؛ وآخرون (1988). "International criteria for diagnosis, staging, and response to treatment in patients with neuroblastoma". J. Clin. Oncol. ج. 6 ع. 12: 1874–81. PMID:3199170. مؤرشف من الأصل في 2020-06-25.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Brodeur GM, Pritchard J, Berthold F؛ وآخرون (1993). "Revisions of the international criteria for neuroblastoma diagnosis, staging, and response to treatment". J. Clin. Oncol. ج. 11 ع. 8: 1466–77. PMID:8336186. مؤرشف من الأصل في 2020-06-25.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Schmidt ML, Lal A, Seeger RC, Maris JM, Shimada H, O'Leary M, Gerbing RB, Matthay KK (2005). "Favorable prognosis for patients 12 to 18 months of age with stage 4 nonamplified MYCN neuroblastoma: a Children's Cancer Group Study". J Clin Oncol. ج. 23 ع. 27: 6474–80. DOI:10.1200/JCO.2005.05.183. PMID:16116154. مؤرشف من الأصل في 2009-07-10.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Maris JM, Hogarty MD, Bagatell R, Cohn SL (2007). "Neuroblastoma". Lancet. ج. 369 ع. 9579: 2106–20. DOI:10.1016/S0140-6736(07)60983-0. PMID:17586306. مؤرشف من الأصل في 2019-12-17.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Cohn SL, London WB, Monclair T, Matthay KK, Ambros PF, Pearson AD, for the INRG Working Group (2007). "Update on the development of the international neuroblastoma risk group (INRG) classification schema". Journal of Clinical Oncology 2007 ASCO Annual Meeting Proceedings Part 1. ج. 25 ع. 18S. مؤرشف من الأصل (abstract) في 23 ديسمبر 2008. اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Woods WG, Gao RN, Shuster JJ؛ وآخرون (2002). "Screening of infants and mortality due to neuroblastoma". N. Engl. J. Med. ج. 346 ع. 14: 1041–6. DOI:10.1056/NEJMoa012387. PMID:11932470. مؤرشف من الأصل في 2020-05-25.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Schilling FH, Spix C, Berthold F؛ وآخرون (2003). "Children may not benefit from neuroblastoma screening at 1 year of age. Updated results of the population based controlled trial in Germany". Cancer Lett. ج. 197 ع. 1–2: 19–28. DOI:10.1016/S0304-3835(03)00077-6. PMID:12880955. مؤرشف من الأصل في 2018-06-09.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Tsubono Y, Hisamichi S (2004). "A halt to neuroblastoma screening in Japan". N. Engl. J. Med. ج. 350 ع. 19: 2010–1. DOI:10.1056/NEJM200405063501922. PMID:15128908.
- ^ "Neuroblastoma Screening - National Cancer Institute". مؤرشف من الأصل في 2015-04-26. اطلع عليه بتاريخ 2008-07-30.
- ^ Darshak Sanghavi, "Screen Alert: How an Ounce of RX Prevention can Cause a Pound of Hurt", Slate magazine, November 28, 2006 نسخة محفوظة 21 يناير 2011 على موقع واي باك مشين.
- ^ Johnson E, Dean SM, Sondel PM (2007). "Antibody-based immunotherapy in high-risk neuroblastoma". Expert Rev Mol Med. ج. 9 ع. 34: 1–21. DOI:10.1017/S1462399407000518. PMID:18081947. مؤرشف من الأصل (abstract) في 2020-05-26.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Brodeur GM (مارس 2003). "Neuroblastoma: biological insights into a clinical enigma". Nat. Rev. Cancer. ج. 3 ع. 3: 203–16. DOI:10.1038/nrc1014. PMID:12612655.
- ^ Schulte JH, Horn S, Otto T؛ وآخرون (2008). "MYCN regulates oncogenic MicroRNAs in neuroblastoma". Int. J. Cancer. ج. 122 ع. 3: 699–704. DOI:10.1002/ijc.23153. PMID:17943719.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Translating Neuroblastoma Genomics to the Clinic - J. Maris presentation ASCO 2007". مؤرشف من الأصل في 2012-02-08. اطلع عليه بتاريخ 2008-01-13.
- ^ Gisselsson D, Lundberg G, Ora I, Höglund M (2007). "Distinct evolutionary mechanisms for genomic imbalances in high-risk and low-risk neuroblastomas". J Carcinog. ج. 6: 15. DOI:10.1186/1477-3163-6-15. PMC:2042979. PMID:17897457.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Neuroblastoma Treatment - National Cancer Institute". مؤرشف من الأصل في 2015-04-06. اطلع عليه بتاريخ 2008-02-02.
- ^ Haase GM, Perez C, Atkinson JB (1999). "Current aspects of biology, risk assessment, and treatment of neuroblastoma". Semin Surg Oncol. ج. 16 ع. 2: 91–104. DOI:10.1002/(SICI)1098-2388(199903)16:2<91::AID-SSU3>3.0.CO;2-1. PMID:9988866.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Fish JD, Grupp SA (2007). "Stem cell transplantation for neuroblastoma". Bone Marrow Transplant. ج. 41 ع. 2: 159. DOI:10.1038/sj.bmt.1705929. PMC:2892221. PMID:18037943.
- ^ Matthay KK, Villablanca JG, Seeger RC؛ وآخرون (1999). "Treatment of high-risk neuroblastoma with intensive chemotherapy, radiotherapy, autologous bone marrow transplantation, and 13-cis-retinoic acid. Children's Cancer Group". N. Engl. J. Med. ج. 341 ع. 16: 1165–73. DOI:10.1056/NEJM199910143411601. PMID:10519894. مؤرشف من الأصل في 2020-05-07.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Yu AL, Gilman AL, Ozkaynak MF؛ وآخرون (سبتمبر 2010). "Anti-GD2 antibody with GM-CSF, interleukin-2, and isotretinoin for neuroblastoma". نيو إنغلاند جورنال أوف ميديسين. ج. 363 ع. 14: 1324–34. DOI:10.1056/NEJMoa0911123. PMID:20879881.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "A phase III randomized trial of the chimeric anti-GD2 antibody ch14.18 with GM-CSF and IL2 as immunotherapy following dose intensive chemotherapy for high-risk neuroblastoma: Children's Oncology Group (COG) study ANBL0032". مؤرشف من الأصل في 2016-03-05.
- ^ "Reduction From Seven to Five Cycles of Intensive Induction Chemotherapy in Children With High-Risk Neuroblastoma -- Kushner et al. 22 (24): 4888 -- Journal of Clinical Oncology". مؤرشف من الأصل في 2009-02-16.
- ^ ا ب "Response and toxicity to a dose-intensive multi-agent chemotherapy induction regimen for high risk neuroblastoma (HR-NB): A Children's Oncology Group (COG A3973) study. - ASCO". مؤرشف من الأصل في 2009-01-03. اطلع عليه بتاريخ 2008-02-02.
- ^ Ceschel S, Casotto V, Valsecchi MG؛ وآخرون (أكتوبر 2006). "Survival after relapse in children with solid tumors: a follow-up study from the Italian off-therapy registry". Pediatr Blood Cancer. ج. 47 ع. 5: 560–6. DOI:10.1002/pbc.20726. PMID:16395684.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Gurney JG, Tersak JM, Ness KK, Landier W, Matthay KK, Schmidt ML (2007). "Hearing loss, quality of life, and academic problems in long-term neuroblastoma survivors: a report from the Children's Oncology Group". Pediatrics. ج. 120 ع. 5: e1229–36. DOI:10.1542/peds.2007-0178. PMID:17974716.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Trahair TN, Vowels MR, Johnston K, Cohn RJ, Russell SJ, Neville KA, Carroll S, Marshall GM (2007). "Long-term outcomes in children with high-risk neuroblastoma treated with autologous stem cell transplantation". Bone Marrow Transplant. ج. 40 ع. 8: 741–6. DOI:10.1038/sj.bmt.1705809. PMID:17724446.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Childhood Cancer Survivors Face Increased Sarcoma Risk", HealthDay News, February 21, 2007 نسخة محفوظة 22 ديسمبر 2016 على موقع واي باك مشين.
- ^ Oeffinger et al., "Chronic Health Conditions in Adult Survivors of Childhood Cancer", New England Journal of Medicine, October 12, 2006 نسخة محفوظة 19 يونيو 2010 على موقع واي باك مشين.
- ^ "Long-term Outcomes in Survivors of Neuroblastoma: A Report From the Childhood Cancer Survivor Study -- Laverdière et al., 10.1093/jnci/djp230 -- JNCI Journal of the National Cancer Institute". مؤرشف من الأصل في 2020-05-25.
- ^ Janoueix-Lerosey I, Schleiermacher G, Michels E؛ وآخرون (مارس 2009). "Overall genomic pattern is a predictor of outcome in neuroblastoma". J. Clin. Oncol. ج. 27 ع. 7: 1026–33. DOI:10.1200/JCO.2008.16.0630. PMID:19171713. مؤرشف من الأصل في 2020-05-25.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Vandesompele, J, M Baudis, K De Preter, N Van Roy, P Ambros, N Bown, C Brinkschmidt, H Christiansen, V Combaret, M Lastowska, J Nicholson, A O'meara, D Plantaz, R Stallings, B Brichard, C Van den Broecke, S De Bie, A De Paepe, G Laureys, and F Speleman. 2005. Unequivocal delineation of clinicogenetic subgroups and development of a new model for improved outcome prediction in neuroblastoma. J Clin Oncol 10, no. 23: 2280-2299.
- ^ Michels, E; Vandesompele, J; Hoebeeck, J; Menten, B; De Preter, K; Laureys, G; Van Roy, N; Speleman, F. Genome wide measurement of DNA copy number changes in neuroblastoma: dissecting amplicons and mapping losses, gains and breakpoints. Cytogenet Genome Res. 2006;115:273–282. doi: 10.1159/000095924. [PubMed]
- ^ Carén H, Erichsen J, Olsson L, Enerbäck C, Sjöberg RM, Abrahamsson J, Kogner P, Martinsson T. High-resolution array copy number analyses for detection of deletion, gain, amplification and copy-neutral LOH in primary neuroblastoma tumors: four cases of homozygous deletions of the CDKN2A gene. BMC Genomics. 2008 Jul 29;9:353.
- ^ Brodeur GM, Castleberry RP. Neuroblastoma. In: Pizzo PA, Poplack DG. Principles and practice of pediatric oncology, 3rd ed. 1997:761-797.
- ^ Franks LM, Bollen A, Seeger RC, Stram DO, Matthay KK (1997). "Neuroblastoma in adults and adolescents: an indolent course with poor survival". Cancer. ج. 79 ع. 10: 2028–35. DOI:10.1002/(SICI)1097-0142(19970515)79:10<2028::AID-CNCR26>3.0.CO;2-V. PMID:9149032.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Ladenstein R, Pötschger U, Hartman O؛ وآخرون (يونيو 2008). "28 years of high-dose therapy and SCT for neuroblastoma in Europe: lessons from more than 4000 procedures". Bone Marrow Transplant. 41 Suppl 2: S118–27. DOI:10.1038/bmt.2008.69. PMID:18545256.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Cheung، Nai-Kong (2005). Neuroblastoma. p. 63. سبرنجر.
- ^ "In Situ Neuroblastomas: a Contribution to the Natural History of Neural Crest Tumors". مؤرشف من الأصل في 2020-06-25.
- ^ Rothenberg AB, Berdon WE, D'Angio GJ, Yamashiro DJ, Cowles RA (فبراير 2009). "Neuroblastoma-remembering the three physicians who described it a century ago: James Homer Wright, William Pepper, and Robert Hutchison". Pediatr Radiol. ج. 39 ع. 2: 155–60. DOI:10.1007/s00247-008-1062-z. ISBN:2470081062. PMID:19034443.
{{استشهاد بدورية محكمة}}: تأكد من صحة|isbn=القيمة: checksum (مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Neuroblastoma Committee - Current Focus of Research". مؤرشف من الأصل في 2011-07-18. اطلع عليه بتاريخ 2008-01-13.
- ^ "A phase III trial of biologically-based therapy reduction for intermediate risk neuroblastoma -- Baker et al. 25 (18 Supplement): 9504 -- ASCO Meeting Abstracts". مؤرشف من الأصل في 2016-04-04.
- ^ Baker DL, Schmidt ML, Cohn SL؛ وآخرون (سبتمبر 2010). "Outcome after reduced chemotherapy for intermediate-risk neuroblastoma". نيو إنغلاند جورنال أوف ميديسين. ج. 363 ع. 14: 1313–23. DOI:10.1056/NEJMoa1001527. PMC:2993160. PMID:20879880.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Pritchard J, Cotterill SJ, Germond SM, Imeson J, de Kraker J, Jones DR (2005). "High dose melphalan in the treatment of advanced neuroblastoma: results of a randomised trial (ENSG-1) by the European Neuroblastoma Study Group". Pediatr Blood Cancer. ج. 44 ع. 4: 348–57. DOI:10.1002/pbc.20219. PMID:15546135.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Pearson AD, Pinkerton CR, Lewis IJ, Imeson J, Ellershaw C, Machin D (2008). "High-dose rapid and standard induction chemotherapy for patients aged over 1 year with stage 4 neuroblastoma: a randomised trial". Lancet Oncol. ج. 9 ع. 3: 247–256. DOI:10.1016/S1470-2045(08)70069-X. PMID:18308250.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Matthay KK, Villablanca JG, Seeger RC؛ وآخرون (أكتوبر 1999). "Treatment of high-risk neuroblastoma with intensive chemotherapy, radiotherapy, autologous bone marrow transplantation, and 13-cis-retinoic acid. Children's Cancer Group". N. Engl. J. Med. ج. 341 ع. 16: 1165–73. DOI:10.1056/NEJM199910143411601. PMID:10519894. مؤرشف من الأصل في 2020-05-30.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Matthay KK, Reynolds CP, Seeger RC؛ وآخرون (مارس 2009). "Long-term results for children with high-risk neuroblastoma treated on a randomized trial of myeloablative therapy followed by 13-cis-retinoic acid: a children's oncology group study". J. Clin. Oncol. ج. 27 ع. 7: 1007–13. DOI:10.1200/JCO.2007.13.8925. PMC:2738615. PMID:19171716. مؤرشف من الأصل في 2020-06-25.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Berthold F, Boos J, Burdach S؛ وآخرون (سبتمبر 2005). "Myeloablative megatherapy with autologous stem-cell rescue versus oral maintenance chemotherapy as consolidation treatment in patients with high-risk neuroblastoma: a randomised controlled trial". Lancet Oncol. ج. 6 ع. 9: 649–58. DOI:10.1016/S1470-2045(05)70291-6. PMID:16129365.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Clinical Trials (PDQ) - National Cancer Institute". مؤرشف من الأصل في 2020-06-25. اطلع عليه بتاريخ 2008-02-02.
- ^ "Autologous Stem Cell Transplantation for High-Risk Neuroblastoma" (PDF). مؤرشف من الأصل (PDF) في 2013-04-13. اطلع عليه بتاريخ 2008-02-02.
- ^ "Clinical Trials - National Cancer Institute". مؤرشف من الأصل في 2020-06-25. اطلع عليه بتاريخ 2008-02-02.
- ^ "Consolidation Treatment With Chimeric Anti-GD2-Antibody ch14.18 in Children Older Than 1 Year With Metastatic Neuroblastoma -- Simon et al. 22 (17): 3549 -- Journal of Clinical Oncology". مؤرشف من الأصل في 2009-04-09. اطلع عليه بتاريخ 2008-02-02.
- ^ "NCI Cancer Bulletin for May 19, 2009 - National Cancer Institute". مؤرشف من الأصل في 2010-12-21.
- ^ "Monoclonal Antibody Ch14.18, Sargramostim, Aldesleukin, and Isotretinoin After Autologous Stem Cell Transplant in Treating Patients With Neuroblastoma - Full Text View - ClinicalTrials.gov". مؤرشف من الأصل في 2017-05-12.
- ^ "Neuroblastoma Education Book" (PDF). مؤرشف من الأصل (PDF) في 2017-09-11. اطلع عليه بتاريخ 2008-02-02.
- ^ "Clinical Trials (PDQ) - National Cancer Institute". مؤرشف من الأصل في 2020-05-25. اطلع عليه بتاريخ 2008-02-02.
- ^ Ladenstein R, Valteau-Couanet D, Brock P؛ وآخرون (يوليو 2010). "Randomized Trial of prophylactic granulocyte colony-stimulating factor during rapid COJEC induction in pediatric patients with high-risk neuroblastoma: the European HR-NBL1/SIOPEN study". J. Clin. Oncol. ج. 28 ع. 21: 3516–24. DOI:10.1200/JCO.2009.27.3524. PMID:20567002.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Observation, Combination Chemotherapy, Radiation Therapy, and/or Autologous Stem Cell Transplant in Treating Young Patients With Neuroblastoma - Full Text View - ClinicalTrials.gov". مؤرشف من الأصل في 2017-05-12.
- ^ "Clinical Trials (PDQ®) - National Cancer Institute". مؤرشف من الأصل في 2015-02-08.
- ^ George RE, Li S, Medeiros-Nancarrow C؛ وآخرون (يونيو 2006). "High-risk neuroblastoma treated with tandem autologous peripheral-blood stem cell-supported transplantation: long-term survival update". J. Clin. Oncol. ج. 24 ع. 18: 2891–6. DOI:10.1200/JCO.2006.05.6986. PMID:16782928.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Tazarotene"&show_desc=Y "Neuroblastoma Protocol 2005: Therapy for Children with Advanced Stage High-Risk Neuroblastoma". مؤرشف من "Tazarotene"&show_desc=Y#desc الأصل في 2014-03-27. اطلع عليه بتاريخ 2008-02-02.
- ^ "Sloan-Kettering - Neuroblastoma: Our Clinical Trials". مؤرشف من الأصل في 2011-09-26. اطلع عليه بتاريخ 2008-02-02.
- ^ "Induction Therapy Followed by 131 I-MIBG and High-Dose Chemotherapy in Treating Patients With Newly Diagnosed High-Risk Neuroblastoma Undergoing Stem Cell Transplant, Radiation Therapy, and Maintenance Therapy With Isotretinoin - Full Text View - ClinicalTrials.gov". مؤرشف من الأصل في 2018-10-10.
- ^ "Recurrent neuroblastoma: Randomized treatment with topotecan + cyclophosphamide (T+C) vs. topotecan alone(T). A POG/CCG Intergroup Study -- Frantz et al. 22 (14 Supplement): 8512 -- ASCO Meeting Abstracts". مؤرشف من الأصل في 2008-12-22. اطلع عليه بتاريخ 2008-03-13.
- ^ "Irinotecan Plus Temozolomide for Relapsed or Refractory Neuroblastoma -- Kushner et al. 24 (33): 5271 -- Journal of Clinical Oncology". مؤرشف من الأصل في 2009-06-22. اطلع عليه بتاريخ 2008-03-13.
- ^ "Phase I study of oral irinotecan and temozolomide in children with relapsed high-risk neuroblastoma: A New Approach to Neuroblastoma Therapy (NANT) Consortium study -- Wagner et al. 25 (18 Supplement): 9567 -- ASCO Meeting Abstracts". مؤرشف من الأصل في 2008-12-22. اطلع عليه بتاريخ 2008-03-13.
- ^ "NANT Home Page". مؤرشف من الأصل في 2019-04-23. اطلع عليه بتاريخ 2008-02-02.
- ^ "Home - Neuroblastoma and Medulloblastoma Translational Research Consortium". مؤرشف من الأصل في 2017-06-10.
- ^ "Haploidentical Stem Cell Transplantation in Neuroblastoma - Full Text View - ClinicalTrials.gov". مؤرشف من الأصل في 2016-03-08.
- ^ Xue C, Haber M, Flemming C؛ وآخرون (2007). "p53 determines multidrug sensitivity of childhood neuroblastoma". Cancer Res. ج. 67 ع. 21: 10351–60. DOI:10.1158/0008-5472.CAN-06-4345. PMID:17974978. مؤرشف من الأصل في 2020-06-25.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Van Maerken T, Ferdinande L, Taildeman J؛ وآخرون (نوفمبر 2009). "Antitumor Activity of the Selective MDM2 Antagonist Nutlin-3 Against Chemoresistant Neuroblastoma With Wild-Type p53". Journal of the National Cancer Institute. ج. 101 ع. 22: 1562–1574. DOI:10.1093/jnci/djp355. PMID:19903807. مؤرشف من الأصل في 2020-06-25.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Erin Buenger had a zest for living life fully, April 12, 2010". Bryan-College Station Eagle. مؤرشف من الأصل في 2012-08-16. اطلع عليه بتاريخ 2010-10-14.
{{استشهاد ويب}}: استعمال الخط المائل أو الغليظ غير مسموح:|ناشر=(مساعدة)
وصلات خارجية
[عدل]- VIDEO - Neuroblastoma: New Advances in the Treatment of a Deadly Disease Dr. Kenneth DeSantes speaks at the University of Wisconsin-Madison School of Medicine and Public Health. 2011.
- ورم الخلايا البدائية العصبية على مشروع الدليل المفتوح

