تيكاغريلور
المظهر
(بالتحويل من Ticagrelor)
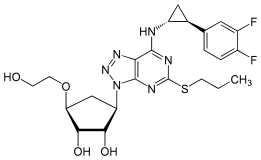
تيكاغريلور (بالإنجليزية: Ticagrelor) (الاسم التجاري: («بريلينتا» Brilinta) ('Brilique) ،(Possia)) هو عقار مضاد تكدس الصفائح الدموية والذي تنتجه شركة أسترا زينيكا. وتمت الموافقة على العقار للاستخدام في الاتحاد الأوروبي من قبل المفوضية الأوروبية في 3 ديسمبر، 2010.[4][5] تمت الموافقة على العقار في الولايات المتحدة من قبل إدارة الغذاء والدواء (الولايات المتحدة) في 20 يوليو 2011.[6]
 |
 |
مراجع
[عدل]- ^ ا ب Simon Maskell; Munir Pirmohamed (4 Mar 2022). "A reference set of clinically relevant adverse drug-drug interactions". Scientific Data (بالإنجليزية). 9 (1). DOI:10.1038/S41597-022-01159-Y. ISSN:2052-4463. QID:Q123478206.
- ^ Simon Maskell; Munir Pirmohamed (4 Mar 2022). "A reference set of clinically relevant adverse drug-drug interactions". Scientific Data (بالإنجليزية). 9 (1). DOI:10.1038/S41597-022-01159-Y. ISSN:2052-4463. QID:Q123478206.
- ^ ا ب Drug Indications Extracted from FAERS، DOI:10.5281/ZENODO.1435999، QID:Q56863002
- ^ "Assessment Report for Brilique" (PDF). وكالة الأدوية الأوروبية. يناير 2011. مؤرشف من الأصل (PDF) في 2018-05-17.
- ^ European Public Assessment Report Possia نسخة محفوظة 04 مارس 2016 على موقع واي باك مشين.
- ^ "FDA approves blood-thinning drug Brilinta to treat acute coronary syndromes". FDA. 20 يوليو 2011. مؤرشف من الأصل في 2017-01-18.
في كومنز صور وملفات عن Ticagrelor.


