سيليكوكسيب
مثل روفيكوكسيب،سيليكوكسيب هو دواء من مضادات الالتهاب اللاستيرويدية من عائلة مثبطات كوكس-2. يستعمل عادة في علاج الأعراض الروماتيزمية (فصال والتهابات المفاصل الروماتيزمية). صنع من قبل الشركة الدولية فايزر.
الأسماء التجارية[عدل]
سيليبركس سيليكوكسيب
الاستخدامات الطبية[عدل]
يستخدم في علاج التهاب المفاصل والروماتويد وآلام الطمث (الدورة الشهرية) يستخدم سيليكوكسيب لعلاج التهاب المفاصل العظمي، التهاب المفاصل الروماتويدي، الألم الحاد، آلام الطمث، التهاب الفَقارِ المُقَسِّط ولتقليل عدد السلائل القولونية والسلائل في المستقيم للأشخاص المصابين بداء السلائل (زوائد) الورمية الغدية الوراثي.[3] ويمكن أن يستخدم للأطفال المصابين بالتهاب المفاصل الروماتيدي اليفعي الذين يزيد عمرهم عن سنتين ووزنهم عن 10 كيلوغرام (22 باوند).[3] يستخدم للآلام بعد العمليات الجراحية بصورة قد تكون مكافئة أو أقل كفاءة أو أعلى كفاءة للإبوبروفين.[4] يكون مشابها في تخفيف الألم لل باراسيتامول (أسيتامينوفين).[5] ويمثل أسيتامينوفين الخط العلاجي الأولي في التهاب المفاصل العظمي.[6][7] خصص بشكل أولي لتخفيف الألم مع تقليل الأعراض الجانبية المعدية المعوية التي ترافق العلاج بمضادات الالتهاب اللاستيرويدية. عمليا يكون استخدامه موجها للأشخاص الذين يحتاجون إلى تخفيف الألم بصورة منتظمة طويلة المدى. غالباً لا توجد مميزات (فوائد) لاستخدام سيليكوكسيب بصورة قصيرة المدى أو لتخفيف الألم الحاد على استخدام مضادات الالتهاب اللاستيرويدية الاعتيادية، باستثناء الحالات التي تتسبب فيها مضادات الالتهاب اللاستيرويدية اللا انتقائية أو ال أسبيرين تفاعلات جلدية (الشرى).
الأمراض النفسية[عدل]
تشير دلالات مبدئية إلى استخدامه في علاج عدد من الاضطرابات النفسية، ما يشمل: الاكتئاب، الاضطراب ذي اتجاهين والفصام.[8][9][10][11][12] داء السلائل الورمية الغدية الوراثي تم استخدامه لتقليل السلائل (الزوائد) في القولون والمستقيم في الأشخاص المصابين بداء السلائل الورمية الغدية الوراثي، ولكن لم يعرف عنه تقليل تفاقم أو تطور مرض السرطان [13] ولذلك لا يعد خيارا جيدا لهذا الهدف.[13]
الأعراض الجانبية[عدل]
لأنه يؤثر فقط على إنزيم كوكس 2 فإن آثاره الجانبية على الجهاز الهضمي أقل من مضادات الالتهاب اللاستيرويدية الأخرى كالكيتوبروفن والديكلوفين
القلبية الوعائية[عدل]
ترتبط مضادات الالتهاب اللاستيرويدية بزيادة خطر وقوع الأعراض الجانبية القلبية الوعائية الخثارية والتي قد تؤدي إلى الوفاة وتشمل احتشاء عضل القلب والسكتة. يمكن للخطر أن يزيد حدة بزيادة مدة الاستخدام أو بوجود أمراض أو عوامل اختطار قلبية وعائية سابقة. يجدر القيام بتقييم الوضع الفردي للمريض فيما يخص عوامل الاختطار القلبية الوعائية قبل وصف العلاج. قد يحدث العلاج ارتفاعاً في ضغط الدم أو تفاقم في فرط ضغط الدم (مضادات الالتهاب اللاستيرويدية قد تعطل التجاوب مع مدرات البول الثيازايدية أو مدرات البول العروية)، وقد تساهم في وقوع الطوارئ القلبية الوعائية؛ قم بفحص ضغط الدم واستخدم الدواء مع توخي الحذر لمرضى فرط ضغط الدم. يوصى استخدامه مع توخي الحذرلمرضى الودمة أو فشل القلب لأنه قد يؤدي إلى احتباس الصوديوم والسوائل. إن أثر الاستخدام طويل المدى على الاختطار القلبي الوعائي لدى الأطفال لم يقيم بعد. يوصى باستخدام أقل جرعة فعالة لأقصر وقت، بالتناسب مع الأهداف العلاجية لكل مريض، لا بد من استخدام بدائل علاجية تختار للمرضى ذوي الاختطار العالي للتقليل من اختطار الأمراض القلبية الوعائية.[14]
المعدية المعوية[عدل]
قد تزيد مضادات الالتهاب اللاستيرويدية من احتمال التقرحات والنزيف والتثقبات (قد تؤدي للوفاة) المعدية المعوية. هذه الأحداث قد تقع في أي وقت خلال العلاج دون سابق إنذار. استخدم مع توخي الحذر لأصحاب التاريخ المرضي في الجهاز المعدي المعوي (نزيف أو تقرحات)، العلاج المتزامن مع الأسبيرين، مضادات التجلط و/أو الكورتيكوستيرويدات، التدخين، الكحول، عند كبار السن أو المرضى الضعاف. استخدم الجرعة الفعالة الأقل لأقصر وقت، بالتناسب مع الأهداف العلاجية لكل مريض، يجب استخدام بدائل علاجية تختار للمرضى ذوي الاختطار العالي للتقليل من اختطار الأعراض الجانبية المعدية المعوية. يتفاقم الوضع سوءاً عندما تستخدم بالتزامن مع جرعة ≥325 مليغرام من الأسبيرين بما يخص اختطار التعقيدات المعدية المعوية (مثل: التقرحات)؛ ينصح بالعلاج المتزامن مع العلاجات الحامية للمعدة (مثل: مثبطات مضخة البروتونات).
عوارض دموية[عدل]
قد يؤدي إلى فقر الدم؛ قم بقياس الهيموجلوبين أو الهيماتوكريت للمرضى الذين استمروا على العلاج طويل المدى. لا يؤثر سيليكوكسيب عادة على اختبار زمن البروثرومبين (لتحديد استعداد الدم للتخثر)، اختبار زمن الثرومبوبلاستين الجزئي (لتحديد خصائص تخثر الدم) أو عد الصفائح؛ إذ لا يثبطت تكدس تجمع الصفائح عند تناول الجرعات المسموحة.
يجب توخي الحذر المسبق للمرضى الذين لديهم تاريخ مرضي للقرحة أو النزيف المعدي المعوي. قد يحدث استخدام مضادات الالتهابات اللاستيرويدية آثار ضارة معتدلة أو وخيمة من قصور الكبد أو التسمم المعدي المعوي مع أو بدون وجود أعراض تحذيرية.
فرط التحسس[عدل]
يحتوي سيليكوكسيب على سالفوناميد وقد يسبب تفاعلات لدى المرضى الذين يعانون من فرط التحسس للأدوية المحتوية على السالفوناميد. يضاف إلى ذلك منع الاستخدام للناس الذين يعانون من فرط تحسس وخيم لمضادات الالتهاب اللاستيرويدية الأخرى. من ناحية أخرى فإن له احتمالية ضئيلة (4% مقررة) لتطوير تفاعلات جلدية لدى الأشخاص الذين لديهم تاريخ لتفاعلات مماثلة تجاه الأسبيرين أومضادات الالتهاب اللاستيرويدية اللا انتقائية. قد تؤدي مضادات الالتهاب اللاستيرويدية إلى آثار جلدية ضارة تشمل التهاب الجلد التقشري، متلازمة ستيفينز-جونسون وتقشر الأنسجة المُتَمَوِّتَةِ البَشْرَوِيَّةِ التسممي. قد تحدث الآثار دون سابق إنذار أوعند المرضى الذين لم يتعرضوا سابقا لفرط تحسس تجاه السلفا. يجب إيقاف الاستخدام عند ظهور أول علامات للطفح (أو أي علامات أخرى لفرط التحسس).
النوبة القلبية والسكتة[عدل]
يزيد الكوكسيب (الذي ينتج السيليكوكسيب) اختطار المشاكل القلبية الوعائية الكبرى بنسبة تقارب ال 37%.[15] أما نابروكسين فلا يزيد خطر المشاكل الوائية القلبية الكبرى بصورة مؤثرة.[15] روفيكوكسيب (Vioxx) وهو مثبط كوكس -2 تم سحبه من الأسواق في عام 2004 بسبب الخطر الذي يسببه. ككل مضادات الالتهاب اللاستيرويدية المتواجدة في السوق الأمريكية، تحوم حول سيليكوكسيب تحذيرات من إدارة الغذاء والدواء حول الاختطار القلبي الوعائي والمعدي المعوي. في فبراير 2007 حذرت جمعية القلب الأمريكية بخصوص «المرضى الذين لديهم تاريخ طبي سابق من الأمراض القلبية الوعائية، تستخدم مثبطات كوكس-2 لأغراض تسكين الألم محدودا للمرضى الذين لا بديل مناسب لهم فعندها يستخدم فقط بالجرعات الأقل وفي أقصر وقت لازم للعلاج.»[16]
تختلف الآثار القلبية الوعائية لمثبطات الكوكس-2 اعتمادا على الدواء نفسه.[17] عند مقارنة مثبطات كوكس-2 الانتقائية الأخرى، مثل روفيكوكسيب بسيليكوكسيب فإنها تزيد بصورة واضحة في احتمالية التسبب باحتشاء القلب.[18] في أبريل 2005، وبعد تدقيق فاحص للبيانات، توصلت إدارة الغذاء والدواء إلى احتمالية «وجود آثار ضارة مرتبطة» بالصنف الدوائي«لزيادة الاختطار القلبي الوعائي لكافة مضادات الالتهاب اللاستيرويدية».[18] في عام 2006 أجري تحليل تلوي لدراسات عشوائية ووجد أن هنالك آثار دماغية وعائية مرتبطة بمثبطات الكوكس-2، ولكن لا وجود لآثار خطيرة كبيرة عند مقارنتها بمضادات الالتهاب اللاستيرويدية اللا انتقائية أو الغفل.[19]
موانع الاستخدام[عدل]
رغم أعراضه الجانبية القليلة على المعدة والجهاز الهضمي بالمقارنة مع مضادات الالتهاب اللاستيرويدية الأخرى إلا أنه يجب أن يستعمل بحذر في حالات القرحة المعدية أو النزيف بالجهاز الهضمي كما أنه يستعمل بحذر في حالات القصور الكبدي. بالنسبة للحمل فإن السيليكوكسيب يصنف ضمن المجموعة (ج) ويمنع استخدامه في الشهور الثلاث الأخيرة من الحمل
الجرعات والأشكال الدوائية المتوفرة[عدل]
كبسولات عيار 100مغ و200مغ حالات الالتهاب العظمي المفصلي كبسولة 100مغ كل 12ساعة حالات التهاب المفاصل الرثواني كبسولة 200مغ كل12ساعة
جرعة الأطفال[عدل]
لا ينصح باستخدامه في الأطفال أو البالغين أقل من 18 سنة.
آلية العمل[عدل]
مضاد الالتهاب[عدل]
سيليكوكسيب هو مثبط قابل للانعكاس وعالي الانتقائية لأيزوفورم كوكس-2 سيكلوكسيجينيز، يثبط سيليكوكسيب تحول حمض الأراكيدونك إلى مصادر البروستاجلاندين ولذلك فإن له استخدامات كخافض للحرارة ومسكن ومضاد للالتهاب. تقوم مضادات الالتهاب اللاستيرويدية اللا انتقائية (مثل الأسبيرين والنابروكسين والإبوبروفين) بتثبيط كلا كوكس-1 وكوكس -2. إن تثبيط كوكس-1 (و الذي لا يمكن الوصول إليه باستخدام سيليكوكسيب في تراكيزه العلاجية) يعمل على تثبيط إنتاج البروستاجلاندين وتثبيط إنتاج ثرومبوكسين A2 والذي يعمل كمفعل للصفائح الدموية. يعرف كوكس-1 تقليديا بأنه إنزيم خادم ينتج باستمرار ويلعب دورا في إنتاج الخلايا المخاطية المعدية المعوية والديناميكية الدموية الكلوية وتكون الخثرات من الصفائح الدموية.[20][21] بالمقابل يتواجد كوكس-2 بصورة كبيرة لدى الخلايا المشاركة في الالتهاب ويزيد تعبيره جينيا بوجود عديد الساريد الشحمي البكتيري، السيتوكينات، عوامل النمو ومحفزات الأورام.[20][22] يكون سيليكوكسيب أكثر قوة في التثبيط بمقدار 10-20 مرة لكوكس-2 مقارنة بتثبيطه لكوكس-1.[21][23] يرتبط الجزء القطبي من السلسة السلفوناميدية لسيليكوكسيب بمنطقة (المحبة للارتباط للماء) القريبة من المقر الرابط الفعال لكوكس-2.[24] نظريا تسمح هذه الانتقائية لسيليكوكسيب ومثبطات كوكس-2 الأخرى بتقليل الالتهاب والألم مع التقليل من التفاعلات الجانبية المعدية المعوية (مثل تقرحات المعدة) والتي تعد شائعة مع استخدام مضادات الالتهاب اللاستيرويدية اللا انتقائية.[25]
مضاد السرطان[عدل]
بسبب استخدامه لتقليل السلائل (الزوائد) القولونية، يؤثر سيليكوكسيب على الجينات والمسارات المرتبطة بتطور الالتهاب والتحول السرطاني للأورام الحميدة وليس النسيج الطبيعي.[26]
يرتبط سيليكوكسيب بكادهرين-11 وذلك قد يفسر تقليله لتقدم السرطان.[27]
العلاقة بين التركيب الكيميائي والنشاط[عدل]
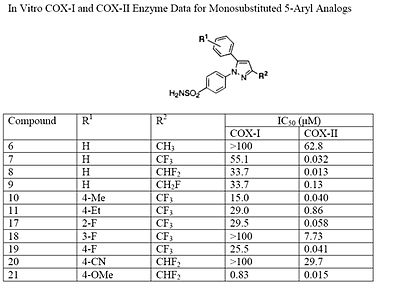
وجدت مجموعة البحث سيرل أن التثبيط الملائم لكوكس-2 يستلزم استقرار الحلقتين الأروماتيكيتين في مواقع متجاورة حول الحلقة المركزية. يمكن القيام بتعديلات مختلفة على 2,1-داي أريل بايرازول لاستنباط العلاقة بين التركيب والنشاط للسيليكوكسيب.[13] أظهر وجود بارا-سلفامويل فينل في الموقع 1 للبايرازول فعالية أكبر في التثبيط الانتقائي لكوكس-2 مقارنة بوجود بارا-ميثوكسي فينل (انظر التركيبان 1 و 2 في الأسفل). بالإضافة لهذا فإن وجود 4-(مثيل سالفونيل) فينل أو 4-سلفامويل فينل معروف بأهميته الإلزامية لتثبيط كوكس-2. وعلى سبيل المثال فإن تبديل أي من هذه الوحدات إلى 2SO3NHCH - يقلل من النشاط التثبيطي لكوكس-2 كما لوحظ على تركيز تثبيطي عال جدا -50. يوفر وجود ثنائي أو ثلاثي فلورو ميثل على الموقع 3 للبرازول زيادة في الانتقائية والفاعلية مقارنة بوجود مجموعة فلورو مثيل أو مثيل.[13]
سيليكوكسيب هو المركب 22(22في الجدول أدناه)؛ وجود ال 4-سلفامويل فينل على ال 1-برازول ضروري لتثبيط الكوكس-2 ووجود مجموعة 4-ميثل على 5-برازول التي لديها (إعاقة منخفضة في الفراغ المحيط بها عند تجاورها مع غيرها)مما يضاعف الفعالية، بينما توفر مجموعة 3-ثلاثي فلورو مثيل انتقائية وفعالية عالية. لتفسير انتقائية السيليكوكسيب فإنه من الضروري تحليل الفرق في الطاقة الحرة للارتباط بين جزيئات الدواء مع كلا إنزيمي كوكس-1 وكوكس-2. إن التعديلات التركيبية تؤكد على أهمية ربط الطرف 523 بجيب الربط الجانبي لإنزيم السيكلوأوكسيجنيز والذي قد يكون أيزولوسين في كوكس-1 أو فالين في كوكس-2.[28] ويبدو أن لهذه الطفرة دور في أفضلية كوكس-2 من خلال خلق إعاقة في الفراغ المحيط بين الاوكسيجين في السالفوناميد ومجموعة الميثل في ال (lle523)مما يحطم بفعالية ثبات المعقد سيليكوكسيب-كوكس-1.[28] لهذا فإنه من المنطقي توقع كون مثبطات كوكس-2 الانتقائية أكثر تشعبا من مضادات الالتهاب اللاستيرويدية اللا انتقائية.
التاريخ[عدل]
ظهر خصيمين حول اكتشاف السيليكوكسيب. اكتشف دانيال سايمونز من جامعة بريغهام يونغ إنزيم كوكس-2 في عام 1988.[29] وفي عام 1991 دخلت الجامعة في شراكة مع مونسانتو لتطوير أدوية لتثبيط الإنزيم. بعد ذلك بيعت مونسانتو لصالح شركة الصناعات الدوائية فايزر. في 2006 قامت جامعة بريغهام يونغ بمقاضاة فايزر لخرق في العقد مدعية بأن فايزر لم تدفع لها الحصة من الارباح حسب العقد.[30] تم التوصل إلى تسوية في أبريل 2012 وافقت من خلالها فايزر على دفع 450 مليون دولار أمريكي.[31][32] من الاكتشافات الأخرى المهمة حول كوكس-2 هي تلك التي قامت بها جامعة روتشيستر والتي سجلت براءة الاختراع باسمها.[33] بعدما تم تسجيل براءة الاختراع قامت الجامعة بمقاضاة سيرل (لاحقا فايزر) بالقضية المعنونة "University of Rochester v. G.D. Searle & Co., 358 F.3d 916 (Fed. Cir. 2004)". حكمت المحكمة لصالح سيرل في 2004، باعتبار ان الجامعة قدمت طريقة بدون وصف كتابي لمركب يستطيع تثبيط كوكس-2 وبذلك فإن براءة الاختراع غير معتبرة.[34][35]
بعد سحب روفيكوكسيب من الأسواق في عام 2004 زادت مبيعات سيليبريكس بصورة كبيرة. مع ذلك فإن نتائج ال APC التجريبية في ديسمبر من السنة ذاتها حذرت من أن سيليبريكس قد يؤدي إلى أخطار مشابهة لتلك الناجمة عن روفيكوكسيب وأصدرت فايزر تعليقا لإعلانات المستهلك بعد ذلك بقليل. بعد انخفاض معتبر في مبيعات سيليبريكس فإنها عادت للتعافي ووصلت إلى 2 بليون دولار أميريكي في 2006.[16] أعادت فايزر الإعلان عن سيليبريكس في المجلات في عام 2006،[36] وأعادة الإعلانات التلفزيونية في أبريل 2007 بصورة غير تقليدية؛ إعلان من دقيقتان ونصف ناقش الآثار الجانبية لسيليبريكس مقارنة بمضادات الاتهاب الأخرى. تلقى الإعلان الانتقادات من جمعية حماية المستهلك والتي اعتبرت المقارنات في الإعلان مضللة.[37] ردت فايزر على الجمعية بأنها كانت تبين بصدق المخاطر والفوائد لسيليبريكس كما نصت عليها إدارة الغذاء والدواء.[37]
في أواخر 2007 أصدرت فايزر إعلانا آخر لسيليبريكس على التلفزيون الأمريكي والذي ناقش الآثار الجانبية للدواء مقارنة بتلك لمضادات الالتهاب الأخرى.



المجتمع والثقافة[عدل]
دراسات الفعالية الملفقة[عدل]
في 11 مارس 2009 قام سكوت روبين، رئيس قسم الآلام الحادة في مركز بايستيت الطبي وسبرينغفيلد وماساتشسوتس بالتصريح بأن البيانات ل 22 من الدراسات المجراة حول فعالية الدواء (بالإضافة إلى أدوية أخرى مثل Vioxx) كانت ملفقة وأن الآثار المسكنة للدواء مبالغ في وصفها. وقد كان روبين يعمل ناطق باسم فايزر في السابق. لم يتم التقدم بأي من الدراسات المذكورة لإدارة الغذاء والدواء الأمريكية أو لمنظمات التنسيق التابعة للاتحاد الأوروبي قبل الموافقة على الدواء. قامت فايزر بإصدار توضيح عام «إنه لمن المخيب للأمل معرفة أفعال الدكتور روبين المزعومة. عندما قررنا دعم أبحاث الدكتور روبين كان يعمل في مركز طبي أكاديمي محترم وظهر أنه محقق حسن السمعة».[38][38]
التوافر[عدل]
تقوم فايزر بتسويق سيليكوكسيب تحت الاسم التجاري سيليبريكس ويتوافر على شكل كبسولات فموية تحتوي 50، 100، 200، 400 مليغرام من السيليكوكسيب.[39]
يتوافر بصلاحيات قانونية مختلفة كدواء جنيس تحت أسماء تجارية مختلفة،[40] في الولايات المتحدة تمت تغطية سيليكوكسيب بثلاث براءات اختراع، اثنان منهما انتهت صلاحيتها في 30 مايو 2014 وواحدة (US RE44048 [41]) يقرر أن تنتهي في 2 ديسمبر 2015 . في 13 مارس 2014 وجد أن براءة الاختراع تلك لم تكن صالحة لمضاعفة البراءة.[42] عند انتهاء صلاحية براءة الاختراع في 30مايو 2014 سمحت إدارة الغذاء والدواء بصدور أول أدوية جنيسة لسيليكوكسيب.[43]
البحث[عدل]
منع السرطان[عدل]
خضع دور السيليكوكسيب في خفض سرعة تطور سرطانات معينة للدراسات العديدة ولكن حتى الآن لا توجد توصيات طبية باستخدام هذا الدواء للتقليل من السرطانات.
تم التحقيق في امكانية استخدام السيليكوكسيب لتقليل احتمالية السرطان القولوني المستقيمي ولكن لم يوجد السيليكوكسيب أو أي دواء آخر لأجل هذا الاستخدام.[44] أظهرت التجارب السريرية على النطاق الضيق في المرضى ذوي الإخطار العالي جدا (الذين ينتمون إلى عائلات FAP) أن للسيليكوكسيب القدرة على منع نمو السلائل.و لذلك تم إجراء تجارب سريرية عشوائية على نطاق واسع.[45] أظهرت النتائج التقليل المتكرر للسلائل بنسبة 33 إلى 45% لدى المرضى المعالجين باستخدام سيليكوكسيب في كل يوم. من ناحية أخرى زادت تكرارية الحوادث قلبية وعائية بصورة معتبرة لدى المجموعات المعالجة باستخدام سيليكوكسيب. أظهر أسبيرين حماية مشابهة (أو أكثر قوة)[46][47][48] كما أظهر تأثيرات لحماية للقلب ويعد أقل سعرا بكثير من سيليكوكسيب، ولكن لم يتم إجراء تجارب سريرية مقارنة بين الدوائين حتى الآن.
معالجة السرطان[عدل]
وتختلف عن منع السرطان؛ معالجة السرطان تعني بعلاج الأورام التي تشكلت بالفعل وثبتت نفسها في داخل الجسم. يتم إجراء العديد من الأبحاث صلاحية السيليكوكسيب في مداواة هذه الحالة.[49] ولكن بدأ واضحاً خلال الدراسات الجزيئية في المختبر أن سيليكوكسيب يمكن أن يتفاعل مع مكونات أخرى داخل الخلية بالإضافة إلى مستهدفه الأشهر الكوكس-2. إن اكتشاف هذه المستهدفات الإضافية خلق جدلا واسعا وأصبح الافتراض الأولي بأن السيليكوكسيب يقلل من نمو الورم عن طريق تثبيط كوكس-2 مثيرا للخلاف.[50]
إن تثبيط الكوكس-2 بالتأكيد هو في غاية الأهمية لتحقيق الوظيفة المضادة للالتهاب والمسكنة للسيليكوكسيب ولكنه ليس من الواضح فيما إذا كان كوكس-2 يلعب دوراً سياديا في التأثير المضاد للسرطان. على سبيل المثال أظهرت دراسة حديثة على خلايا ورمية خبيثة أن لسيليكوكسيب القدرة على تثبيط نمو هذه الخلايا مخبريا، لكن كوكس-2 لم يلعب دورا في هذه النتيجة وعلى نحو مذهل أظهر السيليكوكسيب تأثيرات مضادة للسرطان حتى باستخدام خلايا لا تحتوي إنزيم الكوكس-2.[51]
أظهرت الدراسات باستخدام السيليكوكسيب المعدل كيميائيا دعما إضافيا للفكرة القائلة بأن مستهدفات أخرى بجانب الكوكس-2 تشكل أهمية للتأثير المضاد للسرطان للسيليكوكسيب. تم تكوين العديد من مضاهيات السيليكوكسيب عن طريق تعديلات بسيطة في التركيب الكيميائي.[52] حافظ بعض هذه المضاهيات على النشاط التثبيطي لكوكس-2 بينما العديد منها لم يفعل. ولكن عندما تم التحقيق في قدرة هذه المركبات على قتل الخلايا الورمية في المزرعة الخلوية لم تعتمد أبدا فعالية مضاد التورم على قدرته على تثبيط الكوكس-2. لم يكن مطلوبا إظهار القدرة على تثبيط الكوكس-2 لوجود التأثير المضاد للسرطان.[52][53] واحد من هذه المركبات (5,2- ثنائي المثيل سيليكوكسيب) والذي يخلو كليا من القدرة على تثبيط كوكس-2 أظهر نشاطا أقوى كمضاد للسرطان مقارنة بالسيليكوكسيب.[54]
المصادر والمراجع[عدل]
- Sources
- Malhotra S, Shafiq N, Pandhi P (2004). "COX-2 inhibitors: a CLASS act or Just VIGORously promoted". Medscape General Medicine. ج. 6 ع. 1: 6. PMC:1140734. PMID:15208519. مؤرشف من الأصل في 2009-02-02.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - Silverstein FE, Faich G, Goldstein JL؛ وآخرون (سبتمبر 2000). "Gastrointestinal toxicity with celecoxib vs nonsteroidal anti-inflammatory drugs for osteoarthritis and rheumatoid arthritis: the CLASS study: A randomized controlled trial. Celecoxib Long-term Arthritis Safety Study". Journal of the American Medical Association. ج. 284 ع. 10: 1247–55. DOI:10.1001/jama.284.10.1247. PMID:10979111. مؤرشف من الأصل في 2014-11-12.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - Solomon SD, McMurray JJ, Pfeffer MA؛ وآخرون (مارس 2005). "Cardiovascular risk associated with celecoxib in a clinical trial for colorectal adenoma prevention". New England Journal of Medicine. ج. 352 ع. 11: 1071–80. DOI:10.1056/NEJMoa050405. PMID:15713944.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - DiPiro, Joseph T. 2008
وصلات خارجية[عدل]
- Celebrex website run by فايزر
- FDA Alert for Practitioners on Celebrex (celecoxib), published December 17, 2004
- FDA Alert for Healthcare Professionals published July 4, 2005
- Largest systematic review of adverse renal and arrhythmia risk of Celecoxib and other COX-2 inhibitors, in JAMA 2006
- U.S. National Library of Medicine: Drug Information Portal - Celecoxib
- ^ Simon Maskell; Munir Pirmohamed (4 Mar 2022). "A reference set of clinically relevant adverse drug-drug interactionsxxx". Scientific Data (بالإنجليزية). 9 (1). DOI:10.1038/S41597-022-01159-Y. ISSN:2052-4463. QID:Q123478206.
- ^ celecoxibxxx (بالإنجليزية), QID:Q278487
- ^ ا ب "Celexoxib". The American Society of Health-System Pharmacists. مؤرشف من الأصل في 2019-05-20. اطلع عليه بتاريخ 2015-01-02.
- ^ Derry S, Moore RA (14 مارس 2012). Derry، Sheena (المحرر). "Single dose oral celecoxib for acute postoperative pain in adults". The Cochrane database of systematic reviews. ج. 3: CD004233. DOI:10.1002/14651858.CD004233.pub3. PMID:22419293.
- ^ Yelland MJ, Nikles CJ, McNairn N, Del Mar CB, Schluter PJ, Brown RM (2007). "Celecoxib compared with sustained-release paracetamol for osteoarthritis: a series of n-of-1 trials". Rheumatology. ج. 46 ع. 1: 135–40. DOI:10.1093/rheumatology/kel195. PMID:16777855.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Zhang W, Moskowitz RW, Nuki G, Abramson S, Altman RD, Arden N, Bierma-Zeinstra S, Brandt KD, Croft P, Doherty M, Dougados M, Hochberg M, Hunter DJ, Kwoh K, Lohmander LS, Tugwell P (سبتمبر 2007). "OARSI recommendations for the management of hip and knee osteoarthritis, part I: critical appraisal of existing treatment guidelines and systematic review of current research evidence". Osteoarthr. Cartil. ج. 15 ع. 9: 981–1000. DOI:10.1016/j.joca.2007.06.014. PMID:17719803.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Flood J (مارس 2010). "The role of acetaminophen in the treatment of osteoarthritis". The American journal of managed care. 16 Suppl Management: S48–54. PMID:20297877.
- ^ Fan X, Song X (فبراير 2013). "Review: non-steroidal anti-inflammatory drugs may reduce schizophrenia symptom severity in the short term when added to antipsychotics" (PDF). Evidence-Based Mental Health. ج. 16 ع. 1: 10. DOI:10.1136/eb-2012-100865. PMID:23093694. مؤرشف من الأصل (PDF) في 2016-03-04.
- ^ Müller N, Myint AM, Krause D, Weidinger E, Schwarz MJ (أبريل 2013). "Anti-inflammatory treatment in schizophrenia". Progress in Neuro-Psychopharmacology & Biological Psychiatry. ج. 42: 146–53. DOI:10.1016/j.pnpbp.2012.11.008. PMID:23178230.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Na KS, Lee KJ, Lee JS, Cho YS, Jung HY (يناير 2014). "Efficacy of adjunctive celecoxib treatment for patients with major depressive disorder: a meta-analysis". Progress in Neuro-Psychopharmacology & Biological Psychiatry. ج. 48: 79–85. DOI:10.1016/j.pnpbp.2013.09.006. PMID:24056287.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Rosenblat JD, Cha DS, Mansur RB, McIntyre RS (يناير 2014). "Inflamed moods: A review of the interactions between inflammation and mood disorders". Progress in Neuro-Psychopharmacology & Biological Psychiatry. ج. 53C: 23–34. DOI:10.1016/j.pnpbp.2014.01.013. PMID:24468642.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Fond G, Hamdani N, Kapczinski F, Boukouaci W, Drancourt N, Dargel A, Oliveira J, Le Guen E, Marlinge E, Tamouza R, Leboyer M (مارس 2014). "Effectiveness and tolerance of anti-inflammatory drugs' add-on therapy in major mental disorders: a systematic qualitative review". Acta Psychiatrica Scandinavica. ج. 129 ع. 3: 163–79. DOI:10.1111/acps.12211. PMID:24215721.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب ج د "Celecoxib". The American Society of Health-System Pharmacists. مؤرشف من الأصل في 2019-05-20. اطلع عليه بتاريخ 2014-04-21.
- ^ Solomon SD, McMurray JJ, Pfeffer MA, Wittes J, Fowler R, Finn P, Anderson WF, Zauber A, Hawk E, Bertagnolli M (2005). "Cardiovascular risk associated with celecoxib in a clinical trial for colorectal adenoma prevention". The New England Journal of Medicine. ج. 352 ع. 11: 1071–1080. DOI:10.1056/NEJMoa050405. PMID:15713944.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب Bhala N, Emberson J, Merhi A, Abramson S, Arber N, Baron JA, Bombardier C, Cannon C, Farkouh ME, FitzGerald GA, Goss P, Halls H, Hawk E, Hawkey C, Hennekens C, Hochberg M, Holland LE, Kearney PM, Laine L, Lanas A, Lance P, Laupacis A, Oates J, Patrono C, Schnitzer TJ, Solomon S, Tugwell P, Wilson K, Wittes J, Baigent C (31 أغسطس 2013). "Vascular and upper gastrointestinal effects of non-steroidal anti-inflammatory drugs: meta-analyses of individual participant data from randomised trials". Lancet. ج. 382 ع. 9894: 769–79. DOI:10.1016/S0140-6736(13)60900-9. PMC:3778977. PMID:23726390.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب Antman EM، وآخرون (مارس 2007). "Use of nonsteroidal antiinflammatory drugs: an update for clinicians: a scientific statement from the American Heart Association" (PDF). Circulation. ج. 115 ع. 12: 1634–42. DOI:10.1161/circulationaha.106.181424. مؤرشف من الأصل (PDF) في 2016-06-01.
- ^ Kimmel SE, Berlin JA, Reilly M, Jaskowiak J, Kishel L, Chittams J, Strom BL (2005). "Patients exposed to rofecoxib and celecoxib have different odds of nonfatal myocardial infarction". Ann. Intern. Med. ج. 142 ع. 3: 157–64. DOI:10.7326/0003-4819-142-3-200502010-00005. PMID:15684203.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب Mukherjee D, Nissen SE, Topol EJ (2001). "Risk of cardiovascular events associated with selective COX-2 inhibitors". JAMA. ج. 286 ع. 8: 954–9. DOI:10.1001/jama.286.8.954. PMID:11509060.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Chen LC, Ashcroft DM (2006). "Do selective COX-2 inhibitors increase the risk of cerebrovascular events? A meta-analysis of randomized controlled trials". J Clin Pharm Ther. ج. 31 ع. 6: 565–76. DOI:10.1111/j.1365-2710.2006.00774.x. PMID:17176361.
- ^ ا ب Mathew ST, Devi S G, Prasanth VV, Vinod B (2011). "Efficacy and Safety of COX-2 Inhibitors in the Clinical Management of Arthritis: Mini Review". ISRN pharmacology. ج. 2011: 480291. DOI:10.5402/2011/480291. PMC:3197256. PMID:22084715.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ ا ب Katzung، edited by Bertram G. (2007). Basic & clinical pharmacology (ط. 10th). New York: McGraw-Hill Medical. ص. 579. ISBN:9780071451536.
{{استشهاد بكتاب}}:|الأول=باسم عام (مساعدة) - ^ Shi S, Klotz U (مارس 2008). "Clinical use and pharmacological properties of selective COX-2 inhibitors". European journal of clinical pharmacology. ج. 64 ع. 3: 233–52. DOI:10.1007/s00228-007-0400-7. PMID:17999057.
- ^ Conaghan PG (يونيو 2012). "A turbulent decade for NSAIDs: update on current concepts of classification, epidemiology, comparative efficacy, and toxicity". Rheumatology international. ج. 32 ع. 6: 1491–502. DOI:10.1007/s00296-011-2263-6. PMC:3364420. PMID:22193214.
- ^ DiPiro, Joseph T., Robert L. Talbert, Gary C. Yee, Gary R. Matzke, Barbara G. Wells, and L. Michael Posey. Pharmacotherapy A Pathophysiologic Approach (Pharmacotherapy (Dipiro) Pharmacotherapy (Dipiro)). New York: McGraw-Hill Medical, 2008. Print.
- ^ Bhatt DL, Scheiman J, Abraham NS, Antman EM, Chan FK, Furberg CD, Johnson DA, Mahaffey KW, Quigley EM, Harrington RA, Bates ER, Bridges CR, Eisenberg MJ, Ferrari VA, Hlatky MA, Kaul S, Lindner JR, Moliterno DJ, Mukherjee D, Schofield RS, Rosenson RS, Stein JH, Weitz HH, Wesley DJ (28 أكتوبر 2008). "ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents". Journal of the American College of Cardiology. ج. 52 ع. 18: 1502–17. DOI:10.1016/j.jacc.2008.08.002. PMID:19017521.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Half E, Arber N (فبراير 2009). "Colon cancer: preventive agents and the present status of chemoprevention". Expert opinion on pharmacotherapy. ج. 10 ع. 2: 211–9. DOI:10.1517/14656560802560153. PMID:19236194.
- ^ Assefnia S, Dakshanamurthy S, Guidry Auvil JM, Hampel C, Anastasiadis PZ, Kallakury B, Uren A, Foley DW, Brown ML, Shapiro L, Brenner M, Haigh D, Byers SW (مارس 2014). "Cadherin-11 in poor prognosis malignancies and rheumatoid arthritis: common target, common therapies". Oncotarget. ج. 5 ع. 6: 1458–74. PMID:24681547.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب Price ML, Jorgensen WL (2001). "Rationale for the observed COX-2/COX-1 selectivity of celecoxib from Monte Carlo simulations". Bioorg. Med. Chem. Lett. ج. 11 ع. 12: 1541–4. DOI:10.1016/s0960-894x(00)00522-9. PMID:11412976.
- ^ Yajnik J (27 أكتوبر 2006). "University sues Pfizer over COX-2 research". The Scientist. مؤرشف من الأصل في 2009-02-03. اطلع عليه بتاريخ 2010-11-11.
- ^ Linda Thomson (28 أكتوبر 2009). "Judge orders Pfizer to pay BYU $852K for suit delays". Deseret News. مؤرشف من الأصل في 2018-06-28.
- ^ Tom Harvey (1 مايو 2012). "Pfizer, BYU settle Celebrex lawsuit for $450M". The Salt Lake Tribune. مؤرشف من الأصل في 2016-03-03.
- ^ Associated Press, May 1, 2012 Pfizer Settles B.Y.U. Lawsuit Over Development of Celebrex نسخة محفوظة 27 ديسمبر 2017 على موقع واي باك مشين.
- ^ U.S. Patent 6٬048٬850
- ^ Reach-Through Claims Declared Invalid نسخة محفوظة 22 فبراير 2014 على موقع واي باك مشين.
- ^ Ranjana Kadle (2004) CAFC Court Decision Reach-Through Claims Declared Invalid[وصلة مكسورة] "نسخة مؤرشفة" (PDF). مؤرشف من الأصل في 2016-03-04. اطلع عليه بتاريخ 2016-01-24.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ Berenson A (29 أبريل 2006). "Celebrex Ads Are Back, Dire Warnings and All". The New York Times. مؤرشف من الأصل في 2016-01-07.
- ^ ا ب Saul S (10 أبريل 2007). "Celebrex Commercial, Long and Unconventional, Draws Criticism". The New York Times. مؤرشف من الأصل في 2018-01-17.
- ^ ا ب "Doctor Admits Pain Studies Were Frauds, Hospital Says"، نيويورك تايمز، 11 مارس 2009، مؤرشف من الأصل في 2019-02-07، اطلع عليه بتاريخ 2015-12-27
- ^ CELEBREX indications and dosing: Official Pfizer site نسخة محفوظة 21 أبريل 2014 على موقع واي باك مشين.
- ^ Celecoxib at drugs.com نسخة محفوظة 10 مارس 2016 على موقع واي باك مشين.
- ^ US Re-issued Patent RE44048 نسخة محفوظة 09 يناير 2017 على موقع واي باك مشين.
- ^ Roger Parloff for Fortune Magazine. March 13, 2014 Judge cuts 18 months off patent life of Pfizer's Celebrex نسخة محفوظة 25 يوليو 2017 على موقع واي باك مشين.
- ^ FDA Press Release, May 30, 2014. FDA approves first generic versions of celecoxib نسخة محفوظة 12 يناير 2017 على موقع واي باك مشين. [وصلة مكسورة]
- ^ Rial NS، وآخرون (أغسطس 2012). "Clinical end points for developing pharmaceuticals to manage patients with a sporadic or genetic risk of colorectal cancer". Expert Rev Gastroenterol Hepatol. ج. 6 ع. 4: 507–17. DOI:10.1586/egh.12.23. PMID:22928902.
- ^ Bertagnolli MM, Eagle CJ, Zauber AG, Redston M, Solomon SD, Kim K, Tang J, Rosenstein RB, Wittes J, Corle D, Hess TM, Woloj GM, Boisserie F, Anderson WF, Viner JL, Bagheri D, Burn J, Chung DC, Dewar T, Foley TR, Hoffman N, Macrae F, Pruitt RE, Saltzman JR, Salzberg B, Sylwestrowicz T, Gordon GB, Hawk ET (أغسطس 2006). "Celecoxib for the prevention of sporadic colorectal adenomas". نيو إنغلاند جورنال أوف ميديسين. ج. 355 ع. 9: 873–84. DOI:10.1056/NEJMoa061355. PMID:16943400.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Baron JA, Cole BF, Sandler RS, Haile RW, Ahnen D, Bresalier R, McKeown-Eyssen G, Summers RW, Rothstein R, Burke CA, Snover DC, Church TR, Allen JI, Beach M, Beck GJ, Bond JH, Byers T, Greenberg ER, Mandel JS, Marcon N, Mott LA, Pearson L, Saibil F, van Stolk RU (2003). "A randomized trial of aspirin to prevent colorectal adenomas". نيو إنغلاند جورنال أوف ميديسين. ج. 348 ع. 10: 891–9. DOI:10.1056/NEJMoa021735. PMID:12621133.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Sandler RS, Halabi S, Baron JA, Budinger S, Paskett E, Keresztes R, Petrelli N, Pipas JM, Karp DD, Loprinzi CL, Steinbach G, Schilsky R (2003). "A randomized trial of aspirin to prevent colorectal adenomas in patients with previous colorectal cancer". نيو إنغلاند جورنال أوف ميديسين. ج. 348 ع. 10: 883–90. DOI:10.1056/NEJMoa021633. PMID:12621132.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Bosetti C, Talamini R, Franceschi S, Negri E, Garavello W, La Vecchia C (2003). "Aspirin use and cancers of the upper aerodigestive tract". British Journal of Cancer. ج. 88 ع. 5: 672–4. DOI:10.1038/sj.bjc.6600820. PMC:2376339. PMID:12618872.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Dannenberg AJ, Subbaramaiah K (ديسمبر 2003). "Targeting cyclooxygenase-2 in human neoplasia: rationale and promise". خلية سرطانية. ج. 4 ع. 6: 431–6. DOI:10.1016/S1535-6108(03)00310-6. PMID:14706335. مؤرشف من الأصل في 2018-03-17.
- ^ Schönthal AH (ديسمبر 2007). "Direct non-cyclooxygenase-2 targets of celecoxib and their potential relevance for cancer therapy". Br. J. Cancer. ج. 97 ع. 11: 1465–8. DOI:10.1038/sj.bjc.6604049. PMC:2360267. PMID:17955049.
- ^ Chuang HC, Kardosh A, Gaffney KJ, Petasis NA, Schönthal AH (2008). "COX-2 inhibition is neither necessary nor sufficient for celecoxib to suppress tumor cell proliferation and focus formation in vitro". Molecular Cancer. ج. 7 ع. 1: 38. DOI:10.1186/1476-4598-7-38. PMC:2396175. PMID:18485224. مؤرشف من الأصل في 2015-09-05.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ ا ب Zhu J, Song X, Lin HP, Young DC, Yan S, Marquez VE, Chen CS (ديسمبر 2002). "Using cyclooxygenase-2 inhibitors as molecular platforms to develop a new class of apoptosis-inducing agents" (PDF). Journal of the National Cancer Institute. ج. 94 ع. 23: 1745–57. DOI:10.1093/jnci/94.23.1745. PMID:12464646. مؤرشف من الأصل (PDF) في 2016-01-07.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Schönthal AH, Chen TC, Hofman FM, Louie SG, Petasis NA (فبراير 2008). "Celecoxib analogs that lack COX-2 inhibitory function: preclinical development of novel anticancer drugs". Expert Opinion on Investigational Drugs. ج. 17 ع. 2: 197–208. DOI:10.1517/13543784.17.2.197. PMID:18230053.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Schönthal AH (2006). "Antitumor properties of dimethyl-celecoxib, a derivative of celecoxib that does not inhibit cyclooxygenase-2: implications for glioma therapy". Neurosurgical Focus. ج. 20 ع. 4: E21. DOI:10.3171/foc.2006.20.4.14. PMID:16709027.
| في كومنز صور وملفات عن: سيليكوكسيب |

