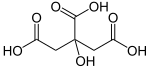
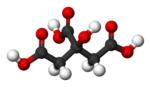
حمض الليمون
| حمض الليمون | |
|---|---|
| الاسم النظامي (IUPAC) | |
2-hydroxypropane- 1,2,3-tricarboxylic acid |
|
| أسماء أخرى | |
حمض الستريك Citric acid |
|
| المعرفات | |
| رقم CAS | 77-92-9 |
| بوب كيم (PubChem) | 311 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | C6H8O7 |
| الكتلة المولية | 192.124 g/mol (لا مائي) 210.14 g/mol (monohydrate) |
| المظهر | بلورات صلبة بيضاء |
| الكثافة | 1.665 غ/سم³ |
| نقطة الانصهار | 153 |
| نقطة الغليان | يتفكك عند 175 °م (448 كيلفن) |
| الذوبانية في الماء | 133 غ/100 مل (22°م) |
| الذوبانية في رباعي هيدرو الفوران، إيثانول، ميثانول | لا مائي: THF 1.80 M، إيثانول 1.86 M، ميثانول 3.08 M [3] monohydrate: THF 1.524 M, ethanol 1.776 M, methanol 2.267 M [4] |
| حموضة (pKa) | pKa1=3.15 pKa2=4.77 pKa3=6.40 |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| NFPA 704 |
|
| مركبات متعلقة | |
| مركبات ذات علاقة | سترات الصوديوم ، سترات الكالسيوم |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
حمض الليمون أو حمض الستريك (أو ملح الليمون) هو حمض عضوي ضعيف يوجد في الموالح. وهو مادة حافظة طبيعية. ويستخدم لإضافة مذاق حمضي للأطعمة والمشروبات. في الكيمياء الحيوية هو وسيط مهم في دورة حمض الستريك وبالتالي فهو يتكون في كل التمثيل الغذائي لكل شيء حي تقريباً. ويخدم أيضاً كعامل منظف للبيئة ويعمل كمضاد للأكسدة.وهو حامض موجود على شكل لامائي وهيدرات احادية.
الخواص[عدل]

حمض الليمون - أو ما يسمى بحمض الستريك - عبارة عن بلورات عديمة اللون شفافة، عند طحنه؛ يتحول إلى حبيبات بلورية بيضاء أو مسحوق أبيض ناعم تتزهر في الهواء الجاف، وهي شديدة الانحلال بالماء، وتنحل بسهولة في الكحول، ويمتاز بطعمه الحامضي الشديد.
تحفظ المادة عادة في عبوات محكمة الإغلاق في أماكن جافة وباردة.
الاستعمالات[عدل]
يستعمل حمض الليمون صيدلانياً كمادة محمضة ومضادة للأكسدة، كما تستعمل أيضاً كمادة موقية، وكعامل ممخلب، وكمنكه.وكذلك يضاف إلى بعض الأغذية بغرض إضافة الطعم الحامضي لها، وكذلك تضاف إلى الصلصة الخاصة بالسلطات لتعزيز النكهة.ويستخدم في تركيبات المعالجة للبشرة والتفتيح
المراجع[عدل]
- ^ أ ب citric acid (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ "Solubility of citric acid anhydrous in non-aqueous solvents". مؤرشف من الأصل في 2020-03-09.
- ^ "Solubility of citric acid monohydrate in non-aqueous solvents". مؤرشف من الأصل في 2020-03-09.
| في كومنز صور وملفات عن: حمض الليمون |