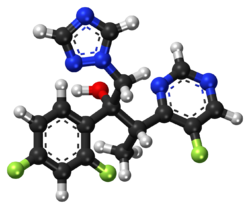
فوريكونازول
المظهر
فوريكونازول Voriconazole (vor-i-KON-a-zole،الزمرة الدوائية مضاد فطري اسم العلامة التجارية Vfend فايزر) هو ترايازول
والاستعمال الطبي
[عدل]داء الرشاشيات الغازية
[عدل]
أصبح Voriconazole المعيار الجديد للرعاية في علاج الغازية داء الرشاشيات، والتي قد تحدث نقص المناعة في المرضى، بما في ذلك الاعضاء المختلفة وراثيا BMT، دواء مضاد للفطور، يستخدم لعلاج الأسبيرجيلوس الغازي، لعلاج الانتانات الفطرية الخطيرة الناجمة عن المغزليات Fusarium أو عن Scedosporium المعندة على الأدوية الأخرى.[3]
الاستخدام خلال الحمل
[عدل]ينتمي هذا المحضر للمجموعة D.
مضادات الاستطباب
[عدل]- فرط الحساسية لهذا المحضر أو لأحد مكوناته.
- الحمل
- لا يجوز إشراكه مع الأدوية التي تسبب تطاول الفاصلة QT ، أو مع الباربيتورات أو مع الكاربامازيين أو مع قلويدات الإرغوت أو مع الريفامبين أو مع الريفابيوتين.
- تحوي أقراصه اللاكتوز لذلك يجب عدم إعطائها للمريض المصاب بعدم تحمل الغالاكتوز الوراثي أو بسوء امتصاص الغلوكوز - الغالاكتوز.
التأثيرات الجانبية
[عدل]تحدث بنسبة تزيد عن 10%
- عينية: اضطرابات عينية.
تحدث بنسبة 1 – 10%
- قلبية وعائية: تسرع القلب، ارتفاع توتر شرياني، انخفاض توتر شرياني، توسع وعائي، وذمة محيطية.
- عصبية مركزية: حمى، قشعريرات، صداع، أهلاس، دوام.
- جلدية: طفح، حكة.
- غدية استقلابية: نقص بوتاس الدم، نقص مغنيزيوم الدم.
- هضمية: غثيان، إقياء، ألم بطني، إسهال، جفاف الفم.
- دموية: قلة صفيحات.
- كلوية: قصور كلوي حاد.
- كبدية: ارتفاع تراكيز الخمائر الناقلة للأمين والفوسفاتاز القلوية، يرقان ركودي..[4]
الثباتية
[عدل]- احفظ الأقراص والبودرة بدرجة حرارة الغرفة 15 – 30 مْ.
- مدد محتوى الفيال (200 ملغ) ب 19 مل من الماء المعقم المعد للحقن (أصبح التركيز 10 ملغ|مل) ومن ثم مدده حتى تركيز 0,5 – 5 ملغ|مل قبل تسريبه، واعلم أن هذا المحلول الممدد يبقى ثابتاً وصالحاً للاستخدام لمدة 24 ساعة فيما لو حفظ بالبراد بدرجة حرارة 2 – 8 مْ.
آلية التأثير والحرائك الدوائية
[عدل]- يثبط هذا المحضر فعالية سيتوكروم F450 ضمن الفطر الممرض وينقص معدل تركيب إرغوستيرول الذي يدخل في بنية غشائه الخلوي ويثبط عملية تصنيعه (تصنيع الغلاف).
- يمتص بشكل جيد عبر الجهاز الهضمي، ويستقلب في الكبد، ويطرح مع البول على شكل مستقلبات غير فعالة.[5]
الجرعة والمستحضرات الصيدلانية
[عدل]- الأطفال بأعمار 12 سنة أو أكثر والبالغين: في البداية نعطي جرعة تحميل وريدية مقدارها 6 ملغ|كغ ثم نكررها بعد 12 ساعة وبعد ذلك يعطى (وريدياً) بجرعة استمرارية مقدارها 4 ملغ|كغ كل 12 ساعة.
- يمكن التحول لاحقاً إلى المعالجة الفموية بإعطاء 200 ملغ كل 12 ساعة للمريض الذي يزيد وزنه عن 40 كغ و100 ملغ كل 12 ساعة للمريض الذي يقل وزنه عن 40 كغ.
- ملحوظة: تسرب جرعته الوريدية على مدى 1 – 2 ساعة بينما تعطى جرعته الفموية قبل الطعام بساعة أو بعده بساعة.
- يجب مراقبة الوظيفة الكبدية والكلوية وإجراء فحص بصري بشكل دوري خلال فترة استخدام هذا المحضر.
- يحضر على شكل بودرة معدة للحقن 200 ملغ وعلى شكل أقراص عيار 50 ملغ و200 ملغ.
المراجع
[عدل]- ^ Simon Maskell; Munir Pirmohamed (4 Mar 2022). "A reference set of clinically relevant adverse drug-drug interactions". Scientific Data (بالإنجليزية). 9 (1). DOI:10.1038/S41597-022-01159-Y. ISSN:2052-4463. QID:Q123478206.
- ^ Drug Indications Extracted from FAERS، DOI:10.5281/ZENODO.1435999، QID:Q56863002
- ^ Herbrecht R, Denning D, Patterson T, Bennett J, Greene R, Oestmann J, Kern W, Marr K, Ribaud P, Lortholary O, Sylvester R, Rubin R, Wingard J, Stark P, Durand C, Caillot D, Thiel E, Chandrasekar P, Hodges M, Schlamm H, Troke P, de Pauw B; Invasive Fungal Infections Group of the European Organisation for Research and Treatment of Cancer and the Global Aspergillus Study Group (8 أغسطس 2002). "Voriconazole versus amphotericin B for primary therapy of invasive aspergillosis". N Engl J Med. ج. 347 ع. 6: 408–15. DOI:10.1056/NEJMoa020191. PMID:12167683.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Epaulard O, Saint-Raymond C, Villier C, Charles J, Roch N, Beani JC, Leccia MT (سبتمبر 2010). "Multiple aggressive squamous cell carcinomas associated with prolonged voriconazole therapy in four immunocompromised patients". Clin Microbiol Infect. ج. 16 ع. 9: 1362–1364. DOI:10.1111/j.1469-0691.2009.03124.x.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Smith J, Safdar N, Knasinski V, Simmons W, Bhavnani S, Ambrose P, Andes D (أبريل 2006). "Voriconazole therapeutic drug monitoring". Antimicrob Agents Chemother. ج. 50 ع. 4: 1570–2. DOI:10.1128/AAC.50.4.1570-1572.2006. PMC:1426935. PMID:16569888. مؤرشف من الأصل في 2019-12-11.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)
| فوريكونازول في المشاريع الشقيقة: | |
| |