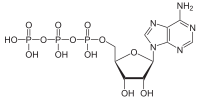
أدينوسين ثلاثي الفوسفات
| أدينوسين ثلاثي الفوسفات | |
|---|---|
 |
 |
| الخواص | |
| الصيغة الجزيئية | C₁₀H₁₆N₅O₁₃P₃[1] |
| المعرفات | |
| CAS | 56-65-5 |
| بوب كيم | 5957 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
الأدينوسين ثلاثيُّ الفوسفات (بالإنجليزية: Adenosine triphosphate) (ATP) نكليوتيد تختزن فيه الطاقة (حرارة) على شكل رابطة غنية بالطاقة بين مجموعة فوسفات غير عضوي ومركب أدينوسين ثنائي الفوسفات ADP.يتواجد الأدينوسين ثلاثي الفوسفات في جميع خلايا جسم الكائن الحي، وبالطبع في خلايا الإنسان. يتم تكوينه في متقدرات الخلايا ويختزن في داخل الخلية خارج المتقدرات . بهذا يعتبر الأدينوسين ثلاثي الفوسفات"بطارية الخلية" التي تمدها بالطاقة.
ويتكون مركب أدينوسين ثلاثي الفوسفات عن طريق تفاعل الأدينوسين ثنائي الفوسفات مع جزيء الفوسفات في وجود طاقة عالية ناتجة عن الطاقة التي اكتسبتها الإلكترونات بعد الإثارة، طبقا للتفاعل:
- P + ADP + طاقة (من فوسفات الكرياتين) ----> ATP
يتألف ATP من القاعدة النيتروجينية أدينين، وسكر الريبوز، وثلاث مجموعات فوسفات . تحتوي الروابط بين مجموعات الفوسفات علي طاقة كيميائية مختزنة بكميات كبيرة التي يمثلها الرمز ΔG . ويمكن لهذه الطاقة أن تنطلق عند تحطم إحدى روابط الفوسفات. فعند تحطم الرابطة بين مجموعتي الفوسفات الثانية والثالثة، تتحرر طاقة مقدارها 12.000 كالوري أو 7.3 كيلو سعرة/ مول تحت الظروف القياسية وذلك أكبر بكثير من الطاقة المخزونة في الرابطة الكيميائية الاعتيادية للمركبات العضوية الأخرى؛ ولذلك أعطيت المصطلح الرابطة العالية الطاقة [3]، وينتج مركب لأدينوسين ثنائي الفوسفات. وقد تنفك الرابطة بين مجموعتي الفوسفات الثانية والأولي لينتج مركب AMP (أدينوسين أحادي الفوسفات ) .
ويتم تكوين ATP في الميتوكوندريات عن طريق أكسدة الجلوكوز فتنتقل الطاقة المختزنة في الروابط الكيميائية الموجودة فيه لتخزن في جزيء ادينوسين ثلاثي الفوسفات ATP ؛ فإن الخلية تخزن طاقتها في هيئة ATP ، ويعتبر جزيء الATP هو "بطارية الخلية" التي تمدها بالطاقة لكي تقوم بوظائفها الحيوية. الروابط الفوسفاتية الموجودة في ادينوسين ثلاثي الفوسفات هي عالية الطاقة وقابلة بسهولة للتفكك أيضاً ، بحيث أنها يمكن أن تتفكك آنياً كلما دعت الحاجة إلى طاقة تحفز التفاعلات الخلوية الأخرى ، أو عند احتياج طاقة لتشغيلخلايا العضلات. لا يتم تخليق ال ATP مباشرة من الجلوكوز وانما عن طريق تخليق مادتين وسطيتين هما FADH و NADH خلال دورة تسمى دورة حمض الستريك ، وهذه جزيئات تتميز أيضا باحتوائهما على طاقة عالية . بعد إنتاج FADH و NADH يمكنهما تخزين طاقة في الخلية أو يمكنهما أيضا في حالة أداء الشخص لمجهود حركي التحول إلى ATP مع إنتاج طاقة ؛ هذه عملية احراق كامل للجولوكوز ( في صورتيه كـ FADH و NADH ) وهي عملية أكسدة تسمى سلسلة تنفس ؛ تتأكسد كل من المادتين FADH و NADH بالأكسجين الآتي من التنفس فتنتج طاقة (مثل ضبط درجة حرارة الجسم عند 37 درجة مئوية ؛ مناسبة يقيام الخلايا بوظائفها المختلفة) ، كما تنتج في نفس الوقت جزيئات ATP للتخزين (يعتبر الـ ATP محطة طاقة الخلية أو بطارية الخلية) ، وهو الذي يشغل الخلايا العضلية لتنقبض ويتحرك الجسم.
عندما يُطلق أدينوسين ثلاثي الفوسفات ATP طاقته فإنه يفك أحد مجموعات الفوسفات فيه ويتكون عند ذاك أدينوسين ثنائي الفوسفات ADP . ولكن سرعان -في أقل من عدةثوان - تقوم جزيئات أخرى مخزونة وهي فوسفات الكرياتين KrP بإعطاء مجموعة الفوسفات تبعها إلى الـ ADP فيتحدا معا لإعادة توليد ATP ليكون باستمرار على اهبة الاستعداد لمد الخلية بالطاقة . ولهذه الأسباب يسمى الـ ATP باسم عملة الطاقة energy currency "للخليةّ" لأنه من الممكن صرفه وإعادة تكوينه مرة بعد أخرى . ولا تطول دورته في العادة لوقت إجمالي أكثر من بضع ثواني فقط .
ويعد الادينوسين ثلاثي الفوسفات من الجزيئات الناقلة الأكثر انتشاراً في خلايا جميع المخلوقات الحية.
استعمالات ATP في الوظائف الخلوية والوظائف الاستقلابية في الجسم[عدل]
يستعمل الـ ATP في ثلاث مجموعات رئيسية من الوظائف الخلوية وهي:
- النقل الغشائي.
- تركيب المركبات الخلوية.
- حركة الجسم.
وهذه الاستعمالات المختلفة الثلاثة هامة لكل من:
- تجهيز الطاقة اللازمة لنقل الصوديوم خلال غشاء الخلية.
- وتنشيط الريبوسومات لتكوين البروتين .
- وتجهيز الطاقة الضرورية للحركة بواسطة العضلات.
وبالإضافة إلى كون طاقة الـ ATP ضرورية للغشاء الخلوي عند نقله الصوديوم فهي ضرورية أيضاً بصورة مباشرة أو غير مباشرة لنقل أيونات البوتاسيوم وأيونات الكالسيوم وأيونات الفوسفات وأيونات الكلوريد واليورات وأيونات الهيدروجين والعديد والأيونات والمواد الأخرى أيضاً.[4] والنقل عبر غشاء الخلية مهم جداً لوظائف الخلية لدرجة أن البعض منها مثل خلايا النبيبات الكلوية تستخدم حوالي 80 % من الـ ATP الذي يتم توليده فيها لهذا الغرض وحده . وبالإضافة لتكوين الخلايا للبروتينات فإنها تقوم أيضاً بتوليد الشحوم الفسفورية والكوليستيرول والبيروينات purines والبيريميدينات ومجموعة أخرى من المواد. ويحتاج تكوين أي مركب كيميائي تقريباً إلى طاقة؛ فمثلاً يمكن أن يكون جزيء بروتين واحد مركباً من عدة آلاف من الأحماض الأمينية ملتصقة ببعضها البعض بارتباطات ببتيدية . ويحتاج تكوين كل واحد من هذه الارتباطات إلى تحليل ثلاثة ارتباطات عالية الطاقة. ولذلك لا بد من إطلاق عدة آلاف من جزيئات الـ ATP أو من جزيئات ثلاثي فوسفات الجوانوزين GTP المقارن لتطلق طاقاتها لكي تولد أحد جزيئات البروتين . وفي الواقع تستعمل بعض الخلايا 75 % تقريباً ندمن كل الـ ATP الذي يتكون فيها لتركيب المركبات الكيميائية الجديدة فيها . ويصدق هذا بصورة خاصة أثناء مرحلة نمو الخلايا.[5] والاستعمال الرئيسي الأخير للـ ATP هو تجهيز الطاقة لبعض الخلايا لتوليد عمل آلي؛ حيث يحتاج تقلض الليف العضلي إلى استهلاك كميت كبيرة من الـ ATP. وتقوم بعض الخلايا الأخرى بأعمال آلية بطرق خاصة أخرى كالحركات الهدبية والأميبية؛ ومصدر الطاقة لكل هذه الأنواع من الأعمال الآلية هو الـ ATP .
وباختصار :
- تحتاج الخلية النشطة حوالي مليوني جزيء ATP كل ثانية فهو مصدر طاقة:
- بناء المواد الغذائية مثل السكريات العديدة، وتحويل الأحماض الأمينية إلى بروتين، وتضاعف DNA.
- الحركة وانقباض العضلات وانقسام الخلية.
- عملية النقل النشط.
- تسريع التفاعلات الكيميائية.
مثال على استعماله الحشرة المسماة سراج الحصادين تحول طاقة ATP إلى طاقة ضوئية، وتسمى هذه الظاهرة بالإضاءة الحيوية.
دور الميتوكوندريات في العمليات الكيميائية المكونة للـ ATP[عدل]
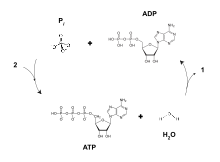
يتعرض الجلوكوز عند دخوله إلى الخلايا للإنزيمات الموجودة في السيتوبلازم التي تحوله إلى حمض البيروفيك، وتسمى هذه العملية باسم الانحلال السكري glycolysis. وتتحول كمية صغيرة من الـ ADP إلى ATP بواسطة الطاقة التي تحرر أثناء هذا التحول ولكن هذه الكمية لا تمثل إلا 5% من مجموع استقلاب الطاقة في الخلية. والمعلوم أن القسم الأكبر من ATP الخلية يتكون في الميتوكوندريا، وتحول كل الأحماض البيروفية وبعض الأحماض الدهنية ومعظم الأحماض الأمينية إلى المركب Co-A مرافق الإنزيم A في العصارة الخلوية وفي الميتوكوندريا. وتعمل على هذه المادة سلسلة من الإنزيمات فتتحلل بعمليات كيميائية متتالية تسمى دورة حمض الستريك أو دورة كريبس Krib's cycle.
وينشطر في دورة حمض الستريك مرافق الإنزيم A إلى مكوناته الأساسية وهي ذرات الهيدروجين وثاني أكسيد الكربون، وينتشر ثاني أكسيد الكربون بدوره إلى خارج الميتوكوندريا وأخيراً إلى خارج الخلية . ومن الناحية الأخرى فإن أيونات الهيدروجين تكون فعالة جداً وتتحد في النهاية مع الأكسجين الذي ينتشر إلى الميتوكوندريا من سيتوبلازم الخلية، ويُحرر ذلك التفاعل كمية كبيرة من الـطاقة التي تستعملها الميتوكوندريا لتحويل كميات كبيرة من الـ ADP إلى الـ ATP، وتحتاج إلى مشاركة أعداد كبيرة من الإنزيمات التي تكوّن أقساماً متكاملة من الرفوف الغشائية للميتوكوندريا التي تبرز إلى العصارة الخلوية .[6] وأولى التفاعلات التي تتم هي إزالة إلكترون ذرة الهيدروجين فيتحول بذلك إلى أيون هيدروجين (بروتون). والتفاعل التالي هو حركة هذه الأيونات خلال بروتينات كروية تسمى سنتاز الـ ATP التي تبرز مثل الأزرار خلال أغشية رفوف الميتوكوندريا . وسنتاز الـ ATP هو إنزيم يستعمل الطاقة المولدة من حركة البروتونات (أيونات الهيدروجين) لتحوّل ADP إلى ATP، بينما تتحد في نفس الوقت مع الأكسجين لتولد الماء . وأخيراً ينقل الأدينوسين ثلاثي الفوسفات ATP المكون حديثاً إلى خارج الميتوكوندريا حيث ينتشر في كل السيتوبلازم وإلى جبلة النواة، بينما تخزن طاقته لتستعمل في مختلف وظائف الخلية .
تسمى هذه العملية الشاملة لتكوين الـ ATP باسم الآلية الكيميائية التناضحية لتكوين الـ ATP .[7]
والخلاصة: تتوفر جزيئات أدينوسين ثلاثي الفوسفات ATP دائماً وتطلق طاقاته بسرعة عندما تحتاجه الخلية. وللتعويض عن الـ ATP الذي يستهلك في الخلية تحلل العمليات الكيميائية البطيئة السكريات والدهون والبروتينات وتستعمل الطاقة المولدة من ذلك لتكوين ATP جديد. ويتكون حوالي 95 % تقريباً من هذا الـ ATP في متقدرات (ميتوكوندريا) الخلايا مما يعلل تسمية المتقدرات بـ محطات توليد الطاقة للخلية .
لهذا فليس من الغريب أن تتواجد المتقدرات بأعداد كبيرة في الخلايا العضلية. كما أن المتقدرات يمكنها الانقسام وتوليد متقدرات أخرى؛ ذلك لأن المتقدرة تمتك حمض نووي ريبوزي منقوص الأكسجين خاص بها، يسمى دنا متقدرة.
اقرأ أيضاً[عدل]
- سلسلة تنفس
- أدينوسين أحادي الفوسفات
- أدينوسين ثنائي الفوسفات
- كيناز نوكليوسيد ثنائي الفوسفات
- تدرج بروتوني
- تحلل مائي
- اتاحة الطاقة
- فلافين مونو نوكليوتيد
- أيه تي بي سينثاز
- سيتوكروم سي
- خلية عضلية
- ثيرموجينين
مراجع[عدل]
- ^ أ ب ت ث Adenosine triphosphate (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Mishra، N.؛ Tuteja، R.؛ Tuteja، N. (2006). "Signaling through MAP kinase networks in plants". Arch. Biochem. Biophys. ج. 452 ع. 1: 55–68. DOI:10.1016/j.abb.2006.05.001. PMID:16806044.
- ^ Fredholm، B. B.؛ Abbracchio، M. P.؛ Burnstock، G.؛ Daly، J. W.؛ Harden، T. K.؛ Jacobson، K. A.؛ Leff، P.؛ Williams، M. (1 يونيو 1994). "Nomenclature and classification of purinoceptors". Pharmacol. Rev. ج. 46 ع. 2: 143–156. PMID:7938164. مؤرشف من الأصل في 2008-06-30.
- ^ Fields، R. D.؛ Burnstock، G. (2006). "Purinergic signalling in neuron-glia interactions". Nature Rev. Neurosci. ج. 7 ع. 6: 423–436. DOI:10.1038/nrn1928. PMC:2062484. PMID:16715052.
- ^ Abbracchio، M. P.؛ Burnstock، G.؛ Verkhratsky، A.؛ Zimmermann، H. (يناير 2009). "Purinergic signalling in the nervous system: an overview". Trends Neurosci. ج. 32 ع. 1: 19–29. DOI:10.1016/j.tins.2008.10.001. PMID:19008000. مؤرشف من الأصل في 2018-12-12.
- ^ Byrnes، Chris (5 يناير 2012). "Treating Small Fiber Neuropathy Symptoms With ATP". Working toward Wellness. مؤرشف من الأصل في 2016-06-30. اطلع عليه بتاريخ 2014-01-06.
| في كومنز صور وملفات عن: أدينوسين ثلاثي الفوسفات |