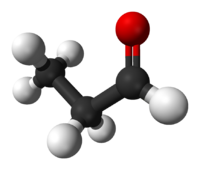
بروبانال
| بروبانال | |
|---|---|
 |
 |
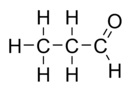
نموذج الكرة والعصا
| |
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
بروبانال |
|
| تسمية الاتحاد الدولي للكيمياء | |
بروبيونالدهيد |
|
| أسماء أخرى | |
ميثيل أسيتالدهيد |
|
| المعرفات | |
| رقم CAS | 123-38-6 |
| بوب كيم (PubChem) | 527 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C3H6O |
| كتلة مولية | 58.08 غ.مول−1 |
| المظهر | سائل شفاف عديم اللون |
| الكثافة | 0.81 غ/مل |
| نقطة الانصهار | -81 |
| نقطة الغليان | 46 إلى 50 °س (115 إلى 122 °ف؛ 319 إلى 323 ك) |
| الذوبانية في الماء | 20 غ/100 مل |
| قابلية مغناطيسية | 34.32- × 10−6 سم3/مول |
| اللزوجة | 0.6 بواز عند 20 °م (68 °ف) |
| البنية | |
| البنية الجزيئية | C1, O: sp2, C2, C3: sp3 |
| عزم جزيئي ثنائي القطب | 2.52 ديباي |
| المخاطر | |
| رمز الخطر وفق GHS |    |
| وصف الخطر وفق GHS | خطر |
| بيانات الخطر وفق GHS | H225, H302, H332, H315, H318, H335[1] |
| NFPA 704 |
|
| مركبات متعلقة | |
| مركبات ذات علاقة | إيثانال بوتانال |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
البروبانال أو ألدهيد البروبان (بالإنجليزية: Propanal أو Propionaldehyde) هو مركب عضوي يحمل الصيغة الجزيئية CH3CH2CHO، وهو ألدهيد ثلاثي الكربون، وهو سائل عديم اللون، وقابل للاشتعال برائحة الفواكه الخفيفة، ويتم إنتاجه على نطاق واسع صناعيًا، وهو قابل للذوبان في الماء والكحول والإيثر[2]
التحضير[عدل]
يتم تحضير ألدهيد البروبان صناعيًا بشكل أساسي عن طريق تفاعل الأوكسو للإيثيلين؛ حيث يجمع الإيثيلين مع غازي أول أكسيد الكربون والهيدروجين باستخدام محفز (عادةً ما يكون عنصر الروديوم):[2]
ويمكن بهذه الطريقة إنتاج عدة مئات الآلاف من الأطنان سنويًا.[3]
تحضير المختبر[عدل]
يمكن أيضًا تحضير البروبانال في المختبرات عن طريق أكسدة 1-بروبانول بمزيج من حمض الكبريتيك وثنائي كرومات البوتاسيوم. يحتوي مكثف الارتداد على ماء مسخّن عند 60°م درجة مئوية، والذي يكثف البروبانول غير المتفاعل، ولكنه يسمح بمرور البروبانال. يتكثف بخار البروبانال على الفور في جهاز استقبال مناسب، وعن طريق هذا التنظيم تتم إزالة أي بروبانال المتكون على الفور من المفاعل، وبالتالي لا يتأكسد بشكل مفرط إلى حمض البروبيونيك.[4]
الاستخدامات[عدل]
يتم استخدام البروبانال في الغالب كطليع لثلاثي ميثيلول إيثان CH3C(CH2OH)2CHO من خلال تفاعل التكثف مع الميثانال. يعد هذا التريول وسيط مهم في إنتاج راتنجات الألكايد. كما يتم استخدامه في تخليق العديد من المركبات العطرية الشائعة، مثل: ألدهيد بخور مريم، والهليونال، والليليال، وهناك تطبيقات أخرى يمكن من خلالها استعمال البروبانال كالاختزال إلى البروبانول، والأكسدة إلى حمض البروبيونيك.[3]
استخدامات المختبر[عدل]
يعد البروبانال كاشفًا شائعًا كونه لبنة في بناء العديد من المركبات.[5] تقوم العديد من هذه الاستخدامات باستغلال مشاركتها في تفاعلات التكثيف.[6] يعطي مع ثالثي بوتيل الأمين هذا الناتج CH3CH2CH=N-t-Bu الذي هو لبنة بناء ثلاثية الكربون تستخدم في الاصطناع العضوي.[7]
ظهوره خارج كوكب الأرض[عدل]
تم اكتشاف البروبانال مع الأكرولين في السحابة الجزيئية قوس B2 الذي يقع بالقرب من مركز مجرة درب التبانة على بعد 390 سنة ضوئية، أي على بعد حوالي 26000 سنة ضوئية من الأرض.[8][9][10]
كشفت القياسات التي أجرتها أجهزة كوساك (COSAC) وبطليموس على سطح المذنب 67 P/تشوريوموف-جيراسيمنكو عن ستة عشر مركبًا عضويًا، شوهد أربعة منها لأول مرة على مذنب، بما في ذلك الأسيتاميد والأسيتون والميثيل أيزوسيانات والبروبانال.[11][12][13]
الأمان[عدل]
تبلغ الجرعة المميتة الوسطية له 1690 مغم/كغم لعينة تجريبية (أي 1690 ميليغرام لكل كيلوغرام واحد من جسم العينة)، وذلك عن طريق الفم،[3] وبالتالي يُظهر البروبانال سمية حادة منخفضة.
انظر أيضًا[عدل]
مراجع[عدل]
- ^ أ ب Record of Propanal in the GESTIS Substance Database from the IFA, accessed on 22 March 2020
- ^ أ ب البروبانال - مصادر الكيمياء للأستاذ أكرم أمير العلي نسخة محفوظة 2021-01-19 على موقع واي باك مشين.
- ^ أ ب ت Hensel، A. (2005)، "Propanal"، موسوعة أولمان للكيمياء الصناعية، فاينهايم: وايلي-في سي إتش، DOI:10.1002/14356007.a22_157.pub3
- ^ Hurd، Charles D.؛ Meinert، R. N. (1932). "Propionaldehyde". Organic Syntheses. ج. 12: 64. DOI:10.15227/orgsyn.012.0064.
- ^ Wehrli، Pius A.؛ Chu، Vera (1978). "Y-Ketoesters from Aldehydes Via Diethyl Acylsuccinates: Ethyl 4-Oxohexanoate". Organic Syntheses. ج. 58: 79. DOI:10.15227/orgsyn.058.0079.
- ^ Sessler، Jonathan L.؛ Mozaffari، Azadeh؛ Johnson، Martin R. (1992). "3,4-Diethylpyrrole and 2,3,7,8,12,13,17,18-Octaethylporphyrin". Org. Synth. ج. 70: 68. DOI:10.15227/orgsyn.070.0068.
- ^ Peralta, M. M. "Propionaldehyde t-Butylimine" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. دُوِي:10.1002/047084289X.
- ^ Scientists Discover Two New Interstellar Molecules: Point to Probable Pathways for Chemical Evolution in Space, National Radio Astronomy Observatory, June 21, 2004 نسخة محفوظة 2021-02-13 على موقع واي باك مشين.
- ^ Two newly found space molecules. By: Goho, Alexandra, Science News, 00368423, 7/24/2004, Vol. 166, Issue 4
- ^ Chemical Precursors to Life Found in Space Scientists say that a universal prebiotic chemistry may be at work نسخة محفوظة 2021-02-14 على موقع واي باك مشين.
- ^ Jordans، Frank (30 يوليو 2015). "Philae probe finds evidence that comets can be cosmic labs". The Washington Post. Associated Press. مؤرشف من الأصل في 2019-10-07. اطلع عليه بتاريخ 2015-07-30.
- ^ "Science on the Surface of a Comet". European Space Agency. 30 يوليو 2015. مؤرشف من الأصل في 2019-08-20. اطلع عليه بتاريخ 2015-07-30.
- ^ Bibring، J.-P.؛ Taylor، M.G.G.T.؛ Alexander، C.؛ Auster، U.؛ Biele، J.؛ Finzi، A. Ercoli؛ Goesmann، F.؛ Klingehoefer، G.؛ Kofman، W.؛ Mottola، S.؛ Seidenstiker، K.J.؛ Spohn، T.؛ Wright، I. (31 يوليو 2015). "Philae's First Days on the Comet - Introduction to Special Issue". ساينس. ج. 349 ع. 6247: 493. Bibcode:2015Sci...349..493B. DOI:10.1126/science.aac5116. PMID:26228139.
وصلات خارجية[عدل]
| بروبانال في المشاريع الشقيقة: | |
| |