تيتانيوم
| ||||||||||||||||||||||||||||||||||||||||||||||
| المظهر | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
أبيض رمادي-فضي
| ||||||||||||||||||||||||||||||||||||||||||||||
| الخواص العامة | ||||||||||||||||||||||||||||||||||||||||||||||
| الاسم، العدد، الرمز | تيتانيوم، 22، Ti | |||||||||||||||||||||||||||||||||||||||||||||
| تصنيف العنصر | فلز انتقالي | |||||||||||||||||||||||||||||||||||||||||||||
| المجموعة، الدورة، المستوى الفرعي | 4، 4، d | |||||||||||||||||||||||||||||||||||||||||||||
| الكتلة الذرية | 47.867 غ·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||
| توزيع إلكتروني | Ar]; 3d2 4s2] | |||||||||||||||||||||||||||||||||||||||||||||
| توزيع الإلكترونات لكل غلاف تكافؤ | 2, 8, 10, 2 (صورة) | |||||||||||||||||||||||||||||||||||||||||||||
| الخواص الفيزيائية | ||||||||||||||||||||||||||||||||||||||||||||||
| الطور | صلب | |||||||||||||||||||||||||||||||||||||||||||||
| الكثافة (عند درجة حرارة الغرفة) | 4.506 غ·سم−3 | |||||||||||||||||||||||||||||||||||||||||||||
| كثافة السائل عند نقطة الانصهار | 4.11 غ·سم−3 | |||||||||||||||||||||||||||||||||||||||||||||
| نقطة الانصهار | 1941 ك، 1668 °س، 3034 °ف | |||||||||||||||||||||||||||||||||||||||||||||
| نقطة الغليان | 3560 ك، 3287 °س، 5949 °ف | |||||||||||||||||||||||||||||||||||||||||||||
| حرارة الانصهار | 14.15 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||
| حرارة التبخر | 425 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||
| السعة الحرارية (عند 25 °س) | 25.060 جول·مول−1·كلفن−1 | |||||||||||||||||||||||||||||||||||||||||||||
| ضغط البخار | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| الخواص الذرية | ||||||||||||||||||||||||||||||||||||||||||||||
| أرقام الأكسدة | 4, 3, 2, 1[1] (أكاسيده مذبذبة) | |||||||||||||||||||||||||||||||||||||||||||||
| الكهرسلبية | 1.54 (مقياس باولنغ) | |||||||||||||||||||||||||||||||||||||||||||||
| طاقات التأين | الأول: 658.8 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||
| الثاني: 1309.8 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||
| الثالث: 2652.5 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر ذري | 147 بيكومتر | |||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر تساهمي | 8±160 بيكومتر | |||||||||||||||||||||||||||||||||||||||||||||
| خواص أخرى | ||||||||||||||||||||||||||||||||||||||||||||||
| البنية البلورية | نظام بلوري سداسي | |||||||||||||||||||||||||||||||||||||||||||||
| المغناطيسية | مغناطيسية مسايرة | |||||||||||||||||||||||||||||||||||||||||||||
| مقاومة كهربائية | 420 نانوأوم·متر (20 °س) | |||||||||||||||||||||||||||||||||||||||||||||
| الناقلية الحرارية | 21.9 واط·متر−1·كلفن−1 (300 كلفن) | |||||||||||||||||||||||||||||||||||||||||||||
| التمدد الحراري | 8.6 ميكرومتر·متر−1·كلفن−1 (25 °س) | |||||||||||||||||||||||||||||||||||||||||||||
| سرعة الصوت (سلك رفيع) | (درجة حرارة الغرفة) 5,090 متر·ثانية−1 | |||||||||||||||||||||||||||||||||||||||||||||
| معامل يونغ | 116 غيغاباسكال | |||||||||||||||||||||||||||||||||||||||||||||
| معامل القص | 44 غيغاباسكال | |||||||||||||||||||||||||||||||||||||||||||||
| معامل الحجم | 110 غيغاباسكال | |||||||||||||||||||||||||||||||||||||||||||||
| نسبة بواسون | 0.32 | |||||||||||||||||||||||||||||||||||||||||||||
| صلادة موس | 6.0 | |||||||||||||||||||||||||||||||||||||||||||||
| صلادة فيكرز | 970 ميغاباسكال | |||||||||||||||||||||||||||||||||||||||||||||
| صلادة برينل | 716 ميغاباسكال | |||||||||||||||||||||||||||||||||||||||||||||
| رقم CAS | 7440-32-6 | |||||||||||||||||||||||||||||||||||||||||||||
| النظائر الأكثر ثباتاً | ||||||||||||||||||||||||||||||||||||||||||||||
| المقالة الرئيسية: نظائر التيتانيوم | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
التيتانيوم عنصرٌ كيميائي رمزه Ti وعدده الذرّي 22، وهو ينتمي إلى عناصر المستوى الفرعي d ويقع على رأس عناصر المجموعة الرابعة في الجدول الدوري؛ وهو من الفلزّات الانتقالية. التيتانيوم فلزٌّ ذو لون فضّي لامع، وهو خفيف ومتين ومقاوم للتآكل حتّى في الظروف القاسية، مثلما هو الحال في ماء البحر والماء الملكي والكلور على سبيل المثال.
اكتشف وليام غريغور هذا العنصر في موقع في مقاطعة كورنوال البريطانية، وأطلق مارتن كلابروت عليه اسم «تيتانيوم»، نسبةً إلى تيتان، وهو عرق من أعراق الآلهة وفق الأساطير الإغريقية. يتوفّر التيتانيوم في عددٍ من المعادن، وخاصّةً الروتيل والإلمينيت، وهي معادن واسعة الانتشار في القشرة الأرضية وفي غلاف الأرض الصخري. يُستخرَج التيتانيوم من خاماته عن طريق عملية كرول وعملية هنتر. يوجد للتيتانيوم عددٌ من المركّبات الكيميائية، وأشهرها هو ثنائي أكسيد التيتانيوم، والذي يستخدم بكثرة في تطبيقات مختلفة، مثل صناعة الخُضُب البيضاء.
يمكن للتيتانيوم أن يُسبَك مع عددٍ من الفلزّات الأخرى، مثل الحديد والألومنيوم والفاناديوم والموليبدنوم، على سبيل المثال. لسبائك التيتانيوم عددٌ كبير من التطبيقات المهمّة في مجالات مختلفة، مثل صناعة الطيران والفضاء وفي الصناعات الكيميائية والعسكرية وفي صناعة المركبات، وكذلك في المجال الطبّي، وخاصّةً في مجال الأطراف الاصطناعية وزراعة العظام.
التاريخ
[عدل]
يعود اكتشاف التيتانيوم إلى سنة 1791، حينما عثر رجل الدين والجيولوجي الهاوي وليام غريغور [ملاحظة 1] على تضمين لهذا الفلزّ داخل عيّنة معدنية من مقاطعة كورنوال البريطانية.[2] تمكّن غريغور من تمييز وجود عنصرٍ جديدٍ في معدن الإلمينيت،[3] وذلك عندما وجد رماداً في العينة ولاحظ أنّه ينجذب إلى المغناطيس.[2] بإجراء تحليلٍ إضافي تأكّد غريغور من وجود أكسيدَين لفلزّين، تمكّن من تمييز أحدهما وهو أكسيد الحديد، أمّا الأكسيد الأبيض الآخر فلم يستطع نسبته إلى فلزّ معروف في ذلك الوقت؛[4] لذلك شَرَع بمراسلة «الجمعية الملكية الجيولوجية في كورنوال» [ملاحظة 2] بالإضافة إلى مجلّة علمية ألمانية متخصّصة في الكيمياء.[ملاحظة 3][2][5][6]
بعد ذلك، وفي فترة تاريخية مقاربة، استطاع فرانز يوزف مولر فون رايشنشتاين [ملاحظة 4] الحصولَ على مادّة مشابهة للأكسيد، لكنّه لم يتمكّن من تحديد تركيبها.[3] ثمّ في سنة 1795، وبشكلٍ مستقلٍّ، استطاع مارتن كلابروت [ملاحظة 5] أن يحصل على الأكسيد في عينة روتيل مُستقدَمة من أوروبّا الوسطى، مؤكّداً بذلك اكتشاف العنصر الجديد، والذي أطلق عليه اسم «تيتانيوم»؛[2][7] نسبةً إلى تيتان، في إشارة إلى عمالقة الأساطير الإغريقية.[8]
إنّ العمليات المعروفة حالياً لاستحصال التيتانيوم من خاماته المختلفة هي عمليات معقّدة ومكلفة؛ إذ ليس من الممكن اختزال الخامة الحاوية على التيتانيوم بالفحم، كما هو الحال في استخراج الحديد، لأنّ التيتانيوم يتفاعل مع الكربون ليعطي كربيد التيتانيوم.[2] استُحصِلَ على فلزّ التيتانيوم النقي أوّل مرّة سنة 1910، وذلك عندما قام ماثيو هنتر [ملاحظة 6] من معهد رينسيلار للعلوم التطبيقية بتسخين رباعي كلوريد التيتانيوم TiCl4 مع الصوديوم بين درجتي الحرارة 700–800 °س تحت الضغط،[9] في عملية على دفعات تدعى باسم «عملية هنتر».[10] لم يُستخدَم فلزّ التيتانيوم خارج المختبرات حتّى سنة 1932، عندما أنتج وليام كرول [ملاحظة 7] هذا الفلز باختزال رباعي كلوريد التيتانيوم باستخدام الكالسيوم أوّلاً؛[11] ثمّ طوّر من عمليته بعد مضي ثمانِ سنوات مستخدماً مزيجاً من المغنيسيوم مع الصوديوم عاملاً للاختزال، فيما يعرف الآن باسم «عملية كرول»،[11] ولا تزال هذه العملية مستخدمة من أجل الإنتاج التجاري من التيتانيوم.[3][10] في جانبٍ آخر، تمكّن أنطون إدوارد فان أركل [ملاحظة 8] ويان هندريك دي بوير [ملاحظة 9] من إنتاج كمّيّاتٍ صغيرةٍ من التيتانيوم مرتفع النقاوة بأسلوب القضيب البلّوري في سنة 1925، وذلك بمفاعلة الفلزّ مع اليود، ثم بتفكيك البخار المتشكّل على وشيعة ساخنة، ممّا يؤدّي إلى الحصول على الفلزّ بنقاوةٍ مرتفعةٍ جدّاً.[12]
كان الاتحاد السوفيتي رائداً في خمسينيّات وستينيّات القرن العشرين باستخدام التيتانيوم في التطبيقات العسكرية، وخاصّةً في مجال الغوّاصات النووية،[9] مثل غوّاصات المشروع 705 ليرا [ملاحظة 10] وغواصة كي-278 كومسوموليتس،[13] وذلك في خضمّ التنافس العسكري مع الولايات المتّحدة الأمريكية أثناء الحرب الباردة.[14] بالمقابل، صنّفت الولايات المتحدة التيتانيوم في تلك الفترة ضمن المواد ذات الأهمّيّة الاستراتيجية، وبقيت الإدارات الأمريكية محتفظةً بأكوام من رغوة التيتانيوم إلى أن وُزِّع في أوائل القرن الحادي والعشرين.[15] كانت شركة فيسيمبو-أفيسما [ملاحظة 11] الروسية أكبر منتجِ للتيتانيوم، بحصّة سوق تبلغ 29% من الإنتاج العالمي.[16] وفق إحصاءات سنة 2015، كانت أكبر سبع دول رائدة في إنتاج رغوة التيتانيوم كلّ من الصين واليابان وروسيا وكازاخستان والولايات المتحدة وأوكرانيا والهند، على الترتيب.[17][18]
الوفرة الطبيعية
[عدل]يأتي التيتانيوم في المرتبة التاسعة وفقاً للوفرة الطبيعية للعناصر الكيميائية في القشرة الأرضية، وذلك يوافق 0.63% بالنسبة للكتلة.[4] من النادر العثور على التيتانيوم بشكله العنصري الحرّ في الطبيعة؛[19] وهو يوجد غالباً على شكل أكسيد في غلاف الأرض الصخري في معظم الصخور النارية والصخور الرسوبية؛ كما يوجد أيضاً في غلاف الأرض المائي في المسطّحات المائية الطبيعية.[10][20] تتراوح نسبة التيتانيوم في التربة بين 0.5 إلى 1.5%.[4] يبلغ تركيز التيتانيوم في مياه المحيطات حوالي 4 بيكومولار؛ أمّا عند درجة غليان الماء فيُقدَّر تركيز التيتانيوم بأقلّ من 10−7 مولار، عند قيمة pH تعادل 7. لم تُحدّد الأنواع الكيميائية للتيتانيوم في المحاليل المائية، وهي لا تزال غير معروفة، وذلك يعود إلى الانحلالية الضعيفة لتلك الأنواع. يوجد آثار من التيتانيوم في الأحجار النيزكية، كما كُشِفَ عن وجود هذا العنصر في الشمس وفي النجوم من النمط M،[10] والتي تصل فيها درجة حرارة السطح إلى 3200 °س.[8] حَوَت بعض عيّنات الصخور المُستجلَبة من القمر خلال بعثة أبولو 17 على حوالي 12.1% من ثنائي أكسيد التيتانيوم TiO2.[10] من المعادن النمطية الحاوية على التيتانيوم كلّ من الأناتاز والبروكيت والإلمينيت والبيروفسكيت والروتيل والتيتانيت.[21]
الاستخراج والإنتاج
[عدل]| البلد | الكمّيّة مقدّرة بآلاف الأطنان |
(%) من الإجمالي |
|---|---|---|
| أستراليا | 1,300 | 19.4 |
| جنوب أفريقيا | 1,160 | 17.3 |
| كندا | 700 | 10.4 |
| الهند | 574 | 8.6 |
| موزمبيق | 516 | 7.7 |
| الصين | 500 | 7.5 |
| فيتنام | 490 | 7.3 |
| أوكرانيا | 357 | 5.3 |
من بين معادن التيتانيوم المعروفة يمتلك الروتيل والإلمينيت أهميةً اقتصادية من أجل استخراج التيتانيوم، رغم أنّه من الصعب العثور على توضّعات مرتفعة التركيز منهما. استُخرجَ حوالي 6 و0.7 مليون طن، على الترتيب، من هذَين المعدَنَين المذكورَين من المناجم في العالم سنة 2011.[22] توجد توضّعات رسوبية كبيرة من الإلمينيت الحاوي على التيتانيوم في غربي أستراليا وفي كندا والصين والهند وموزمبيق ونيوزيلندا والنرويج وسيراليون وجنوب أفريقيا وأوكرانيا.[21]
أُنتِج في سنة 2011 قرابة 186 ألف طن من رغوة التيتانيوم، وتصدّرت حينها الصينُ الدولَ المنتجة بحوالي 60 ألف طن، تلتها روسيا (40 ألف طن)، ثم الولايات المتّحدة (32 ألف طن)، ثمّ كازاخستان (قرابة 21 ألف طن). قُدِّرَت الاحتياطات الإجمالية من التيتانيوم بحوالي 600 مليون طن.[22] تمرّ عملية إنتاج التيتانيوم بأربع خطوات رئيسية؛ وهي اختزال خامة التيتانيوم إلى رغوة معدنية، ثمّ صهرها بوجود سبيكة أمّ [ملاحظة 12] لتشكيل صبّة، ثمّ المعالجة الميكيانيكية الأوّلية بالتحويل إلى كتل خام على أشكال مختلفة، ثمّ بالمعالجة الثانوية على شكل منتجات جاهزة.[23]
لا يمكن الحصول صناعياً على التيتانيوم من اختزال الأكسيد الموافق TiO2،[24] ولكن يُستَحصل من اختزال رباعي كلوريد التيتانيوم TiCl4 باستخدام فلزّ المغنيسيوم وفق عملية كرول.[10] إلّا أنّها عملية معقّدة غير مستمرّة، وذلك يفسّر ارتفاع القيمة السوقية للتيتانيوم.[25] وعلى الرغم من أنّ عملية كرول من حيث المبدأ أقلّ كلفة من عملية هنتر؛[9] إلّا أنّ الكلفة الإنتاجية لهذا الفلزّ على العموم مرتفعة، إذ إنّ سعر التيتانيوم أغلى بحوالي 35 مرّة من الفولاذ، وبحوالي 200 مرّة من الفولاذ الخام (بيانات سنة 2013)؛ وفي سنة 2008 كانت كلفة إنتاج طن واحد من رغوة التيتانيوم الإسفنجية حوالي 12 ألف يورو.[26]

للحصول على TiCl4 اللازم لعملية كرول يخضع الأكسيد TiO2 إلى اختزال كربوحراري بوجود غاز الكلور. في هذه العملية يُمرَّر غاز الكلور فوق مزيجِ مسخّن لدرجة الاحمرار من الروتيل أو الإلمينيت بوجود الكربون (الفحم)؛ وبعد عمليّات تنقية مكثّفة ومتعدّدة بأسلوب التقطير بالتجزئة، يُختَزل رباعي كلوريد التيتانيوم TiCl4 الناتج بمصهور المغنيسيوم عند الدرجة 800 °س في وسطٍ من غاز الآرغون.[27]
يمكن في الخطوة الأخيرة أن يُستخدَم الصوديوم مختزِلاً وفق عملية هنتر:[28]
يمكن إجراء عملية تنقية لاحقة بأسلوب القضيب البلوري (أو عملية فان أركل-دي بوير)، [ملاحظة 13]، والتي تتضمّن تفاعل نقل كيميائي بالتفكّك الحراري لمركّب رباعي يوديد التيتانيوم TiI4. طُوّرت طرق جديدة لاستحصال التيتانيوم،[ملاحظة 14][29] وذلك اعتماداً على الاختزال الكيميائي الكهربائي لثنائي أكسيد التيتانيوم في مصهور كلوريد الكالسيوم، وبذلك يمكن الحصول على فلزّ التيتانيوم إمّا على شكل مسحوق أو رغوة معدنية إسفنجية.[30] يمكن الحصول على مسحوق التيتانيوم بعملية إنتاج شامل تدعى باسم عملية أرمسترونغ،[ملاحظة 15][31] وهي مشابهة للإنتاج وفق عملية هنتر، إذ يضاف تيّار من بخار رباعي كلوريد التيتانيوم إلى تيّار من مصهور فلزّ الصوديوم، ثم يُنقّى التيتانيوم الناتج من المركّبات الثانوية المرافقة ويُغسَل ويُجفََف، كما يعاد تدوير الصوديوم والكلور لمعالجات لاحقة.[32] أعلنت شركة التصنيع الوطنية السعودية (تصنيع) أنّ مشروعاً جديداً لإنتاج مادة التيتانيوم الإسفنجي يضم الشركة المنتجة للبتروكيماويات سيبدأ عملياته التجارية في النصف الثاني من 2017.[ar 1]
السبائك
[عدل]من السبائك المعروفة للتيتانيوم كلّ من Ti-6Al-4V مع الألومنيوم والفاناديوم؛ وسبيكة نيتينول مع النيكل. يمكن الحصول على سبائك التيتانيوم المختلفة بأسلوب مباشر أثناء عملية الاختزال لإنتاج التيتانيوم؛ فعلى سبيل المثال، يُستحصَل على السبيكة مع النحاس [ملاحظة 16] بإضافة النحاس عند اختزال الروتيل، وعلى السبيكة مع المغنيسيوم [ملاحظة 17] بإضافة المغنيسيوم أو أكسيده إلى الروتيل أثناء الاختزال؛ أو السبيكة مع الحديد [ملاحظة 18] باختزال الإلمينيت FeTiO3 بفحم الكوك في فرن كهربائي.[33]

على الرغم من وجود قرابة خمسين درجة من سبائك التيتانيوم المُطوّرة، إلّا أنّ بضعة دزّينات منها قيد الاستخدام التجاري؛[34] أمّا الجمعية الأمريكية لاختبار المواد [ملاحظة 19] فقد حدّدت 39 درجة من سبائك التيتانيوم،[35] ومنها أربعة درجات للتيتانيوم غير المسبوك، وتلك الدرجات الأربع تتفاوت فيما بينها بقيم مقاومة الشد بشكل متعلّق بمحتوى الأكسجين فيها، بحيث أنّ الدرجة الأولى تكون الأكثر قابليةً للسحب والطرق (أقلّ مقاومة شدّ بمحتوى أكسجيني 0.18%)، والدرجة الرابعة هي الأقلّ قابليةً للسحب والطرق (أكبر مقاومة شدّ بمحتوى أكسجيني 0.40%).[21] أمّا الدرجات المتبقّية فهي سبائك تتمايز فيما بينها بخواصّها النوعية مثل المطيلية والمتانة والصلادة والمقاومة الكهربائية ومقاومة الزحف والمقاومة النوعية للتآكل.[36] بالإضافة إلى ذلك، توجد مواصفات إنتاج خاصّة لسبائك التيتانيوم حسب نوع التطبيق، مثل السبائك المخصّصة للتطبيقات العسكرية أو الصناعية أو الطبّية.[37]
التصنيع
[عدل]في تصنيع التيتانيوم يمكن أن تُستعمَل الآلات والعمليات ذاتها المستخدَمة في تصنيع الفولاذ المقاوم للصدأ.[38] يمكن الحصول على أشكال تجارية جاهزة من صفائح التيتانيوم النقي، ولكن ينبغي إجراء معالجة خاصّة، وذلك بسبب قابلية الانثناء، وخاصّةً لأنواع محدّدة من السبائك مرتفعة المتانة.[39][40] يجب أن تجرى كافة أنواع اللحام للتيتانيوم تحت جوٍّ من غاز خامل من الآرغون أو الهيليوم ليحجُبَه عن غازات الهواء الجوّي (الأكسجين والنتروجين).[38] لا يمكن إجراء لحام بالقصدير للتيتانيوم قبل طليه بفلزّ قابل للحام من هذا النوع.[41]
إعادة التدوير
[عدل]من الممكن إعادة تدوير خردة التيتانيوم ذات درجة النقاوة المنخفضة، والمُلوَّثة إمّا بالأكسجين أو الحديد، وذلك في إنتاج سبيكة فرّوتيتانيوم [ملاحظة 20] المستخدمة في صناعة الفولاذ. في حال ازدياد الطلب العالمي على هذا الفلز بشكل مفاجئ، سيكون من الضروري تطوير وسائل فعالة واقتصادية لإزالة الأكسجين والحديد من الخردة من أجل إعادة تدوير التيتانيوم، وذلك بغرض تأمين احتياجات السوق التطبيقية من هذا الفلز.[42]
النظائر
[عدل]للتيتانيوم ستّة وعشرون نظيراً تتراوح أعدادها الكتلة بين 39 و 64،[43] من بينها خمسة نظائر مستقرّة وهي تيتانيوم-46 46Ti وتيتانيوم-47 47Ti وتيتانيوم-48 48Ti وتيتانيوم-49 49Ti وتيتانيوم-50 50Ti. إنّ أكثر نظائر التيتانيوم وفرةً طبيعية هو النظير تيتانيوم-48 48Ti والذي يشكّل 73.8% من إجمالي نظائر التيتانيوم. هناك 21 نظيراً مشعّاً للتيتانيوم أكثرها استقراراً هو النظير تيتانيوم-44 44Ti الذي له عمر نصف 63 سنة، والنظير تيتانيوم-45 45Ti بعمر نصف مقداره 184.8 دقيقة، والنظير تيتانيوم-51 51Ti بعمر نصف مقداره 5.76 دقيقة، والنظير تيتانيوم-52 52Ti بعمر نصف مقداره 1.7 دقيقة. لباقي النظائر المشعّة عمر نصف أقلّ من 33 ثانية، ومعظمها أقلّ من نصف ثانية.[44] وأقلّها استقراراً هو النظير تيتانيوم-61 61Ti الذي يزيد عمر نصفه قليلاً عن 300 نانوثانية. إنّ نمط الاضمحلال الأساسي لنظائر التيتانيوم المشعّة التي لها عدد كتلة أصغر من النظير المستقرّ تيتانيوم-48 48Ti هو اضمحلال بيتا من النمط الموجب β+ متحوّلةً بذلك إلى نظائر السكانديوم الموافقة. بالمقابل؛ فإنّ للنظائر المشعّة التي لها عدد كتلة أكبر من 48 تتضمحلّ بشكلٍ أساسيٍّ على النمط السالب من اضمحلال بيتّا β- إلى نظائر الفاناديوم الموافقة.[44]
الخواص الفيزيائية
[عدل]
في الظروف القياسية من الضغط ودرجة الحرارة يوجد التيتانيوم على شكل فلزٍّ أبيض فضّي لامع؛[24] وهو فلزّ متين ذو كثافة منخفضة، ويتميّز بقابليته للسحب والطرق.[20] إنّ أكثر ما يميّز فلزّ التيتانيوم هو مقاومته للتآكل، إذ يتشكّل على سطحه طبقةٌ رقيقةٌ من الأكسيد، والتي تقوم بدور مُخَمِّل، وتقيه من تأثير العديد من المواد. كما يتميّز التيتانيوم بنسبة المتانة إلى الوزن،[27] وهي الأعلى من بين جميع الفلزّات.[45]
يوجد هناك شكلان متآصلان من التيتانيوم،[27] الأوّل من النمط ألفا α ذو بنية سداسية، والتي تتغير إلى بنية بيتّا β المكعّبة مركزية الجسم عند درجة حرارة مقدارها 882 °س؛[38] إذ تزداد قيمة الحرارة النوعية للشكل ألفا بشكل مطّرد عندما يُسخَّن إلى درجة حرارة التحوّل تلك، ثم تنخفض وتبقى ثابتة نسبياً في الشكل بيتّا، بغضّ النظر عن درجة الحرارة.[38] نظراً للارتفاع النسبي لنقطة انصهار لهذا الفلز (1668 °س)، فإنّ التيتانيوم يُصنَّف ضمن الفلزّات الحرارية. وهو فلزّ ذو مغناطيسية مسايرة، ولديه موصلية كهربائية وحرارية ضعيفة نسبياً مقارنةً بالفلزّات الأخرى.[20] يصبح التيتانيوم ذا موصلية فائقة عندما يُبرَّد إلى درجات حرارة دون درجة الحرارة الحرجة (0.49 كلفن).[46][47]
الخواص الهندسية
[عدل]تبلغ قيمة مقاومة الشد للتيتانيوم المتوفّر تجارياً بنقاوة 99.2% مقدار 434 ميغاباسكال (63 ألف رطل لكل بوصة مربعة psi)، وتلك قيم مساوية لقيم متانة بعض أنواع الفولاذ ولكنّه أقلّ كثافة.[48] من جهةٍ أخرى، فإنّ التيتانيوم أكثف من الألومنيوم بحوالي 60%، ولكنّه أمتن بأكثر من مرّتين من بعض أنواع سبائك الألومنيوم شائعة الاستخدام.[48][ملاحظة 21] هناك أنواع محدّدة من سبائك التيتانيوم [ملاحظة 22] تتميّز بأنّ لها مقاومة شدّ تفوق 1400 ميغاباسكال،[49] ولكن من جهةٍ أخرى، فإنّ التيتانيوم يفقد متانته عند تسخينه إلى درجات حرارة تفوق 430 °س،[38] إذ يتَقصّف عند درجات حرارة مرتفعة نتيجة الارتباط مع الأكسجين والنتروجين والهيدروجين. تتطلّب المعالجة الصناعية للتيتانيوم اتخاذ الاحتياطات اللازمة، لأنّ هذه المادة قد تهترئ بالاحتكاك، [ملاحظة 23] إلّا إذا استُخدِمَت أدوات حادّة ووسائل تبريد ملائمة.[50][51] كما هو الحال في البُنَى المصنوعة من الفولاذ فإنّ البُنَى المصنوعة من التيتانيوم ذات حدّ إجهاد مرتفع، ممّا يؤهلّها للاستخدام في بعض التطبيقات طويلة الأمد.[24]
الخواص الكيميائية
[عدل]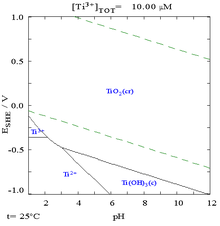
كما هو الحال مع الألومنيوم والمغنيسيوم فإنّ سطح فلزّ التيتانيوم وسبائِكُه يتأكسد تلقائياً إبّان التعرّض للهواء مشكّلاً بذلك طبقةً رقيقةً غير مسامية مُخَمِّلَة، وهي تقي معظم كتلة الفلز المتبقيّة من استمرار الأكسدة ومن التآكل.[20] عندما تبدأ تلك الطبقة بالتشكّل فإنها تكون بسماكة حوالي 1-2 نانومتر، ولكنها تنمو بشكلٍ مستمرٍّ، ممّا يوفّر وقاية ممتازة ضد التآكل بشكلٍ مكافئٍ لِمَا لفلزّ البلاتين. لذلك، فإنّ التيتانيوم قادرٌ على مقاومة أثر حمض الكبريتيك وحمض الهيدروكلوريك المُمَدَّدَين، بالإضافة إلى مقاومة محاليل الكلوريد وأغلب الأحماض العضوية؛[10] إلّا أنّ التيتانيوم قد يتآكل بأثر الأحماض المعدنية المُرَكّزة.[53] كما يُستقرَأ من قيمة جهد الأكسدة/الاختزال السالبة فإنّ التيتانيوم من الناحية الديناميكية الحرارية نشيط كيميائياً، بحيث أنّه يشتعل في الجوّ العادي عند درجات حرارة أقلّ من نقطة انصهاره. ولا يمكن صهر التيتانيوم إلّا في وسطٍ خاملٍ أو تحت الفراغ. عند درجات حرارة مرتفعة يتّحد التيتانيوم مع الأكسجين عند الدرجة 1200 °س في الهواء، وعند الدرجة 610 °س في الأكسجين النقي مشكّلاً ثنائي أكسيد التيتانيوم.[27] ويعدّ التيتانيوم واحداً من بين عددٍ محدودٍ من العناصر القادرة على الاشتعال في وسط من النتروجين النقي، بحيث يتفاعل معه عند الدرجة 800 °س ليشكّل نتريد التيتانيوم، وذلك أمرٌ يزيد من قابلية التقصّف.[54] وعند حوالي 550 °س يتّحد هذا الفلزّ مع الكلور؛[10] كما يتفاعل أيضاً مع باقي الهالوجينات ويمتصّ الهيدروجين.[3] يستفاد من التفاعلية المرتفعة للتيتانيوم مع الأكسجين والنتروجين والغازات الأخرى عند درجات حرارة مرتفعة في تصميم مضخّة تسامي التيتانيوم، حيث يكون التيتانيوم المُبَخَّر من على سطح وشيعة ساخنة قادراً على التقاط تلك الغازات وعزلها من الوسط، وتلك المضخّة قادرة على تأمين نظام فراغ فائق.[ملاحظة 24][55]
المركبات الكيميائية
[عدل]| أمثلة على مركّبات التيتانيوم بحالات أكسدة مختلفة | |
|---|---|
| +2 | TiO، TiCl2 |
| +3 | Ti2O3، TiCl3، TiF3، TiP |
| +4 | TiO2، TiS2، TiCl4، TiF4 |
تهيمن حالة الأكسدة +4 على كيمياء التيتانيوم،[56] على الرغم من وجود بعض المركّبات الكيميائية الشائعة التي يشكّلها هذا العنصر بحالة أكسدة +2 أو +3.[57] يتبنّى التيتانيوم عادةً بنية جزيئية ثمانية السطوح في معقّداته،[58][59] أمّا بالنسبة لمركّباته الكيميائية في حالة الأكسدة +4 فهي تكون ذات بنية جزيئية رباعية السطوح، وتكون الرابطة الكيميائية فيها ذات سمة تناسقية.[56]
اللاعضوية
[عدل]- الأكاسيد
إنّ أكثر أكاسيد التيتانيوم شهرةً هو ثنائي أكسيد التيتانيوم (أكسيد التيتانيوم الرباعي) TiO2، والذي يوجد في الطبيعة على هيئة ثلاثة أشكال: وهي الأناتاز والبروكيت والروتيل. تتَّبعُ تلك المعادن بنىً بوليميرية تكون فيها ذرّة التيتانيوم محاطةً بست ربيطات من الأكسيد، والتي تكون بدورها مرتبطةً بمراكز تيتانيوم أخرى.[60] يُستخدَم ثنائي أكسيد التيتانيوم بشكلٍ شائعٍ في تحضير الخضاب الأبيض، وفي التحفيز الضوئي.[3] من الأكاسيد الأخرى بحالات أكسدة دنيا للتيتانيوم كلّ من أكسيد التيتانيوم الثلاثي Ti2O3 وأكسيد التيتانيوم الثنائي TiO.[61]

يوجد عددٌ من تحت أكاسيد التيتانيوم المعروفة، والتي تُستحصَل من ثنائي أكسيد التيتانيوم عندما يُرَش حرارياً في البلازما تحت الضغط العادي.[ملاحظة 25] من الأمثلة على ذلك تحت الأكسيد Ti3O5، وهو يحوي على التيتانيوم بحالَتي الأكسدة +3 و+4، وهو شبه موصل قرمزي اللون، والذي ينتج عند اختزال TiO2 بالهيدروجين عند درجات حرارة مرتفعة،[62] ويُستخدَم صناعياً من أجل تلبيس المواد.[63]
- التيتانات
التيتانات هي مجموعة من المركّبات الكيميائية بين الأكسجين والتيتانيوم بحالة الأكسدة الرباعية، وأشهرها أورثوتيتانات [ملاحظة 26]، الذي له الصيغة العامّة M2TiO4، وميتاتيتانات [ملاحظة 27]، الذي له الصيغة العامة MTiO3. من الأمثلة على التيتانات كلّ من تيتانات الرصاص PbTiO3 وتيتانات المغنيسيوم MgTiO3 وتيتانات الكالسيوم CaTiO3؛ بالإضافة إلى تيتانات الباريوم BaTiO3، وهي مادّة لها بنية البيروفسكيت، ولها خواص كهربائية انضغاطية، وتُستخدَم في مجال تحويل الإشارة.[27]
- الكبريتيدات
يشكّل التيتانيوم عدداً من الكبريتيدات، أشهرها كبريتيد التيتانيوم الرباعي (ثنائي كبريتيد التيتانيوم) TiS2، والذي يُستخدَم مهبطاً في بطّاريات الليثيوم. تتألّف بنية ثنائي كبريتيد التيتانيوم من عدّة طبقات، بشكلٍ مشابهٍ لبنية يوديد الكادميوم.[64]
- الهاليدات


يشكّل التيتانيوم عدّة هاليدات مختلفة بعدّة حالات أكسدة؛ وأشهرها مركّب كلوريد التيتانيوم الرباعي TiCl4، وهو سائل متطاير عديم اللون، وهو قابل للحلمهة مشكّلاً بذلك سحابة بيضاء. يُستخدَم كلوريد التيتانيوم الرباعي في إنتاج التيتانيوم وفق عملية كرول،[65] وفي تحضير ثنائي أكسيد التيتانيوم لأغراض الطلاء.[66] كما أنّ كلوريد التيتانيوم الرباعي واسع الاستخدام في الكيمياء العضوية على هيئة حمض لويس، مثلما الحال في تفاعل ألدول موكاياما.[67] أمّا يوديد التيتانيوم الرباعي TiI4 فيُستخدَم في عملية القضيب البلوري للحصول على التيتانيوم مرتفع النقاوة.[68]
يشكّل التيتانيوم مختلف الهاليدات في حالة الأكسدة +3 (فلوريد التيتانيوم الثلاثي TiF3 وكلوريد التيتانيوم الثلاثي TiCl3 وبروميد التيتانيوم الثلاثي TiBr3 ويوديد التيتانيوم الثلاثي TiI3)؛ وكان قد استُخدِم كلوريد التيتانيوم الثلاثي حفّازاً في إنتاج البولي بروبيلين.[20] كما يشكّل التيتانيوم أيضاً الهاليدات في حالة الأكسدة +2 (كلوريد التيتانيوم الثنائي TiCl2 وبروميد التيتانيوم الثنائي TiBr2 ويوديد التيتانيوم الثنائي TiI2)، وهي مركّبات ذات نظام بلوري ثلاثي متساوي الأحرف، تتبع نمط بنية يوديد الكادميوم.[69]
- مركبات لاعضوية أخرى
يُصنَّف نتريد التيتانيوم TiN ضمن مجموعة من نتريدات الفلزات الانتقالية، التي تعدّ من المواد الحرارية ذات الثباتية الكبيرة والصلادة المرتفعة؛[70] إذ أنّ صلادة TiN تكافئ صلادة الياقوت الأزرق وكربيد السيليكون (قيمة 9.0 على مقياس موس)،[71] وعادةً ما يُستخدَم من أجل تغطية ريش المثقب،[72] وكمادة حاجزة [ملاحظة 28] في تصنيع عناصر أشباه الموصلات.[73]
نظراً لارتفاع صلادة بوريد التيتانيوم TiB2 فهو يستخدم في التَدريع؛ كما يعدّ كربيد التيتانيوم TiC من المواد ذات الصلادة المرتفعة أيضاً، ويدخل في تركيب الأدوات القاطعة وفي تغطية المواد.[74]
العضوية
[عدل]
تحتوي مركّبات التيتانيوم العضوية على رابطة بين التيتانيوم والكربون، وتعدّ ذات أهمّيّة في الكيمياء العضوية، وتوجد لها تطبيقات في عددٍ من العمليّات الصناعية الرئيسية؛[75] إذ تُستخدَم تلك المركّبات على هيئة حفّازات لعمليّات البلمرة. من أشهر الأمثلة عليها ثنائي كلوريد التيتانوسين TiCl2(C5H5)2، والحاوي على وحدة تيتانوسين فيه، والمُكَوّنة من ذرّة تيتانيوم مركزية محصورة بين مجموعتين من أنيون حلقي البنتاديينيل؛ ومن الأمثلة المتعلّقة بهذه البنية كلّ من كاشف تيبي [ملاحظة 29] وكاشف بتاسيس [ملاحظة 30]. كما يشكّل التيتانيوم أيضاً معقّدات كربونيلية، مثل ثنائي كربونيل التيتانوسين.[76] توجد هناك بعض الأبحاث التي تدرس إمكانية استخدام معقّدات التيتانيوم الرباعي العضوية في تركيب العقاقير المضادّة للسرطان.[77]
التحليل الكيميائي
[عدل]عند تفاعل ثنائي أكسيد التيتانيوم مع حمض الكبريتيك المُدخّن يُستَحصل على مركّب كبريتات التيتانيل TiOSO4، والذي يتحلمه إلى ثنائي أكسيد تيتانيوم مُمَيّه. تؤدّي إضافة كمّيّات قليلة جدّاً من بيروكسيد الهيدروجين إلى الحصول على معقّد ذي لون أصفر-برتقالي مميّز، والذي يمكن الاستعانة به للكشف النوعي المطيافي عن التيتانيوم. عادةً ما تعالج العينة بكمّيّة فائضة من حمض الكبريتيك المركّز داخل حمامٍ ثلجيٍّ حاوٍ على بيروكسيد الهيدروجين.[78][79]

الدور الحيوي
[عدل]لا يوجد دورٌ حيويٌّ معروفٌ للتيتانيوم؛ على الرغم من أنّ بعض الكائنات تحوي على تراكيز من التيتانيوم.[80] إذ تحوي بعض النباتات على التيتانيوم بنسبٍ ضئيلة، ولا تزال الآلية أو الدور الحيوي الذي يقوم به التيتانيوم في تلك النباتات غير معروف؛ وقد يصل تركيز التيتانيوم في القرّاص الكبير أو الكِنباث (ذنب الخيل) إلى حوالي 80 جزء في المليون.[8]
الاستخدامات
[عدل]للتيتانيوم ومركّباته العديد من التطبيقات في مختلف المجالات، مثل المجالات الصناعية والهندسية والطبّية والعسكرية وغيرها.

تحضير السبائك
[عدل]من التطبيقات المهمّة للتيتانيوم إضافته بكمّيّات نزرة (تتراوح بين 0.01 إلى 0.1%) في صناعة الفولاذ، للحصول على سبائك مميّزة مثل سبيكة فرّوتيتانيوم.[ملاحظة 31] إذ يساعد التيتانيوم على التقليل من حجم الحُبَيبَات البلّورية، ويحول دون التآكل بين الحُبَيبات،[ملاحظة 32] ويعمل على سحب الأكسجين من الوسط، كما يقوم بالتقليل من المحتوى الكربوني في الفولاذ.[20] عادةً ما يُسبَك التيتانيوم مع الألومنيوم والفاناديوم والنحاس والحديد والمنغنيز والموليبدنوم؛ وكذلك مع فلزّات أخرى.[81]
التغطية والطلاءات
[عدل]يُستخدَم أكثر من 95% من خامات التيتانيوم في إنتاج الأكسيد TiO2، وهو خضاب ذو لون أبيض ناصع ويدخل مادّةً إضافية بشكلٍ واسعٍ في صناعة الطلاءات ومعاجين الأسنان واللدائن؛[22] وكذلك في الورق.[82]
ما يميّز خضاب ثنائي أكسيد التيتانيوم أنّه خاملٌ كيميائياً، ويقاوم البهوت في أشعّة الشمس، كما أنه مُعتِم وغيرُ شافٍّ بشكل كبير، لذلك يضاف بكثرة إلى المنتجات البلاستيكية لمنحها اللون الأبيض.[3] يصمد الطلاء الأبيض المصنوع من ثنائي أكسيد التيتانيوم في مختلف درجات الحرارة وحتّى في الظروف المناخية البحرية؛[3] كما يمتلك ثنائي أكسيد التيتانيوم النقي قدرةً كبيرةً على تشتيت الضوء؛[10] ولذلك يدخل في تركيب الواقيات الشمسية.[24]
الطيران والملاحة
[عدل]
يمتلك التيتانيوم العديد من الخواص المميّزة، مثل ارتفاع مقاومة الشد مقارنةً مع كثافته،[27] ومقاومته للتآكل،[10] وللإجهاد ولتشكّل الصدوع،[83] وبمقدرته على تحمّل درجات حرارة مرتفعة من غير حدوث زحف؛ ولذلك فإنّه يُستخدَم في صناعة الطائرات وفي تدريع المَركَبات وفي صناعة السفن الحربية والقذائف المُوَجَّهة.[3][10] من أجل ذلك يُسبَك التيتانيوم مع الألومنيوم والزركونيوم والفاناديوم والنيكل،[84] من أجل صناعة مكوّنات مختلفة في المَركَبات الملاحية والعسكرية، وكذلك المَركَبات الفضائية،[85] متضمّنةً الأجزاء الهيكلية الحسّاسة، وجُدُر الحماية وعدّة الهبوط، بالإضافة إلى تركيب الأنظمة الهيدروليكية.[86] ويقدّر بأنّ حوالي ثلثي الكمّيّة المنتَجة من فلزّ التيتانيوم تذهب إلى تلك التطبيقات؛[87] أمّا أكثر سبائك التيتانيوم المستخدَمة في هذا الغرض فهي سبيكة Ti-6Al-4V، والتي تشكّل أكثر من 50% من كافة السبائك المستخدمة في الصناعات الفضائية.[88] من الأمثلة على دخول سبائك التيتانيوم في صناعة هياكل الطائرات كلّ من لوكهيد إيه-12،[ملاحظة 33] ولوكهيد إس آر-71 بلاك بيرد؛ [ملاحظة 34] كما يدخل التيتانيوم في تركيب طائرات مدنية عدّة مثل بوينغ 737 وبوينغ 747 وبوينغ 777، وكذلك في إيرباص إيه 320 وإيرباص إيه 330 وإيرباص إيه 340؛ فطائرة إيرباص إيه 380 يدخل في تركيبها حوالي 77 طن من التيتانيوم، منها حوالي 11 طن في المحرّكات.[89] يقاوم التيتانيوم التآكل في ماء البحر، ولذلك يُستخدَم في صناعة عواميد التدوير والمبادلات الحرارية في محطّات تحلية المياه.[10] كان الاتحاد السوفيتي سابقاً يستخدم سبائك التيتانيوم في صناعة الغوّاصات.[84][90]
الصناعية
[عدل]يدخل التيتانيوم وسبائكه في تركيب المنشآت الصناعية من تمديدات الأنابيب الملحومة ومن معدّات العمليات مثل المبادلات الحرارية والحاويات والخزّانات والصمّامات وغيرها، وخاصّةً في الصناعات الكيميائية والصناعات النفطية، وذلك بشكلٍ أساسيٍّ نظراً لمقاومته للتآكل. فعلى سبيل المثال، يُستخدَم التيتانيوم في تركيب التجهيزات في صناعة اللب والورق بسبب الطبيعة المخرّشة الأكّالة للمواد القاصرة (المبيّضة) مثل هيبوكلوريت الصوديوم أو غاز الكلور الرطب.[91] تتضمّن التطبيقات الصناعية الأخرى للتيتانيوم كلّ من اللحام فوق الصوتي [ملاحظة 35] واللحام الموجي؛ [ملاحظة 36][92] وكذلك في مجال الرشّ المهبطي.[93]
الهندسية
[عدل]
يُستخدَم فلزّ التيتانيوم في مجال صناعة المركبات، خاصّةً في مجال سباقات السيّارات والدرّاجات النارية، حيث تكون خواص الفلزّات خفيفة الوزن ومرتفعة المتانة والصلادة ذات أهميّة كبيرة.[94] إنّ هذا الفلز مرتفع الثمن عموماً من أجل صناعة السلع الاستهلاكية، ولكن بالرغم من ذلك صُنّعت موديلات من سيارة شيفروليه كورفيت كانت فيها العوادم مصنوعةً من التيتانيوم؛[95] كما صُنّعَت أجزاء من محرّكات جنرال موتورز [ملاحظة 37] من التيتانيوم، والتي تميّزت بمتانتها ومقاومتها للحرارة.[96]
في بعض الأحيان يدخل التيتانيوم مكوّناً في بعض الإنشاءات المعمارية والفنّية، فعلى سبيل المثال صُنّع نصب يوري غاغارين والنصب التذكاري لغزاة الفضاء في مدينة موسكو من التيتانيوم، وذلك نظراً للألوان الجذّابة لهذا الفلزّ، ولعلاقته بصناعة الفضاء الروسية.[97][98] ومن الأمثلة كذلك متحف غوغنهايم بلباو، المكسوّ بألواحٍ من التيتانيوم؛[87] وغيرها من الأبنية الأخرى في أمريكا الشمالية.[99]
الحلي
[عدل]
نظراً لديمومته أصبح التيتانيوم مع مرور الوقت مُفضَلاً لاستخدامه في صناعة الحلي والمجوهرات من قبل بعض المصمّمين، خاصّةً في تصميم الخواتم المصنوعة من التيتانيوم النقي.[100] كما يُسبَك التيتانيوم أيضاً مع الذهب، وذلك يعطي متانةً أكبر للسبيكة، مع الحفاظ على رونق التصميم.[101]
من الممكن التحكّم بلون سطح التيتانيوم، إذ أنه عندما يخضع للأكسدة المصعدية، تتغيّر سماكة طبقة الأكسيد السطحية، وذلك يسبب تداخلاً بصرياً، ممّا يؤدّي إلى تنوّع في الألوان الظاهرة على السطح.[102] لذلك يكثر استخدام هذا الفلزّ في صناعة هياكل ساعات اليد؛[100] كما يُستخدَم أيضاً في صناعة التصاميم والقطع الفنّية؛[103] وكذلك في تصميم حلي الجسد.[104] في بعض الأحيان تُسَكّ بعض النقود التذكارية والميداليات من التيتانيوم، وكانت منطقة جبل طارق ذاتية الحكم أوّل من سكّ نقوداً من التيتانيوم، وذلك سنة 1999 احتفالاً بقدوم الألفية.[105]
الطبية
[عدل]بسبب التوافقية الحيوية للتيتانيوم (غير سامّ ولا يُرفَض من الجسم)، فإنّ هذا الفلزّ وسبائكه يدخل في العديد من التطبيقات الطبّية،[106] بما في ذلك صناعة الأدوات الجراحية وزراعة العظام والمفاصل الاصطناعية، وكذلك في مجال زراعة الأسنان؛ ويمكن لتلك البدائل أن تبقى مكانها وقيد الاستخدام لفترةٍ تصل إلى 20 سنة.[2] عادةً ما يُسبَك التيتانيوم لتلك الأغراض مع 4% ألومنيوم أو 6% ألومنيوم و4% فاناديوم.[107]

للتيتانيوم قدرة جوهرية على الالتحام بالعظم، وهذه الخاصّة مفيدة في عمليات التثبيت الداخلي.[2] كما أن انخفاض معامل المرونة للتيتانيوم بشكلٍ قريبٍ من قيمته بالنسبة للعظام يجعل من هذا الفلزّ أيضاً ملائماً لعمليات الزرع، إذ أن الأحمال على الجهاز العظمي ستكون موزّعةً بذلك بين العظم والزرع، ممّا يؤدّي إلى تضاؤل نسبة حدوث حالة تدهور للعظام بسبب الجهد أو حدوث كسر على المناطق الفاصلة بين العظم والزرع. ولكن بالرغم من ذلك، فإنّ قساوة التيتانيوم لا تزال أكبر مرّتين من تلك التي للعظام، بالتالي فإنّ العظام القريبة من أماكن الزرع قد يحدث لها حالة من التدهور.[108][109]
نظراً لأنّ التيتانيوم غير مغناطيسي فإنّ المصابين الذين لديهم زرعات من التيتانيوم يمكن لهم بأمان أن يفحصوا باستخدام التصوير بالرنين المغناطيسي. [ملاحظة 38] قبل إجراء الزرع تخضع قطع التيتانيوم إلى تهيئة بالتعريض إلى درجات حرارة مرتفعة بواسطة قوس من البلازما، ممّا يساعد على إزالة الذرّات الموجودة على السطح، ممّا يدفع ذرّات التيتانيوم المكشوفة إلى التأكسد الفوري، ويتشكّل بذلك طبقة مُخَمِّلة من أكسيد التيتانيوم على السطح.[2] يمكن أن تُصمَّم الزرعات المعقّدة من التيتانيوم باستخدام طباعة ثلاثية الأبعاد، ممّا يفيد بتلبية حاجات المريض الخاصّة، ويزيد من فرصة اندماج الزرعة بالعظام بشكل أكثر ملائمة.[110]
متفرقات
[عدل]
تُستخدَم سبائك التيتانيوم في بعض الأحيان بهدف صنع إطارات النظارات، والتي تتميّز رغم ارتفاع ثمنها بأنّها طويلة العمر والتحمّل، وخفيفة الوزن، ولا تسبّب أيّة حساسية للجلد. كما يُستخدَم التيتانيوم في صناعة هياكل بعض موديلات الحواسيب المحمولة من شركة أبل.[111]
يفضّل بياطرة الخيول استخدام الحَدَوات المصنوعة من التيتانيوم على تلك المصنوعة من الفولاذ، لأنّها أخفّ وزناً وأكثر تحملاً.[100] يُستخدَم التيتانيوم في صناعة العديد من التجهيزات لعدّة ألعاب رياضية، مثل أدوات اللعب في رياضات التنس والغولف واللاكروس والكريكت والهوكي؛ وفي صناعة شَبَك الخُوَذ في كرة القدم الأمريكية، وكذلك في تركيب هياكل الدرّاجات الهوائية ومكوّناتها.[112]
نظراً لمقاومة التيتانيوم للتآكل فإنّ الحاويات المصنوعة من التيتانيوم يمكن أن تُستخدَم لأغراض التخزين طويل الأمد للمخلّفات الإشعاعية.[113][114]
المخاطر
[عدل]التيتانيوم غير سامّ، وليس له أيّ دور حيوي بالنسبة للإنسان.[8] ويُقدَّر بأنّ كمّيّة مقدارها حوالي 0.8 ميليغرام من التيتانيوم تدخل إلى جسم الإنسان يومياً عن طريق الغذاء، من غير أن تحدث عملية امتصاص لها؛[8] ولكنّها في بعض الأحيان قد تتراكم حيوياً داخل الأنسجة، خاصّة تلك التي قد تحوي على السيليكا. بَيّنت دراسة وجود علاقة محتملة بين التيتانيوم ومتلازمة الظفر الأصفر.[115]
يشكّل مسحوق التيتانيوم وخراطته خطراً مسبّباً للحرائق عند التسخين في الهواء، إذ أنّه يشتعل، وهناك خطر حدوث اشتعال انفجاري.[116] لا تُطفَأ حرائق التيتانيوم، مثل أيّ حرائق فلزّات أخرى، باستخدام مطافئ الماء أو ثنائي أكسيد الكربون، ولكن ينبغي استخدام مطافئ من الفئة D الحاوية على بودرة جافة أو رمل بدلاً من ذلك.[3]
هناك احتمالية وقوع حوادث في المنشآت التي تنتج التيتانيوم بسبب وجود غاز الكلور، حيث هناك إمكانية لاندلاع حريق تيتانيوم كلوري.[ملاحظة 39][117] ينبغي أن تُبعَد المؤكسدات عن أماكن تخزين التيتانيوم، فهذا الفلزّ يمكن له أن يشتعل مثلاً بالتماس مع الأكسجين السائل.[118]
طالع أيضاً
[عدل]الهوامش
[عدل]- ^ William Gregor
- ^ Royal Geological Society of Cornwall
- ^ Crell's Annalen
- ^ Franz Joseph Müller von Reichenstein
- ^ Martin Heinrich Klaproth
- ^ Matthew A. Hunter
- ^ William Justin Kroll
- ^ Anton Eduard van Arkel
- ^ Jan Hendrik de Boer
- ^ Project 705 Lira
- ^ VSMPO-AVISMA
- ^ master alloy
- ^ Crystal bar process / van Arkel–de Boer process
- ^ FFC Cambridge process
- ^ Armstrong process
- ^ cuprotitanium
- ^ manganotitanium
- ^ ferrocarbon titanium
- ^ ASTM
- ^ Ferrotitanium
- ^ 6061-T6
- ^ Beta C
- ^ galling
- ^ ultra-high vacuum systems
- ^ atmospheric plasma spraying
- ^ Orthotitanates
- ^ Metatitanates
- ^ barrier metal
- ^ Tebbe's reagent
- ^ Petasis reagent
- ^ Ferrotitanium
- ^ Intergranular corrosion
- ^ Lockheed A-12
- ^ SR-71 Blackbird
- ^ Ultrasonic welding
- ^ Wave soldering
- ^ Lockheed A-12
- ^ Magnetic resonance imaging MRI
- ^ titanium–chlorine fire
المراجع
[عدل]- بلغات أجنبية
- ^ Andersson, N. (2003). "Emission spectra of TiH and TiD near 938 nm" (PDF). J. Chem. Phys. ج. 118: 10543. DOI:10.1063/1.1539848.
- ^ ا ب ج د ه و ز ح Emsley 2001، صفحة 452
- ^ ا ب ج د ه و ز ح ط Krebs، Robert E. (2006). The History and Use of Our Earth's Chemical Elements: A Reference Guide (ط. 2). Westport, CT: Greenwood Press. ISBN:978-0-313-33438-2. مؤرشف من الأصل في 2021-08-31.
- ^ ا ب ج Barksdale 1968، صفحة 732
- ^ Gregor, William (1791) "Beobachtungen und Versuche über den Menakanit, einen in Cornwall gefundenen magnetischen Sand" (Observations and experiments regarding menaccanite [i.e., ilmenite], a magnetic sand found in Cornwall), Chemische Annalen …, 1, pp. 40–54, 103–119. نسخة محفوظة 2021-08-24 على موقع واي باك مشين.
- ^ Gregor, William (1791) "Sur le menakanite, espèce de sable attirable par l'aimant, trouvé dans la province de Cornouilles" (On menaccanite, a species of magnetic sand, found in the county of Cornwall), Observations et Mémoires sur la Physique, 39: 72–78, 152–160. نسخة محفوظة 30 سبتمبر 2020 على موقع واي باك مشين.
- ^ Klaproth, Martin Heinrich (1795) "Chemische Untersuchung des sogenannten hungarischen rothen Schörls" (Chemical investigation of the so-called Hungarian red tourmaline [rutile]) in: Beiträge zur chemischen Kenntniss der Mineralkörper (Contributions to the chemical knowledge of mineral substances), vol. 1, (Berlin, (Germany): Heinrich August Rottmann, 233–244. نسخة محفوظة 2021-08-24 على موقع واي باك مشين.
- ^ ا ب ج د ه Emsley 2001، صفحة 451
- ^ ا ب ج Roza 2008، صفحة 9
- ^ ا ب ج د ه و ز ح ط ي يا يب Lide, D. R.، المحرر (2005)، دليل سي آر سي المرجعي للكيمياء والفيزياء (ط. 86th)، Boca Raton (FL): CRC Press، ISBN:0-8493-0486-5
- ^ ا ب Greenwood & Earnshaw 1997، صفحة 955
- ^ van Arkel، A. E.؛ de Boer, J. H. (1925). "Preparation of pure titanium, zirconium, hafnium, and thorium metal". Zeitschrift für anorganische und allgemeine Chemie. ج. 148: 345–50. DOI:10.1002/zaac.19251480133.
- ^ Yanko، Eugene؛ Omsk VTTV Arms Exhibition and Military Parade JSC (2006). "Submarines: general information". مؤرشف من الأصل في 2020-11-01. اطلع عليه بتاريخ 2015-02-02.
- ^ Stainless Steel World (يوليو–أغسطس 2001). "VSMPO Stronger Than Ever" (PDF). KCI Publishing B.V. ص. 16–19. مؤرشف من الأصل (PDF) في 2006-10-05. اطلع عليه بتاريخ 2007-01-02.
- ^ Defense National Stockpile Center (2008). Strategic and Critical Materials Report to the Congress. Operations under the Strategic and Critical Materials Stock Piling Act during the Period October 2007 through September 2008 (PDF). United States Department of Defense. ص. 3304. مؤرشف من الأصل (PDF) في 2010-02-11.
- ^ Bush، Jason (15 فبراير 2006). "Boeing's Plan to Land Aeroflot". BusinessWeek. مؤرشف من الأصل في 2009-04-09. اطلع عليه بتاريخ 2006-12-29.
{{استشهاد بخبر}}: صيانة الاستشهاد: مسار غير صالح (link) - ^ "Roskill Information Services: Global Supply of Titanium is Forecast to Increase", Titanium Metal: Market Outlook to 2015 (5th edition, 2010). نسخة محفوظة 2021-04-23 على موقع واي باك مشين.
- ^ "ISRO's titanium sponge plant in Kerala fully commissioned". The Economic Times. 10 أغسطس 2015. مؤرشف من الأصل في 2015-08-18. اطلع عليه بتاريخ 2015-11-08.
- ^ Titanium. Mindat نسخة محفوظة 26 أغسطس 2021 على موقع واي باك مشين.
- ^ ا ب ج د ه و "Titanium". Encyclopædia Britannica. 2006. مؤرشف من الأصل في 2008-11-18. اطلع عليه بتاريخ 2006-12-29.
- ^ ا ب ج Emsley 2001، صفحة 453
- ^ ا ب ج د United States Geological Survey. "USGS Minerals Information: Titanium". مؤرشف من الأصل في 2019-02-27.
- ^ Donachie 1988، Ch. 4
- ^ ا ب ج د Stwertka، Albert (1998). "Titanium". Guide to the Elements (ط. Revised). Oxford University Press. ص. 81–82. ISBN:978-0-19-508083-4.
- ^ Barksdale 1968، صفحة 733
- ^ Alexander Stirn: Vom Triebwerk bis zum Campanile. In: Süddeutsche Zeitung. 25. April 2009, S. 22.
- ^ ا ب ج د ه و "Titanium". Columbia Encyclopedia (ط. 6th). New York: Columbia University Press. 2000–2006. ISBN:978-0-7876-5015-5. مؤرشف من الأصل في 2021-09-10.
- ^ Titanium, Titanium Alloys, and Titanium Compounds. Ullmann's Encyclopedia of Industrial Chemistry, doi:10.1002/14356007.a27_095
- ^ Chen، George Zheng؛ Fray, Derek J.؛ Farthing, Tom W. (2000). "Direct electrochemical reduction of titanium dioxide to titanium in molten calcium chloride". Nature. ج. 407 ع. 6802: 361–364. Bibcode:2000Natur.407..361C. DOI:10.1038/35030069. PMID:11014188. S2CID:205008890.
- ^ Roza 2008، صفحة 23
- ^ Roza 2008، صفحة 25
- ^ "Titanium". The Essential Chemical Industry online. York, UK: CIEC Promoting Science at the University of York. 15 يناير 2015. مؤرشف من الأصل في 2021-10-11.
- ^ "Titanium". Microsoft Encarta. 2005. مؤرشف من الأصل في 2006-10-27. اطلع عليه بتاريخ 2006-12-29.
- ^ Donachie 1988، صفحة 16, Appendix J
- ^ "Specification for Titanium and Titanium Alloy Strip, Sheet, and Plate". ASTM International. مؤرشف من الأصل في 2021-08-28.
- ^ ASTM International (2006). Annual Book of ASTM Standards (Volume 02.04: Non-ferrous Metals). West Conshohocken, PA: ASTM International. section 2. ISBN:978-0-8031-4086-8. مؤرشف من الأصل في 2023-03-06. ASTM International (1998). Annual Book of ASTM Standards (Volume 13.01: Medical Devices; Emergency Medical Services). West Conshohocken, PA: ASTM International. sections 2 & 13. ISBN:978-0-8031-2452-3. مؤرشف من الأصل في 2021-08-28.
- ^ Donachie 1988، صفحات 13–16, Appendices H and J
- ^ ا ب ج د ه Barksdale 1968، صفحة 734
- ^ AWS G2.4/G2.4M:2007 Guide for the Fusion Welding of Titanium and Titanium Alloys. Miami: American Welding Society. 2006. مؤرشف من الأصل في 2010-12-10.
{{استشهاد بكتاب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ Titanium Metals Corporation (1997). Titanium design and fabrication handbook for industrial applications. Dallas: Titanium Metals Corporation. مؤرشف من الأصل في 2009-02-09.
{{استشهاد بكتاب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ "Solderability". مؤرشف من الأصل في 2021-06-09. اطلع عليه بتاريخ 2011-06-16.
- ^ Takeda, O., Ouchi, T. & Okabe, T.H. (2020). "Recent Progress in Titanium Extraction and Recycling". Metallurgical and Materials Transactions B. ج. 51: 1315–1328. DOI:10.1007/s11663-020-01898-6.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ G. Audi, A. H. Wapstra, C. Thibault, J. Blachot and O. Bersillon (2003). "The NUBASE evaluation of nuclear and decay properties" (PDF). Nuclear Physics A. ج. 729: 3–128. Bibcode:2003NuPhA.729....3A. DOI:10.1016/j.nuclphysa.2003.11.001. مؤرشف من الأصل (PDF) في 2021-04-20.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ ا ب Barbalace, Kenneth L. (2006). "Periodic Table of Elements: Ti – Titanium". مؤرشف من الأصل في 2012-07-14. اطلع عليه بتاريخ 2006-12-26.
- ^ Donachie 1988، صفحة 11
- ^ Steele، M. C.؛ Hein، R. A. (1953). "Superconductivity of Titanium". Phys. Rev. ج. 92 ع. 2: 243–247. Bibcode:1953PhRv...92..243S. DOI:10.1103/PhysRev.92.243.
- ^ Thiemann، M.؛ وآخرون (2018). "Complete electrodynamics of a BCS superconductor with μeV energy scales: Microwave spectroscopy on titanium at mK temperatures". Phys. Rev. B. ج. 97 ع. 21: 214516. arXiv:1803.02736. Bibcode:2018PhRvB..97u4516T. DOI:10.1103/PhysRevB.97.214516. S2CID:54891002.
- ^ ا ب Barksdale 1968، صفحة 738
- ^ Donachie 1988، Appendix J, Table J.2
- ^ Verarbeitung von Titanwerkstoffen, Teil 1 form-technik.biz, Juli 2014, abgerufen 5. Dezember 2019. نسخة محفوظة 2021-08-28 على موقع واي باك مشين.
- ^ Der Werkstoff Titan: Verarbeitung gustoc.de, abgerufen 5. Dezember 2019. نسخة محفوظة 28 أغسطس 2021 على موقع واي باك مشين.
- ^ Puigdomenech, Ignasi (2004) Hydra/Medusa Chemical Equilibrium Database and Plotting Software, KTH Royal Institute of Technology.
- ^ Casillas, N.؛ Charlebois, S.؛ Smyrl, W. H.؛ White, H. S. (1994). "Pitting Corrosion of Titanium" (PDF). J. Electrochem. Soc. ج. 141 ع. 3: 636–642. Bibcode:1994JElS..141..636C. DOI:10.1149/1.2054783. مؤرشف من الأصل في 2020-08-27.
- ^ Forrest، A. L. (1981). "Effects of Metal Chemistry on Behavior of Titanium in Industrial Applications". Industrial Applications of Titanium and Zirconium. ص. 112.
- ^ "Titanium Sublimation Pump". vacuum-guide.com. مؤرشف من الأصل في 2021-08-29.
- ^ ا ب Greenwood & Earnshaw 1997، صفحة 958
- ^ Greenwood & Earnshaw 1997، صفحة 970
- ^ Greenwood & Earnshaw 1997، صفحة 960
- ^ Greenwood & Earnshaw 1997، صفحة 967
- ^ Greenwood & Earnshaw 1997، صفحة 961
- ^ Greenwood & Earnshaw 1997، صفحة 962.
- ^ Liu, Gang; Huang, Wan-Xia; Yi, Yong (26 Jun 2013). "Preparation and Optical Storage Properties of λTi3O5 Powder". Journal of Inorganic Materials (بالصينية). 28 (4): 425–430. DOI:10.3724/SP.J.1077.2013.12309.
- ^ Bonardi، Antonio؛ Pühlhofer، Gerd؛ Hermanutz، Stephan؛ Santangelo، Andrea (2014). "A new solution for mirror coating in $γ$-ray Cherenkov Astronomy". Experimental Astronomy. ج. 38 ع. 1–2: 1–9. arXiv:1406.0622. Bibcode:2014ExA....38....1B. DOI:10.1007/s10686-014-9398-x. S2CID:119213226.
- ^ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 91.–100., verbesserte und stark erweiterte Auflage. Walter de Gruyter, Berlin 1985, ISBN 3-11-007511-3, S. 1065
- ^ Seong, S.؛ وآخرون (2009). Titanium: industrial base, price trends, and technology initiatives. Rand Corporation. ص. 10. ISBN:978-0-8330-4575-1. مؤرشف من الأصل في 2021-08-30.
- ^ Richard W. Johnson (1998). The Handbook of Fluid Dynamics. Springer. ص. 38–21. ISBN:978-3-540-64612-9. مؤرشف من الأصل في 2021-08-31.
- ^ Coates، Robert M.؛ Paquette, Leo A. (2000). Handbook of Reagents for Organic Synthesis. John Wiley and Sons. ص. 93. ISBN:978-0-470-85625-3. مؤرشف من الأصل في 2021-08-30.
- ^ Greenwood & Earnshaw 1997، صفحة 965
- ^ J. D. Fast: The preparation of pure titanium iodides. In: Recueil des Travaux Chimiques des Pays-Bas. 58, 1939, S. 174–180, دُوِي:10.1002/recl.19390580209.
- ^ Saha، Naresh (1992). "Titanium nitride oxidation chemistry: An x-ray photoelectron spectroscopy study". Journal of Applied Physics. ج. 72 ع. 7: 3072–3079. Bibcode:1992JAP....72.3072S. DOI:10.1063/1.351465.
- ^ Schubert, E.F. "The hardness scale introduced by Friederich Mohs" (PDF). مؤرشف (PDF) من الأصل في 2010-06-03.
- ^ Truini، Joseph (مايو 1988). "Drill Bits". Popular Mechanics. ج. 165 ع. 5: 91. ISSN:0032-4558. مؤرشف من الأصل في 2021-08-30.
- ^ Baliga، B. Jayant (2005). Silicon carbide power devices. World Scientific. ص. 91. ISBN:978-981-256-605-8. مؤرشف من الأصل في 2021-08-30.
- ^ "Titanium carbide product information". H. C. Starck. مؤرشف من الأصل في 2017-09-22. اطلع عليه بتاريخ 2015-11-16.
- ^ "Organotitanium Reagents in Organic Synthesis (Reactivity and Structure Concepts in Organic Chemistry, Vol 24)" Manfred T. Reetz 1986 (ردمك 0-387-15784-0)
- ^ John F. Hartwig (2010) Organotransition Metal Chemistry, from Bonding to Catalysis. University Science Books: New York. (ردمك 189138953X)
- ^ Tshuva، Edit Y.؛ Miller، Maya (2018). "Chapter 8. Coordination Complexes of Titanium(IV) for Anticancer Therapy". في Sigel، Astrid؛ Sigel، Helmut؛ Freisinger، Eva؛ Sigel، Roland K. O. (المحررون). Metallo-Drugs: Development and Action of Anticancer Agents. Berlin: de Gruyter GmbH. ج. 18. ص. 219–250. DOI:10.1515/9783110470734-014. ISBN:9783110470734. PMID:29394027.
{{استشهاد بكتاب}}:|صحيفة=تُجوهل (مساعدة) - ^ Jander, Blasius: Anorganische Chemie I. Hrsg.: Eberhard Schweda. 17., völlig neu bearbeitete Auflage. S. Hirzel Verlag, Stuttgart 2011, ISBN 978-3-7776-2134-0, S. 369
- ^ Eberhard Gerdes: Qualitative Anorganische Analyse. 2., korrigierte und überarbeitete Auflage. Springer-Verlag, Berlin/ Heidelberg, S. 255.
- ^ Buettner، K. M.؛ Valentine، A. M. (2012). "Bioinorganic Chemistry of Titanium". Chemical Reviews. ج. 112 ع. 3: 1863–81. DOI:10.1021/cr1002886. PMID:22074443.
- ^ Hampel، Clifford A. (1968). The Encyclopedia of the Chemical Elements. Van Nostrand Reinhold. ص. 738. ISBN:978-0-442-15598-8.
- ^ Smook، Gary A. (2002). Handbook for Pulp & Paper Technologists (ط. 3rd). Angus Wilde Publications. ص. 223. ISBN:978-0-9694628-5-9. مؤرشف من الأصل في 2021-09-15.
- ^ Moiseyev، Valentin N. (2006). Titanium Alloys: Russian Aircraft and Aerospace Applications. Taylor and Francis, LLC. ص. 196. ISBN:978-0-8493-3273-9. مؤرشف من الأصل في 2021-09-01.
- ^ ا ب Kramer, Andrew E. (5 يوليو 2013). "Titanium Fills Vital Role for Boeing and Russia". The New York Times. مؤرشف من الأصل في 2021-09-06. اطلع عليه بتاريخ 2013-07-06.
- ^ Scharf, Caleb A. (June 17, 2016) The Jupiter Vault. Scientific American. نسخة محفوظة 2021-09-01 على موقع واي باك مشين.
- ^ Leibniz-Institut für Werkstofforientierte Technologien: Vorlesung „Werkstoffe des Leichtbaus II, Teil 3“, abgerufen am 20. August 2018 نسخة محفوظة 2018-08-20 على موقع واي باك مشين.
- ^ ا ب Emsley 2001، صفحة 454
- ^ Donachie 1988، صفحة 13
- ^ Sevan، Vardan (23 سبتمبر 2006). "Rosoboronexport controls titanium in Russia". Sevanco Strategic Consulting. مؤرشف من الأصل في 2012-11-11. اطلع عليه بتاريخ 2006-12-26.
{{استشهاد ويب}}: صيانة الاستشهاد: مسار غير صالح (link) - ^ "GlobalSecurity". GlobalSecurity.org. أبريل 2006. مؤرشف من الأصل في 2021-08-24. اطلع عليه بتاريخ 2008-04-23.
- ^ Donachie 1988، صفحات 11–16
- ^ Kleefisch, E.W.، المحرر (1981). Industrial Application of Titanium and Zirconium. West Conshohocken, PA: ASTM International. ISBN:978-0-8031-0745-8. مؤرشف من الأصل في 2021-09-17.
- ^ Bunshah, Rointan F.، المحرر (2001). "Ch. 8". Handbook of Hard Coatings. Norwich, NY: William Andrew Inc. ISBN:978-0-8155-1438-1.
- ^ Bell، Tom؛ وآخرون (2001). Heat Treating. Proceedings of the 20th Conference, 9–12 October 2000. ASM International. ص. 141. ISBN:978-0-87170-727-7. مؤرشف من الأصل في 2021-09-02.
- ^ National Corvette Museum (2006). "Titanium Exhausts". مؤرشف من الأصل في 3 يناير 2013. اطلع عليه بتاريخ 26 ديسمبر 2006.
- ^ Compact Powerhouse: Inside Corvette Z06’s LT4 Engine 650-hp supercharged 6.2L V-8 makes world-class power in more efficient package. media.gm.com. 20 August 2014 نسخة محفوظة 15 أبريل 2021 على موقع واي باك مشين.
- ^ Mike Gruntman (2004). Blazing the Trail: The Early History of Spacecraft and Rocketry. Reston, VA: American Institute of Aeronautics and Astronautics. ص. 457. ISBN:978-1-56347-705-8. مؤرشف من الأصل في 2021-09-17.
- ^ Lütjering, Gerd؛ Williams, James Case (12 يونيو 2007). "Appearance Related Applications". Titanium. ISBN:978-3-540-71397-5.
- ^ "Denver Art Museum, Frederic C. Hamilton Building". SPG Media. 2006. مؤرشف من الأصل في 2021-09-03. اطلع عليه بتاريخ 2006-12-26.
- ^ ا ب ج Donachie 1988، صفحات 11, 255
- ^ Gafner, G. (1989). "The development of 990 Gold-Titanium: its Production, use and Properties" (PDF). Gold Bulletin. ج. 22 ع. 4: 112–122. DOI:10.1007/BF03214709. S2CID:114336550. مؤرشف من الأصل في 2010-11-29.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: مسار غير صالح (link) - ^ Alwitt, Robert S. (2002). "Electrochemistry Encyclopedia". مؤرشف من الأصل في 2008-07-02. اطلع عليه بتاريخ 2006-12-30.
{{استشهاد ويب}}: صيانة الاستشهاد: مسار غير صالح (link) - ^ "Fine Art and Functional Works in Titanium and Other Earth Elements". مؤرشف من الأصل في 2008-05-13. اطلع عليه بتاريخ 2009-08-08.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ "Body Piercing Safety". doctorgoodskin.com. مؤرشف من الأصل في 2021-09-02. اطلع عليه بتاريخ 2009-08-01.
- ^ "World Firsts | British Pobjoy Mint". www.pobjoy.com (بالإنجليزية). Archived from the original on 2021-08-20. Retrieved 2017-11-11.
- ^ Harun, W. S. W., et al. "A review of powdered additive manufacturing techniques for Ti-6al-4v biomedical applications." Powder Technology 331 (2018): 74-97.
- ^ "Orthopaedic Metal Alloys". Totaljoints.info. مؤرشف من الأصل في 2021-09-04. اطلع عليه بتاريخ 2010-09-27.
- ^ "Titanium foams replace injured bones". Research News. 1 سبتمبر 2010. مؤرشف من الأصل في 2021-06-04. اطلع عليه بتاريخ 2010-09-27.
- ^ Lavine, Marc S., Make no bones about titanium, Science Magazine, 2018.01.08, Volume 359, Issue 6372, pp. 173-174 دُوِي:10.1126/science.359.6372.173-f نسخة محفوظة 19 يونيو 2021 على موقع واي باك مشين.
- ^ Trevisan, Francesco, et al. "Additive manufacturing of titanium alloys in the biomedical field: processes, properties and applications." Journal of applied biomaterials & functional materials 16.2 (2018): 57-67
- ^ "Apple PowerBook G4 400 (Original – Ti) Specs". everymac.com. مؤرشف من الأصل في 2012-04-03. اطلع عليه بتاريخ 2009-08-08.
- ^ Davis، Joseph R. (1998). Metals Handbook. ASM International. ص. 584. ISBN:978-0-87170-654-6. مؤرشف من الأصل في 2020-07-29.
- ^ Shoesmith، D. W.؛ Noel، J. J.؛ Hardie، D.؛ Ikeda، B. M. (2000). "Hydrogen Absorption and the Lifetime Performance of Titanium Nuclear Waste Containers". Corrosion Reviews. ج. 18 ع. 4–5: 331–360. DOI:10.1515/CORRREV.2000.18.4-5.331. S2CID:137825823.
- ^ Carter, L. J.؛ Pigford, T. J. (2005). "Proof of Safety at Yucca Mountain". Science. ج. 310 ع. 5747: 447–8. DOI:10.1126/science.1112786. PMID:16239463. S2CID:128447596. مؤرشف من الأصل في 2021-09-04.
- ^ Berglund، Fredrik؛ Carlmark, Bjorn (أكتوبر 2011). "Titanium, Sinusitis, and the Yellow Nail Syndrome". Biological Trace Element Research. ج. 143 ع. 1: 1–7. DOI:10.1007/s12011-010-8828-5. PMC:3176400. PMID:20809268.
- ^ Cotell، Catherine Mary؛ Sprague, J. A.؛ Smidt, F. A. (1994). ASM Handbook: Surface Engineering (ط. 10th). ASM International. ص. 836. ISBN:978-0-87170-384-2. مؤرشف من الأصل في 2021-09-04.
- ^ Compressed Gas Association (1999). Handbook of compressed gases (ط. 4th). Springer. ص. 323. ISBN:978-0-412-78230-5. مؤرشف من الأصل في 2021-09-18.
- ^ Solomon، Robert E. (2002). Fire and Life Safety Inspection Manual. National Fire Prevention Association (ط. 8th). Jones & Bartlett Publishers. ص. 45. ISBN:978-0-87765-472-8. مؤرشف من الأصل في 2021-09-18.
- باللغة العربية
- ^ "تشغيل مصنع للتيتانيوم الإسفنجي في السعودية 2017". صحيفة البيان الإماراتية. 04 مارس 2016. مؤرشف من الأصل في 2022-03-20.
المعلومات الكاملة للمصادر
[عدل]- Barksdale، Jelks (1968). "Titanium". في Clifford A. Hampel (المحرر). The Encyclopedia of the Chemical Elements. New York: Reinhold Book Corporation. ص. 732–738. LCCN:68029938.
- Donachie، Matthew J., Jr. (1988). TITANIUM: A Technical Guide. Metals Park, OH: ASM International. ص. 11. ISBN:978-0-87170-309-5. مؤرشف من الأصل في 2023-01-24.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - Emsley، John (2001). "Titanium". Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, England, UK: Oxford University Press. ISBN:978-0-19-850340-8.
- Flower، Harvey M. (2000). "Materials Science: A moving oxygen story". Nature. ج. 407 ع. 6802: 305–306. DOI:10.1038/35030266. PMID:11014169.
- Greenwood، N. N.؛ Earnshaw، A. (1997). Chemistry of the Elements (ط. 2). Oxford: Butterworth-Heinemann. ISBN:978-0-7506-3365-9.
- Roza، Greg (2008). Titanium (ط. 1). New York, NY: The Rosen Publishing Group. ISBN:978-1-4042-1412-5. مؤرشف من الأصل في 2023-01-24.
| H | He | |||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||





![{\displaystyle [Ti(OH)_{2}(H_{2}O)_{4}]^{2+}+H_{2}O_{2}\rightarrow \underbrace {[Ti(O_{2})\cdot aq]^{2+}} _{orange}+6H_{2}O}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6609d76654c06a4d553761c126e93c03d2fda39e)


